一种脂肪羧酸脱羧合成三氟甲基烷基溴的方法
1.本发明涉及有机合成技术领域,具体涉及一种对脂肪羧酸脱羧合成三氟甲基烷基溴的方 法。
背景技术:
2.三氟甲基取代的烷基化合物在生物医药领域有着十分重要的应用,目前对将三氟甲基连 接在烷基链上方法具有强烈的需求。其中利用三氟甲基烷基溴为原料合成三氟甲基取代的烷 基化合物是目前一类较为重要的一种方法。然而,目前合成这类化合物的方法十分的少。目 前的方法是利用ruppert试剂对醛进行亲核加成然后溴化得到(如下式所示)。
3.以前的方法:
[0004][0005]
但是该方法步骤繁琐,反应条件苛刻,同时,由于原料醛的来源少,使得底物实用性较 窄,这大大限制了这一类化合物在合成三氟甲基取代的烷基化合物的应用。因此亟需发展一 种高效、简洁、绿色的方法合成这一类化合物。
技术实现要素:
[0006]
本发明针对现有技术的不足,设计一种高效、简洁、绿色的合成三氟甲基烷基溴的方法。
[0007]
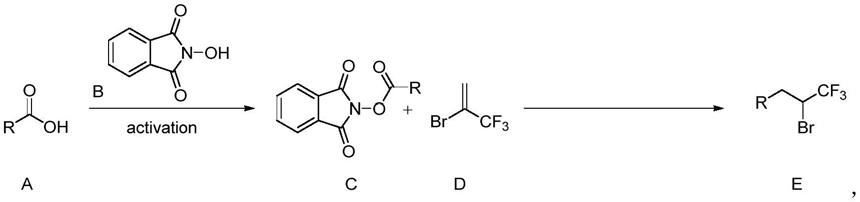
本发明的目的之一是提供一种脂肪羧酸脱羧合成三氟甲基烷基溴的方法,由式a化合物 脂肪羧酸为原料,在室温以及溶剂存在的条件下,与式b化合物n-羟基邻苯二甲酰亚胺反 应,得到式c化合物邻苯二甲酰亚胺酯;随后在光照条件下,以2,6-二甲基-1,4-二氢-3,5-吡 啶二羧酸二乙酯为给电子给体,再与式d化合物2-溴-3,3,3-三氟丙烯进行偶联,得到多种三 氟甲基烷基溴,具体的反应式如下:
[0008][0009]
其中,上述各式中,r为烷基、连有酯基、芳环、氨基或者酰胺的烷基。
[0010]
优选的,所述烷基为c
1-23
烷基。
[0011]
进一步的,式a化合物和式b化合物的摩尔比为1:1~1.2。
[0012]
进一步的,式c化合物、电子给体和式d化合物的摩尔比为1:1.5:2~3。
[0013]
进一步的,反应在20℃~40℃下进行。
[0014]
进一步的,光照为蓝光。
[0015]
进一步,溶剂为甲醇、二甲基亚砜、四氢呋喃、n,n-二甲基甲酰胺、n,n-二甲基乙酰 胺或者n-甲基吡咯烷酮中的一种。
[0016]
羧酸类化合物在工业上十分常见,在本发明中,发明人发展了一种利用廉价易得的脂 肪羧酸类化合物作为起始原料,经简单的活化后,在光诱导下实现了脱羧合成二级的三氟甲 基烷基溴化合物反应,具体是由简单易得的脂肪羧酸a为原料,在室温条件下,与n-羟基 邻苯二甲酰亚胺b反应,得到n-羟基邻苯二甲酰亚胺酯c;随后在光照条件下,选用商业 易得的2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯为给电子体,与2-溴-3,3,3-三氟丙烯进行 偶联,得到多种结构二级的三氟甲基烷基溴化合物。该方法所选用的原料来自于工业原料, 具有优异的经济性;同时该合成策略简单以及具有优异的官能团兼容性。
[0017]
该方法合成简单、底物多样和反应体系经济。此外,该反应体系简单且为均相反应, 因此适合较大规模的生产合成。且通过该合成方法可获得具有潜在应用价值的二级的三氟甲 基烷基溴化合物结构,在医药、农药和材料领域具有潜在价值。
[0018]
本发明的有益效果:(1)本方法所选用的原料来自于工业原料,反应条件温和,经济、 绿色、环保。(2)反应体系简单且为均相,适合较大规模的生产;(3)该反应具有优异的官 能团兼容性以及反应多样性(4)本方法合成的部分产物在生物、材料科学有着十分重要的应 用。
[0019]
应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述 的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再 一一赘述。
[0020]
术语:如本文所用,术语“c
1-23
烷基”指具有1-23个碳原子的直链或支链烷基,例如甲 基、乙基、丙基、异丙基、丁基、异丁基、戊基、己基、庚基、辛基、壬基、癸基或类似基 团。
具体实施方式
[0021]
下面通过具体实施方式进一步详细说明:
[0022]
本发明提供的一种对脂肪羧酸脱羧合成二级的三氟甲基烷基溴的方法,优选地,所述方 法包括步骤:由简单易得的脂肪羧酸a为原料,在室温条件下,与n-羟基邻苯二甲酰亚胺 b反应,得到n-羟基邻苯二甲酰亚胺酯c;随后在蓝光条件下,选用商业易得的2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯为给电子体,将式n-羟基邻苯二甲酰亚胺酯c与式d化合 物进行反应,从而形成式e化合物;
[0023][0024]
各式中,上述各式中,r为c
1-23
烷基、酯基、苯基或者酰胺取代基。
[0025]
更优选地,所述的式a化合物为选自下组的化合物:
[0026][0027]
其中,式c化合物可通过式a化合物与式b化合物用所属领域技术人员所熟知的方法 制备得到,如下:
[0028][0029]
制备方法:向25ml的反应管中,加入326.3mg(2mmol,1equiv.)化合物b,453.9mg (2.2mmol,1.1equiv.)化合物n,n'-二环己基碳二亚胺(dcc),24.4mg(10%mmol)化合物 4-二甲氨基吡啶(dmap),324.4mg(2mmol,1equiv.)化合物a-1室温下搅拌过夜后,得化 合物c-1。其他化合物均按照此方法制备。
[0030][0031]
其中,式d化合物为2-溴-3,3,3-三氟丙烯。
[0032]
本发明式a化合物、式b化合物、式d化合物可通过市售或本发明所属领域技术人员 所熟知的方法制备获得,然而该方法的具体条件,例如反应物、溶剂、所用化合物的量、反 应温度、反应所需时间等不限于下面的解释。
[0033]
作为给电子体可以选用本领域技术人员所熟知的2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二 乙酯。
[0034]
该反应体系中,所使用的给电子体为式a化合物摩尔量的50%-300%,优选为150%。
[0035]
所述的溶剂包括选自下组的溶剂:甲醇、二甲基亚砜、四氢呋喃、n,n-二甲基甲酰胺、 n,n-二甲基乙酰胺和n-甲基吡咯烷酮,溶剂优选为甲醇。
[0036]
本发明制备方法制得的产物可以通过多种方法进行分离纯化,所述方法包括:薄层层析、 柱层析等。以上纯化方法均为本领域的常规方法,例如,使用薄层层析和柱层析时,所用的 展开剂可采用单一的溶剂,也可采用混合溶剂,例如石油醚或石油醚-乙酸乙酯
的混合溶剂 等。
[0037]
本发明提到的上述特征,或实施例提到的特征可以任意组合。本案说明书所揭示的所有 特征可与任何组合物形式并用,说明书中所揭示的各个特征,可以被任何提供相同、均等或 相似目的替代性特征取代。因此除有特别说明,所揭示的特征仅为均等或相似特征的一般性 例子。
[0038]
下面结合具体实施,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用 于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按 照制造厂商所建议的条件。除非另外说明,否则百分比和份数按重量计算。
[0039]
以下实施例中均采用本领域常规的后处理方法进行纯化。
[0040]
实施例1-8
[0041][0042]
向25ml的反应管中,加入61.4mg(0.2mmol,1equiv.)化合物c-1,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入下表中相应2ml的 溶剂和31.1μl(0.3mmol,1.5equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物 e-1,产率如下(氟谱产率,括号内为分离产率)。1h nmr(400mhz,cdcl3)δ7.26
–
7.21(m, 2h),7.20
–
7.14(m,2h),4.23
–
4.14(m,1h),3.22
–
3.09(m,2h),2.89
–
2.77(m,1h),2.71(dd, j=8.4,15.6hz,1h),2.57(dd,j=8.0,15.2hz,1h),2.23
–
2.12(m,2h);13c nmr(101mhz, cdcl3)δ142.9,142.3,126.8(d,j=6.6hz),124.8(d,j=9.3hz),124.4(q,j=278.6hz),47.0 (q,j=32.7hz),39.6,38.0,37.6,37.3;19f nmr(376mhz,cdcl3)δ-72.42(d,j=6.8hz,3f). e-1为新化合物。
[0043][0044]
实施例9
[0045][0046]
向25ml的反应管中,加入61.4mg(0.2mmol,1equiv.)化合物c-1,(0.3mmol,
1.5equiv.) 以下给电子体,氩气置换三次后加入2ml甲醇(meoh)和41.5μl(0.4mmol,2equiv.)化合 物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-1,产率为95%。1h nmr(400mhz,cdcl3) δ7.26
–
7.21(m,2h),7.20
–
7.14(m,2h),4.23
–
4.14(m,1h),3.22
–
3.09(m,2h),2.89
–
2.77(m, 1h),2.71(dd,j=8.4,15.6hz,1h),2.57(dd,j=8.0,15.2hz,1h),2.23
–
2.12(m,2h);
13
cnmr(101mhz,cdcl3)δ142.9,142.3,126.8(d,j=6.6hz),124.8(d,j=9.3hz),124.4(q,j= 278.6hz),47.0(q,j=32.7hz),39.6,38.0,37.6,37.3;
19
f nmr(376mhz,cdcl3)δ-72.42(d,j =6.8hz,3f).e-1为新化合物。
[0047][0048]
实施例10
[0049][0050]
向25ml的反应管中,加入61.4mg(0.2mmol,1equiv.)化合物c-1,不同当量的2,6-二 甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh)和41.5μl(0.4 mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-1,产率为82%。 1
h nmr(400mhz,cdcl3)δ7.26
–
7.21(m,2h),7.20
–
7.14(m,2h),4.23
–
4.14(m,1h),3.22
–ꢀ
3.09(m,2h),2.89
–
2.77(m,1h),2.71(dd,j=8.4,15.6hz,1h),2.57(dd,j=8.0,15.2hz,1h), 2.23
–
2.12(m,2h);
13
c nmr(101mhz,cdcl3)δ142.9,142.3,126.8(d,j=6.6hz),124.8(d,j =9.3hz),124.4(q,j=278.6hz),47.0(q,j=32.7hz),39.6,38.0,37.6,37.3;
19
f nmr(376 mhz,cdcl3)δ-72.42(d,j=6.8hz,3f).e-1为新化合物。
[0051][0052]
实施例11
[0053][0054]
向25ml的反应管中,加入54.6mg(0.2mmol,1equiv.)化合物c-2,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-2, 产率为44%。1h nmr(400mhz,cdcl3)δ4.20
–
4.11(m,1h),1.87
–
1.56(m,8h),1.36
–
1.25 (m,2h),1.21
–
1.14(m,1h),1.12
–
0.99(m,1h),0.87
–
0.79(m,1h);
13
c nmr(101mhz, cdcl3)δ124.6(q,j=278.5hz),45.8(q,j=32.5hz),38.8,34.8,34.1,31.3,26.6,26.4,26.1;
19fꢀꢀ
nmr(376mhz,cdcl3)δ-72.51(d,j=7.1hz,3f).
[0055]
实施例12
[0056][0057]
向25ml的反应管中,加入57.4mg(0.2mmol,1equiv.)化合物c-1,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-3, 产率为86%。1h nmr(400mhz,cdcl3)δ4.14
–
4.06(m,1h),2.09(dd,j=2.0,16.0hz,1h), 2.01(dd,j=8.0,16.0hz,1h),1.55
–
1.43(m,5h),1.41
–
1.25(m,5h),1.00(s,3h);
13
c nmr (101mhz,cdcl3)δ124.8(q,j=278.2hz),44.0,42.1(q,j=32.5hz),38.1,37.8,33.2,26.4, 25.0,22.1(d,j=3.5hz);
19
f nmr(376mhz,cdcl3)δ-73.08(d,j=7.9hz,3f).e-3为新化合 物。
[0058]
实施例13
[0059][0060]
向25ml的反应管中,加入61.8mg(0.2mmol,1equiv.)化合物c-4,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-4, 产率为91%。1h nmr(400mhz,cdcl3)δ4.17
–
4.08(m,1h),2.18
–
2.06(m,2h),1.97
–
1.65 (m,7h),1.48
–
1.38(m,1h),1.29
–
1.17(m,1h);
13
c nmr(101mhz,cdcl3)δ124.4(q,j= 278.6hz),123.5(td,j=242.0,3.1hz),45.7(q,j=32.8hz),37.29
–
37.28(m),33.492(dd,j= 2.6,34.8hz),33.5(dd,j=34.6,48.7hz),33.2(d,j=1.1hz),29.8(d,j=9.7hz),27.2(d,j= 10.0hz);
19
f nmr(376mhz,dmso-d6)δ-70.66(d,j=4.5hz,3f),-89.28(d,j=234.6hz, 1f),-99.17(d,j=230.1hz,1f).e-4为新化合物。
[0061]
实施例14
[0062][0063]
向25ml的反应管中,加入55.0mg(0.2mmol,1equiv.)化合物c-5,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-5, 产率为73%。1h nmr(400mhz,cdcl3)δ4.19
–
4.10(m,1h),4.01
–
3.95(m,2h),3.41(qd,j= 11.0,2.0hz,2h),1.93
–
1.79(m,3h),1.61(d,j=13.2hz,2h),1.47
–
1.37(m,1h),1.27
–
1.17 (m,1h);
13
c nmr(101mhz,cdcl3)δ124.5(q,j=278.4hz),68.1,67.8,45.0(q,j=32.9hz), 38.3,33.5,32.5,31.3;
19
f nmr(376mhz,cdcl3)δ-72.51(d,j=6.4hz,3f).e-5为
新化合物。
[0064]
实施例15
[0065][0066]
向25ml的反应管中,加入74.8mg(0.2mmol,1equiv.)化合物c-6,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-6, 产率为75%。1h nmr(400mhz,cdcl3)δ4.17
–
4.08(m,3h),2.70(q,j=12.4hz,2h),1.92
–ꢀ
1.74(m,3h),1.68
–
1.63(m,2h),1.44(s,9h),1.28
–
1.17(m,1h),1.08
–
0.98(m,1h);
13
c nmr (101mhz,cdcl3)δ155.0,124.4(q,j=278.6hz),79.8,45.1(q,j=32.8hz),43.8(br),37.9, 33.5,32.7,30.3,28.7;
19
f nmr(376mhz,cdcl3)δ-72.53(d,j=6.8hz,3f).
[0067]
实施例16
[0068][0069]
向25ml的反应管中,加入77.6mg(0.2mmol,1equiv.)化合物c-7,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-7, 产率为94%。1h nmr(400mhz,cdcl3)δ4.13
–
4.05(m,1h),3.64
–
3.54(m,2h),3.24
–
3.16 (m,2h),2.08
–
2.06(m,2h),1.60
–
1.46(m,2h),1.44(s,9h),1.40
–
1.32(m,2h),1.06(s,3h); 13
c nmr(101mhz,cdcl3)δ155.1,124.6(q,j=278.4hz),79.8,43.8,41.5(q,j=32.9hz), 39.6(br),37.2,36.6,32.0,28.7,23.3;
19
f nmr(376mhz,dmso-d6)δ-71.23(d,j=8.3hz,3f). e-7为新化合物。
[0070]
实施例17
[0071][0072]
向25ml的反应管中,加入61.4mg(0.2mmol,1equiv.)化合物c-8,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-8, 产率为51%。for the mixture:1h nmr(400mhz,cdcl3)δ7.29(t,j=7.6hz,2h,minor andmajor),7.19(t,j=7.4hz,1h,minor and major),7.10(d,j=8.0hz,2h,minor and major),4.29
ꢀ–
4.17(m,1h,minor and major),2.23
–
2.13(m,1h,minor and major),2.04
–
1.95(m,1h,minorand major),1.91
–
1.86(m,1h,major),1.76
–
1.71(m,1h,minor),1.40
–
1.27(m,1h,minor andmajor),1.11
–
0.96(m,1h,minor and major),1.01
–
0.96(m,1h,minor),0.85
–
0.80(m,1h, minor and major);for the mixture:
13
c nmr(101mhz,cdcl3)δ142.5(major),142.4(minor), 128.73(minor),128.70(major),126.3(major),126.2(minor),126.1(minor and major),124.2(q,j =278.8hz,minor and major),47.44(q,j=32.5hz,major),47.40(q,j=32.5hz,minor),36.9 (d,j=1.7hz,minor),36.7(d,j=1.4hz,major),24.0(major),23.0(minor),21.0(major),20.5 (minor),16.5(minor),15.0(major);for the mixture:
19
f nmr(376mhz,cdcl3)δ-72.14(dd,j =7.1,62.4hz,3f).e-8为新化合物。
[0073]
实施例18
[0074][0075]
向25ml的反应管中,加入77.4mg(0.2mmol,1equiv.)化合物c-9,76.0mg(0.3mmol,1.5 equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh) 和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化合物e-9, 产率为52%。1h nmr(400mhz,cdcl3)δ7.14(d,j=8.0hz,1h),7.12(s,1h),7.00(d,j=8.0 hz,1h),3.84
–
3.76(m,1h),2.73(dd,j=1.6,15.2hz,1h),1.66(dd,j=3.6,11.2hz,1h),1.14
ꢀ–
1.05(m,2h),0.78
–
0.71(m,2h);
13
c nmr(101mhz,cdcl3)δ144.2,143.0,138.9,132.0(t,j =256.5hz),125.1,124.2(q,j=278.8hz),111.1,109.8,45.9(q,j=32.2hz),41.7,23.6,14.0, 12.3;
19
f nmr(376mhz,cdcl3)δ-49.9(s,2f),-72.34(d,j=7.1hz,3f).e-9为新化合物
[0076]
实施例19
[0077][0078]
向25ml的反应管中,加入71.4mg(0.2mmol,1equiv.)化合物c-10,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-10,产率为85%。1h nmr(400mhz,cdcl3)δ4.10
–
4.01(m,1h),3.63(s,3h),2.00(dd, j=1.6,16.0hz,1h),1.88(dd,j=8.8,16.0hz,1h),1.80(t,j=8.0hz,6h),1.58
–
1.45(m,6h); 13
c nmr(101mhz,cdcl3)δ178.3,124.6(q,j=278.3hz),52.1,43.3,41.8(q,j=32.9hz), 39.0,30.9,30.6,28.5;
19
f nmr(376mhz,dmso-d6)δ-71.40(d,j=6.8hz,3f).e-10为新化合 物。
[0079]
实施例20
[0080][0081]
向25ml的反应管中,加入65.0mg(0.2mmol,1equiv.)化合物c-11,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-11,产率为88%。1h nmr(400mhz,cdcl3)δ4.17
–
4.09(m,1h),2.00(s,3h),1.94(dd, j=1.6,15.6hz,1h),1.85(dd,j=8.4,16.0hz,1h),1.69(dd,j=12.4,36.4hz,6h),1.58(t,j= 16.6hz,6h);
13
c nmr(101mhz,cdcl3)δ124.8(q,j=278.2hz),46.5,42.5,41.1(q,j=32.6 hz),37.1,32.6,28.7;
19
f nmr(376mhz,cdcl3)δ-73.13(d,j=7.5hz,3f).e-11为新化合物。
[0082]
实施例21
[0083][0084]
向25ml的反应管中,加入68.2mg(0.2mmol,1equiv.)化合物c-12,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-12,产率为93%。1h nmr(400mhz,cdcl3)δ6.83
–
6.73(m,3h),4.45
–
4.36(m,1h), 4.22
–
4.16(m,1h),2.92
–
2.84(m,1h),2.79
–
2.73(m,1h),2.42(t,j=7.0hz,2h),2.06
–
2.00 (m,1h),1.80
–
1.69(m,1h);
13
c nmr(101mhz,cdcl3)δ157.2(d,j=239.7hz),150.4(d,j= 2.0hz),124.5(q,j=278.1hz),123.1(d,j=7.5hz),117.9(d,j=8.3hz),115.7(d,j=22.7 hz),114.4(d,j=23.3hz),72.1,44.2(q,j=33.3hz),37.7,27.6,25.1;
19
f nmr(376mhz, cdcl3)δ-70.78(d,j=7.9hz,3f),-123.40
–‑
123.41(m,1f).e-12为新化合物。
[0085]
实施例22
[0086][0087]
向25ml的反应管中,加入57.8mg(0.2mmol,1equiv.)化合物c-13,75.99mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-13,产率为85%。for the mixture:1h nmr(400mhz,cdcl3)δ4.19
–
4.09(m,1h),1.97
ꢀ–
1.77(m,3h),1.68
–
1.58(m,1h),1.36
–
1.22(m,7h),1.05
–
0.97(m,2h),0.93
–
0.88(m,4h); for the mixture:
13
c nmr(101mhz,cdcl3)δ124.6(q,j=278.4hz),46.7(q,j=32.5hz, major),46.2(q,j=32.4hz,minor),39.0(minor),38.3(major),37.6(major),
34.7(minor),32.35 (minor),32.29(major),30.4(minor and major),26.8(major),26.3(minor),23.0(minor andmajor),20.3(minor),18.3(major),14.43(major),14.41(minor);for the mixture:
19
f nmr(376 mhz,cdcl3)δ-72.37(d,j=6.8hz,3f,minor),-72.52(d,j=6.4hz,3f,major).e-13为新化合 物。
[0088]
实施例23
[0089][0090]
向25ml的反应管中,加入57.4mg(0.2mmol,1equiv.)化合物c-14,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇(meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-14,产率为70%。1h nmr(400mhz,cdcl3)δ4.12
–
4.03(m,1h),2.06
–
1.97(m,1h), 1.91
–
1.83(m,1h),1.81
–
1.70(m,3h),1.69
–
1.38(m,6h),1.37
–
1.25(m,2h),1.11
–
1.04(m, 2h);
13
c nmr(101mhz,cdcl3)δ124.4(q,j=278.6hz),48.1(q,j=32.5hz),40.1,35.4,33.0, 32.9,31.9,26.3,25.5;
19
f nmr(376mhz,cdcl3)δ-72.33(d,j=6.8hz,3f).e-14为新化合 物。
[0091]
实施例24
[0092][0093]
向25ml的反应管中,加入58.2mg(0.2mmol,1equiv.)化合物c-15,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-15,产率为65%。1h nmr(400mhz,cdcl3)δ4.11
–
4.03(m,1h),3.68(s,3h),2.35(t, j=7.0hz,2h),2.09
–
2.01(m,1h),1.93
–
1.83(m,1h),1.74
–
1.62(m,3h),1.53
–
1.43(m,1h); 13
c nmr(101mhz,cdcl3)δ174.0,124.7(q,j=278.8hz),52.0,47.6(q,j=32.7hz),33.9, 31.4.26.7,24.2;
19
f nmr(376mhz,cdcl3)δ-72.36(d,j=6.8hz,3f).e-15为新化合物。
[0094]
实施例25
[0095][0096]
向25ml的反应管中,加入61.8mg(0.2mmol,1equiv.)化合物c-16,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,
得化 合物e-16,产率为78%。1h nmr(400mhz,cdcl3)δ7.32(t,j=7.4hz,2h),7.26
–
7.20(m, 3h),4.12
–
4.03(m,1h),2.73
–
2.62(m,2h),2.12
–
2.04(m,1h),1.96
–
1.87(m,1h),1.76
–
1.65 (m,3h),1.55
–
1.46(m,1h);
13
c nmr(101mhz,cdcl3)δ142.2,128.7(d,j=3.2hz),126.2, 124.4(q,j=278.7hz),47.9(q,j=32.6hz),35.9,31.6.30.8,26.8;
19
f nmr(376mhz,cdcl3) δ-72.33(d,j=6.0hz,3f).e-16为新化合物。
[0097]
实施例26
[0098][0099]
向25ml的反应管中,加入65.0mg(0.2mmol,1equiv.)化合物c-17,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-17,产率为79%。1h nmr(400mhz,cdcl3)δ7.10(d,j=8.4hz,2h),6.85(d,j=8.8 hz,2h),4.13
–
4.04(m,1h),3.80(s,3h),2.68
–
2.56(m,2h),2.09
–
1.96(m,2h),1.94
–
1.84(m, 1h),1.78
–
1.69(m,1h);
13
c nmr(101mhz,cdcl3)δ158.3,133.4,129.6,124.3(q,j=278.7 hz),114.2,55.6,47.8(q,j=32.7hz),34.2,31.2,29.1;
19
f nmr(376mhz,cdcl3)δ-72.25(d,j =7.1hz,3f).e-17为新化合物。
[0100]
实施例27
[0101][0102]
向25ml的反应管中,加入74.8mg(0.2mmol,1equiv.)化合物c-18,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-18,产率为87%。1h nmr(400mhz,cdcl3)δ7.42(d,j=8.4hz,2h),7.06(d,j=8.4 hz,2h),4.12
–
4.04(m,1h),2.69
–
2.56(m,2h),2.10
–
1.95(m,2h),1.93
–
1.84(m,1h),1.79
–ꢀ
1.70(m,1h);
13
c nmr(101mhz,cdcl3)δ140.3,131.9,130.4,124.3(q,j=278.7hz),120.3, 47.6(q,j=32.7hz),34.6,31.2,28.7;
19
f nmr(376mhz,cdcl3)δ-72.22(d,j=4.1hz,3f). e-18为新化合物。
[0103]
实施例28
[0104][0105]
向25ml的反应管中,加入62.6mg(0.2mmol,1equiv.)化合物c-19,76.0mg
(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-19,产率为72%。1h nmr(400mhz,cdcl3)δ7.29
–
7.24(m,1h),6.97
–
6.89(m,3h), 4.13
–
4.04(m,1h),2.74
–
2.61(m,2h),2.11
–
1.86(m,3h),1.83
–
1.71(m,1h);
13
c nmr(101 mhz,cdcl3)δ163.3(d,j=246.7hz),143.9(d,j=7.2hz),130.3(d,j=8.3hz),124.32(d,j= 2.8hz),124.29(q,j=278.6hz),115.5(d,j=21.0hz),113.4(d,j=21.1hz),47.6(q,j=32.8 hz),34.9,31.2,28.6;
19
f nmr(376mhz,dmso-d6)δ-70.45(d,j=7.9hz,3f),-113.09
–ꢀ‑
113.19(m,1f).e-19为新化合物。
[0106]
实施例29
[0107][0108]
向25ml的反应管中,加入69.0mg(0.2mmol,1equiv.)化合物c-20,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-20,产率为91%。1h nmr(400mhz,cdcl3)δ8.05(d,j=8.4hz,1h),7.91(d,j=7.6 hz,1h),7.78(d,j=8.4hz,1h),7.59
–
7.51(m,2h),7.45(t,j=7.6hz,1h),7.35(d,j=6.8hz, 1h),4.18
–
4.09(m,1h),3.21
–
3.09(m,2h),2.25
–
2.11(m,2h),2.09
–
1.87(m,2h);
13
c nmr (101mhz,cdcl3)δ137.4,134.3,132.0,129.2,127.4,126.3(d,j=5.9hz),125.9(d,j=6.6hz), 124.3(q,j=278.8hz),123.8,47.8(q,j=32.7hz),32.3,31.6,28.2;
19
f nmr(376mhz,cdcl3) δ-72.18(s,3f).e-20为新化合物。
[0109]
实施例30
[0110][0111]
向25ml的反应管中,加入59.2mg(0.2mmol,1equiv.)化合物c-21,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜(dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-21,产率为53%。1h nmr(400mhz,cdcl3)δ8.52
–
8.47(m,2h),7.61(d,j=7.6hz, 1h),7.32(dd,j=4.8,7.6hz,1h),4.14
–
4.05(m,1h),2.78
–
2.65(m,2h),2.13
–
2.00(m,2h), 1.97
–
1.88(m,1h),1.83
–
1.73(m,1h);
13
c nmr(101mhz,cdcl3)δ149.9,147.9,136.7, 136.2,124.2(q,j=278.8hz),123.8,47.4(q,j=32.8hz),32.3,31.2,28.6;
19
f nmr(376mhz, dmso-d6)δ-70.45(s,3f).e-21为新化合物。
[0112]
实施例31
[0113][0114]
向25ml的反应管中,加入65.0mg(0.2mmol,1equiv.)化合物c-22,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-22,产率为79%。1h nmr(400mhz,cdcl3)δ6.76(d,j=8.0hz,1h),6.70
–
6.66(m, 2h),5.95(s,2h),4.01
–
3.92(m,1h),2.95
–
2.88(m,1h),2.72
–
2.64(m,1h),2.32
–
2.23(m, 1h),2.18
–
2.09(m,1h);
13
c nmr(101mhz,cdcl3)δ148.2,146.6,133.2,124.4(q,j=278.6 hz),121.8,109.2,108.8,101.3,46.9(q,j=32.8hz),33.4,32.4;
19
f nmr(376mhz,cdcl3)δ
ꢀ‑
72.14(d,j=6.0hz,3f).e-22为新化合物。
[0115]
实施例32
[0116][0117]
向25ml的反应管中,加入59.8mg(0.2mmol,1equiv.)化合物c-23,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-23,产率为51%。1h nmr(400mhz,cdcl3)δ7.29(q,j=7.5hz,1h),7.00(d,j=8.0 hz,1h),6.97
–
6.92(m,2h),4.01
–
3.93(m,1h),3.03
–
2.97(m,1h),2.80
–
2.73(m,1h),2.38
–ꢀ
2.29(m,1h),2.23
–
2.13(m,1h);
13
c nmr(101mhz,cdcl3)δ163.4(d,j=247.5hz),142.0 (d,j=7.3hz),130.6(d,j=8.4hz),124.5(d,j=2.7hz),124.3(q,j=278.7hz),115.8(d,j=21.1hz),114.0(d,j=21.1hz),46.8(q,j=32.9hz),33.0,32.6;
19
f nmr(376mhz,cdcl3)δ
ꢀ‑
72.17(d,j=6.8hz,3f),-112.89
–‑
112.95(m,1f).e-23为新化合物。
[0118]
实施例33
[0119][0120]
向25ml的反应管中,加入71.4mg(0.2mmol,1equiv.)化合物c-24,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8小时后, 得化合物e-24,产率为73%。1h nmr(400mhz,cdcl3)δ7.60(dd,j=7.2,12.8hz,4h),7.47 (t,j=7.8hz,2h),7.37(t,j=7.2hz,1h),7.32(d,j=8.4hz,2h),4.09
–
4.00(m,
1h),3.10
–ꢀ
3.03(m,1h),2.87
–
2.79(m,1h),2.45
–
2.36(m,1h),2.29
–
2.19(m,1h);
13
c nmr(101mhz, cdcl3)δ141.1,140.0,138.6,129.3,129.1,127.8,127.6,127.3,124.4(q,j=278.7hz),47.1(q,j =32.8hz),33.2,32.4;
19
f nmr(376mhz,cdcl3)δ-72.07(d,j=7.1hz,3f).e-24为新化合 物。
[0121]
实施例34
[0122][0123]
向25ml的反应管中,加入66.2mg(0.2mmol,1equiv.)化合物c-25,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-25,产率为80%。1h nmr(400mhz,cdcl3)δ7.85
–
7.81(m,3h),7.69(s,1h),7.52
–ꢀ
7.45(m,2h),7.35(dd,j=1.6,8.4hz,1h),4.05
–
3.96(m,1h),3.21
–
3.14(m,1h),2.98
–
2.91 (m,1h),2.49
–
2.41(m,1h),2.33
–
2.23(m,1h);
13
c nmr(101mhz,cdcl3)δ136.9,133.9, 132.6,128.9,128.0,127.8,127.3,127.1,126.6,126.0,124.4(q,j=278.7hz),47.1(q,j=32.8 hz),33.1,32.9;
19
f nmr(376mhz,cdcl3)δ-72.10(d,j=7.1hz,3f).e-25为新化合物。
[0124]
实施例35
[0125][0126]
向25ml的反应管中,加入66.2mg(0.2mmol,1equiv.)化合物c-26,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-26,产率为43%。1h nmr(400mhz,cdcl3)δ8.03(d,j=8.4hz,1h),7.89(d,j=8.0 hz,1h),7.78(d,j=8.0hz,1h),7.59
–
7.50(m,2h),7.45
–
7.39(m,2h),4.15
–
4.06(m,1h), 3.57
–
3.50(m,1h),3.21
–
3.14(m,1h),2.54
–
2.45(m,1h),2.37
–
2.27(m,1h);
13
c nmr(101 mhz,cdcl3)δ135.7,134.3,131.9,129.3,127.9,126.8,126.7,126.1,125.9,124.3(q,j=278.8 hz),123.6,47.6(q,j=32.8hz),32.7,30.2;
19
f nmr(376mhz,cdcl3)δ-72.01(d,j=6.4hz, 3f).e-26为新化合物。
[0127]
实施例36
[0128]
[0129]
向25ml的反应管中,加入57.4mg(0.2mmol,1equiv.)化合物c-27,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-27,产率为51%。1h nmr(400mhz,cdcl3)δ7.31(dd,j=3.2,4.8hz,1h),7.05
–
7.03 (m,1h),6.96(dd,j=1.2,4.8hz,1h),4.03
–
3.94(m,1h),3.03
–
2.96(m,1h),2.88
–
2.80(m, 1h),2.39
–
2.30(m,1h),2.22
–
2.12(m,1h);
13
c nmr(101mhz,cdcl3)δ139.7,128.1,126.6, 121.8,124.4(q,j=278.6hz),47.1(q,j=32.8hz),32.4,27.3;
19
f nmr(376mhz,cdcl3)δ
ꢀ‑
72.15(d,j=7.1hz,3f).e-27为新化合物。
[0130]
实施例37
[0131][0132]
向25ml的反应管中,加入69.2mg(0.2mmol,1equiv.)化合物c-28,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-28,产率为56%。1h nmr(400mhz,cdcl3)δ4.91(br,1h),4.39
–
4.30(m,1h),2.77 (dd,j=2.8,15.2hz,1h),1.76
–
1.67(m,1h),1.43(s,9h),0.94
–
0.80(m,3h),0.72
–
0.64(m, 1h);
13
c nmr(101mhz,cdcl3)δ155.7,124.3(q,j=278.6hz),80.2,45.2(q,j=32.3hz), 38.0,31.4,28.6,15.6,13.7;
19
f nmr(376mhz,dmso-d6)δ-70.95(d,j=6.4hz,3f).e-28为 新化合物。
[0133]
实施例38
[0134][0135]
向25ml的反应管中,加入69.6mg(0.2mmol,1equiv.)化合物c-29,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-29,产率为73%。1h nmr(400mhz,cdcl3)δ4.52(br,1h),4.20
–
4.11(m,1h),2.73(d, j=16.0hz,1h),2.29
–
2.23(m,1h),1.42(s,9h),1.35(d,j=8.0hz,6h);
13
c nmr(101mhz, cdcl3)δ154.4,124.6(q,j=278.4hz),79.7,51.9,42.3(q,j=33.0hz),41.0,28.7,28.3,28.1; 19
f nmr(376mhz,cdcl3)δ-72.84(s,3f).e-29为新化合物。
[0136]
实施例39
[0137]
[0138]
向25ml的反应管中,加入72.4mg(0.2mmol,1equiv.)化合物c-30,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-30,产率为98%。1h nmr(400mhz,cdcl3)δ4.54(br,1h),4.09
–
4.01(m,1h),3.11(t, j=6.8hz,2h),2.06
–
1.97(m,1h),1.90
–
1.80(m,1h),1.71
–
1.59(m,1h),1.54
–
1.46(m,2h), 1.43(s,9h),1.40
–
1.24(m,3h);
13
c nmr(101mhz,cdcl3)δ156.3,124.3(q,j=278.7hz), 79.5,47.8(q,j=32.6hz),40.7,31.6,30.1,28.7,26.8,26.1;
19
f nmr(376mhz,cdcl3)δ-72.35 (d,j=7.1hz,3f).e-30为新化合物。
[0139]
实施例40
[0140][0141]
向25ml的反应管中,加入81.2mg(0.2mmol,1equiv.)化合物c-31,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-31,产率为68%。1h nmr(400mhz,cdcl3)δ5.08(br,1h),4.36
–
4.32(m,1h),4.09
–ꢀ
4.01(m,1h),3.75(s,3h),2.12
–
1.99(m,1h),1.95
–
1.80(m,2h),1.71
–
1.59(m,2h),1.54
–ꢀ
1.48(m,1h),1.44(s,9h);for the mixture:
13
c nmr(101mhz,cdcl3)δ173.3,155.6,124.2(q, j=278.6hz),80.4,53.3,52.8,47.4(q,j=32.8hz),36.2,32.3,32.1,31.2,28.6,23.0(d,j=11.5 hz);for the mixture:
19
f nmr(376mhz,cdcl3)δ-72.30(d,j=6.8hz,3f,minor),-72.36(d,j =6.8hz,3f,major).e-31为新化合物。
[0142]
实施例41
[0143][0144]
向25ml的反应管中,加入79.0mg(0.2mmol,1equiv.)化合物c-32,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-32,产率为90%。1h nmr(400mhz,cdcl3)δ7.04(d,j=7.2hz,1h),6.69(d,j=7.6 hz,1h),6.65(s,1h),4.17
–
4.09(m,1h),4.00
–
3.91(m,2h),2.34(s,3h),2.21(s,3h),2.15(dd, j=2.0,16.0hz,1h),2.04(dd,j=8.4,16.0hz,1h),1.88
–
1.74(m,2h),1.57
–
1.45(m,2h), 1.06(d,j=4.4hz,6h);
13
c nmr(101mhz,cdcl3)δ157.3,136.8,130.7,124.8(q,j=278.3 hz),123.9,121.1,112.2,68.3,43.4,42.5(q,j=32.5hz),38.4,33.1,27.5,27.3,24.4,21.7,16.2; 19
f nmr(376mhz,cdcl3)δ-73.04(d,j=7.5hz,3f).e-32为新化合物。
[0145]
实施例42
[0146][0147]
向25ml的反应管中,加入77.8mg(0.2mmol,1equiv.)化合物c-33,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-33,产率为69%。for the mixture:1h nmr(400mhz,cdcl3)δ7.56
–
7.54(m,2h,minor
ꢀꢀ
and major),7.48
–
7.36(m,4h,minor and major),7.10
–
7.02(m,2h,minor and major),4.21
–ꢀ
4.13(m,1h,major),3.75
–
3.66(m,1h,minor),3.20
–
3.08(m,1h,minor and major),2.30
–
2.12 (m,2h,minor and major),1.40
–
1.39(d,j=6.8hz,1h,minor and major),1.35(d,j=35.6hz, 2h,minor and major);for the mixture:
13
c nmr(101mhz,cdcl3)δ160.3(d,j=249.9hz, minor),160.2(d,j=249.6hz,major),147.3(d,j=7.3hz,major),145.5(d,j=7.1hz,minor), 135.9(d,j=1.1hz,major),135.8(d,j=1.2hz,minor),131.6(d,j=4.0hz,minor),131.3(d,j =4.0hz,major),129.3(d,j=2.9hz,minor and major),128.82(minor and major)),128.81 (minor and major),128.04(minor),127.98(major),127.7(d,j=13.6hz,minor and major),124.5 (q,j=278.8hz,major)),124.3(q,j=278.5hz,minor),123.4(d,j=3.2hz,minor),123.2(d,j =3.3hz,major),115.0(d,j=23.0hz,minor),114.8(d,j=23.2hz,major),46.5(q,j=32.8hz, minor),45.7(q,j=32.9hz,major),40.2(major),39.4(minor),37.1(minor),36.7(major),23.0 (minor and major),20.0(minor and major);for the mixture:
19
f nmr(376mhz,cdcl3)δ-71.89 (d,j=7.1hz,3f,major),-72.40(d,j=7.1hz,3f,minor),-117.14(t,j=9.6hz,1f,minor),
ꢀ‑
117.59(t,j=9.8hz,1f,major).e-33为新化合物。
[0148]
实施例43
[0149][0150]
向25ml的反应管中,加入71.8mg(0.2mmol,1equiv.)化合物c-34,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml甲醇 (meoh)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-34,产率为46%。1h nmr(400mhz,cdcl3)δ4.48
–
4.34(m,1h,minor and major),3.87
ꢀ–
3.84(m,1h,minor),3.75(td,j=9.8,3.2hz,1h,major),3.54
–
3.49(m,1h,major),3.43(td,j =10.0,3.2hz,1h,minor),3.10
–
3.01(m,1h,minor and major),2.38
–
2.30(m,1h,minor andmajor),2.20
–
2.08(m,2h,minor and major),1.97
–
1.89(m,1h,minor and major),1.67
–
1.59 (m,2h,minor and major),1.40
–
1.29(m,1h,minor and major),1.26
–
1.16(m,1h,minor andmajor),1.03
–
0.98(m,1h,minor and major),0.96
–
0.88(m,6h,
minor and major),0.87
–
0.75 (m,5h,minor and major);for the mixture:
13
c nmr(101mhz,cdcl3)δ124.6(q,j=278.3hz, minor and major),80.0(minor),79.5(major),64.0(major),63.9(minor),48.7(minor),48.5 (major),45.2(q,j=33.0hz,minor),45.1(q,j=32.9hz,major),40.6(major),40.5(minor),34.9 (major),34.8(minor),32.6(minor),32.5(major),31.9(major),31.8(minor),26.1(major),26.0 (minor),23.7(major),23.4(minor),22.7(minor and major),21.4(minor),21.3(major),16.6 (major),16.4(minor);for the mixture:
19
f nmr(376mhz,cdcl3)δ-72.34(d,j=7.5hz,3f, major),-72.39(d,j=7.5hz,3f,minor).e-34为新化合物。
[0151]
实施例44
[0152][0153]
向25ml的反应管中,加入86.6mg(0.2mmol,1equiv.)化合物c-35,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-35,产率为70%。1h nmr(400mhz,cdcl3)δ8.25(d,j=9.2hz,1h),8.18(dd,j=3.2, 7.6hz,2h),8.13(s,1h),8.11(d,j=2.0hz,1h),8.06
–
7.99(m,3h),7.86(d,j=7.6hz,1h), 4.13
–
4.03(m,1h),3.44
–
3.32(m,2h),2.15
–
2.06(m,1h),2.00
–
1.80(m,4h),1.65
–
1.55(m, 1h);
13
c nmr(101mhz,cdcl3)δ136.4,131.8,131.2,130.2,128.9,127.8,127.7,127.5,127.0, 126.2,124.4(q,j=278.7hz),125.4,125.33,125.29,125.2,125.1,123.5,47.9(q,j=32.6hz), 33.5,31.7,31.1,27.3;
19
f nmr(376mhz,cdcl3)δ-72.25(d,j=6.8hz,3f).e-35为新化合 物。
[0154]
实施例45
[0155][0156]
向25ml的反应管中,加入109.5mg(0.2mmol,1equiv.)化合物c-36,76.0mg(0.3mmol, 1.5equiv.)2,6-二甲基-1,4-二氢-3,5-吡啶二羧酸二乙酯,氩气置换三次后加入2ml二甲亚砜 (dmso)和41.5μl(0.4mmol,2equiv.)化合物d-1。在蓝光照射下,40℃搅拌8h后,得化 合物e-36,产率为83%。for the mixture:1h nmr(400mhz,cdcl3)δ4.11
–
4.02(m,1h),2.93
ꢀ–
2.81(m,3h),2.36
–
2.10(m,8h),2.07
–
1.69(m,8h),1.64
–
1.53(m,2h),1.39(s,3h),1.32
–ꢀ
1.12(m,5h),1.06(s,3h),0.84(dd,j=1.6,6.4hz,3h);for the mixture:
13
c nmr(101mhz, cdcl3)δ212.3,209.4,209.1,124.4(q,j=278.7hz),57.2,52.1(d,j=2.1hz),49.3,48.0(qd,j =32.4,2.8hz),47.1,46.0(d,j=9.3hz),45.8,45.3,43.1,38.9,36.8,36.3(d,j=7.9hz),36.1, 35.5,34.7(d,j=21.1hz),32.0(d,j=35.4hz),
28.1(d,j=6.1hz),25.4,24.2(d,j=5.3hz), 22.2,19.2(d,j=14.6hz),12.1;for the mixture:
19
f nmr(376mhz,cdcl3)δ-72.22(d,j=7.1 hz,3f,minor),-72.34(d,j=6.8hz,3f,major).e-36为新化合物。
[0157]
实施例1~44合成的化合物e-1、化合物e-3、化合物e-4、化合物e-5、化合物e-7、化 合物e-8、化合物e-9、化合物e-10、化合物e-11、化合物e-12、化合物e-13、化合物e-14、 化合物e-15、化合物e-16、化合物e-17、化合物e-18、化合物e-19、化合物e-20、化合物 e-21、化合物e-22、化合物e-23、化合物e-24、化合物e-25、化合物e-26、化合物e-27、 化合物e-28、化合物e-29、化合物e-30、化合物e-31、化合物e-32、化合物e-33、化合物 e-34、化合物e-35、化合物e-36都是新化合物,在农药,材料,以及分子影像学有着潜在 的应用。
[0158]
以上所述的仅是本发明的实施例,方案中公知的具体结构及特性等常识在此未作过多描 述。应当指出,对于本领域的技术人员来说,在不脱离本发明结构的前提下,还可以作出若 干变形和改进,这些也应该视为本发明的保护范围,这些都不会影响本发明实施的效果和专 利的实用性。本技术要求的保护范围应当以其权利要求的内容为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1