金刚烷尾链脂质及其在细胞转染中的应用
1.本发明涉及化学与制剂领域,具体涉及金刚烷尾链脂质及其在细胞转染中的应用。
背景技术:
2.细胞转染是指将外源基因如脱氧核糖核酸(dna)和核糖核酸(rna)导入真核细胞的技术。核酸具有易被降解、负电性强、亲水性强等特点,难以穿过质膜进入靶细胞,因而需要借助适宜的载体将核酸安全高效地递送至靶细胞并发挥作用。
3.用于细胞转染的载体主要分为病毒载体和非病毒载体。病毒载体载量小,存在免疫原性和插入突变的可能性,并且制备成本高。因此,有效载量大、安全性好、成本低且易于制备的非病毒载体受到越来越多的关注。近年来,以脂质载体为代表的非病毒转染方式取得了突破性进展。脂质纳米粒(lipid nanoparticle,lnp)是目前最领先的非病毒递送系统。截至2021年12月,fda已批准3款基于lnp的基因药物,证实了lnp在核酸递送中的应用优势和巨大潜能。lnp的处方主要由可离子化脂质、辅助脂质和聚乙二醇化脂质组成,因此,可以通过设计不同的功能性脂质和改变脂质组成灵活地调控lnp的性质,实现载体的多功能性。
4.由于lnp转染细胞需要克服摄取入胞、内体逃逸、质粒入核等多重屏障,其中摄取入胞作为第一道屏障对于能否实现高效转染至关重要。lnp主要通过网格蛋白介导的内吞作用摄取入胞,这种内吞途径倾向于内化直径小于200nm的粒子。此外,大多数体外研究表明,无论纳米粒的核心成分或表面电荷如何,大小为30~60nm的粒子在非吞噬性细胞中的摄取量最大。
技术实现要素:
5.针对本领域的上述不足,本发明以减小lnp粒径和提高细胞摄取率为目的,设计了一系列金刚烷尾链脂质,即将脂质材料两条疏水烷烃链中的一条替换为刚性极强的金刚烷尾链,用于显著降低lnp的粒径。本发明的金刚烷尾链脂质及其制备的lnp安全性良好,对原代免疫细胞或肿瘤细胞均具有较好的转染能力,在一定程度上解决了目前非病毒载体对细胞转染效率低下的问题,对于开发具有我国自主知识产权的生物功能载体材料具有重要意义。
6.本发明的目的通过如下技术方案实现:
7.本发明公开一类金刚烷尾链脂质,具有通式(i)的结构。
8.2)。
18.羟甲基丙二醇-单脂肪酸(i-2)合成反应式:
[0019][0020]
b.将羟甲基丙二醇-单脂肪酸(i-2)溶解于二氯甲烷(或四氢呋喃,或氯仿),在0℃下依次加入4-二甲氨基吡啶(dmap)、n,n-二异丙基乙胺(dipea)、1-金刚烷乙酸和1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edci),搅拌10~30min后移至室温,反应6~20h。反应结束后,反应液用适量水洗涤两次,1m硫酸氢钾水溶液洗涤两次,饱和食盐水洗涤一次,无水硫酸钠干燥后,抽滤浓缩,粗产物经石油醚/乙酸乙酯柱层析纯化,得到羟甲基丙二醇-双脂肪酸(i-3)。
[0021]
羟甲基丙二醇-双脂肪酸(i-3)合成反应式:
[0022][0023]
c.将羟甲基丙二醇-双脂肪酸(i-3)溶解于二氯甲烷(或四氢呋喃,或氯仿),在室温下向其中依次加入4-二甲氨基吡啶(dmap)、4-硝基苯基氯甲酸酯,搅拌反应1~3h;随后加入r1oh,室温反应1~3h。反应结束后,反应液用适量水洗涤两次,1m硫酸氢钾水溶液洗涤两次,饱和食盐水洗涤一次,无水硫酸钠干燥后,抽滤浓缩,粗产物经二氯甲烷/甲醇柱层析纯化,得到叔胺-羟甲基丙二醇-双脂肪酸(i)。
[0024]
叔胺-羟甲基丙二醇-双脂肪酸(i)合成反应式:
[0025][0026]
本发明所述的金刚烷尾链脂质在制备包载核酸药物的脂质纳米粒中的应用。
[0027]
一种包载核酸药物的脂质纳米粒,含有金刚烷尾链脂质、可离子化脂质、中性磷脂、胆固醇和聚乙二醇化脂质,金刚烷尾链脂质:可离子化脂质:中性磷脂:胆固醇:聚乙二醇化脂质的摩尔比为10~30:10~30:10~30:30~60:0.5~10。
[0028]
本发明包载核酸药物的脂质纳米粒具有30~200nm的平均粒径,+5~+40mv的表面电位。
[0029]
作为本发明的一种优选,可离子化脂质是一类头基含有一个或多个可电离氨基基团,尾链为一条或多条长度为c
6-c
20
的饱和或不饱和烷烃链的脂质材料,其能够在酸性环境下质子化带有正电并与核酸药物通过静电作用结合,如已上市的dlin-kc2-dma、dlin-mc3-dma、alc-0315和sm102等。
[0030]
作为本发明的一种优选,中性磷脂为1,2-二油酰-sn-甘油-3-磷酸乙醇胺(dope)、
1,2-二硬脂酰-sn-甘油-3-磷酸胆碱(dspc)、二肉豆蔻酰磷脂酰胆碱(dmpc)、大豆磷脂(spc)、1,2-二硬脂酰-sn-甘油-3-磷酸乙醇胺(dspe)、1-硬脂酰-2-油酰-sn-甘油-3-磷酸胆碱(sopc)、1-棕榈酰基-2-油酰基卵磷脂(popc)、二芥酰基卵磷脂(depc)、1,2-二油酰-sn-甘油-3-磷酸胆碱(dopc)、二棕榈酰基卵磷脂(dppc)中的一种或多种,优选dope。
[0031]
作为本发明的一种优选,聚乙二醇化脂质,其尾链包括但不限于长度为c
6-c
20
的饱和或不饱和烷烃链,如1,2-二肉豆蔻酰-rac-甘油-3-甲氧基聚乙二醇2000(dmg-peg
2000
)、二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000(dspe-peg
2000
)、胆固醇-聚乙二醇2000(chol-peg
2000
)等。
[0032]
作为本发明的一种优选,金刚烷尾链脂质:可离子化脂质:中性磷脂:胆固醇:聚乙二醇化脂质的摩尔比为15~20:15~20:10~20:40~60:0.5~2.5。
[0033]
作为本发明的一种优选,核酸药物为pdna、sirna、shrna、microrna和mrna等,优选pdna;可离子化脂质和核酸药物的氮磷比为1:1~30:1,优选3:1~8:1。
[0034]
本发明公开的脂质纳米粒制备方法包括:乙醇注入法,微流控法,t型管混合法,过膜挤压法。脂质纳米粒制备方法优选乙醇注入法和微流控法。
[0035]
采用乙醇注入法制备脂质纳米粒的过程如下:称取适量金刚烷尾链脂质、可离子化脂质、中性磷脂、胆固醇和聚乙二醇化脂质,溶解于无水乙醇。同时,将核酸药物溶解于10mm柠檬酸盐缓冲液(ph=4.0)中。在剧烈搅拌状态下,将乙醇相快速注入水相,水相和乙醇相的体积比为1:1~5:1。注入完成后,在室温下用超纯水透析2~8h即可得到脂质纳米粒溶液,4℃保存备用。
[0036]
采用微流控法制备脂质纳米粒的过程如下:称取适量金刚烷尾链脂质、可离子化脂质、中性磷脂、胆固醇和聚乙二醇化脂质,溶解于无水乙醇,作为乙醇相。将核酸药物溶解于10mm柠檬酸盐缓冲液(ph=4.0)中,作为水相。两相以0.02~6ml/min的流速和1:1~5:1的比例同时通过微流控设备混合,在室温下用超纯水透析2~8h即可得到脂质纳米粒溶液,4℃保存备用。
[0037]
本发明所述的脂质纳米粒在pdna转染、sirna基因沉默、mrna疫苗或crispr/cas9基因编辑中的应用;优选用于转染原代免疫细胞或肿瘤细胞,其中免疫细胞包括t细胞、中性粒细胞、巨噬细胞、树突细胞等,肿瘤细胞包括乳腺癌mcf-7细胞、胰腺癌panc-1细胞、肝癌hepg2细胞、肺癌a549细胞等。
[0038]
有益效果:
[0039]
本发明公开的脂质纳米粒粒径均一,电位为正,掺入金刚烷尾链脂质的lnp粒径显著减小(见实施例10)。本发明的脂质纳米粒能稳定荷载sirna(见实施例11)、mrna(见实施例12)和pdna(见实施例13),并具有良好的体外稳定性(见实施例14)。本发明的脂质纳米粒能有效转染原代免疫细胞(见实施例15)和肿瘤细胞(见实施例16),转染效果显著优于阳性对照lipofectamine2000和未加金刚烷尾链脂质的lnp。
[0040]
本发明的创新之处为设计合成了一系列金刚烷尾链脂质,用于减小lnp粒径和提高细胞摄取率,为核酸递送提供转染效率高、安全性好且合成简便的脂质材料。
附图说明
[0041]
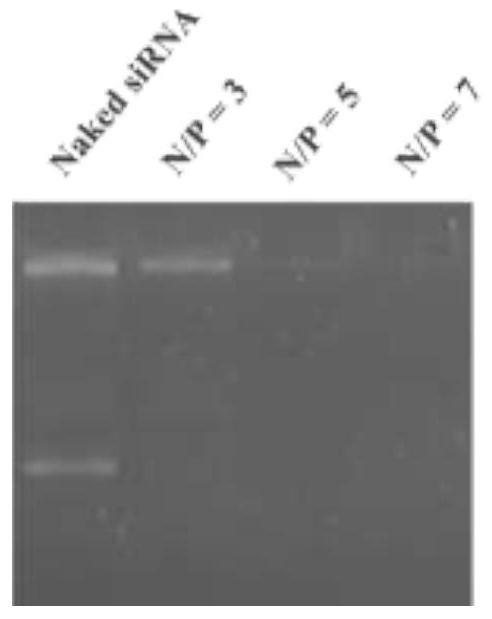
图1是本发明的脂质纳米粒ad8np按不同氮磷比荷载sirna后的琼脂糖凝胶电泳
图;
[0042]
图2是本发明的脂质纳米粒ad8np按不同氮磷比荷载mrna后的琼脂糖凝胶电泳图;
[0043]
图3是本发明的脂质纳米粒ad1np~ad9np按不同氮磷比荷载pdna后的琼脂糖凝胶电泳图;
[0044]
图4是本发明的脂质纳米粒ad1np~ad9np荷载pdna后在不同氮磷比下的粒径和电位;
[0045]
图5是本发明的脂质纳米粒ad8np的体外稳定性;
[0046]
图6是本发明的脂质纳米粒荷载pdna转染人源t细胞后的绿色荧光蛋白(gfp)表达情况(倒置荧光显微镜,比例尺:100μm);
[0047]
图7是本发明的脂质纳米粒荷载pdna转染人源t细胞后的绿色荧光蛋白(gfp)表达情况(流式细胞仪);
[0048]
图8是本发明的脂质纳米粒荷载pdna转染人乳腺癌mcf-7细胞后的绿色荧光蛋白(gfp)表达情况(倒置荧光显微镜,比例尺:100μm);
[0049]
图9是本发明的脂质纳米粒荷载pdna转染人乳腺癌mcf-7细胞后的绿色荧光蛋白(gfp)表达情况(流式细胞仪)。
具体实施方式
[0050]
通过以下实施例对本发明进一步解释,但这些实施例不对本发明构成任何限制。
[0051]
实施例1
[0052]
制备化合物ad1,化学结构式如下:
[0053][0054]
将
ⅰ‑
3(300mg,0.55mmol)溶解于二氯甲烷,在室温下向其中依次加入dmap(154mg,1.26mmol)、4-硝基苯基氯甲酸酯(221mg,1.10mmol),搅拌反应1.5h;随后加入1-(3-羟丙基)吡咯烷(433μl,3.29mmol),室温反应1.5h。反应结束后,反应液用适量水洗涤两次,1m硫酸氢钾水溶液洗涤两次,饱和食盐水洗涤一次,无水硫酸钠干燥后,抽滤浓缩,得到淡黄色凝胶状物。经柱层析纯化(二氯甲烷︰甲醇=30︰1),得到无色透明油状物193mg,收率:30.0%。1h nmr(300mhz,cdcl3):δ(ppm)5.34(t,j=5.6hz,2h,ch2chchch2),4.24-4.18(m,2h,ocooch2,2h,cooch2),4.13(t,j=6.6hz,2h,cooch2,2h,ocooch2),2.90(dd,j=17.3,9.4hz,1h,och2ch,4h,n(ch2ch2)2),2.48-2.36(m,2h,nch2ch2),2.29(d,j=7.6hz,2h,ococh2ch2),2.15(d,j=8.5hz,2h,ococh2c),2.10(d,j=11.3hz,4h,chchch2),1.98(d,j=4.1hz,9h,c
10h15
),1.68(s,4h,n(ch2ch2)2),1.59(d,j=2.0hz,6h,c
10h15
,2h,ococh2ch2,2h,och2ch2),1.34-1.25(m,20h,ch
2(oleoyl)
),0.88(t,j=6.6hz,3h,ch2ch3).
13
c nmr(75mhz,cdcl3):δ(ppm)173.40(1c,ococh2),171.37(1c,cch2coo),154.71(1c,ocoo),129.95(1c,chch),129.63(1c,chch),65.75(1c,ocooch2),65.29(1c,ocooch2),61.29(1c,cooch2ch),60.95(1c,cooch2ch),53.82(1c,nch2ch2ch2o),52.62(2c,nch2ch2),48.72(1c,ococh2c),
42.36(3c,cch2ch
(adamantane)
),37.48(1c,cooch2ch),36.63(3c,chch
2(adamantane)
),34.06(1c,ococh2),32.74(1c,ococh2c),31.82(1c,ch
2(oleoyl)
),29.61(4c,ch
2(oleoyl)
),29.23(2c,ch
2(oleoyl)
),29.05(2c,ch
2(oleoyl)
),28.54(3c,chch
2(adamantane)
),27.10(2c,ch2chchch2),26.55(1c,ocooch2ch2),24.81(1c,ococh2ch2),23.37(2c,nch2ch2),22.58(1c,ch2ch3),13.98(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
42h72
no7[m+h]
+
,702.5303;found,702.5294.
[0055]
实施例2
[0056]
制备化合物ad2,化学结构式如下:
[0057][0058]
标题化合物ad2以化合物
ⅰ‑
3(300mg,0.55mmol)和3-二甲氨基-1-丙醇(390μl,3.29mmol)为原料,按照制备ad1的方法,得到淡黄色油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=30︰1),得到淡黄色油状物210mg,收率:56.6%。1h nmr(300mhz,cdcl3):δ(ppm)5.33(dd,j=12.3,6.8hz,2h,ch2chchch2),4.21(s,2h,ocooch2),4.19(s,2h,cooch2),4.15(d,j=7.0hz,2h,cooch2),4.12(s,2h,ocooch2),2.46-2.40(m,1h,och2ch),2.37(d,j=7.5hz,2h,ococh2),2.29(d,j=7.6hz,2h,(ch3)2nch2),2.24(s,6h,n(ch3)2),2.08(s,2h,c
10h15
ch2),1.98(d,j=9.8hz,4h,chchch2),1.88-1.79(m,2h,(ch3)2nch2ch2),1.72(s,3h,c
10h15
),1.66(d,j=13.1hz,6h,c
10h15
),1.59(s,6h,c
10h15
,2h,ococh2ch2),1.28(dd,j=8.9,3.9hz,20h,ch
2(oleoyl)
),0.87(d,j=6.9hz,3h,ch2ch3).
13
c nmr(75mhz,cdcl3):δ(ppm)173.37(1c,ococh2),171.34(1c,cch2coo),154.92(1c,ocoo),129.93(1c,chch),129.66(1c,chch),66.57(1c,ocooch2ch2),65.21(1c,ocooch2ch),61.42(1c,cooch2ch),61.06(1c,cooch2ch),55.84(1c,(ch3)2nch2),48.71(2c,n(ch3)2),45.25(1c,ococh2c),42.35(3c,cch2ch
(adamantane)
),37.44(1c,cooch2ch),36.64(3c,chch
2(adamantane)
),34.06(1c,ococh2ch2),32.72(1c,ococh2c),31.82(1c,ch
2(oleoyl)
),29.62(2c,ch
2(oleoyl)
),29.43(2c,ch
2(oleoyl)
),29.24(2c,ch
2(oleoyl)
),29.06(2c,ch
2(oleoyl)
),28.55(3c,chch
2(adamantane)
),27.15(2c,ch2chchch2),26.77(1c,(ch3)2nch2ch2),24.81(1c,ococh2ch2),22.59(1c,ch2ch3),13.98(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
40h70
no7[m+h]
+
,676.5147;found,676.5151.
[0059]
实施例3
[0060]
制备化合物ad3,化学结构式如下:
[0061][0062]
标题化合物ad3以化合物
ⅰ‑
3(300mg,0.55mmol)和1-哌啶丙醇(491μl,3.29mmol)
为原料,按照制备ad1的方法,得到淡黄色油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=25︰1),得到无色凝胶状物133mg,收率:33.8%。1h nmr(500mhz,cdcl3):δ(ppm)5.34(dd,j=8.3,5.6hz,2h,chch),4.24(s,2h,ocooch2),4.20(d,j=6.0hz,2h,ocooch2),4.13(dd,j=12.0,6.0hz,4h,cooch2),3.54(s,1h,ch(ch2)3),3.08-2.99(m,2h,ch2ch2n),2.64(s,2h,ocooch2ch2),2.47-2.33(m,4h,nch2ch2),2.30(t,j=7.6hz,4h,ococh2),2.09-2.01(m,4h,chchch2),1.94(t,j=31.2hz,6h,c
10h15
),1.70(d,j=12.1hz,3h,c
10h15
),1.66-1.55(m,6h,c
10h15
,2h,ococh2ch2,4h,nch2ch2),1.50-1.20(m,20h,ch
2(oleoyl)
,2h,nch2ch2ch2),0.87(t,j=6.8hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.50(1c,ococh2),171.46(1c,cch2coo),154.57(1c,ocoo),130.03(1c,chch),129.67(1c,chch),65.42(1c,ocooch2),65.16(1c,ocooch2ch),61.24(1c,cooch2ch),60.90(1c,cooch2ch),54.85(1c,nch2ch2ch2o),53.46(2c,nch2ch2),48.78(1c,ococh2c),42.42(3c,cch2ch
(adamantane)
),37.52(1c,och2ch),36.66(3c,chch
2(adamantane)
),34.11(1c,ococh2ch2,1c,ococh2c),32.80(1c,ch
2(oleoyl)
),31.87(1c,ch
2(oleoyl)
),29.74(1c,ch
2(oleoyl)
),29.68(1c,ch
2(oleoyl)
),29.49(1c,ch
2(oleoyl)
),29.30(1c,ch
2(oleoyl)
),29.14(1c,ch
2(oleoyl)
),29.11(2c,ch
2(oleoyl)
),28.58(3c,chch
2(adamantane)
),27.21(1c,chch),27.15(1c,chch),24.87(1c,ocooch2ch2),23.38(2c,nch2ch2),22.64(1c,ococh2ch2),22.55(1c,nch2ch2ch2),22.13(1c,ch2ch3),14.06(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
43h74
no7[m+h]
+
,716.5460;found,716.5452.
[0063]
实施例4
[0064]
制备化合物ad4,化学结构式如下:
[0065][0066]
标题化合物ad4以化合物
ⅰ‑
3(300mg,0.55mmol)和1-(2-羟乙基)-4-甲基哌嗪(474μl,3.29mmol)为原料,按照制备ad1的方法,得到无色透明油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=20︰1),得到无色凝胶状物120mg,收率:30.5%。1h nmr(500mhz,cdcl3):δ(ppm)5.33(s,2h,chch),4.23(t,j=5.8hz,2h,ocooch2),4.19(d,j=6.0hz,2h,ocooch2),4.14(d,j=6.0hz,2h,cooch2),4.11(d,j=5.9hz,2h,cooch2),2.65(t,j=5.8hz,2h,cooch2ch2),2.55(s,4h,ch3nch2ch2),2.47-2.35(m,4h,ch3nch2ch2),2.31(s,1h,cooch2ch),2.28(s,3h,nch3),2.06(s,2h,ococh2ch2),2.00(dd,j=12.1,6.3hz,4h,chchch2),1.95(s,2h,ococh2c),1.69(d,j=12.1hz,3h,c
10h15
),1.64-1.52(m,9h,c
10h15
),1.36(s,3h,c
10h15
),1.27(dd,j=14.9,7.1hz,2h,ococh2ch2,20h,ch
2(oleoyl)
),0.87(t,j=6.7hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.29(1c,ococh2),171.27(1c,cch2coo),154.84(1c,ocoo),129.85(1c,chch),129.58(1c,chch),65.22(2c,cooch2ch),61.32(1c,ocooch2ch),60.96(1c,ocooch2ch2),56.30(1c,cooch2ch2),54.75(2c,ch3nch2ch2),53.02(2c,ch3nch2ch2),48.63(1c,nch3),45.68(1c,ococh2c),42.27(3c,cch2ch
(adamantane)
),37.34(1c,cooch2ch),36.56(3c,chch
2(adamantane)
),33.98(1c,ococh2ch2),32.65(1c,ococh2c),31.75(1c,ch
2(oleoyl)
),31.36(1c,ch
2(oleoyl)
),30.01(1c,ch
2(oleoyl)
),29.61(1c,ch
2(oleoyl)
),29.54(1c,
ch
2(oleoyl)
),29.36(1c,ch
2(oleoyl)
),29.17(1c,ch
2(oleoyl)
),29.01(1c,ch
2(oleoyl)
),28.98(1c,ch
2(oleoyl)
),28.46(3c,chch
2(adamantane)
),27.07(1c,ch2chch),27.02(1c,chchch2),24.73(1c,ococh2ch2),22.52(1c,ch2ch3),13.93(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
42h73
n2o7[m+h]
+
,717.5412;found,717.5407.
[0067]
实施例5
[0068]
制备化合物ad5,化学结构式如下:
[0069][0070]
标题化合物ad5以化合物
ⅰ‑
3(300mg,0.55mmol)和3-二乙氨基-1-丙醇(489μl,3.29mmol)为原料,按照制备ad1的方法,得到无色透明油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=25︰1),得到淡黄色油状物206mg,收率:53.3%。1h nmr(500mhz,cdcl3):δ(ppm)5.42-5.28(m,2h,ch2chchch2),4.25(t,j=5.6hz,2h,ocooch2),4.20(d,j=6.0hz,2h,cooch2),4.15(d,j=6.1hz,2h,cooch2),4.12(d,j=6.0hz,2h,ocooch2),3.18-3.10(m,4h,n(ch2ch3)2),2.42(dt,j=12.0,6.0hz,1h,och2ch),2.31(t,j=7.6hz,2h,(ch3ch2)2nch2,2h,ococh2ch2),2.08(s,2h,ococh2c),2.01(dd,j=12.1,6.3hz,4h,chchch2),1.97(s,3h,c
10h15
),1.71(d,j=12.1hz,3h,c
10h15
),1.66-1.59(m,9h,c
10h15
),1.59(s,2h,ocooch2ch2,2h,ococh2ch2),1.42(t,j=7.3hz,6h,n(ch2ch3)2),1.28(dd,j=15.1,7.6hz,20h,ch
2(oleoyl)
),0.87(d,j=7.1hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.48(1c,ococh2),171.44(1c,cch2coo),154.56(1c,ocoo),130.02(1c,chch),129.67(1c,chch),65.48(1c,nch2ch2ch2o),65.09(1c,ocooch2ch),61.23(2c,cooch2ch),60.90(1c,(ch3ch2)2nch2),49.12(1c,nch2ch3),48.76(1c,nch2ch3),46.65(1c,ococh2c),42.41(3c,cch2ch
(adamantane)
),37.51(1c,cooch2ch),36.66(3c,chch
2(adamantane)
),34.10(1c,ococh2),32.79(1c,ococh2c),31.87(1c,ch2ch2ch3),29.73(1c,ch
2(oleoyl)
),29.66(1c,ch
2(oleoyl)
),29.49(1c,ch
2(oleoyl)
),29.29(1c,ch
2(oleoyl)
),29.27(1c,ch
2(oleoyl)
),29.14(1c,ch
2(oleoyl)
),29.10(1c,ch
2(oleoyl)
),29.08(1c,ch
2(oleoyl)
),28.57(3c,chch
2(adamantane)
),27.20(1c,chch),27.14(1c,chch),24.86(1c,cooch2ch2),23.46(1c,ch
2(oleoyl)
),22.64(1c,ch
2(oleoyl)
),14.06(1c,ch2ch2ch3),8.49(2c,nch2ch3).hrms,esi
+
,m/z:calcd for c
42h74
no7[m+h]
+
,704.5460;found,704.5451.
[0071]
实施例6
[0072]
制备化合物ad6,化学结构式如下:
[0073][0074]
标题化合物ad6以化合物
ⅰ‑
3(300mg,0.55mmol)和1-甲基-4-哌啶甲醇(434μl,
3.29mmol)为原料,按照制备ad1的方法,得到淡黄色油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=30︰1),得到无色凝胶状物176mg,收率:45.7%。1h nmr(500mhz,cdcl3):δ(ppm)5.40-5.27(m,2h,ch2chchch2),4.20(d,j=6.0hz,2h,ocooch2),4.13(dd,j=11.8,5.9hz,4h,cooch2),4.04(d,j=6.6hz,2h,ocooch2),3.55(d,j=11.7hz,1h,och2ch),2.76(s,3h,nch3),2.69(t,j=11.5hz,2h,ch3nch2),2.41(s,1h,ocooch2ch),2.29(d,j=7.6hz,2h,ch3nch2),2.07(s,4h,chchch2),2.00(d,j=5.9hz,2h,ococh2c,2h,ch3nch2),1.96(s,6h,c
10h15
),1.69(s,3h,c
10h15
),1.64-1.56(m,6h,c
10h15
,4h,ch3nch2ch2,2h,ococh2ch2),1.35-1.23(m,20h,ch
2(oleoyl)
),0.87(t,j=6.8hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.50(1c,ococh2),171.46(1c,cch2coo),153.74(1c,ocoo),130.05(1c,chch),129.65(1c,chch),68.48(1c,nch2ch2chch2),65.40(1c,ocooch2),61.19(1c,cooch2ch),60.84(1c,cooch2ch),52.49(2c,ch3nch2),48.74(1c,nch3),46.97(1c,ococh2c),42.41(3c,cch2ch
(adamantane)
),37.53(1c,och2ch,1c,ococh2ch2),36.65(3c,chch
2(adamantane)
),34.09(1c,ococh2c),31.87(1c,ch
2(oleoyl)
),29.74(1c,ocooch2ch),29.67(2c,ch
2(oleoyl)
),29.49(1c,ch
2(oleoyl)
),29.28(2c,ch
2(oleoyl)
),29.13(1c,ch
2(oleoyl)
),29.08(2c,ch
2(oleoyl)
),28.57(3c,chch
2(adamantane)
),27.21(1c,chch),27.14(1c,chch),26.84(2c,ch3nch2ch2),24.85(1c,ococh2ch2),22.64(1c,ch2ch3),14.06(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
42h72
no7[m+h]
+
,702.5303;found,702.5304.
[0075]
实施例7
[0076]
制备化合物ad7,化学结构式如下:
[0077][0078]
标题化合物ad7以化合物
ⅰ‑
3(300mg,0.55mmol)和1-甲基-2-吡咯烷乙醇(448μl,3.29mmol)为原料,按照制备ad1的方法,得到淡黄色油状粗产物,经柱层析纯化(二氯甲烷︰甲醇=25︰1),得到淡黄色油状物275mg,收率:71.4%。1h nmr(500mhz,cdcl3):δ(ppm)5.40-5.27(m,2h,chch),4.42-4.09(m,8h,cooch2ch),3.87(d,j=12.1hz,1h,cooch2ch),3.19(s,1h,nchch2),2.83(s,3h,nch3),2.42(dd,j=12.1,6.0hz,2h,ch3nch2,2h,ch3nchch2),2.30(t,j=7.6hz,4h,ococh2),2.07(s,4h,chchch2),2.01
–
1.94(m,6h,c
10h15
),1.70(d,j=12.1hz,3h,c
10h15
),1.60(dd,j=14.6,7.6hz,6h,c
10h15
,2h,ococh2ch2,4h,ch3nch2ch2),1.34-1.22(m,20h,ch
2(oleoyl)
),0.87(t,j=6.9hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.49(1c,ococh2),171.46(1c,cch2coo),154.59(1c,ocoo),130.02(1c,chch),129.65(1c,chch),66.15(1c,ch3nch),65.43(1c,ocooch2ch),64.57(1c,ocooch2ch2),61.19(1c,cooch2),60.86(1c,cooch2),56.00(1c,ch3nch2),48.77(1c,ococh2c),42.41(3c,cch2ch
(adamantane)
),37.53(1c,nch3),36.65(3c,chch
2(adamantane)
),34.10(1c,ococh2c),32.79(1c,ococh2ch2,1c,cooch2ch),31.86(1c,ocooch2ch2),29.72(1c,ch3nchch2),29.66(2c,ch
2(oleoyl)
),29.48(1c,ch
2(oleoyl)
),29.28(1c,ch
2(oleoyl)
),29.26(1c,ch
2(oleoyl)
),29.12(2c,ch
2(oleoyl)
),29.09(1c,ch
2(oleoyl)
),29.07(1c,ch
2(oleoyl)
),28.56(3c,chch
2(adamantane)
),27.19
(1c,chch),27.13(1c,chch),24.86(1c,ococh2ch2),22.63(1c,ch2ch3),21.37(1c,ch3nch2ch2),14.05(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
42h70
no7[m+h]
+
,700.5147;found,700.5141.
[0079]
实施例8
[0080]
制备化合物ad8,化学结构式如下:
[0081][0082]
标题化合物ad8以化合物
ⅰ‑
3(300mg,0.55mmol)和三乙醇胺(437μl,3.29mmol)为原料,按照制备ad1的方法,得到黄白色凝胶状粗产物,经柱层析纯化(二氯甲烷︰甲醇=30︰1),得到无色透明油状物174mg,收率:43.9%。1h nmr(500mhz,cdcl3):δ(ppm)5.39-5.27(m,2h,chch),4.21(d,j=5.5hz,2h,cooch2),4.19(d,j=6.2hz,2h,cooch2),4.13(d,j=5.9hz,2h,cooch2),4.11(d,j=5.9hz,2h,cooch2),3.58(t,j=5.1hz,4h,n(ch2ch2oh)2),2.84(t,j=5.5hz,2h,nch2ch2o),2.83-2.74(m,2h,oh),2.71(dd,j=12.8,7.7hz,4h,n(ch2ch2oh)2),2.40(dt,j=11.9,5.9hz,1h,cooch2ch),2.28(t,j=7.6hz,2h,ococh2ch2),2.06(s,2h,ococh2c),1.99(dd,j=14.5,8.5hz,4h,ch2chchch2),1.94(s,3h,c
10h15
),1.68(d,j=12.2hz,3h,c
10h15
),1.62-1.54(m,9h,c
10h15
),1.33(d,j=18.4hz,2h,ococh2ch2),1.26(dd,j=14.9,7.2hz,20h,ch
2(oleoyl)
),0.86-0.83(m,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.58(1c,ococh2),171.53(1c,cch2coo),155.23(1c,ocoo),129.98(1c,chch),129.72(1c,chch),66.12(1c,ocooch2ch),65.43(1c,ocooch2ch2),61.34(1c,cooch2ch),61.03(1c,cooch2ch),59.85(2c,ch2ch2oh),57.07(2c,ch2ch2oh),53.92(1c,nch2ch2o),48.76(1c,ococh2c),42.39(3c,cch2ch
(adamantane)
),37.52(1c,och2ch),36.68(3c,chch
2(adamantane)
),34.12(1c,ococh2ch2),32.79(1c,ococh2c),31.88(1c,ch
2(oleoyl)
),31.48(1c,ch
2(oleoyl)
),30.14(1c,ch
2(oleoyl)
),29.75(1c,ch
2(oleoyl)
),29.68(1c,ch
2(oleoyl)
),29.49(1c,ch
2(oleoyl)
),29.30(1c,ch
2(oleoyl)
),29.14(1c,ch
2(oleoyl)
),29.09(1c,ch
2(oleoyl)
),28.59(3c,chch
2(adamantane)
),27.20(1c,chchch2),27.16(1c,chchch2),24.86(1c,ococh2ch2),22.64(1c,ch2ch3),14.06(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
41h72
no9[m+h]
+
,722.5202;found,722.5203.
[0083]
实施例9
[0084]
制备化合物ad9,化学结构式如下:
[0085][0086]
标题化合物ad9以化合物
ⅰ‑
3(300mg,0.55mmol)和1-甲基-3-吡咯烷醇(362μl,3.29mmol)为原料,按照制备ad1的方法,得到无色透明油状粗产物,经柱层析纯化(二氯甲
烷︰甲醇=25︰1),得到无色透明油状物166mg,收率:44.9%。1h nmr(500mhz,cdcl3):δ(ppm)5.35-5.27(m,2h,chch),4.15(dddd,j=11.4,9.5,8.3,4.8hz,6h,cooch2ch),3.90(s,1h,ocooch),3.63(s,1h,ch(ch2)3),3.09(d,j=12.5hz,2h,nch2ch),2.87(s,3h,nch3),2.53-2.36(m,2h,ococh2),2.29(d,j=7.6hz,2h,ococh2),2.04(d,j=32.6hz,4h,chchch2),2.00-1.88(m,6h,c
10h15
),1.70(d,j=12.1hz,3h,c
10h15
),1.60(dd,j=14.8,7.5hz,6h,c
10h15
,2h,ococh2ch2,4h,ch3nch2ch2),1.32-1.22(m,20h,ch
2(oleoyl)
),0.87(t,j=6.9hz,3h,ch2ch3).
13
c nmr(126mhz,cdcl3):δ(ppm)173.48(1c,ococh2),171.44(1c,cch2coo),153.82(1c,ocoo),130.03(1c,chch),129.66(1c,chch),76.54(1c,ocooch),65.70(1c,ch3nch2ch),61.07(1c,ocooch2ch),60.74(1c,cooch2ch),60.10(1c,cooch2ch),54.27(1c,ch3nch2ch2),48.75(1c,ococh2c),42.41(3c,cch2ch
(adamantane)
),42.01(1c,nch3),37.59(1c,ch3nch2ch2),36.65(3c,chch
2(adamantane)
),34.09(1c,och2ch),32.80(1c,ococh2ch2),31.87(1c,ococh2c),31.77(1c,ch
2(oleoyl)
),29.73(1c,ch
2(oleoyl)
),29.67(1c,ch
2(oleoyl)
),29.49(1c,ch
2(oleoyl)
),29.29(2c,ch
2(oleoyl)
),29.13(1c,ch
2(oleoyl)
),29.10(2c,ch
2(oleoyl)
),28.56(3c,chch
2(adamantane)
),27.20(1c,chchch2),27.14(1c,chchch2),24.85(1c,ococh2ch2),22.64(1c,ch2ch3),14.06(1c,ch2ch3).hrms,esi
+
,m/z:calcd for c
40h68
no7[m+h]
+
,674.4990;found,674.4991.
[0087]
实施例10
[0088]
脂质纳米粒的制备与表征
[0089]
制备方法:按照一定摩尔比精密称取所需的金刚烷尾链脂质、可离子化脂质、中性磷脂、胆固醇和聚乙二醇化脂质溶解于无水乙醇作为乙醇相。同时制备处方中不含金刚烷尾链脂质的noadnp作为对照。具体处方如表1所示。
[0090]
表1本发明脂质纳米粒的处方
[0091][0092]
将pdna溶于10mm柠檬酸盐缓冲液(ph=4.0)作为水相。在剧烈搅拌状态下,将乙醇相快速注入水相,水相和乙醇相的体积比为5:1。注入完成后,样品用超纯水在室温下透析4h即可得到lnp溶液,置于4℃保存备用。使用omni粒度电位分析仪测定lnp的粒径、电位和多分散系数,结果如表2所示。
[0093]
表2本发明脂质纳米粒的性质(n=3)
[0094]
[0095][0096]
上述数据表明,本发明的lnp粒径在30~200nm之间,处方中掺入金刚烷尾链脂质的lnp的粒径显著小于处方中不掺入金刚烷尾链脂质的lnp的粒径,说明金刚烷尾链脂质具有减小lnp粒径的作用;本发明lnp的zeta电位在+5~+40mv之间,表明其具有良好的安全性,符合作为基因载体转染的要求。
[0097]
实施例11
[0098]
脂质纳米粒对sirna的荷载能力考察
[0099]
使用上述乙醇注入法按照不同的氮磷比(n/p=3,5,7)制备荷载sirna的脂质纳米粒ad8np。通过琼脂糖凝胶电泳实验考察脂质纳米粒荷载sirna的能力,如图1所示。结果表明,本发明的脂质纳米粒在一定n/p下能够稳定荷载sirna不发生泄漏,可进一步用于细胞转染实验。
[0100]
实施例12
[0101]
脂质纳米粒对mrna的荷载能力考察
[0102]
使用上述乙醇注入法按照不同的氮磷比(n/p=1,3,5,7)制备荷载mrna的脂质纳米粒ad8np。通过琼脂糖凝胶电泳实验考察脂质纳米粒荷载mrna的能力,如图2所示。结果表明,本发明的脂质纳米粒在一定n/p下能够稳定荷载mrna不发生泄漏,可进一步用于细胞转染实验。
[0103]
实施例13
[0104]
脂质纳米粒对pdna的荷载能力考察
[0105]
使用上述乙醇注入法按照不同的氮磷比(n/p=1,3,5,7,9)制备荷载pdna的脂质纳米粒ad1np~ad9np。通过琼脂糖凝胶电泳实验考察脂质纳米粒荷载pdna的能力(如图3所示),并测定不同n/p下ad1np~ad9np的粒径和电位(如图4所示)。结果表明,本发明的所有lnp在一定n/p下均能够稳定荷载pdna不发生泄漏,且所有lnp的粒径在30~200nm之间,zeta电位在+10~+40mv之间,可进一步用于细胞转染实验。
[0106]
实施例14
[0107]
脂质纳米粒的体外稳定性考察
[0108]
按上述方法制备荷载pdna质粒的脂质纳米粒ad8np,加入不同介质后在37℃分别静置0、2、4、6、8、12h后,通过粒径仪测量其粒径变化,结果如图5所示。数据显示ad8np在培养基、血清、pbs和超纯水中孵育12h后粒径基本不变,表明本发明的脂质纳米粒ad8np具有
良好的体外稳定性。
[0109]
实施例15
[0110]
脂质纳米粒转染人源t细胞
[0111]
按上述方法制备荷载pdna的脂质纳米粒ad1np~ad9np。转染时以1
×
106cells/ml的密度将人源t细胞接种于24孔板中,每孔加入0.5ml含cd3/cd28刺激剂和人源il-2的t细胞培养基,最后加入100μl脂质纳米粒(含1μg pdna),置于含5%二氧化碳的37℃细胞孵箱中培养48h后采用倒置荧光显微镜观察人源t细胞中绿色荧光蛋白的表达情况,并用流式细胞仪定量考察人源t细胞中的绿色荧光强度。本实验以商业化转染试剂lipofectamine 2000为阳性对照,并与处方中不含金刚烷尾链脂质的noadnp对比,评价本发明所提供的脂质纳米粒的转染效果。实验结果图6和图7所示。
[0112]
上述实验结果表明,相比于处方中不含金刚烷尾链脂质的lnp,本发明的所有脂质纳米粒ad1np~ad9np均能高效转染人源t细胞。其中,ad8np的转染效果显著优于阳性对照lipofectamine 2000。
[0113]
实施例16
[0114]
脂质纳米粒转染mcf-7细胞
[0115]
按上述方法制备荷载pdna的脂质纳米粒ad1np~ad9np,同时制备不含有金刚烷尾链的脂质纳米粒noadnp作为对照。取对数生长期的mcf-7细胞,调整细胞密度为2
×
105个/ml的细胞悬液,接种于24孔细胞板中,每孔接种细胞悬液500μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入100μl脂质纳米粒(含1μg pdna)和400μl dmem高糖培养基,继续培养6h后弃去旧培养基,用pbs洗涤三次,加入500μl含10%胎牛血清的dmem高糖培养基继续培养48h后,通过倒置荧光显微镜观察mcf-7中绿色荧光蛋白的表达情况,并用流式细胞仪定量考察mcf-7中的阳性率。实验结果如图8和9所示,相比于处方中不含金刚烷尾链脂质的lnp,本发明的脂质纳米粒ad1np~ad9np均能高效转染mcf-7细胞。其中,ad3np、ad5np、ad8np的转染阳性率显著优于阳性对照lipofectamine 2000。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1