一种四种肠道病毒的核酸检测试剂盒、引物探针组及检测方法与流程
p,其中上游引物的核苷酸序列分别如seq id no:5所示;下游引物的核苷酸序列如seq id no:6所示;特异性探针的核苷酸序列如seq id no:7所示;ca16的上游引物为序列ca16-f;下游引物为序列ca16-r,特异性探针为序列ca16-p,其中上游引物的核苷酸序列分别如seq id no:8所示;下游引物的核苷酸序列如seq id no:9所示;特异性探针的核苷酸序列如seq id no:10所示;ca6的上游引物为序列ca6-f;下游引物为序列ca6-r,特异性探针为序列ca6-p1、ca6-p2,其中上游引物的核苷酸序列分别如seq id no:11所示;下游引物的核苷酸序列如seq id no:12所示;特异性探针的核苷酸序列如seq id no:13、seq id no:14所示。
7.作为本发明的进一步改进,该试剂盒包括上述的引物探针组。
8.作为本发明的进一步改进,所述肠道病毒ev的特异性探针序列的5’端用rox修饰,3’端用bhq2修饰;所述ev71的特异性探针序列的5’端用cy5修饰,3’端用bhq2修饰;所述ca16的特异性探针序列9的5’端用joe修饰,3’端用bhq1修饰;所述ca6的特异性探针序列的5’端用fam修饰,3’端用bhq1修饰。
9.作为本发明的进一步改进,由荧光pcr检测反应液、上述的引物探针组混合液、酶混合液、阳性对照品、阴性对照品组成。
10.作为本发明的进一步改进,肠道病毒ev、ev71、ca16、ca6的正向引物:反向引物:特异性荧光探针的摩尔量为:ev:200nm:200nm:160nm;ev71:400nm:200nm:600nm;ca16:200nm:300nm:600nm;ca6:200nm:200nm:60um:60nm。
11.作为本发明的进一步改进,成分如下所示:(1)rt-pcr反应液:包括荧光pcr缓冲液、dntp、depc水;(2)引物探针混合液:包括上述的引物探针组;(3)混合酶液:包括rna酶抑制剂、逆转录酶、dna聚合酶;(4)阳性对照:包括含上述引物探针组的扩增目的片段的ev、ev71、ca16、ca6源性rna;(5)阴性对照:为te溶液。
12.作为本发明的进一步改进,所述试剂盒于-20℃避光储存。
13.本发明进一步保护一种四重荧光pcr方法,包括如下步骤:s1.提取待测样本的总rna;s2.以所述总rna为模板,并使用上述的引物探针组,进行重组酶聚合酶扩增反应;s3.收集fam、joe、cy5、rox检测通道荧光信号,得到检测结果:s301.质控标准:阳性对照的fam、joe、cy5、rox荧光信号有荧光指数增长,且ct值≤30;阴性对照和空白对照无荧光指数增长,ct值≥40;s302.阳性样品:当步骤s301成立时,fam或/和joe或/和cy5或/和rox有荧光指数增长,且ct值≤37,表明该样品检出ca6或/和ca16型或/和ev71型或/和肠道病毒通用;s303.阴性样品:当步骤s301成立时,fam或/和joe或/和cy5或/和rox无荧光指数增长,ct值≥40,表明该样品未检出ca6或/和ca16型或/和ev71型或/和肠道病毒通用;
s304.疑似样品:当步骤s301成立时,fam或/和joe或/和cy5或/和rox有荧光指数增长,且37≤ct值≤40,重复检测一次;如复检结果仍在37≤ct值≤40,有明显指数增长,则判定为阳性,否则为阴性。
14.作为本发明的进一步改进,所述反应液配制如下表1所示:表1。
15.作为本发明的进一步改进,所述反应条件如下表2所示:表2。
16.本发明具有如下有益效果:本发明运用一步法实时荧光定量rt-pcr技术,采用ev及ev71、cval6、cva6病毒高度特异的引物和荧光标记探针,研制用于肠道病毒ev以及其三个亚型(ev71、cval6、cva6)检测的四重实时荧光定量rt-pcr检测试剂盒。该发明是通过一个pcr反应,可以从粪便标本中同时检测出是否有肠道病毒的存在,并同时进行主要肠道病毒型别的分型鉴定,比单重荧光定量pcr方法更便捷迅速、节约成本。同时,对检测的病毒进行实时准确定量,根据病毒感染的滴度,为临床上患者提供早期诊断,为临床治疗方案的制定提供参考依据;可应用于肠道病毒引起暴发疫情的实验室应急诊断、肠道病毒快速筛查分型、临床诊断及手足口病的流行病学的研究。
附图说明
17.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
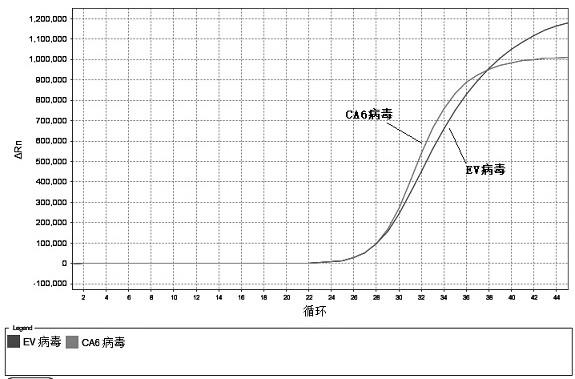
18.图1为实施例1中ca6病毒阳性标本扩增曲线图;图2为实施例1中ca16病毒阳性标本扩增曲线图;图3为实施例1中ev71病毒阳性标本扩增曲线图;
图4为实施例1中其他肠道病毒阳性标本扩增曲线图;图5为本试剂盒阳性对照扩增曲线图;图6为本试剂盒阴性对照扩增曲线图。
具体实施方式
19.下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
20.在以下实施例中,未详细描述的各种过程和方法是本领域中公知的常规方法。下述实例中所用的材料、试剂、装置、仪器、设备等,如无特殊说明,均可从商业途径获得。
21.实施例1自制样品使用外购的核酸提取试剂盒(硕世核酸提取试剂盒)分别提取含有ev、ev71、ca16、ca6的病毒标本进行检测。引物溶液、探针溶液和阳性对照为本专利所述的试剂盒主要成分,阴性对照为te溶液。按表3进行配置,按表4设置相关参数上机检测(abi荧光定量pcr仪,型号为7500)。
22.表3反应体系试剂25μl体系rt-pcr反应液17μl引物探针混合液2μl混合酶液1μl样品5μl表4反应条件检测结果见表5:
①
质控标准:阳性对照的fam、joe、cy5、rox荧光信号有荧光对数增长,且ct值≤30。
②
检测样品:fam、joe、cy5、rox均有荧光对数增长,且ct值≤35 .0,表明该试剂盒分别检出ev、ev71、ca16、ca6。
23.③
阴性对照:fam、joe、cy5、rox均无荧光对数增长,ct值≥40 .0的结果,表明了本
申请方法的特异性和抗干扰性。
24.表5实验结果结论:在实施例1中,使用荧光定量pcr仪(abi-7500)进行扩增,得到曲线图:根据扩增曲线(图1-6)我们可以得出:1.阳性对照的fam、joe、cy5、rox通道有荧光对数增长,其中fam的ct值为24,joe的ct值为24,cy5的ct值为24,rox的ct值为24,阳性对照结果正常(图5)。
25.2.ca6阳性病毒标本的fam通道有荧光对数增长,ct值为28,rox通道有荧光对数增长,ct值为28;joe、cy5通道没有荧光对数增长,检测结果与已验证病毒种类一致(图1)。
26.3.ca16阳性病毒标本的joe通道有荧光对数增长,ct值为32,rox通道有荧光对数增长,ct值为32;fam、cy5通道没有荧光对数增长,检测结果与已验证病毒种类一致(图2)。
27.4.ev71阳性病毒标本的cy5通道有荧光对数增长,ct值为23,rox通道有荧光对数增长,ct值为23;fam、joe通道没有荧光对数增长,检测结果与已验证病毒种类一致(图3)。
28.5.其他肠道病毒阳性病毒标本的rox通道有荧光对数增长,ct值为29;fam、joe、cy5通道没有荧光对数增长,检测结果与已验证病毒种类一致(图4)。
29.6.阴性对照的fam、joe、cy5、rox通道均无荧光对数增长,阴性对照结果正常(图6)。
30.表明了本技术方法的特异性和抗干扰性。
31.以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1