一种诱导T细胞重编程为类NK细胞的组合物及其应用的制作方法
一种诱导t细胞重编程为类nk细胞的组合物及其应用
技术领域
1.本发明属于生物医药技术领域,涉及一种诱导t细胞重编程为类nk细胞的组合物及其应用。
背景技术:
2.自然杀伤细胞(natural killer cell,nk)是机体重要的免疫细胞,不仅与抗肿瘤、抗病毒感染和免疫调节有关,而且在某些情况下参与超敏反应和自身免疫性疾病的发生。nk细胞是天然免疫系统的重要组成部分,其杀伤活性无mhc(主要组织相容性复合体,major histocompatibility complex)限制,不依赖抗体。nk细胞是人体内最有效、活力最强的免疫细胞之一,通过nkp46等nk细胞受体(ncr)识别病毒及病毒感染细胞,参与多种病毒的免疫应答反应。
3.然而,由于人体内自然存在的nk细胞数量和再生能力有限,细胞来源成为限制nk细胞应用于肿瘤治疗的主要障碍。t细胞表面的t细胞受体(tcr)识别病毒感染细胞或外源抗原,并做出反应。类nk细胞不仅可以表达ncr受体如nkp46、nkp30、nkp44和nkg2d等,而且可以表达功能完整的tcr受体,同时具备t细胞和nk细胞的功能。类nk细胞具有比正常nk细胞更强的杀伤活性及更广谱的抗肿瘤效应,同时还能在体外条件下大量增殖,体外增殖的类nk细胞能在体内继续存活三周以上。将t细胞重编程为类nk细胞,为肿瘤及相关疾病的免疫治疗提供一种全新的细胞源,将极大地推动肿瘤细胞免疫治疗的发展。
4.目前,t细胞重编程方法主要基于转基因手段,包括慢病毒转染、pb系统电转、crispr/cas9系统敲除等,然而这些方法存在诸多缺陷,例如,慢病毒转染方式处理周期长、过程繁琐,电转方式会损失大量原代t细胞、效率较低,基因过表达或敲除过程存在脱靶几率,且以上三种方式均较难实现规模化应用,仍然不能从根本上实现体外大规模获取nk细胞的效果。此外也有研究人员采用化学小分子诱导t细胞重编程为类nk细胞,但此方法的效率一般,而且化学小分子对t细胞存在一定的毒性,因此限制了此方法的应用。
5.因此,如何开发一种诱导t细胞重编程为类nk细胞的方法,以提高重编程效率,且不影响或者促进t细胞的生长,成为了本领域亟待解决的问题。
技术实现要素:
6.针对现有技术的不足,本发明的目的在于提供一种诱导t细胞重编程为类nk细胞的组合物及其应用。
7.为达到此发明目的,本发明采用以下技术方案:
8.第一方面,本发明提供一种诱导t细胞重编程为类nk细胞的组合物,所述诱导t细胞重编程为类nk细胞的组合物包括维生素c和小分子化合物;
9.所述小分子化合物包括dna甲基转移酶抑制剂、组蛋白去乙酰酶抑制剂或组蛋白甲基转移酶ezh2抑制剂中的任意一种或至少两种的组合。
10.所述至少两种的组合例如dna甲基转移酶抑制剂和组蛋白去乙酰酶抑制剂的组
合、组蛋白去乙酰酶抑制剂和组蛋白甲基转移酶ezh2抑制剂的组合、dna甲基转移酶抑制剂和组蛋白甲基转移酶ezh2抑制剂的组合等,其他任意的组合方式均可。
11.本发明创造性地发现维生素c能够显著促进小分子化合物诱导t细胞重编程为类nk细胞,并能够促进细胞增殖。(而其他抗凋亡药物如q-vd-oph等对小分子化合物诱导t细胞重编程为类nk细胞的过程并无促进作用)因此将维生素c与小分子化合物进行组合,形成一种诱导t细胞重编程为类nk细胞的组合物。利用所述组合物诱导t细胞重编程为类nk细胞,显著地提高了重编程效率且促进了t细胞增殖,在细胞免疫治疗等领域具有重要的应用价值。
12.优选地,所述dna甲基转移酶抑制剂包括地西他滨和/或gsk-3484862。
13.优选地,所述组蛋白去乙酰酶抑制剂包括mocetinostat、givinostat或entinostat中的任意一种或至少两种的组合,所述至少两种的组合例如mocetinostat和givinostat的组合、givinostat和entinostat的组合、mocetinostat和entinostat的组合等,其他任意的组合方式均可。
14.优选地,所述组蛋白甲基转移酶ezh2抑制剂包括tazemetostat和/或gsk126。
15.第二方面,本发明提供一种诱导t细胞重编程为类nk细胞的方法,所述方法包括将激活的t细胞与第一方面所述的诱导t细胞重编程为类nk细胞的组合物共培养,得到类nk细胞。
16.优选地,所述维生素c的终浓度为40-60ng/ml,例如40ng/ml、42ng/ml、45ng/ml、48ng/ml、50ng/ml、52ng/ml、55ng/ml、58ng/ml、60ng/ml等。
17.优选地,所述地西他滨的终浓度为0.05-0.5μm,例如0.05μm、0.07μm、0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm等。
18.优选地,所述gsk-3484862的终浓度为0.5-8μm,例如0.5μm、0.7μm、1μm、1.5μm、2μm、2.5μm、3μm、3.5μm、4μm、4.5μm、5μm、5.5μm、6μm、6.5μm、7μm、7.5μm、8μm等。
19.优选地,所述mocetinostat的终浓度为0.1-0.5μm,例如0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm等。
20.优选地,所述givinostat的终浓度为0.05-1μm,例如0.05μm、0.07μm、0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm、0.55μm、0.6μm、0.65μm、0.7μm、0.75μm、0.8μm、0.85μm、0.9μm、0.95μm、1μm等。
21.优选地,所述entinostat的终浓度为0.05-1μm,例如0.05μm、0.07μm、0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm、0.55μm、0.6μm、0.65μm、0.7μm、0.75μm、0.8μm、0.85μm、0.9μm、0.95μm、1μm等。
22.优选地,所述tazemetostat的终浓度为0.1-5μm,例如0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm、0.7μm、1μm、1.5μm、2μm、2.5μm、3μm、3.5μm、4μm、4.5μm、5μm等。
23.优选地,所述gsk126的终浓度为0.05-1μm,例如0.05μm、0.07μm、0.1μm、0.15μm、0.2μm、0.25μm、0.3μm、0.35μm、0.4μm、0.45μm、0.5μm、0.55μm、0.6μm、0.65μm、0.7μm、0.75μm、0.8μm、0.85μm、0.9μm、0.95μm、1μm等。
24.优选地,所述共培养的时间为3-10天。
25.优选地,在所述共培养过程中,每天进行半数换液。
26.第三方面,本发明提供一种由第二方面所述的方法制备得到的类nk细胞,所述类nk细胞表达nk细胞受体和t细胞受体。
27.优选地,所述nk细胞受体包括nkp46、nkp30、nkp44或nkg2d中的任意一种或至少两种的组合,所述至少两种的组合例如nkp46和nkp30的组合、nkp44和nkg2d的组合、nkp30和nkp44的组合等,其他任意的组合方式均可。
28.优选地,所述nk细胞受体包括nkp46和/或nkp30。
29.第四方面,本发明提供如第一方面所述的诱导t细胞重编程为类nk细胞的组合物、如第二方面所述的诱导t细胞重编程为类nk细胞的方法或如第三方面所述的类nk细胞在制备细胞免疫治疗药物中的应用。
30.第五方面,本发明提供维生素c在促进小分子化合物诱导t细胞重编程为类nk细胞中的应用;
31.所述小分子化合物包括:dna甲基转移酶抑制剂、组蛋白去乙酰酶抑制剂或组蛋白甲基转移酶ezh2抑制剂中的任意一种或至少两种的组合。
32.优选地,所述dna甲基转移酶抑制剂包括地西他滨和/或gsk-3484862;
33.优选地,所述组蛋白去乙酰酶抑制剂包括mocetinostat、givinostat或entinostat中的任意一种或至少两种的组合。
34.优选地,所述组蛋白甲基转移酶抑制剂ezh2包括tazemetostat和/或gsk126。
35.优选地,所述类nk细胞表达nk细胞受体和t细胞受体。
36.优选地,所述nk细胞受体包括nkp46、nkp30、nkp44或nkg2d中的任意一种或至少两种的组合。
37.优选地,所述nk细胞受体包括nkp46和/或nkp30。
38.本发明所述的数值范围不仅包括上述列举的点值,还包括没有列举出的上述数值范围之间的任意的点值,限于篇幅及出于简明的考虑,本发明不再穷尽列举所述范围包括的具体点值。
39.相对于现有技术,本发明具有以下有益效果:
40.本发明创造性地发现维生素c能够显著促进小分子化合物诱导t细胞重编程为类nk细胞,并能够促进细胞增殖,因此将维生素c与小分子化合物进行组合,形成一种诱导t细胞重编程为类nk细胞的组合物。利用所述组合物诱导t细胞重编程为类nk细胞,显著地提高了重编程效率且促进了t细胞增殖,在细胞免疫治疗等领域具有重要的应用价值。
附图说明
41.图1a是未经小分子药物诱导的cd4 t细胞nkp30和nkp46的表达结果图。
42.图1b是添加vc的未经小分子药物诱导的cd4 t细胞nkp30和nkp46的表达结果图。
43.图1c是经dac药物诱导的cd4 t细胞中nkp30和nkp46的表达结果图。
44.图1d是经vc+dac药物诱导的cd4 t细胞中nkp30和nkp46的表达结果图。
45.图1e是经gsk3484862药物诱导的cd4 t细胞中nkp30和nkp46的表达结果图。
46.图1f是经vc+gsk3484862药物诱导的cd4 t细胞中nkp30和nkp46的表达结果图。
47.图1g是经dac+gsk3484862药物联合诱导cd4 t细胞中nkp30和nkp46的表达结果图。
48.图1h是经vc+dac+gsk3484862药物联合诱导cd4 t细胞中nkp30和nkp46的表达结果图。
49.图2a是未经小分子药物诱导的cd8 t细胞nkp30和nkp46的表达结果图。
50.图2b是添加vc的未经小分子药物诱导的cd8 t细胞nkp30和nkp46的表达结果图。
51.图2c是经dac药物诱导的cd8 t细胞中nkp30和nkp46的表达结果图。
52.图2d是经vc+dac药物诱导的cd8 t细胞中nkp30和nkp46的表达结果图。
53.图2e是经gsk3484862药物诱导的cd8 t细胞中nkp30和nkp46的表达结果图。
54.图2f是经vc+gsk3484862药物诱导的cd8 t细胞中nkp30和nkp46的表达结果图。
55.图2g是经dac+gsk3484862药物联合诱导cd8 t细胞中nkp30和nkp46的表达结果图。
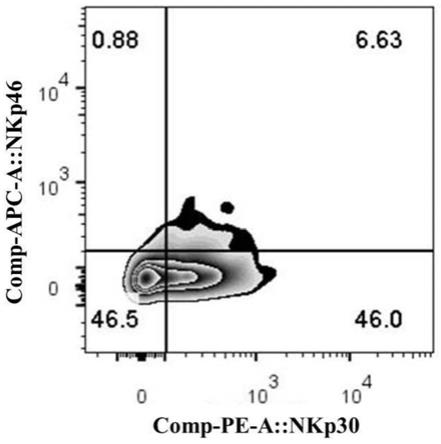
56.图2h是经vc+dac+gsk3484862药物联合诱导cd8 t细胞中nkp30和nkp46的表达结果图。
57.图3a是vc对gsk-3484862诱导t细胞重编程为类nk细胞的增殖促进结果图。
58.图3b是vc对dac诱导t细胞重编程为类nk细胞的增殖促进结果图。
59.图3c是vc对gsk-3484862+mocetinostat共同诱导t细胞重编程为类nk细胞的增殖促进结果图。
具体实施方式
60.下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
61.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
62.下述实施例所涉及的材料来源如下:
63.脐带血来自广东省脐带血造血干细胞库;
64.维生素c(vc)购自sigma-aldrich(美国)。
65.pan t细胞分离试剂盒购自stemcell technologies(加拿大);
66.transact购自德国美天旎生物技术有限公司;
67.地西他滨(decitabine,dac)购自selleck(中国,上海蓝木化工有限公司);
68.gsk-3484862、mocetinostat均购自mce(medchemexpress)公司;
69.cd3 pe-cy7、cd4 apc-cy7、cd8 fitc、nkp30 pe和nkp46 apc均购自biolegend(美国)。
70.实施例1
71.人脐血原代t细胞的分离和体外培养
72.采用ficoll-hypaque(聚蔗糖-泛影葡胺)密度梯度离心法从脐带血中分离单个核细胞(ucbmc),取4
×
107个cd3阳性ucbmc过夜培养,细胞密度为2
×
106/ml,剩余ucbmc冻存;使用pan t细胞分离试剂盒进行t细胞分选,培养一段时间获得≥4
×
107个cd3阳性t细胞,活率≥70%,无细菌、真菌、支原体等外源微生物污染。
73.实施例2
74.小分子药物诱导t细胞重编程
75.(1)取transact激活培养36小时的t细胞,300g离心5min,用t551+5%fbs+1%双抗(100
×
青霉素-链霉素混合溶液)+il2(300u)重悬t细胞并调整t细胞密度为(2~3)
×
105个/ml;
76.(2)分别向重悬的t细胞中加入各组小分子药物,各药物添加的终浓度如表1所示。每天进行半数换液,并根据换液后的体积补加新的药物;以初次加药记为day0(第0天),持续补药到day5(第5天)时,300g离心5min换液,之后采用t551+5%fbs+1%双抗(100
×
青霉素-链霉素混合溶液)继续培养。
77.表1
[0078][0079]
实施例3
[0080]
利用流式细胞术检测vc对t细胞重编程为类nk细胞表型的影响
[0081]
(1)取实施例2中表1中的各药物组诱导(即经不含vc的gsk-3484862单组分诱导后、不含vc的dac单组分诱导后,不含vc的gsk-3484862+mocetinostat共同诱导后,以及添加vc的dac诱导后、添加vc的gsk-3484862诱导后,添加vc的gsk-3484862+mocetinostat共同诱导后)day6(第6天)的t细胞、未诱导处理的t细胞以及添加50ng/ml vc的未诱导处理的t细胞各200μl,400g离心4min,弃上清后,加入50μl磷酸盐缓冲液(pbs)重悬细胞,随后分别加入cd3 pe-cy7、cd4 apc-cy7、cd8 fitc、nkp30 pe和nkp46 apc各0.5μl,4℃避光孵育30min;加入500μl pbs稀释抗体,400g离心4min,小心弃去上清,加入300μl pbs重悬细胞转移到流式管中,上机;
[0082]
(2)应用bd-flowcyto分析软件进行数据分析,每管收取10000个细胞,计算nkp46阳性t细胞与nkp30阳性t细胞的百分比。
[0083]
如图1a、图1b所示,未诱导处理组的cd4 t细胞中nkp30的表达率与添加vc的未诱导处理组的cd4 t细胞nkp30的表达率相近;如图1c、图1d所示,dac诱导组中cd4 t细胞中nkp30的表达率约为15.1%,而dac+vc组中cd4 t细胞nkp30的表达率约为22.8%;如图1e、
图1f所示,gsk3484862诱导组中cd4 t细胞中nkp30的表达率约为12.6%,而gsk3484862+vc组中cd4 t细胞nkp30的表达率约为22.9%;如图1g、图1h所示,gsk-3484862+mocetinostat共同诱导组中cd4 t细胞中nkp30的表达率约为57.3%,而gsk-3484862+mocetinostat+vc共同诱导组中cd4 t细胞nkp30的表达率约为67.6%。综上,在小分子药物中添加vc后,各组cd4 t细胞中nkp30的表达率明显有增加,充分证明了vc对小分子药物诱导t细胞重编程为nk类细胞的显著促进作用,尤其对cd4 t细胞中nkp30的表型影响更明显。
[0084]
如图2a、图2b所示,未处理组中cd8 t细胞中nkp30的表达率约为14.7%,而添加vc的未处理组中cd8 t细胞nkp30的表达率约为10.3%;如图2c、图2d所示,dac诱导组中cd8 t细胞中nkp30的表达率约为23.2%,而dac+vc组中cd8 t细胞nkp30的表达率约为47.8%,且明显开始出现nkp46的表型(从0.62%增至3.3%);如图2e、图2f所示,gsk3484862诱导组中cd8 t细胞中nkp30的表达率约为24.6%,而gsk3484862+vc组中cd8 t细胞nkp30的表达率约为36.7%,且同时开始明显的出现nkp46的表型(从0.56%增至5.6%);如图2g、图2h所示,gsk-3484862+mocetinostat共同诱导组中cd8t细胞中nkp30的表达率约为49.6%,而gsk-3484862和mocetinostat+vc共同诱导组中cd8 t细胞nkp30的表达率约为46.0%,vc的加入使其nkp30的表型表达稍微降低,但是nkp46开始出现表型(从2.51%增至6.63%)。以上结果说明,在cd8 t细胞中,vc的加入除了影响nkp30表型以外还可提升nkp46的表达。
[0085]
以上结果说明:vc本身并不能诱导t细胞重编程为类nk细胞。但vc的加入显著地促进了小分子化合物诱导t细胞重编程为类nk细胞。
[0086]
实施例4
[0087]
绘制细胞增殖曲线
[0088]
取dac诱导、gsk-3484862诱导、gsk-3484862+mocetinostat共同诱导、dac+vc诱导、gsk-3484862+vc诱导、以及gsk-3484862+mocetinostat+vc共同诱导2、4、6、10天的t细胞以及未处理的t细胞各10μl,分别与苔盼蓝10μl以1:1比例混合进行计数,绘制细胞增殖曲线。
[0089]
结果如图3a、图3b、图3c所示,加入vc后,细胞增殖速度显著加快,说明vc明显促进了小分子化合物诱导t细胞重编程为类nk细胞的增殖。
[0090]
申请人声明,本发明通过上述实施例来说明本发明的一种诱导t细胞重编程为类nk细胞的组合物及其应用,但本发明并不局限于上述实施例,即不意味着本发明必须依赖上述实施例才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
[0091]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0092]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1