一种两性离子修饰的多糖类聚合物及其制备方法与应用与流程
1.本发明属于高分子材料技术领域,具体涉及一种两性离子修饰的多糖类聚合物及其制备方法与应用。
背景技术:
2.相关技术中,传统的植入材料如海藻酸盐,因其具有低免疫原性,良好的生物相容性,可控降解而作为植入材料被广泛应用于免疫隔离工具上。然而,异物反应(fbr)是一个复杂的过程,主要来自细胞过度生长(co)和纤维化,涉及蛋白质吸附、单核细胞/粒细胞/巨噬细胞粘附、巨细胞形成以及巨噬细胞/巨细胞与其它免疫/成纤维细胞之间的串扰,仅凭单一的聚合物材料,如海藻酸盐材料等,很难做到抑制植入装置上的细胞过度生长(co)和纤维化,出现减少甚至切断营养物质和氧气向包裹细胞的扩散,从而导致细胞凋亡/坏死现象。因此,传统的植入材料如海藻酸盐的抑制异物反应性能较弱,存在更佳植入材料的临床需求。
技术实现要素:
3.本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种两性离子修饰的多糖类聚合物,具有抑制异物反应性能较强的特点。
4.本发明还提出上述两性离子修饰的多糖类聚合物的制备方法。
5.本发明还提出一种水凝胶。
6.本发明还提出一种生物材料。
7.本发明还提出一种医疗产品。
8.本发明还提出上述两性离子修饰的多糖类聚合物的应用。
9.本发明的第一方面,提出了一种两性离子修饰的多糖类聚合物,所述两性离子修饰的多糖类聚合物上含有含氮杂环阳离子基团,所述两性离子修饰的多糖类聚合物是由含氮杂环两性离子通过酰胺化反应接枝于多糖类聚合物上制备得到。
10.根据本发明实施例的两性离子修饰的多糖类聚合物,至少具有以下有益效果:本发明中的两性离子修饰的多糖类聚合物,可通过含氮杂环阳离子基团的离子溶剂化与水分子发生强相互作用,能够最大限度地减少对蛋白质和细胞的非特异性吸附,并抑制异物反应和炎症,效果明显优于常规的植入材料,如聚(甲基丙烯酸2-羟乙酯)(phema)、peg及其衍生物、海藻酸盐等,抑制异物反应性能强。
11.在本发明的一些实施方式中,所述含氮杂环阳离子基团包括含氮五元环类阳离子基团、含氮六元环类阳离子基团或含氮稠环类阳离子基团中的至少一种,所述含氮杂环两性离子包括含氮五元环类两性离子、含氮六元环类两性离子或含氮稠环类两性离子。
12.在本发明的一些优选的实施方式中,所述含氮杂环阳离子基团包括咪唑鎓阳离子基团、吡咯鎓阳离子基团、噻唑鎓阳离子基团、吡啶鎓阳离子基团、吡嗪鎓阳离子基团、嘧啶鎓阳离子基团、哒嗪鎓阳离子基团、吲哚鎓阳离子基团、喹啉鎓阳离子基团、蝶啶鎓阳离子
基团、吖啶鎓阳离子基团、三氮唑鎓阳离子基团、苯并咪唑鎓阳离子基团、苯并噻唑鎓阳离子基团、苯并三唑阳离子基团、喹喔啉鎓阳离子基团、喹唑啉鎓阳离子基团、苯并哒嗪鎓阳离子基团或吡咯并嘧啶鎓阳离子基团中的至少一种,所述含氮杂环两性离子包括咪唑鎓两性离子、吡咯鎓两性离子、噻唑鎓两性离子、吡啶鎓两性离子、吡嗪鎓两性离子、嘧啶鎓两性离子、哒嗪鎓两性离子、吲哚鎓两性离子、喹啉鎓两性离子、蝶啶鎓两性离子、吖啶鎓两性离子、三氮唑鎓两性离子、苯并咪唑鎓两性离子、苯并噻唑鎓两性离子、苯并三唑鎓两性离子、喹喔啉鎓两性离子、喹唑啉鎓两性离子、苯并哒嗪鎓两性离子或吡咯并嘧啶鎓两性离子中的至少一种。
13.通过上述实施方式,本发明中两性离子修饰的多糖类聚合物含有杂环鎓类阳离子基团,通过p-π轨道共轭效应将所带正电荷均匀地分散在五元环、六元环或多稠环上以及通过有效地能量耗散机制,形成高稳定性的鎓类两性离子,不会因正电荷脱落导致失去两性离子的防纤维化、抗排斥功能,作为植入材料可在体内复杂的环境中保持稳定性。
14.在本发明的一些优选的实施方式中,所述含氮杂环阳离子基团为咪唑鎓阳离子基团,所述含氮杂环两性离子为咪唑鎓两性离子。
15.通过上述实施方式,本发明中的两性离子修饰的多糖类聚合物,可通过咪唑鎓阳离子基团的离子溶剂化与水分子发生强相互作用,能够最大限度地减少对蛋白质和细胞的非特异性吸附,并抑制异物反应和炎症,效果明显优于常规的植入材料,如聚(甲基丙烯酸2-羟乙酯)(phema)、peg及其衍生物、海藻酸盐等,抑制异物反应性能强。
16.同时,本发明中两性离子修饰的多糖类聚合物含有咪唑鎓阳离子基团(含咪唑五元杂环),通过p-π轨道共轭效应将所带正电荷均匀地分散在五元环上以及通过有效地能量耗散机制,形成高稳定性的咪唑鎓两性离子,不会因正电荷脱落导致失去两性离子的防纤维化、抗排斥功能,作为植入材料可在体内复杂的环境中保持稳定性。本发明将咪唑鎓两性离子通过酰胺化反应接枝至多糖类聚合物上,得到一种具有良好的生物相容性、低异物反应性特点的新材料,可用作植入材料长期稳定存在于体内,应用前景好。
17.在本发明的一些优选的实施方式中,所述咪唑鎓两性离子含有氨基,所述多糖类聚合物含有羧基或羧酸盐基团,所述羧基或所述羧酸盐基团与所述氨基发生酰胺化反应。
18.在本发明的一些更优选的实施方式中,所述咪唑鎓两性离子含有氨基,所述多糖类聚合物的结构单元上含有羧基或羧酸盐基团,所述羧基或所述羧酸盐基团与所述氨基发生酰胺化反应。
19.在本发明的一些优选的实施方式中,所述多糖类聚合物包括海藻酸盐、透明质酸、羧甲基纤维素、羧甲基变性半纤维素、羧甲基壳聚糖、羧甲基葡聚糖、羧甲基卡拉胶、羧甲基茯苓多糖、羧甲基淀粉、果胶或肝素中的至少一种。
20.在本发明的一些更优选的实施方式中,所述海藻酸盐包括海藻酸钠。
21.其中,海藻酸钠,简称为:naalg。
22.在本发明的一些优选的实施方式中,所述咪唑鎓两性离子包括磺酸甜菜碱、羧酸甜菜碱或磷酰胆碱中的至少一种。
23.在本发明的一些更优选的实施方式中,所述咪唑鎓两性离子包括1-(3-氨基丙基)咪唑磺酸甜菜碱、1-(3-氨基丙基)咪唑乙酸甜菜碱或1-(3-氨基丙基)咪唑丁酸甜菜碱中的至少一种。
24.在本发明的一些优选的实施方式中,所述两性离子修饰的多糖类聚合物包括磺酸甜菜碱类物质、羧酸甜菜碱类物质或磷酰胆碱类物质中的至少一种。
25.在本发明的一些优选的实施方式中,所述两性离子修饰的多糖类聚合物为两性离子修饰海藻酸盐。
26.在本发明的一些优选的实施方式中,所述两性离子修饰的多糖类聚合物包括式(1)聚合物、式(2)聚合物或式(3)聚合物中的至少一种:
[0027][0028][0029]
其中,式(1)聚合物为1-(3-氨基丙基)咪唑磺酸甜菜碱改性海藻酸钠,简称为:sb-alg;式(2)聚合物为1-(3-氨基丙基)咪唑乙酸甜菜碱改性海藻酸钠,简称为:cb
1-alg;式(3)聚合物为1-(3-氨基丙基)咪唑丁酸甜菜碱改性海藻酸钠,简称为:cb
2-alg。
[0030]
在本发明的一些实施方式中,所述两性离子修饰的多糖类聚合物包括光敏基团。
[0031]
通过上述实施方式,两性离子修饰的多糖类聚合物包括光敏基团,可使两性离子修饰的多糖类聚合物发生光聚合或光交联反应,得到相应的生物材料,从而更好地应用于生物材料或药物技术领域中。
[0032]
在本发明的一些优选的实施方式中,所述两性离子修饰的多糖类聚合物包括式(4)聚合物、式(5)聚合物或式(6)聚合物中的至少一种:
[0033][0034]
式(4)聚合物为甲基丙烯酰化1-(3-氨基丙基)咪唑磺酸甜菜碱改性海藻酸钠,简称为sb-alg-ma;式(5)聚合物为甲基丙烯酰化1-(3-氨基丙基)咪唑乙酸甜菜碱改性海藻酸钠,简称为cb
1-alg-ma;式(6)聚合物为甲基丙烯酰化1-(3-氨基丙基)咪唑丁酸甜菜碱改性海藻酸钠,简称为cb
2-alg-ma。
[0035]
本发明的第二方面,提出了一种两性离子修饰的多糖类聚合物的制备方法,包括如下步骤:含氮杂环两性离子通过酰胺化反应接枝于多糖类聚合物上制备得到所述两性离子修饰的多糖类聚合物,所述两性离子修饰的多糖类聚合物上含有含氮杂环阳离子基团。
[0036]
在本发明的一些实施方式中,所述含氮杂环阳离子基团为咪唑鎓阳离子基团,所述含氮杂环两性离子为咪唑鎓两性离子,所述两性离子修饰的多糖类聚合物的制备方法包括如下步骤:
[0037]
sa-1,将海藻酸钠的溶液ⅰ和咪唑鎓两性离子的溶液ⅰ混合,加热反应后,除去溶剂,得到混合物ⅰ;
[0038]
sa-2,将混合物ⅰ与水混合后,调节ph至中性,透析后,沉析,分离。
[0039]
在本发明的一些优选的实施方式中,在步骤sa-1中,向海藻酸钠与水、乙腈的混合溶液中加入2-氯-4,6-二甲氧基-1,3,5-三嗪、n-甲基吗啉,得到所述海藻酸钠的溶液ⅰ。
[0040]
在本发明的一些更优选的实施方式中,在步骤sa-1中,海藻酸钠、2-氯-4,6-二甲氧基-1,3,5-三嗪和n-甲基吗啉的摩尔比为(4.9-5.1):(2.4-2.6):(4.9-5.1)。
[0041]
在本发明的一些更优选的实施方式中,在步骤sa-1中,海藻酸钠、2-氯-4,6-二甲氧基-1,3,5-三嗪和n-甲基吗啉的摩尔比约为5.04:2.56:5.04。
[0042]
在本发明的一些优选的实施方式中,在步骤sa-1中,海藻酸钠与咪唑鎓两性离子
的摩尔比为1:(1-2)。
[0043]
在本发明的一些优选的实施方式中,在步骤sa-1中,所述加热反应的条件为55-60℃下反应24h。
[0044]
在本发明的一些优选的实施方式中,在步骤sa-1中,除去溶剂的方式为减压浓缩。
[0045]
在本发明的一些优选的实施方式中,在步骤sa-2中,使用1mol/l的naoh水溶液调节ph至中性。
[0046]
在本发明的一些优选的实施方式中,在步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,用水透析后,再用甲醇进行沉析,离心,得到所述两性离子修饰的多糖类聚合物。
[0047]
在本发明的一些更优选的实施方式中,在步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,用水透析3d,再用无水甲醇沉析,离心,所述沉析和离心的步骤重复3次,约40℃真空干燥48h。
[0048]
在本发明的一些优选的实施方式中,步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐发生亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物;
[0049]
在本发明的一些更优选的实施方式中,步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐发生羟基与酸酐的亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0050]
在本发明的一些更优选的实施方式中,步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐于碱性环境下发生羟基与酸酐的亲核取代反应,室温下反应24h,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0051]
在本发明的一些更优选的实施方式中,步骤sa-2中,将混合物ⅰ与水混合后,调节ph至中性,透析,沉析分离后,得到产物ⅰ,所述产物ⅰ的羟基与甲基丙烯酸酐反应发生亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0052]
在本发明的一些实施方式中,所述制备方法包括如下步骤:
[0053]
sb-1,将海藻酸钠的溶液ⅱ和咪唑鎓两性离子的溶液ⅱ混合,反应后,粗纯化,得到混合物ⅱ;
[0054]
sb-2,将混合物ⅱ与水混合后,调节ph至中性,透析后,沉析,分离。
[0055]
在本发明的一些优选的实施方式中,在步骤sb-1中,海藻酸钠与mes缓冲液的混合溶液,经活化后,得到所述海藻酸钠的溶液ⅱ。
[0056]
在本发明的一些优选的实施方式中,在步骤sb-1中,向海藻酸钠与mes缓冲液的混合溶液中加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐、n-羟基琥珀酰亚胺,活化,得到所述海藻酸钠的溶液ⅱ。
[0057]
其中,1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐,简写为:edc
·
hcl;n-羟基琥珀酰亚胺,简写为:nhs。
[0058]
在本发明的一些更优选的实施方式中,mes缓冲液中溶质浓度为0.1mol/l,ph为6。
[0059]
在本发明的一些更优选的实施方式中,在步骤sb-1中,海藻酸钠、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐和n-羟基琥珀酰亚胺的摩尔比为1:(0.9-1.1):(0.9-1.1)。
[0060]
在本发明的一些优选的实施方式中,在步骤sb-1中,海藻酸钠与咪唑鎓两性离子的摩尔比为1:(1-2)。
[0061]
在本发明的一些优选的实施方式中,在步骤sb-1中,所述反应条件为室温反应24h。
[0062]
在本发明的一些优选的实施方式中,在步骤sb-1中,所述粗提纯的方式为使用无水甲醇进行粗提纯。
[0063]
在本发明的一些优选的实施方式中,在步骤sb-2中,使用1mol/l的naoh水溶液调节ph至中性。
[0064]
在本发明的一些优选的实施方式中,在步骤sb-2中,将混合物ⅱ与水混合后,调节ph至中性,用水透析后,再用甲醇进行沉析,离心,得到所述两性离子修饰的多糖类聚合物。
[0065]
在本发明的一些更优选的实施方式中,在步骤sb-2中,用水透析3d,再用无水甲醇沉析,离心,所述沉析和离心的步骤重复3次,约40℃真空干燥48h。
[0066]
在本发明的一些优选的实施方式中,步骤sb-2中,将混合物ⅱ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐发生亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0067]
在本发明的一些更优选的实施方式中,步骤sb-2中,将混合物ⅱ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐发生羟基与酸酐的亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0068]
在本发明的一些更优选的实施方式中,步骤sb-2中,将混合物ⅱ与水混合后,调节ph至中性,透析,沉析分离后,与甲基丙烯酸酐于碱性环境下发生羟基与酸酐的亲核取代反应,室温下反应24h,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0069]
在本发明的一些更优选的实施方式中,步骤sb-2中,将混合物ⅱ与水混合后,调节ph至中性,透析,沉析分离后,得到产物ⅱ,所述产物ⅱ的羟基与甲基丙烯酸酐反应发生亲核取代反应,再透析纯化,得到所述两性离子修饰的多糖类聚合物。
[0070]
在本发明的一些实施方式中,所述咪唑鎓两性离子包括1-(3-氨基丙基)咪唑磺酸甜菜碱,所述1-(3-氨基丙基)咪唑磺酸甜菜碱的制备方法,包括如下步骤:
[0071]
s-1-1,将1-[3-(n-boc-氨基)丙基]咪唑与1,3-丙磺酸内酯反应,制备得到1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱;
[0072]
s-1-2,1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱水解后,得到1-(3-氨基丙基)咪唑磺酸甜菜碱。
[0073]
1-[3-(n-boc-氨基)丙基]咪唑,简称:n-boc-丙胺咪唑。
[0074]
1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱,简称为:n-boc-丙胺咪唑磺酸甜菜碱。
[0075]
其中1-(3-氨基丙基)咪唑磺酸甜菜碱的制备如下反应式所示:
[0076][0077]
在本发明的一些优选的实施方式中,在步骤s-1-1中,将1-[3-(n-boc-氨基)丙基]咪唑、3-丙磺酸内酯的四氢呋喃混合液,加热反应,得到粘稠状液体,用四氢呋喃洗涤后,过滤,得到所述1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱。
[0078]
在本发明的一些优选的实施方式中,在步骤s-1-1中,1-[3-(n-boc-氨基)丙基]咪唑与3-丙磺酸内酯的摩尔比为(0.9-1.1):(0.9-1.1)。
[0079]
在本发明的一些更优选的实施方式中,在步骤s-1-1中,1-[3-(n-boc-氨基)丙基]咪唑、3-丙磺酸内酯的四氢呋喃混合液,于约室温下搅拌反应48h,得到白色粘稠状液体,用四氢呋喃洗涤后,过滤,于约40℃真空干燥48h,得到所述1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱。
[0080]
在本发明的一些优选的实施方式中,在步骤s-1-2中,1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱的氯化氢甲醇溶液于室温下反应,用离子交换树脂进行酸碱中和后,过滤,除去溶剂,洗涤。
[0081]
在本发明的一些更优选的实施方式中,在步骤s-1-2中,1-[3-(n-boc-氨基)丙基]咪唑磺酸甜菜碱的氯化氢甲醇溶液于室温下反应,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂进行酸碱中和,然后进行过滤,真空浓缩除去溶剂,再用乙醚进行洗涤。再进行浓缩,干燥。
[0082]
在本发明的一些实施方式中,所述咪唑鎓两性离子包括1-(3-氨基丙基)咪唑乙酸甜菜碱,所述1-(3-氨基丙基)咪唑乙酸甜菜碱的制备方法,包括如下步骤:
[0083]
s-2-1-1,将1-[3-(n-boc-氨基)丙基]咪唑与溴乙酸叔丁酯反应,制备得到1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅰ;
[0084]
s-2-1-2,1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅰ水解后,得到1-(3-氨基丙基)咪唑乙酸甜菜碱。
[0085]
1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅰ,简称为:n-boc-丙胺咪唑乙酸甜菜碱ⅰ。
[0086]
其中1-(3-氨基丙基)咪唑乙酸甜菜碱的制备如下反应式所示:
[0087][0088]
在本发明的一些优选的实施方式中,在步骤s-2-1-1中,1-[3-(n-boc-氨基)丙基]咪唑、溴乙酸叔丁酯的乙腈混合液,经加热反应,浓缩反应液,沉淀,洗涤和过滤后,得到所述1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅰ。
[0089]
在本发明的一些优选的实施方式中,在步骤s-2-1-1中,1-[3-(n-boc-氨基)丙基]咪唑与溴乙酸叔丁酯的摩尔比为(0.9-1.1):(0.9-1.1)。
[0090]
在本发明的一些更优选的实施方式中,在步骤s-2-1-1中,1-[3-(n-boc-氨基)丙基]咪唑、溴乙酸叔丁酯的乙腈混合液,于约40℃下搅拌反应2d,浓缩反应液,加入无水乙醚沉淀、洗涤,过滤,真空干燥得到所述1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱。
[0091]
在本发明的一些优选的实施方式中,在步骤s-2-1-2中,1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅰ的氯化氢甲醇溶液于室温下反应,用离子交换树脂进行酸碱中和后,过滤,除去溶剂,洗涤。
[0092]
在本发明的一些更优选的实施方式中,在步骤s-2-1-2中,1-[3-(n-boc-氨基)丙
基]咪唑乙酸甜菜碱ⅰ的氯化氢甲醇溶液于室温下反应,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂进行酸碱中和,然后进行过滤,真空浓缩除去溶剂,再用乙醚进行洗涤。最后,将滤液进行浓缩,干燥。
[0093]
在本发明的一些实施方式中,所述咪唑鎓两性离子包括1-(3-氨基丙基)咪唑乙酸甜菜碱,所述1-(3-氨基丙基)咪唑乙酸甜菜碱的制备方法,包括如下步骤:
[0094]
s-2-2-1,将1-[3-(n-boc-氨基)丙基]咪唑与溴乙酸乙酯反应,制备得到1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅱ;
[0095]
s-2-2-2,1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅱ水解后,得到1-(3-氨基丙基)咪唑乙酸甜菜碱。
[0096]
1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅱ,简称为:n-boc-丙胺咪唑乙酸甜菜碱ⅱ。
[0097]
其中1-(3-氨基丙基)咪唑乙酸甜菜碱的制备如下反应式所示:
[0098][0099]
在本发明的一些优选的实施方式中,在步骤s-2-2-1中,1-[3-(n-boc-氨基)丙基]咪唑、溴乙酸乙酯的乙腈混合液,经加热反应,浓缩反应液,洗涤,得到所述1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅱ。
[0100]
在本发明的一些优选的实施方式中,在步骤s-2-2-1中,1-[3-(n-boc-氨基)丙基]咪唑与溴乙酸乙酯的摩尔比为(1.5-1.7):(1.8-2.0)。
[0101]
在本发明的一些优选的实施方式中,在步骤s-2-2-2中,1-[3-(n-boc-氨基)丙基]咪唑乙酸甜菜碱ⅱ的氯化氢甲醇溶液于室温下反应,用离子交换树脂进行酸碱中和后,过滤,除去溶剂,洗涤。
[0102]
在本发明的一些实施方式中,所述咪唑鎓两性离子包括1-(3-氨基丙基)咪唑丁酸甜菜碱,所述1-(3-氨基丙基)咪唑丁酸甜菜碱的制备方法,包括如下步骤:
[0103]
s-3-1,将1-[3-(n-boc-氨基)丙基]咪唑与4-溴丁酸乙酯反应,制备得到1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱;
[0104]
s-3-2,1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱水解后,得到1-(3-氨基丙基)咪唑丁酸甜菜碱。
[0105]
1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱,简称为:n-boc-丙胺咪唑丁酸甜菜碱。
[0106]
其中1-(3-氨基丙基)咪唑丁酸甜菜碱的制备如下反应式所示:
[0107][0108]
在本发明的一些优选的实施方式中,在步骤s-3-1中,1-[3-(n-boc-氨基)丙基]咪
唑、4-溴丁酸乙酯的乙腈混合液,经加热反应,浓缩反应液,洗涤及浓缩后,得到所述1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱。
[0109]
在本发明的一些优选的实施方式中,在步骤s-3-1中,1-[3-(n-boc-氨基)丙基]咪唑与4-溴丁酸乙酯的摩尔比为(0.9-1.1):(1-1.4)。
[0110]
在本发明的一些更优选的实施方式中,在步骤s-3-1中,1-[3-(n-boc-氨基)丙基]咪唑、4-溴丁酸乙酯的乙腈混合液,于约45℃下搅拌反应5d,浓缩反应液,加入无水乙醚洗涤,真空浓缩得到所述1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱。
[0111]
在本发明的一些优选的实施方式中,在步骤s-3-2中,1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱的氯化氢甲醇溶液于室温下反应,用离子交换树脂进行酸碱中和后,过滤,除去溶剂,洗涤。
[0112]
在本发明的一些更优选的实施方式中,在步骤s-3-2中,1-[3-(n-boc-氨基)丙基]咪唑丁酸甜菜碱的氯化氢甲醇溶液于室温下反应,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂进行酸碱中和,然后进行过滤,真空浓缩除去溶剂,再用乙醚进行洗涤。最后,将滤液进行浓缩,干燥。
[0113]
本发明的第三方面,提出了一种水凝胶,所述水凝胶的原料包括上述含有光敏基团的两性离子修饰的多糖类聚合物,所述两性离子修饰的多糖类聚合物通过光交联反应得到所述水凝胶。
[0114]
在本发明的一些实施方式中,所述水凝胶的原料还包括pegda,所述两性离子修饰的多糖类聚合物与所述pegda通过光交联反应得到所述水凝胶。
[0115]
本发明的第四方面,提出了一种生物材料,所述生物材料的原料包括上述两性离子修饰的多糖类聚合物。
[0116]
在本发明的一些实施方式中,所述生物材料的制备方法包括步骤:由含有双键的所述两性离子修饰的多糖类聚合物发生自光交联或者与pegda光交联制备得到。
[0117]
在本发明的一些实施方式中,所述生物材料为一种植入材料,所述植入材料的原料包括上述两性离子修饰的多糖类聚合物。
[0118]
本发明的第五方面,提出了一种医疗产品,包括上述两性离子修饰的多糖类聚合物或上述水凝胶中的至少一种。
[0119]
在本发明的一些实施方式中,所述医疗产品包括医疗器械或药物中的至少一种。
[0120]
本发明的第六方面,提出了上述两性离子修饰的多糖类聚合物或水凝胶在制备生物材料或医疗产品中的应用。
[0121]
在本发明的一些实施方式中,提出了上述两性离子修饰的多糖类聚合物或水凝胶在医疗器械的涂层、药物的包裹或生物墨水中的应用。
[0122]
本发明中两性离子修饰的多糖类聚合物是由含氮杂环两性离子通过酰胺化反应接枝于多糖类聚合物上制备得到,可通过含氮杂环阳离子基团的离子溶剂化与水分子发生强相互作用,能够最大限度地减少对蛋白质和细胞的非特异性吸附,并抑制异物反应和炎症,效果明显优于常规的植入材料,抑制异物反应性能强。
[0123]
进一步地,本发明中两性离子修饰的多糖类聚合物含有杂环鎓类阳离子基团,如含氮五元环类阳离子基团、含氮六元环类阳离子基团或含氮稠环类阳离子基团(具体如咪唑鎓阳离子基团),通过p-π轨道共轭效应将所带正电荷均匀地分散在五元环、六元环或多
稠环上以及通过有效的能量耗散机制,形成高稳定性的鎓类两性离子,不会因正电荷脱落导致失去两性离子的防纤维化、抗排斥功能,作为植入材料可在体内复杂的环境中保持稳定性。
[0124]
进一步地,两性离子修饰的多糖类聚合物包括光敏基团,可使两性离子修饰的多糖类聚合物发生光聚合或光交联反应,得到相应的生物材料,从而更好地应用于生物材料或药物技术领域中。
[0125]
本发明提出的生物材料,其原料包括所述两性离子修饰的多糖类聚合物。其制备方法包括步骤:由含有双键的所述两性离子修饰的多糖类聚合物发生自光交联或者与pegda光交联制备得到。从而将两性离子修饰的多糖类聚合物更好地应用于生物材料技术领域中。
附图说明
[0126]
下面结合附图和实施例对本发明做进一步的说明,其中:
[0127]
图1为本发明实施例1中n-boc-丙胺咪唑的1hnmr谱图;
[0128]
图2为本发明实施例1中n-boc-丙胺咪唑磺酸甜菜碱的1hnmr谱图;
[0129]
图3为本发明实施例1中1-(3-氨基丙基)咪唑磺酸甜菜碱的1hnmr谱图;
[0130]
图4为本发明实施例1中1-(3-氨基丙基)咪唑磺酸甜菜碱的ms谱图;
[0131]
图5为本发明实施例1中sb-alg的1hnmr谱图;
[0132]
图6为本发明实施例2中n-boc-丙胺咪唑乙酸甜菜碱ⅰ的1hnmr谱图;
[0133]
图7为本发明实施例2中1-(3-氨基丙基)咪唑乙酸甜菜碱的1hnmr谱图;
[0134]
图8为本发明实施例2中1-(3-氨基丙基)咪唑乙酸甜菜碱的ms谱图;
[0135]
图9为本发明实施例2中cb
1-alg的1hnmr谱图;
[0136]
图10为本发明实施例3中n-boc-丙胺咪唑乙酸甜菜碱ⅱ的1hnmr谱图;
[0137]
图11为本发明实施例4中n-boc-丙胺咪唑丁酸甜菜碱的1hnmr谱图;
[0138]
图12为本发明实施例4中1-(3-氨基丙基)咪唑丁酸甜菜碱的1hnmr谱图;
[0139]
图13为本发明实施例4中1-(3-氨基丙基)咪唑丁酸甜菜碱的ms谱图;
[0140]
图14为本发明实施例4中cb
2-alg的1hnmr谱图;
[0141]
图15为本发明实施例采用的naalg的1hnmr谱图;
[0142]
图16为本发明试验例测得的bsa标准曲线图;
[0143]
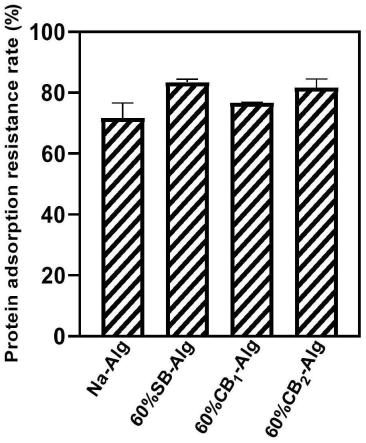
图17为本发明试验例中sb-alg,cb
1-alg,cb
2-alg蛋白吸附含量测试结果图;
[0144]
图18为本发明试验例中sb-alg,cb
1-alg,cb
2-alg,sb-alg-ma,cb
1-alg-ma细胞毒性测试结果图;
[0145]
图19为本发明实施例5中sb-alg-ma的1hnmr谱图;
[0146]
图20为本发明实施例6中cb
1-alg-ma的1hnmr谱图;
[0147]
图21为本发明实施例5和6制备得到的sb-alg-ma自交联水凝胶/cb
1-alg-ma自交联水凝胶/sb-alg-ma-pegda水凝胶/cb
1-alg-ma-pegda水凝胶图。
具体实施方式
[0148]
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以
充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其它实施例,均属于本发明保护的范围。
[0149]
本发明合成1-[3-(n-boc-氨基)丙基]咪唑(即:n-boc-丙胺咪唑),包括如下步骤:
[0150]
将二碳酸二叔丁酯(10.9g,50mmol)溶解在50ml四氢呋喃中并冷却至0℃。然后将1-(3-氨基丙基)咪唑(5.75g,46mmol)溶解在20ml 1mol/ml naoh溶液中并在0℃条件下缓慢滴加至上述溶液,滴加完毕后,恢复至室温并将溶液搅拌15h。最后蒸发浓缩去除溶剂,得到油状粗产物并将其重新溶于乙酸乙酯,再用去离子水水洗3-5次。有机相再用无水mgso4干燥2-3h,并过滤除去mgso4结晶水合物,最后浓缩除去乙酸乙酯,得到淡黄色粘性液体,产率约75%。该步骤的反应如下所示:
[0151][0152]
其1hnmr谱图如图1所示,结构解析如下:
[0153]1hnmr(400mhz,cdcl3),δ(ppm):
[0154]
7.49(s,1h),7.05(s,1h),6.94(s,1h),4.86(bs,nh),3.98-4.01(t,2h),3.11-3.16(m,2h),1.94-1.99(q,2h),1.45(s,9h)。
[0155]
合成方法参考文献:weiss e,gertopski d,gupta m k,et al.encapsulation of ionic liquid bmim[pf6]within polyurea microspheres[j].reactive&functional polymers,2015,96(nov.):32-38.
[0156]
实施例1
[0157]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(1)聚合物,其制备过程包括:
[0158]
(ⅰ)n-boc-丙胺咪唑磺酸甜菜碱的制备:
[0159]
称取(5.4g,24mmol)n-boc-丙胺咪唑和(2.93g,24mmol)1,3-丙磺酸内酯溶解在35ml四氢呋喃中,然后在室温下搅拌反应48h。48h后底部出现白色粘稠状液体。最后,用四氢呋喃进行洗涤3-5次,并进行过滤,最后在40℃真空干燥48h,得到纯的白色粉末产物,产率约97.7%。该步骤的反应如下所示:
[0160][0161]
其1hnmr谱图如图2所示,结构解析如下:
[0162]1hnmr(400mhz,d2o),δ(ppm):
[0163]
8.87(s,1h),7.55-7.60(d,2h),4.38-4.41(t,2h),4.26-4.29(t,2h),3.12-3.16(t,2h),2.93-2.97(t,2h),2.35-2.39(m,2h),2.06-2.11(m,2h),1.43(s,9h)。
[0164]
(ⅱ)1-(3-氨基丙基)咪唑磺酸甜菜碱(简称:sb-nh2)的制备:
[0165]
将5g n-boc-丙胺咪唑磺酸甜菜碱溶于50ml 1.25mol/l hcl的甲醇溶液。然后将溶液在室温下搅拌过夜。最后,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂(oh-)进行酸碱中和,然后依次进行过滤,真空浓缩除去甲醇溶剂,再用乙醚对粗产物进行洗涤。最后,将乙醚倒掉再将纯化后的粘稠状产物进行浓缩,干燥。该步骤的反应如下所示,其中引入了磺酸基,磺酸基具有优良的生物相容性,并引入氨基,为下一步酰胺化反应提供反应基团:
[0166][0167]
其1hnmr谱图如图3所示,结构解析如下:
[0168]1hnmr(400mhz,d2o),δ(ppm):
[0169]
8.89(s,1h),7.56-7.59(d,2h),4.32-4.39(m,4h),3.04-3.08(t,2h),2.90-2.94(t,2h),2.24-2.35(m,2h)。
[0170]
其ms谱图如图4所示,解析如下:
[0171]
[m+h]=248,[2m+h]=495,这和m
(sb-nh2)
=247的理论值相对应。
[0172]
(ⅲ)合成式(1)聚合物,1-(3-氨基丙基)咪唑磺酸甜菜碱改性海藻酸钠(sb-alg):
[0173]
将1g(5.04mmol)海藻酸钠溶于80ml去离子水和20ml乙腈混合溶剂中。然后加入450mg(2.56mmol)2-氯-4,6-二甲氧基-1,3,5-三嗪和560μl(5.04mmol)n-甲基吗啉。随后将1.254g(5.04mmol)1-(3-氨基丙基)咪唑磺酸甜菜碱溶解在20ml去离子水中,并添加到上述混合溶液中。在55-60℃下反应24h。最后,减压浓缩除去溶剂并将其重新溶解在去离子水中,并用1mol/l naoh溶液将ph调至中性。然后用去离子水进行透析3d,再用无水甲醇沉析,离心,并重复3次,40℃真空干燥48h。
[0174]
该步骤的反应如下所示:
[0175][0176]
其中,由sb-nh2制备sb-alg,还可以通过如下步骤制备得到:
[0177]
将1g(5.04mmol)海藻酸钠溶于100ml ph=6.0,0.1mol/l mes缓冲液溶液中。然后加入0.97g(5.04mmol)1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc
·
hcl)和0.582g(5.04mmol)n-羟基琥珀酰亚胺(nhs),活化15min,随后将1.254g(5.04mmol)1-(3-氨基丙基)咪唑磺酸甜菜碱溶解在6ml ph=6.0,0.1mol/l mes缓冲液溶液中,并添加到上述混合溶液中。室温下反应24h。然后用无水甲醇进行粗纯化。最后,进行分离,重新用去离子水溶解,并用1mol/l naoh溶液调至中性,然后进行透析3d,再用无水甲醇沉析,离心,并重复3次,40℃真空干燥48h。
[0178]
其1hnmr谱图如图5所示,结构解析如下:
[0179]1hnmr(400mhz,d2o),δ(ppm):
[0180]
8.91(s,1h),7.58-7.60(d,2h),4.35-4.40(t,2h),4.26(t,2h),3.78
–
4.04(m,naalg上的h),3.35(t,2h),3.05-3.09(t,2h),2.92-2.97(t,2h),2.28-2.36(t,2h)。
[0181]
本实施例提供了一种生物材料,其原料包括本实施例制备得到的两性离子修饰的多糖类聚合物。
[0182]
本实施例提供了一种医疗器械,包括本实施例制备得到的两性离子修饰的多糖类聚合物。
[0183]
本实施例提供了一种药物,包括本实施例制备得到的两性离子修饰的多糖类聚合物。
[0184]
实施例2
[0185]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(2)聚合物,其制备过程包括:
[0186]
(ⅰ)n-boc-丙胺咪唑乙酸甜菜碱ⅰ的制备:
[0187]
称取(4.5g,20mmol)n-boc-丙胺咪唑和(3.90g,20mmol)溴乙酸叔丁酯溶解在75ml乙腈中,然后在40℃下搅拌反应2d。最后,对反应液进行浓缩大部分溶剂后加入无水乙醚进行沉淀并洗涤3-5次,然后依次进行过滤,真空干燥得到白色粉末产物,产率约82%。该步骤的反应如下所示:
[0188][0189]
其1hnmr谱图如图6所示,结构解析如下:
[0190]1hnmr(400mhz,d2o),δ(ppm):
[0191]
8.92(s,1h),7.56-7.62(d,2h),5.10(s,2h),4.31-4.35(t,2h),3.14-3.16(t,2h),2.09-2.16(m,2h),1.45-1.51(d,18h)。
[0192]
(ⅱ)1-(3-氨基丙基)咪唑乙酸甜菜碱(简称:cb
1-nh2)的制备:
[0193]
将5g n-boc-丙胺咪唑乙酸甜菜碱ⅰ溶于100ml 1.25mol/l hcl的甲醇溶液。然后将溶液在室温下搅拌过夜。接着,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂(oh-)进行酸碱中和,然后依次进行过滤,真空浓缩除去溶剂,并再用乙醚进行洗涤。最后,将滤液进行浓缩,干燥。该步骤的反应如下所示:
[0194][0195]
其1hnmr谱图如图7所示,结构解析如下:
[0196]1hnmr(400mhz,d2o),δ(ppm):
[0197]
8.93(s,1h),7.56-7.63(d,2h),4.97(s,2h),4.40-4.44(t,2h),3.11-3.15(t,2h),2.32-2.39(m,2h).
[0198]
其ms谱图如图8所示,解析如下:
[0199]
[m+h]=184,[2m+h]=367,[3m+h]=550,这和m
(cb1-nh2)
=183的理论值相对应。
[0200]
综上,cb
1-nh2的合成是成功的。
[0201]
(ⅲ)合成式(2)聚合物,1-(3-氨基丙基)咪唑乙酸甜菜碱改性海藻酸钠(cb
1-alg):
[0202]
将1g(5.04mmol)海藻酸钠溶于80ml去离子水和20ml乙腈混合溶剂。然后加入450mg(2.56mmol)2-氯-4,6-二甲氧基-1,3,5-三嗪和560μl(5.04mmol)n-甲基吗啉。随后将0.924g(5.04mmol)1-(3-氨基丙基)咪唑乙酸甜菜碱溶解在20ml去离子水中,并添加到上述混合溶液中。在55-60℃下反应24h。最后,减压浓缩除去溶剂并将其重新溶解在去离子水中,并用1mol/l naoh溶液将ph调至中性。最后用去离子水进行透析3d,用无水甲醇沉析,离心,并重复3次,于40℃真空干燥48h。
[0203]
该步骤的反应如下所示,羧基参与离子交联,引入了外源羧基,降低海藻酸钠自身羧基被改性后离子交联强度减少的影响:
[0204][0205]
其中,由cb
1-nh2制备cb
1-alg,还可以通过如下步骤制备得到:
[0206]
将1g(5.04mmol)海藻酸钠溶于100ml ph=6.0,0.1mol/l mes缓冲液溶液中。然后加入0.97g(5.04mmol)1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc
·
hcl)和0.582g(5.04mmol)n-羟基琥珀酰亚胺(nhs),活化15min,随后将0.924g(5.04mmol)1-(3-氨基丙基)咪唑乙酸甜菜碱溶解在6ml ph=6.0,0.1mol/l mes缓冲液溶液中,并添加到上述混合溶液中。室温下反应24h。然后用无水甲醇进行粗纯化。最后,进行分离,重新用去离子水溶解,并用1mol/l naoh溶液调至中性,然后进行透析3d,并用无水甲醇沉析,离心,重复3次,40℃真空干燥48h。
[0207]
其1hnmr谱图如图9所示,结构解析如下:
[0208]1hnmr(400mhz,d2o),δ(ppm):
[0209]
8.82(s,1h),7.48-7.56(d,2h),4.84(s,2h),4.47(t,2h),3.76
–
4.29(m,naalg上的h),3.33(m,2h),2.17(t,2h)。
[0210]
实施例3
[0211]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(2)聚合物,其制备过程与实施例2的区别之处在于:
[0212]
(ⅰ)n-boc-丙胺咪唑乙酸甜菜碱ⅱ的制备:
[0213]
称取(3.6g,16mmol)n-boc-丙胺咪唑和(3.206g,19.2mmol)溴乙酸乙酯溶解在12ml乙腈中,然后在45℃搅拌反应24h。24h后,用旋转蒸发仪除去大部分溶剂,粗产物用无
水乙醚洗涤4次,最后浓缩除去所有溶剂得到黄色油状液体,产率约85%。该步骤的反应如下所示:
[0214][0215]
其1hnmr谱图如图10所示,结构解析如下:
[0216]1hnmr(400mhz,d2o),δ(ppm):
[0217]
8.95(s,1h),7.59-7.64(d,2h),5.21(s,2h),4.31-4.36(m,4h),3.15-3.18(t,2h),2.10-2.17(m,2h),1.46(s,9h),1.31-1.34(t,3h)。
[0218]
(ⅱ)1-(3-氨基丙基)咪唑乙酸甜菜碱(简称:cb
1-nh2)的制备:
[0219]
将5g n-boc-丙胺咪唑乙酸甜菜碱ⅱ溶于100ml 1.25mol/l hcl的甲醇溶液。然后将溶液在室温下搅拌过夜。真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂(oh-)进行酸碱中和,然后依次进行过滤,真空浓缩除去溶剂,再用乙醚进行洗涤。最后,将滤液进行浓缩,干燥。该步骤的反应如下所示:
[0220][0221]
其1hnmr谱图和ms谱图的测试结果与实施例2基本一致,表明本实施例同样成功制备出1-(3-氨基丙基)咪唑乙酸甜菜碱(cb
1-nh2)。
[0222]
实施例3和实施例2中的两性离子修饰的多糖类聚合物的各项实验测试结果相当。
[0223]
实施例4
[0224]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(3)聚合物,其制备过程包括:
[0225]
(ⅰ)n-boc-丙胺咪唑丁酸甜菜碱的制备:
[0226]
称取(4.5g,20mmol)n-boc-丙胺咪唑和(3.74g,24mmol)4-溴丁酸乙酯溶解在20ml乙腈中,在45℃下搅拌反应5d。然后,对反应液进行浓缩除去溶剂后加入无水乙醚进行洗涤3-5次,最后进行真空浓缩得到黄色粘稠液体,产率约85%。该步骤的反应如下所示:
[0227][0228]
其1hnmr谱图如图11所示,结构解析如下:
[0229]1hnmr(400mhz,d2o),δ(ppm):
[0230]
8.88(s,1h),7.58-7.60(d,2h),4.28-4.33(m,4h),4.14-4.20(q,2h),3.14-3.17(t,2h),2.48-2.51(t,2h),2.21-2.56(m,2h),2.09-2.15(m,2h),1.47(s,9h),1.26-1.30(t,3h)。
[0231]
(ⅱ)1-(3-氨基丙基)咪唑丁酸甜菜碱(简称:cb
2-nh2)的制备:
[0232]
将5g n-boc-丙胺咪唑丁酸甜菜碱溶于100ml 1.25mol/l hcl的甲醇溶液,将溶液在室温下搅拌过夜。然后,真空浓缩除去溶剂,用甲醇重新溶解再用离子交换树脂(oh-)进行酸碱中和,依次进行过滤,真空浓缩除去溶剂,并用乙醚进行洗涤。最后,将滤液进行浓缩,干燥。该步骤的反应如下所示:
[0233][0234]
其1hnmr谱图如图12所示,结构解析如下:
[0235]1hnmr(400mhz,d2o),δ(ppm):
[0236]
8.88(s,1h),7.55-7.56(d,2h),4.32-4.37(t,2h),4.21-4.25(t,2h),3.05-3.09(t,2h),2.23-2.35(m,2h),2.20-2.22(t,2h),2.10-2.15(m,2h).
[0237]
其ms谱图如图13所示,解析如下:
[0238]
[m+h]=212,[2m+h]=413,这和m
(cb2-nh2)
=211的理论值相对应。
[0239]
综上,cb
2-nh2的合成是成功的。
[0240]
(ⅲ)合成式(3)聚合物,1-(3-氨基丙基)咪唑丁酸甜菜碱改性海藻酸钠(cb
2-alg):
[0241]
将1g(5.04mmol)海藻酸钠溶于80ml去离子水和20ml乙腈混合溶剂。然后加入450mg(2.56mmol)2-氯-4,6-二甲氧基-1,3,5-三嗪和560μl(5.04mmol)n-甲基吗啉。随后将1.066g(5.04mmol)1-(3-氨基丙基)咪唑丁酸甜菜碱溶解在20ml去离子水中,并添加到上述混合溶液中,在55-60℃下反应24h。然后,减压浓缩除去溶剂并将其重新溶解在去离子水中,并用1mol/l naoh溶液将ph调至中性。最后用去离子水进行透析3d,再用无水甲醇沉析,离心,并重复3次,40℃真空干燥48h。
[0242]
该步骤的反应如下所示,羧基参与离子交联,引入了外源羧基,降低海藻酸钠自身羧基被改性后离子交联强度减少的影响:
[0243][0244]
其中,由cb
2-nh2制备cb
2-alg,还可以通过如下步骤制备得到:
[0245]
将1g(5.04mmol)海藻酸钠溶于100ml ph=6.0,0.1mol/l mes缓冲液溶液中。然后加入0.97g(5.04mmol)1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc
·
hcl)和
0.582g(5.04mmol)n-羟基琥珀酰亚胺(nhs),活化15min,随后将1.066g(5.04mmol)1-(3-氨基丙基)咪唑丁酸甜菜碱溶解在6ml ph=6.0,0.1mol/l mes缓冲液溶液中,并添加到上述混合溶液中,室温下反应24h,用无水甲醇进行粗纯化。然后,进行分离,重新用去离子水溶解,并用1mol/l naoh溶液调至中性,透析3d,最后用无水甲醇沉析,离心,并重复3次,40℃真空干燥48h。
[0246]
cb
2-alg的1hnmr谱图如图14所示,结构解析如下:
[0247]1hnmr(400mhz,d2o),δ(ppm):
[0248]
8.90(s,1h),7.58(d,2h),4.32-4.38(t,4h),3.74
–
4.01(m,naalg上的h),3.04-3.08(t,2h),2.91-2.95(m,2h),2.26-2.36(m,4h)。
[0249]
实施例5
[0250]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(4)聚合物:甲基丙烯酰化1-(3-氨基丙基)咪唑磺酸甜菜碱改性海藻酸钠(sb-alg-ma),其制备原料包括实施例1中制备得到的sb-alg,sb-alg-ma的制备过程包括:
[0251]
将2.5g(12.6mmol)sb-alg溶解在125ml去离子水中,随后将11.28ml(75.6mmol)的甲基丙烯酸酐滴加到溶液中,并通过添加少量5mol/l氢氧化钠(naoh)溶液将ph值提高到8。混合物在室温下反应24小时。之后,用去离子水透析3d,以去除未反应的甲基丙烯酸酐和形成的甲基丙烯酸,最后进行冷冻干燥。
[0252][0253]
sb-alg-ma的1hnmr谱图如图19所示,结构解析如下:
[0254]1hnmr(400mhz,d2o),δ(ppm):
[0255]
8.87(s,1h),7.57(d,2h),6.22(s,1h),5.79(s,1h),4.36-4.30(t,2h),4.26(t,2h),3.93-4.05(m,naalg上的h),3.31(t,2h),2.93-2.97(m,2h),2.32-2.35(t,2h),2.16(t,2h),1.95(t,2h)。
[0256]
本实施例提供了一种生物材料,其制备原料包括本实施例制备得到的sb-alg-ma,生物材料的制备过程包括:
[0257]
配制0.2%蓝光引发剂lap溶液,然后称取25mg sb-alg-ma溶解至1.25ml蓝光引发剂lap溶液,最后在蓝光作用下交联固化1-2min,得到sb-alg-ma自交联水凝胶,如图21(a)所示;
[0258]
配制0.2%蓝光引发剂lap溶液,然后分别称取25mg sb-alg-ma和12.5mg的聚乙二醇二丙烯酸酯pegda溶解至1.25ml蓝光引发剂lap溶液,最后在蓝光作用下交联固化1-2min,得到sb-alg-ma-pegda水凝胶,如图21(c)所示。
[0259]
实施例6
[0260]
本实施例公开了一种两性离子修饰的多糖类聚合物,为式(5)聚合物:甲基丙烯酰
化1-(3-氨基丙基)咪唑乙酸甜菜碱改性海藻酸钠(cb
1-alg-ma),其制备原料包括实施例2中制备得到的cb
1-alg,cb
1-alg-ma的制备过程包括:
[0261]
将2.5g(12.6mmol)乙酸甜菜碱-海藻酸钠溶解在125ml去离子水中,随后将11.28ml(75.6mmol)的甲基丙烯酸酐滴加到溶液中,并通过添加少量5mol/l氢氧化钠(naoh)溶液将ph值提高到8。混合物在室温下反应24小时。之后,用去离子水透析3d,以去除未反应的甲基丙烯酸酐和形成的甲基丙烯酸,最后进行冷冻干燥。
[0262][0263]
cb
1-alg-ma的1hnmr谱图如图20所示,结构解析如下:
[0264]1hnmr(400mhz,d2o),δ(ppm):
[0265]
8.82(s,1h),7.48-7.56(d,2h),6.23(s,1h),5.78(s,1h),4.84(s,2h),4.29(t,2h),3.78-4.04(m,naalg上的h),3.33-3.34(t,2h),2.15-2.18(t,3h),1.92-1.95(m,2h)。
[0266]
本实施例提供了一种生物材料,其制备原料包括本实施例制备得到的cb
1-alg-ma,生物材料的制备过程包括:
[0267]
配制0.2%蓝光引发剂lap溶液,然后称取25mg cb
1-alg-ma溶解至1.25ml蓝光引发剂lap溶液,最后在蓝光作用下交联固化1-2min,得到cb
1-alg-ma自交联水凝胶,如图21(b)所示。
[0268]
配制0.2%蓝光引发剂lap溶液,然后分别称取25mg cb
1-alg-ma和12.5mg的聚乙二醇二丙烯酸酯pegda溶解至1.25ml蓝光引发剂lap溶液,最后在蓝光作用下交联固化1-2min,得到cb
1-alg-ma-pegda水凝胶,如图21(d)所示。
[0269]
试验例
[0270]
本试验例测试了实施例1、2、4得到的两性离子修饰的多糖类聚合物及海藻酸钠进行了性能测试,具体为:
[0271]
(一)甜菜碱改性海藻酸盐的体外抗蛋白黏附测试
[0272]
1、bsa标准曲线的测定
[0273]
(1)蛋白标准品的准备
[0274]
a.取0.8ml蛋白标准配置液加入到一管蛋白标准(20mg bsa)中,充分溶解后配制成25mg/ml的蛋白标准液;
[0275]
b.用0.9%nacl将蛋白标准液稀释成0.5mg/ml。
[0276]
(2)bca工作液的配制
[0277]
按50体积bca试剂a加1体积bca试剂b(50:1)配制bca工作液,充分混匀。
[0278]
(3)bsa标准曲线
[0279]
a.将标准品按0μl、1μl、2μl、4μl、8μl、12μl、16μl、20μl加到96孔板的标准品孔中,加0.9%nacl补足到20μl,相当于标准品浓度分别为0mg/ml、0.025mg/ml、0.05mg/ml、
0.1mg/ml、0.2mg/ml、0.3mg/ml、0.4mg/ml、0.5mg/ml;
[0280]
b.各孔加入200μl bca工作液,37℃放置20-30分钟;
[0281]
c.用酶标仪测定在562nm波长的吸光度。
[0282]
不同浓度下的bsa吸光度测试结果如表1所示,所得bsa标准曲线如图16所示。
[0283]
表1不同浓度下的bsa吸光度测试结果表
[0284][0285]
2、sb-alg,cb
1-alg,cb
2-alg的蛋白吸附含量检测
[0286]
(1)分别用0.9%nacl配制浓度为2%的naalg、sb-alg、cb
1-alg、cb
2-alg溶液;
[0287]
(2)配制20mmol/l bacl2溶液;
[0288]
(3)按v
甜菜碱改性海藻酸钠
:v
海藻酸钠
=6:4分别配制sb-alg+naalg、cb
1-alg+naalg、cb
2-alg+naalg溶液;
[0289]
(4)往96孔板上分别加入400μl sb-alg+naalg、cb
1-alg+naalg、cb
2-alg+naalg溶液,然后各加入400μl bacl2溶液;
[0290]
(5)固化1h,形成大小约10mm*10mm*4mm的凝胶;
[0291]
(6)将sb-alg+naalg、cb
1-alg+naalg、cb
2-alg+naalg凝胶转移至小培养皿上,并用pbs洗5次;
[0292]
(7)分别加入800μl 1.5mg/ml bsa,37℃,孵育4h;
[0293]
(8)取出sb-alg+naalg、cb
1-alg+naalg、cb
2-alg+naalg凝胶;
[0294]
(9)各取20μl剩下的bsa,再加入200μl bca工作液,在562nm测蛋白吸附量。测试结果如图17及表2所示:
[0295]
表2蛋白吸附量测试结果表
[0296][0297]
由表2可知,相较于海藻酸钠,60%的sb-alg、cb
1-alg和cb
2-alg都能起到提高海藻酸钠的抗蛋白黏附效果,从而降低其异物反应,降低免疫排斥现象。
[0298]
(二)、sb-alg、cb
1-alg、cb
2-alg、sb-alg-ma、cb
1-alg-ma的细胞毒性测试
[0299]
(1)分别配制2%sb-alg、cb
1-alg、cb
2-alg、sb-alg-ma、cb
1-alg-ma的无菌dmem培养液
[0300]
分别称取500mg sb-alg、cb
1-alg、cb
2-alg、sb-alg-ma、cb
1-alg-ma溶解在25ml含10%fbs的dmem培养液中,然后用0.22μm的滤头过滤除去细菌,得到2%含sb-alg、cb
1-alg、cb
2-alg、sb-alg-ma、cb
1-alg-ma的dmem培养液。
[0301]
(2)制备细胞悬液:将对数生长期生长旺盛的小鼠成纤维细胞l929(活细胞数》99%),用0.25%胰酶消化后,配制成浓度为1*105/ml的细胞悬液备用。
[0302]
(3)mtt法检测
[0303]
将配好的细胞悬液加入96孔板中,每孔加100μl,置于5%co2培养箱培养18-24h。待贴壁完全后,移去培养液,并用pbs洗三次,然后每孔加入100μl含有待测材料的dmem培养液,并平行设置3孔,空白对照和阴性对照孔加等量含10%fbs的dmem的培养液,放入37℃,5%co2培养箱中培养。在24h后加入10μl/孔浓度为5mg/ml的mtt液,继续培养4h。最后,除去培养液,加入100μl dmso溶液,用酶标仪测吸光值(λ=570nm),通过以下公式计算相对增殖率(rgr%),进行毒性分级。
[0304]
rgr%=(试验组吸光值-空白对照吸光值)/(阴性对照组吸光值-空白对照吸光值)*100%。
[0305]
细胞毒性测试结果如图18所示:2%的sb-alg、cb
1-alg、cb
2-alg、sb-alg-ma、cb
1-alg-ma的相对增殖率均大于85%,远超70%,属于无细胞毒性,具有良好的生物相容性。
[0306]
(三)实施例5和6制备得到的生物材料(sb-alg-ma自交联水凝胶、cb
1-alg-ma自交联水凝胶、sb-alg-ma-pegda水凝胶、cb
1-alg-ma-pegda水凝胶),如图21所示:
[0307]
sb-alg-ma与cb
1-alg-ma自身或者可以和pegda一起作为生物墨水,膜的改性基材等进行应用,同时海藻酸钠除了本身固有的离子交联之外,双键的引入也有助于其采用化学交联形成稳定的三维网络结构,或者为其增加了一种新的交联方式有助于其在离子交联受局限的领域范围中应用(相关技术中,离子交联通常采用的二价金属离子,而这些金属往往是重金属离子,当其作为体内植入材料或者以载体的形式进入体内时往往会因为重金属离子造成中毒现象)。
[0308]
本发明披露的部分实施例通过合成一类带有咪唑五元杂环的两性离子,利用p-π轨道共轭效应将所带正荷均匀地分散在五元环上以及通过有效的能量耗散机制,形成高稳定性的咪唑鎓两性离子(如sb-alg、cb
1-alg、cb
2-alg),最后将此类两性离子通过酰胺化反应接枝至海藻酸钠上,得到一种具有良好的生物相容性的材料,低异物反应性的可长期稳定存在于体内的植入材料。
[0309]
需要说明的是,本文中的“常温”或“室温”,如无特殊说明,均约为25℃;本文中涉及数值的“约”或“左右”的含义为误差
±
2%。
[0310]
上面结合附图对本发明实施例作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1