一种用于检测人细胞色素P4503A4的荧光底物及其制备方法和应用
一种用于检测人细胞色素p450 3a4的荧光底物及其制备方法和应用
技术领域
1.本发明属于医药技术领域,涉及一种用于检测人细胞色素p450 3a4(cytochromep450 3a4)的荧光底物及其制备方法和应用。
背景技术:
2.细胞色素p450 3a(cytochrome p450 3a enzymes,cyp3a)是机体内重要的i相氧化代谢酶,催化多种内源性和外源性化合物发生氧化代谢,在药物代谢清除和代谢激活过程中发挥了重要作用。据统计,约有50%的上市药物(如紫杉醇、顺铂、咪达唑仑等)可被cyp3a代谢。cyp3a亚家族包括四个成员,分别为cyp3a4,cyp3a5, cyp3a7和cyp3a43。其中cyp3a4最为重要,其不仅在多个器官中高表达,还参与众多药物、中药和食品化学成分、环境毒物的代谢清除和代谢活化。因此,cyp3a4 的活性与药物毒性和药效发挥密切相关。cyp3a4抑制剂或诱导剂可通过调控cyp3a4 的活性/表达影响cyp3a4底物药物的代谢清除,进而引发药代学层面的药物相互作用。因此,业界一直期待研发可高效精准表征cyp3a4活性/残余活性的方法,进而用于cyp3a4相关基础研究和药物早期安全性评价。
3.目前cyp3a4酶活检测方法主要以cyp3a4的内源性底物(如睾酮)和药物底物 (如多烯紫杉醇、咪达唑仑等)为底物,该类方法需要借助液质联用等技术,样品前处理和分析过程复杂、难以实现高通量筛选;同时该类方法还需要专业的分析测试人员且仪器和分析成本高。与之相比的是,基于荧光底物的荧光检测法无需样品前处理,检测和操作流程简单,可实现高通量和超高通量检测。但目前cyp3a4的特异性光学底物鲜有报道,且存在诸多缺陷。因此,有必要研发更实用和更特异的cyp3a4 光学底物,进而用于生物样本中cyp3a4酶活的定量评估,以及cyp3a4调控剂的筛选和评价。
4.为此,本发明提供了一类1,8-萘酰亚胺类化合物及其作为cyp 3a4酶荧光底物的应用。该类底物经cyp 3a4氧化后可生成荧光发射波谱不同于原型的氧化产物。该类底物还具有特异性高、代谢产物单一且易检测、亲和力高且符合米氏动力学、适于高通量检测等优势。
技术实现要素:
5.针对现有技术中的上述技术问题,本发明提供了一种用于检测人细胞色素p450 3a4(cytochrome p450 3a4)的荧光底物及其制备方法和应用,所述的这种用于检测人细胞色素p450 3a4(cytochrome p450 3a4)的荧光底物及其制备方法和应用要解决现有技术中检测cyp3a4酶活检的方法复杂的技术问题。
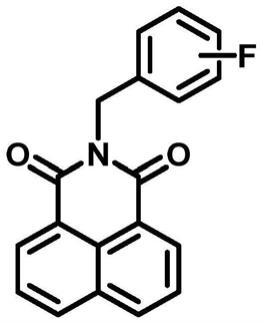
6.本发明提供了一种人细胞色素p450 3a4的荧光底物,为n-氟代苄基-1,8-萘酰亚胺类化合物,其结构通式如式(1)所示:
[0007][0008]
本发明还提供了上述的一种人细胞色素p450 3a4的荧光底物的制备方法,以1,8
‑ꢀ
萘二甲酸酐和氟苄胺为原料,在无水乙醇中加热回流后获得n-氟代苄基-1,8-萘酰亚胺粗品,然后经过色谱分离后获得n-氟代苄基-1,8-萘酰亚胺。
[0009]
本发明还提供了上述的的化合物在检测生物样本中cyp3a4的活性或残余活性中的用途。
[0010]
进一步的,所述的人细胞色素p450 3a4的荧光底物被cyp3a4特异性催化发生c
‑ꢀ
4羟化反应并产生单一的4-羟化产物,通过检测人细胞色素p450 3a4的荧光底物在单位时间内的消除或4-羟化产物的生成量来定量检测生物样本中cyp3a4的活性或残余活性。
[0011]
进一步的,人细胞色素p450 3a4的荧光底物被cyp3a4催化后产生的羟化产物可显示与底物不同的发射波谱,其底物的激发波长300~370nm和发射波长350~400 nm;产物激发波长410~480nm,发射波长在500~580nm。
[0012]
本发明还提供了一种检测生物样本中cyp3a4活性的方法,采用上述人细胞色素 p450 3a4的荧光底物,在生理条件下将待测样品和底物混合后加入nadph起始反应;孵育5-60分钟后借助荧光检测设备检测底物在单位时间内的消除或4-羟化产物的生成量进而定量评估生物样本中cyp3a4的活性。
[0013]
进一步的,所述待测样品包括但不限于cyp3a4重组单酶、表达cyp3a4的各类细胞或细胞制备物、过表达cyp3a4的工程细胞或其制备物,或者商品化的组织制备物。
[0014]
本发明还提供了一种cyp3a4调控剂的筛选和评价方法,采用上述人细胞色素p450 3a4的荧光底物用于测定任意待测化合物对cyp3a4活性的调控作用(包括抑制、激活、灭活和诱导作用)。
[0015]
进一步的,以上述人细胞色素p450 3a4的荧光底物为探针底物,在生理条件下将含有cyp3a4的生物样品和待评价化合物混合后温孵3-63分钟,然后加入底物和 nadph起始反应;孵育5-60分钟后终止反应,测定底物在单位时间内4-羟化产物的生成速率并与无待评价化合物组的产物生成速率比较,获得待评价化合物对cyp3a4 的调控能力。
[0016]
进一步的,所述含有cyp3a4的生物样品可选择cyp3a4重组单酶、表达 cyp3a4的各类细胞或细胞制备物、过表达cyp3a4的工程细胞或其制备物,或者商品化的组织制备物。
[0017]
所述待评价化合物为:cyp3a4的调控剂,测的是调控剂对cyp3a4的调控能力 (抑制、激活、灭活和诱导作用)。底物经过酶(不同来源的酶中的cyp3a4)代谢,产生产物,发出荧光。测定底物在单位时间内产物的生成速率并与无待评价化合物组的产物生成速率比较,获得待评价化合物(调控剂)对cyp3a4的调控能力。
[0018]
本发明的人细胞色素p450 3a4特异性荧光底物可被cyp 3a4特异性氧化为相应氧化产物并显示与底物不同的发射波谱。本发明的底物作为cyp 3a4的特异性底物,可以发生4-羟化代谢反应,通过定量检测单位时间内羟化产物的生成量来测定不同酶源中cyp 3a4
的活性。
[0019]
本发明可通过评估重组cyp酶、商品化细胞/组织制备物等生物产品中cyp3a4的活性进而对上述产品进行质控。
[0020]
本发明还可测定任意待测化合物对重组cyp酶、商品化细胞/组织制备物等生物产品中cyp3a4活性的调控作用(包括抑制、激活、灭活和诱导作用),所述生物产品包括但不限于cyp3a4重组单酶、表达cyp3a4的各类细胞或细胞制备物、过表达 cyp3a4的工程细胞或其制备物,以及商品化的组织制备物。
[0021]
本发明和已有技术相比,其技术进步是显著的。选用本发明所述cyp3a4特异性荧光底物检测cyp3a4酶活性具有以下优势:
[0022]
(1)特异性好且代谢产物单一:该类底物可被cyp3a4高特异性地代谢并生成单一的代谢产物,即4位羟化产物。
[0023]
(2)亲和力高:该类底物与cyp3a4具有高亲和力,km小于1微摩。
[0024]
(3)产物易于检测:该类底物及其氧化代谢产物具有不同的荧光发射光谱特征,能较好的进行区分检测;同时该类底物的4-羟化产物在500~600nm具有很强的荧光发信号,可借助配有荧光检测器的任意设备检测。
[0025]
(4)检测通量高:利用该类荧光底物建立的抑制剂筛选方法可实现96、384孔板的高效快速实时检测,可实现每日2万个样品的高通量检测,具有单个测试成本低廉 (《0.5元)的优势。
[0026]
(5)底物和产物均易于合成:1,8-萘酰亚胺类衍生物及其氧化产物均可经化学合成获得,合成工艺简单易行。
附图说明
[0027]
图1.n-氟代苄基-1,8-萘酰亚胺类的结构通式;
[0028]
图2.n-氟代苄基-1,8-萘酰亚胺类的结构式;
[0029]
图3.n-氟代苄基-1,8-萘酰亚胺类的合成路线图;
[0030]
图4.n-氟代苄基-1,8-萘酰亚胺类底物的代谢表型分析;
[0031]
图5.b-1的酶促反应动力学参数测定;
[0032]
图6.b-1在肝微粒体中代谢产物液相谱图;
[0033]
图7.b-1定量测定不同商品化组织制备物中cyp 3a4酶活;
[0034]
图8.b-1测定诱导hepg2细胞及小鼠中cyp 3a4的活性;
[0035]
图9.b-1测定利血平及五味子乙素对cyp 3a4抑制活性。
具体实施方式
[0036]
下面的实施例将对本发明予以进一步的说明,但并不因此而限制本发明。
[0037]
实施例1 n-氟代苄基-1,8-萘酰亚胺类化合物的化学合成
[0038]
(1)将一当量的1,8-萘二甲酸酐溶于20ml无水乙醇中,加入1.2当量的2-氟苄胺/3-氟苄胺/4-氟苄胺,搅拌并缓慢加热至回流,并持续3h;
[0039]
(2)反应液自然冷却至室温,过滤得到白色滤饼为粗产品,并采用硅胶色谱法进行纯化(洗脱剂:二氯甲烷),得白色固体粉末状纯品n-(2
’‑
氟苄基)-1,8-萘酰亚胺(b
‑ꢀ
2,产
率:89.8%,见图2a)。
[0040]1h nmr(600mhz,cdcl3)δ8.63(d,j=7.3hz,2h),8.23(d,j=8.2hz,2h),7.77(t, j=7.7hz,2h),7.30(t,j=7.5hz,1h),7.24
–
7.18(m,1h),7.10
–
6.99(m,2h),5.48(s, 2h).
13
c nmr(150mhz,cdcl3)δ164.13,161.60,159.96,134.17,131.66,131.58,129.25, 129.22,128.92,128.86,128.29,127.01,124.19,124.09,124.07,124.05,122.54,115.54, 115.39,37.49,37.46。
[0041]
如上所述得白色固体粉末状纯品n-(3
’‑
氟苄基)-1,8-萘酰亚胺(b-3,产率: 90.2%,见图2b)。
[0042]1h nmr(600mhz,cdcl3)δ8.62(d,j=7.3hz,2h),8.22(d,j=7.9hz,2h),7.76(t, j=7.7hz,2h),7.32(d,j=7.7hz,1h),7.29
–
7.23(m,2h),6.93(td,j=8.3,1.9hz,1h), 5.37(s,2h).
13
c nmr(150mhz,cdcl3)δ164.19,163.64,162.01,139.68,139.63,134.21, 131.64,131.57,129.93,129.88,128.24,127.01,124.50,124.48,122.51,115.84,115.69, 114.50,114.36,43.10。
[0043]
如上所述得白色固体粉末状纯品n-(4
’‑
氟苄基)-1,8-萘酰亚胺(b-1,产率: 81.4%,见图2c)。
[0044]1h nmr(600mhz,cdcl3)δ8.61(d,j=7.3hz,2h),8.21(d,j=8.2hz,2h),7.75(t, j=7.7hz,2h),7.56(dd,j=8.5,5.5hz,2h),6.98(t,j=8.7hz,2h),5.34(s,1h).
13c‑ꢀ
nmr(150mhz,cdcl3)δ164.22,163.01,161.38,134.14,133.15,133.13,131.62,131.49, 131.02,130.96,128.20,126.98,122.58,115.31,115.17,42.83。(合成路线图见图3)
[0045]
实施例2代谢表型分析n-氟代苄基-1,8-萘酰亚胺类底物的特异性
[0046]
(1)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、商品化的人p450酶(10nm)、b-1(1μm)、b-2(1μm)、b-3(1μm)于37℃条件下震荡预孵3分钟;
[0047]
(2)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0048]
(3)30分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0049]
(4)检测产物的荧光信号(e
x
=450nm,em=555nm);得到各样品中产物的荧光强度,b-2,b-3,b-1同家族亚型选择性分别为3.6,7.9,72.6倍(图4a,4b,4c)。
[0050]
结论:三种荧光底物中b-1产物生成快,特异性好。
[0051]
实施例3底物b-1的酶促动力学分析
[0052]
(1)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、商品化的人cyp 3a4(0.025nm)/商品化人肝微粒体(0.005mg/ml)、不同浓度的b-1于 37℃条件下震荡预孵3分钟;
[0053]
(2)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0054]
(3)20分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0055]
(4)检测产物的荧光信号(e
x
=450nm,em=555nm);得到各样品中产物的荧光强度,拟合酶促反应动力学曲线。在单酶和商品化人肝微粒体中,都呈现米氏动力学,且km非常接近,分别为0.42
±
0.03μm(图5a),0.46
±
0.04μm(图5b);v
max
分别为3.53
±
0.09nmol/min/nmol p450,0.97
±
0.02nmol/min/mg protein。
[0056]
结论:b-1在单酶和商品化人肝微粒体中km非常接近,进一步佐证了其特异性,代谢符合米氏动力学,可以采用米氏方程表征其酶动力学参数。
[0057]
实施例4 b-1代谢产物的单一性分析
[0058]
(1)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、商品化人肝微粒体(0.2mg/ml)、b-1(10μm)于37℃条件下震荡预孵3分钟;
[0059]
(2)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0060]
(3)30分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0061]
(4)取底物及产物标准品及代谢反应样品进行液相色谱分析(见图6)。
[0062]
结论:b-1经代谢后可生成单一代谢产物。
[0063]
实施例5不同组织制备物中cyp 3a4酶活的定量测定
[0064]
(1)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、不同商品化组织制备物(0.01mg/ml)、b-1(10μm)于37℃条件下震荡预孵3分钟;
[0065]
(2)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0066]
(3)20分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0067]
(4)进行荧光检测(e
x
=450nm,em=555nm);不同商品化组织制备物中cyp 3a4酶的最大催化速率为0.049
±
0.0016nmol/min/mg protein(见图7)。
[0068]
结论:b-1可作为荧光底物用于商品化组织制备物中cyp3a4酶活的定量测定。
[0069]
实施例6 cyp 3a4诱导剂的筛选与评价
[0070]
(1)hepg2细胞分为3组,分别为dmso组、柳穿鱼黄素组(10μm)和利福平组(10μm),连续给药3天。末次给药24小时后采集hepg2细胞,制备细胞s9。
[0071]
(2)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、细胞 s9(20μl)、b-1(10μm)于37℃条件下震荡预孵3分钟;
[0072]
(3)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0073]
(4)20分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0074]
(5)进行荧光检测(e
x
=450nm,em=555nm)及western blot实验;计算人三组细胞s9中cyp3a4酶活性及蛋白表达量(见图8a,8b)。
[0075]
(6)将雄性icr小鼠随机分为2组,每组6只。利福平组50mg/kg,腹腔注射,给药4天;对照组给予同体积玉米油。末次给药24小时后采集小鼠肝脏,制备肝 s9。
[0076]
(7)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、小鼠肝s9(5μl)、b-1(10μm)于37℃条件下震荡预孵3分钟;
[0077]
(8)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0078]
(9)20分钟后,加入100μl冰乙腈,剧烈震荡后,终止反应,20000g离心30分钟取上清液待测;
[0079]
(10)进行荧光检测(e
x
=450nm,em=555nm)及western blot实验;计算人两组小鼠中cyp3a4酶活性及蛋白表达量(见图8c,8d)。
[0080]
结论:b-1可作为荧光底物用于cyp3a4诱导剂的筛选。
[0081]
实施例7 cyp 3a4抑制剂的筛选与评价
[0082]
(1)准备180μl i相代谢反应体系,包括ph 7.4的pbs缓冲液(100mm)、商品化人肝微粒体(0.01mg/ml)、b-1(5μm)、乙腈或不同浓度的利血平/五味子乙素于 37℃条件下震荡预孵3分钟;
[0083]
(2)向反应体系中加入20μl终浓度为1mm的nadph起始反应;
[0084]
(3)反应20分钟进行荧光连续检测(e
x
=450nm,em=555nm),根据抑制剂组 555nm下的荧光强度与乙腈组的荧光强度比值计算不同浓度点抑制cyp 3a4的强度,发现了这2种化合物对cyp3a4酶均有较强的抑制效果。拟合ic
50
曲线后得到利血平 ic
50
为0.64
±
0.07μm,五味子乙素ic
50
为0.26
±
0.0025μm(见图9a,9b)。
[0085]
结论:b-1可作为荧光底物用于cyp3a4抑制剂的筛选。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1