一种界面水接触角可调控的快速交联固化的有机硅材料及其制备方法和应用
1.本发明涉及高分子化学领域,具体涉及一种界面水接触角可调控的快速交联固化的有机硅材料及其制备方法和应用。
背景技术:
2.有机硅高分子材料以螺旋结构的重复si-o-si链节为主链结构且侧基连接有不同种类有机官能团,具有优异的热稳定性、高气体渗透性、耐候性、耐化学品等性能。有机硅材料为憎水性材料,其与空气的水接触角大于90
°
,因此硅烷、硅树脂溶液、硅树脂乳液、有机硅粉末、硅丙乳液、硅酮密封胶等各种有机硅材料广泛应用于纺织材料、建筑、文物、管道等多种领域的防水处理、密封、粘接、堵漏等用途,在航空航天、国防军工及国民经济各个方面发挥了重要的作用。
3.另外有机硅材料及各种改性的有机硅聚合物材料根据其具体用途可以分为不固化和可固化的有机硅材料,前者如用作热传递介质的二甲基硅油,后者如硅橡胶、硅树脂、硅烷偶联剂、交联剂、硅油乳液等,这些可固化的有机硅材料分子中含有各种可参与化学反应的活性官能团,如si-oh、si-h、si-ch=ch2、si-cl、si-or等等。除了热传递介质、高真空扩散泵油、减震、密封、润滑等应用领域要求有机硅材料保持原有的液体状态即有机硅分子中不能含有活性官能团外,服务于其它大多数领域的有机硅材料通常都是以交联固化的产品形式存在。
4.当前有机硅高分子材料主要通过室温硫化硅橡胶(rtv)、加成硫化型硅橡胶(lsr)和热硫化硅橡胶(rtv)这3种产品形式存在。室温硫化硅橡胶以羟基封端的聚二甲基硅氧烷为基础聚合物,以含有烷氧基、酰氧基、酮肟基等官能团有机硅小分子化合物作为交联剂,经有机锡或钛酸酯类催化剂作用下缓慢交联固化,其表层交联固化速度较快,但胶料内部固化速度通常较慢,受空气中水分扩散速率影响较大,同时固化过程中不可避免地会同时释放出醇、酮、酮肟等小分子,导致固化后硅橡胶收缩率较大,影响尺寸稳定性。加成硫化型硅橡胶以乙烯基封端或侧链含有乙烯基或端基和侧基均含有乙烯基的聚二甲基硅氧烷为基础聚合物,端基或侧基或端基和侧基同时含有硅氢官能团的低粘度聚二甲基硅氧烷为交联剂,以铂的乙烯基络合物为催化剂,经硅氢加成机理交联固化,其优点是交联固化速度受催化剂活性和炔醇类抑制剂沸点制约,在中高温度范围内可调节固化速度;加成型硅橡胶另一优点是固化过程中无小分子释放,固化后样品尺寸变化小,应用范围非常广泛,但该交联固化中需使用催化剂,且铂催化剂受有机氮、硫、磷化合物的影响容易存在铂中毒现象,限制了其应用领域。热硫化硅橡胶(htv)以端基或侧基含有乙烯基的高分子量聚二甲基硅氧烷为基础聚合物,以2,5-二甲基-2,5-双(叔丁基过氧基)己烷(简称双二五,dbph)或2,4-二氯过氧苯甲酰(简称双二四,dcbp)为硫化剂,利用高温(150~170℃)下过氧化物分解产生的自由基引发聚硅氧烷端基或侧基的乙烯基官能团进行交联固化。虽然高温下可实现有机硅材料的快速固化,但存在固化温度高、需要二段硫化且自由基残留导致产品有异味等
问题。
5.有机硅材料虽然经历近80年的发展并在上述三种固化机理基础上形成了三大类可交联固化的有机硅聚合物材料,并且国外产业界和学术界广泛利用有机硅材料固有的疏水性能、优异的耐高低温性能、耐紫外辐射性能、憎水迁移性能等特性对其他合成聚合物材料进行改性,研发生产了有机硅改性环氧树脂、有机硅改性聚氨酯、有机硅改性聚酯等新型聚合物材料,但均存在常温下难以快速交联固化的问题,而且引入有机硅组分的主要目的在于将聚合物材料的界面性能由亲水性转变为疏水性能,或者由原本的疏水性能向超疏水性能方向转变。
6.众所周知,商品名为502的胶水也称瞬间固化胶,其主要成分为α-氰基丙烯酸酯,这类氰基丙烯酸酯化合物常温下在空气中微量水分引发下即可在数秒内快速交联固化,形成硬度大的脆性聚合物材料。2015年,szanka等人(szankaa,szanka i,kennedy j p.breathable rubbery skin protectors:design,synthesis,characterization,andproperties ofcyanoacrylated silicone rubber networks.journal of polymer science parta:polymer chemistry,2016,54(10):1367-1372)基于α-氰基丙烯酸酯在常温和空气中具有的快速固化的特性,利用diels-alder反应、硅氢加成、缩合法、retro diels-alder反应等一系列步骤将α-氰基丙烯酰氧基接枝到聚硅氧烷长链上,得到α-氰基丙烯酰氧基官能化的硅橡胶材料,该材料保持了α-氰基丙烯酸酯快速交联固化的特性,不需要外加任何催化剂,在空气中微量水分引发下就可以交联固化,将其应用于皮肤表面的局部非闭阻塞性伤口具有其他合成材料无法替代的优势。2016年,kennedy和szanka等人(kennedy j,szanka i,szanka a.rubbery polysiloxanes carrying cyanoacrylate functions and related methods for their preparation and uses therefor.us patent,us9695286,2017-07-04)采用蒽保护α-氰基丙烯酰氯与聚二甲基硅氧烷两端的si-oh、或羟烃基、或含醚键的羟烃基之间的缩合反应将蒽保护的氰基丙烯酰氧基官能团引入聚硅氧烷分子链两端,再经retro diels-alder反应脱除蒽保护基团后,得到可快速交联固化的柔性有机硅材料,以用于人体关节、膝盖等活动部位伤口保护和治疗用生物医学材料。
7.尽管szanka及其合作者采用硅氢加成和缩合反应这两种技术途径并结合retro diels-alder反应将氰基丙烯酰氧基官能团引入聚硅氧烷分子中,并报道所得的氰基丙烯酰氧基官能化的有机硅材料在常温下与空气中水分接触即可快速交联固化,加入dmt(n,n-二甲基对苯二胺)可进一步缩小交联固化时间,但从结构上看,szanka及其合作者在聚硅氧烷分子中引入氰基丙烯酰氧基或其衍生官能团的位置要么是在聚硅氧烷分子的两端,要么是在聚硅氧烷分子的侧链,所得改性聚合物材料虽然具备快速交联固化特性,但因交联位点少、交联密度低,导致改性的有机硅材料的本体交联固化速度仍然较慢,完全固化时间约为10min,即使加入少量的dmt后,完全固化时间仍需要4min左右,与α-氰基丙烯酸酯固化时间相比,仍有待提高。
8.人类生活各个领域除了需要疏水性材料外,表面接触角小于90
°
的各种亲水透气性材料也在各个领域得到广泛应用,因此结合有机硅材料优异的耐高低温性能、耐紫外光辐照、耐候等特性的亲水材料尤其是可快速交联固化的亲水性有机硅材料在油水界面分离、亲水亲肤医用材料、水凝胶界面材料等领域具有其他合成材料不可替代的作用。
技术实现要素:
9.本发明的一个目的是为解决现有氰基丙烯酰氧基官能化的有机硅聚合物材料固化速度仍然较慢,固化时间较长,固化产物交联密度较低且固化产物界面水接触角不能调控的问题,提出一种可快速交联固化且界面水接触角可以调整的有机硅材料;该氰基丙烯酰氧基官能化的有机硅聚合物材料的最短固化时间为3min,加入dmt促进剂后的固化时间缩短至3~5s,而且交联固化产物呈现亲水性,在空气中的水接触角可在65~85
°
范围内变化,具有优异快速固化和水接触角调控性能。
10.本发明是通过以下技术方案实现的:一种界面水接触角可调控的快速交联固化的有机硅材料,其化学结构式如下:
[0011][0012]
式中m优选为1~50的正整数,n为0~500的正整数;更优选m为1~100的正整数,n为0~150的正整数;最优选m为3~20的正整数,n为0~100的正整数。
[0013]
本发明的另一个目的是提供一种界面水接触角可调控的快速交联固化的有机硅材料的制备方法,该方法包括以下步骤:
[0014]
步骤(1)、硅氢加成制备α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物
[0015]
在干燥和惰性气体保护下的反应容器中,搅拌下,将羟乙基烯丙基醚,甲苯和karstedt催化剂于一定温度下活化一段时间,得到活化体系混合物;然后将α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物在活化温度下滴加至上述活化体系混合物中;滴加完毕后再在该温度下继续维持反应一段时间。反应完成后脱除溶剂和低沸物,得到化合物a,即α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物;其合成路线如下:
[0016][0017]
作为优选,所述的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物25℃时的粘度为5~1000cp,每克α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物中氢的质量
分数为0.01wt%~1.67wt%,m为1~100的正整数,n为0~500的正整数。
[0018]
更为优选,所述的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物的粘度(25℃)为8~800cp,每克α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物中氢的质量分数为0.03wt%~1.50wt%,m为1~50的正整数,n为0~150的正整数。
[0019]
最为优选,所述的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物的粘度(25℃)为10~500cp,每克α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物中氢的质量分数为0.05wt%~1.00wt%,m为3~20的正整数,n为0~100的正整数。
[0020]
作为优选,所述的甲苯中含水量小于500ppm,更为优选小于200ppm,最为优选小于100ppm。
[0021]
作为优选,所述的活化体系混合物中,羟乙基烯丙基醚与甲苯的质量比为0.05~2.0:1,更为优选为0.1~1.5:1,最为优选为0.15~0.80:1。
[0022]
作为优选,所述的karstedt催化剂中pt原子的质量与α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物和羟乙基烯丙基醚质量之和的比值为(1~1000)
×
10-6
:1,更为优选为(2~500)
×
10-6
:1,最为优选为(3~200)
×
10-6
:1。
[0023]
作为优选,所述的活化与反应温度为40~110℃,活化时间为10min~240min,更为优选,所述的活化与反应温度为50~95℃,活化时间为15min~120min。最为优选,所述的活化与反应温度为60~85℃,活化时间为25min~100min。
[0024]
作为优选,α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物滴加完毕后的维持反应时间为15min~600min,更为优选为20min~400min,最为优选为30min~300min。
[0025]
作为优选,所述的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物的滴加时间为15min~500min,更为优选为25min~300min,最为优选为30min~200min。
[0026]
作为优选,所述的惰性气体选自氮气、氦气或氩气中的一种或几种,惰性气体中水分含量小于或等于500ppm。更为优选,所述的惰性气体选自氮气或氦气,惰性气体中水分含量小于或等于200ppm。最为优选,所述的惰性气体选自氮气,氮气中水分含量小于或等于100ppm。
[0027]
步骤(2)、将步骤(1)化合物a溶于甲苯和三乙胺的混合溶液后,得到化合物a溶液;
[0028]
步骤(3)、缩合反应制备α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基))硅氧烷共聚物
[0029]
在干燥和惰性气体保护下的反应容器中,常温和搅拌下,加入蒽保护的α-氰基丙烯酰氯加合物和甲苯,再在一段时间内滴加化合物a溶液;滴加完毕后,再在常温下继续反应一段时间。抽滤除去固体残留物后,将滤液旋蒸除去溶剂,得到化合物b,也就是蒽保护的α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷,即α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物;其合成路线如下:
[0030][0031]
作为优选,所述的蒽保护的α-氰基丙烯酰氯加合物和甲苯的质量比为0.02~1.0:1,更为优选为0.05~0.75:1,最为优选为0.10~0.5:1。
[0032]
作为优选,所述的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物和甲苯的质量比为0.01~1.5:1,更为优选为0.05~1.0:1,最为优选为0.10~0.50:1。
[0033]
作为优选,所述的蒽保护的α-氰基丙烯酰氯加合物和α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物的摩尔比为0.8~4.0:1,更为优选为0.9~2.5:1,最为优选为1.0~2.0:1。
[0034]
作为优选,所述的蒽保护的α-氰基丙烯酰氯加合物和三乙胺的摩尔比为0.25~2.5:1,更为优选为0.40~2.0:1,最为优选为0.60~1.25:1。
[0035]
作为优选,所述的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物与甲苯和三乙胺的混合溶液的滴加时间为5~120min,更为优选10~90min,最为优选15~60min;
[0036]
作为优选,所述的滴加完毕后的继续反应时间为0.5~24h,更为优选1.0~12h,最为优选2.0~8h。
[0037]
作为优选,所述的惰性气体选自氮气、氦气或氩气中的一种或几种,惰性气体中水分含量小于或等于500ppm。更为优选,所述的惰性气体选自氮气或氦气,惰性气体中水分含量小于或等于200ppm。最为优选,所述的惰性气体选自氮气,氮气中水分含量小于或等于100ppm。
[0038]
作为优选,所述的甲苯中含水量小于500ppm,更为优选小于200ppm,最为优选小于100ppm。
[0039]
作为优选,所述的三乙胺中含水量小于500ppm,更为优选小于200ppm,最为优选小于100ppm。
[0040]
步骤(4)、retro diels-alder反应制备α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基))硅氧烷共聚物
[0041]
常温和干燥的惰性气体保护下将化合物b、顺丁烯二酸酐、五氧化二磷、对苯二酚、对二甲苯加入到干燥的反应容器中,采用干燥的so2气体抽换气3次后,在干燥的惰性气体保护下于一定温度下回流反应一段时间。冷却至常温后,过滤,将收集的滤液旋蒸除去溶剂后,得到淡黄色粘稠状的化合物c,也就是α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷液体,即α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物;其合成路线如下:
[0042]
作为优选,所述的蒽保护的α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷与顺丁烯二酸酐的摩尔比为0.1~2.0:1,更为优选为0.25~1.5:1,最为优选为0.4~1.0:1。
[0043]
作为优选,所述的蒽保护的α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷与五氧化二磷的质量比为5~200:1,更为优选为10~150:1,最为优选为20~100:1。
[0044]
作为优选,所述的蒽保护的α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷与对苯二酚的质量比为3~100:1,更为优选为5~80:1,最为优选为10~50:1。
[0045]
作为优选,所述的蒽保护的α-氰基丙烯酰氧乙基氧丙基官能化的聚硅氧烷与对二甲苯的质量比为0.01~0.40:1,更为优选为0.03~0.35:1,最为优选为0.05~0.30:1。
[0046]
作为优选,所述的回流反应温度为130~160℃,反应时间为2.0~24.0h。更为优选,所述的回流反应温度为135~155℃,反应时间为3.0~20.0h。最为优选,所述的回流反应温度为140~150℃,反应时间为4.0~15.0h。
[0047]
作为优选,所述的惰性气体选自氮气、氦气或氩气中的一种或几种,惰性气体中水分含量小于或等于500ppm。更为优选,所述的惰性气体选自氮气或氦气,惰性气体中水分含量小于或等于200ppm。最为优选,所述的惰性气体选自氮气,氮气中水分含量小于或等于100ppm。
[0048]
作为优选,所述的so2气体中水分含量小于或等于500ppm,更为优选小于或等于200ppm,最为优选小于或等于100ppm。
[0049]
作为优选,所述的对二甲苯中含水量小于500ppm,更为优选小于200ppm,最为优选
小于100ppm。
[0050]
本发明的又一个目的是提供上述有机硅材料在无催化剂、常温条件下实现与空气中水分交联固化上的应用。
[0051]
作为优选,还可以加入促进剂有机胺。
[0052]
更为优选,促进剂为n,n-二甲基对苯甲胺。
[0053]
与现有技术相比,本发明的有益效果是:
[0054]
(1)本发明制备得到的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物在常温下与空气中水分接触后即可自然交联固化,最短固化时间为3min,加入少量的有机胺固化时间最短可缩短至3s,且交联固化过程不需要升温温度,也不需要加入其它的催化剂,尤其是铂等贵金属催化剂或有机锡、有机钛酸酯等对环境存在危害的金属催化剂,在快速定型和快速粘接等相关领域具有广阔的应用前景。
[0055]
(2)有机硅材料表面的水/空气接触角为102
°
,而本发明制备工艺可实现α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的水/空气接触角为65~85
°
可调,具有亲水性,拓宽有机硅聚合物材料的应用范围。
附图说明
[0056]
图1为实施例1制备的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物样品的1hnmr谱图;
[0057]
图2为实施例1制备的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物样品的
13
c nmr谱图;
[0058]
图3为实施例17制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的1h nmr谱图;
[0059]
图4为实施例17制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的
13
c nmr谱图;
[0060]
图5实施例19制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的1h nmr谱图;
[0061]
图6为实施例20制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的固化图片;其中a.未处理淡黄色粘稠液体,b.滴加一滴dmt,c.搅拌1s,d.搅拌3s;
[0062]
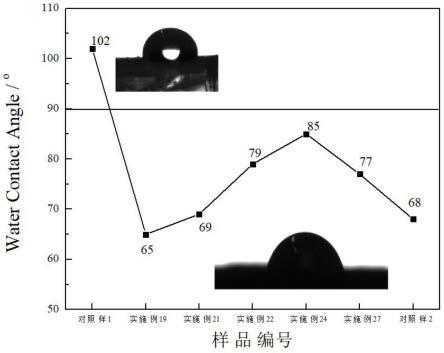
图7为聚二甲基硅氧烷(对照样1)、聚α-氰基丙烯酸乙酯(对照样2)及α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物固化后的水接触角。
具体实施方式
[0063]
下面通过实施例对本发明作进一步详细说明,但实施例不是对本发明保护范围的
限制,实施例中所用原料均可市购或采用常规方法制备。
[0064]
实施例1
[0065]
在干燥且充满n2的三口烧瓶内,加入4.60g(0.045mol)的羟乙基烯丙基醚,20ml甲苯和0.2371g pt含量为0.1wt%的karstedt催化剂,开启搅拌,在70℃下活化30min。将市售含氢量为0.15wt%、25℃粘度为45cp的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物20.0g(含si-h 0.030mol)经2h通过注射泵匀速滴加到反应体系中。加料完毕后再在70℃下继续反应3h,脱除溶剂和低沸物后,得到α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物20.25g,收率为87.8%,其核磁氢谱(1h nmr)如附图1所示,核磁碳谱(
13
c nmr)如附图2所示。1h nmr(400mhz,chloroform-d):δ=3.66ppm(q,j=4.6hz,2h),δ=3.46ppm(q,j=4.9hz,2h),δ=3.37ppm(td,j=7.0,4.7hz,2h),δ=1.79ppm(s,2h),δ=1.61
–
1.41ppm(m,1h),δ=0.63
–
0.31ppm(m,2h),δ=0.00ppm(d,j=2.5hz,56h);
13
c nmr(101mhz,chloroform-d):δ=77.70
–
74.77ppm,δ=73.55
–
69.26ppm,δ=60.78ppm,δ=22.23ppm,δ=12.73ppm,δ=0.03ppm。
[0066]
实施例2~实施例9
[0067]
改变α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物的结构参数和用量,代替实施例1使用的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物,按实施例1类似方法制备得到其他规格的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物,实施例2~实施例9所用原料及所得结果如表1所示。其中pdms-h代表α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物。
[0068]
表1实施例2~实施例9投料及反应结果
[0069][0070]
实施例10
[0071]
在氮气保护下的50ml三口烧瓶内加入1.15g(0.0039mol)蒽保护的α-氰基丙烯酰氯加合物,再加入10ml甲苯进行溶解。将实施例1制备的2.50g(0.0033mol)α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物与10ml甲苯和0.49g(0.0048mol)三乙胺混合均匀后,采用注射泵经30min滴加至蒽保护的α-氰基丙烯
酰氯加合物的甲苯溶液中。滴加完毕后再在常温(25℃)下反应3h。抽滤除去固体残留物,将收集的滤液旋蒸除去溶剂后得到2.32gα,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物。
[0072]
实施例11~实施例18
[0073]
分别采用实施例2~实施例9制备的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物代替实施例10所使用的实施例1制备的α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物,调整各反应物料的用量,按实施例10类似的步骤,制备得到实施例11~实施例18所述的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物,结果列于表2中。其中“甲苯1”表示在反应容器中溶解蒽保护的α-氰基丙烯酰氯加合物所使用的甲苯;“甲苯2”表示与α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物及三乙胺混合时所使用的甲苯;pdms-oh代表α,ω-双端二甲基羟乙基氧丙基硅氧基封端的聚(二甲基-甲基(羟乙基氧丙基))硅氧烷共聚物。
[0074]
表2实施例11~实施例18投料及反应结果
[0075][0076][0077]
实施例17制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物的1h nmr谱图如附图3所示,其
13
c nmr谱图如附图4所示。1h nmr(400mhz,chloroform-d):δ=7.48
–
6.82ppm(m,13h),δ=4.84ppm(d,j=15.6hz,2h),δ=4.51
–
4.24ppm(m,2h),δ=4.21
–
4.01ppm(m,3h),δ=3.46ppm(s,5h),δ=3.34ppm(s,3h),δ=2.88ppm(q,j=7.3hz,3h),δ=2.79
–
2.55ppm(m,2h),δ=2.28ppm(s,1h),δ=2.11ppm(dd,j=12.9,2.8hz,1h),δ=1.71
–
1.44ppm(m,3h),δ=0.48ppm(s,h),δ=0.12
–‑
0.18ppm(m,21h)。
[0078]
实施例19
[0079]
在常温和干燥氮气保护下,将2.32g实施例10制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物(蒽保护基团的物质的量为0.0023mol),0.4118g(0.0042mol)顺丁烯二酸酐,0.0412g五氧化二磷,0.08237g对苯二酚及30ml对二甲苯加入到100ml的三颈圆底烧瓶中。整个体系经so2抽换气3次后,在n2氛围下,升温至140℃并在此温度下回流10h。冷却至常温后过滤,收集滤液,旋蒸除去溶剂后,得到1.74g淡黄色粘稠液体,其1h nmr谱图如附图5所示。1h nmr(400mhz,chloroform-d):δ=7.06
–
6.93ppm(m,1h),δ=6.64ppm(s,1h),δ=4.36ppm(d,j=4.0hz,1h),δ=3.64ppm(q,j=5.1hz,1h),δ=3.37ppm(td,j=7.0,5.1hz,1h),δ=1.58ppm(ddt,j=28.6,11.0,5.8hz,2h),δ=0.94
–
0.66ppm(m,2h),δ=0.36
–‑
0.18ppm(m,43h)。
[0080]
实施例20~实施例27
[0081]
分别采用实施例11~实施例18制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物代替实施例19所使用的实施例10制备的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物,调整各反应物料的用量,按实施例19类似的步骤,制备得到实施例20~实施例27所述的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物,结果列于表3中。其中“pdms-en”代表实施例11~实施例18制得的α,ω-双端二甲基-蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(蒽保护的α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物。
[0082]
表3实施例20~实施例27投料及反应结果
[0083][0084]
应用效果测试:
[0085]
(1)25℃及相对湿度60%条件下固化实验
[0086]
(1.1)自然固化实验
[0087]
分别取实施例19~实施例27制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物各0.5g放置在9个洁净的培养皿中,在25℃及相对湿度60%的条件下,采用针尖触碰各样品表面及内部,测定其完全固化所需时间,结果如表4所示。
[0088]
表4各样品固化时间测定结果(25℃,相对湿度60%)
[0089][0090][0091]
(1.2)n,n-二甲基对苯二胺促进下的固化实验
[0092]
分别取实施例19~实施例27制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物各0.5g放置在9个洁净的培养皿中,分别向每个样品中滴加0.05ml的n,n-二甲基对苯二胺,迅速混合均匀后,在25℃及相对湿度60%的条件下,采用针尖触碰各样品表面及内部,测定其完全固化所需时间,结果如表5所示。其实施例20制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物在n,n-二甲基对苯二胺(dmt)促进下的固化过程如附图6所示。
[0093]
表5 n,n-二甲基对苯二胺促进下各样品固化时间测定结果(25℃,相对湿度60%)
[0094][0095]
(2)水接触角测试
[0096]
对照样1的制备
[0097]
取68.0544gα,ω-二甲基乙烯基封端的聚二甲基硅氧烷(η
25
=3000mpa
·
s)和1.3823g含氢量为0.44%的α,ω-二甲基封端的聚(二甲基-甲基氢)硅氧烷共聚物放于100ml纸杯中,加入0.0129g pt的质量含量为0.1wt%的karstedt催化剂,样品混合均匀后置于真空烘箱中于120℃加热固化2h,制备得到无色透明的硅凝胶(对照样1)。
[0098]
对照样2的制备
[0099]
将2.5gα-氰基丙烯酸乙酯放置在培养皿中,放入常温(25℃)及相对湿度60%的恒温恒湿箱中,24h后取出,制备得到无色透明坚硬的聚α-氰基丙烯酸乙酯(对照样2)。
[0100]
空气/水接触角测试
[0101]
采用德国kruss公司生产的kruss dsa30水接触角测试仪,测试各固化样品光滑表
面的水接触角,在每个样品的不同位置测量5次水接触角数值,取平均值后进行比较。
[0102]
水接触角测量仪测试纯pdms样品(对照样1)、聚α-氰基丙烯酸乙酯(对照样2)及实施例19、实施例21、实施例22、实施例24和实施例27制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物固化产物样品的水接触角,结果如附图7所示。由附图7可见,纯pdms样品(对照样1)的水接触角为102
°
,表明其具有疏水性,聚α-氰基丙烯酸乙酯样品的水接触角为68
°
,具有亲水性,本发明实施例19、实施例21、实施例22、实施例24和实施例27制备的α,ω-双端二甲基-α-氰基丙烯酰氧乙基氧丙基硅氧基封端的聚(二甲基-甲基(α-氰基丙烯酰氧乙基氧丙基硅氧基))硅氧烷共聚物固化产物样品的水接触角分别为65
°
、69
°
、79
°
、85
°
及77
°
,均小于90
°
,表明在聚硅氧烷分子中引入氰基丙烯酰氧基官能团,不仅赋予聚硅氧烷具备快速交联固化的特性,而且引入氰基丙烯酰氧基官能团可将聚硅氧烷由疏水材料转变为亲水材料。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1