一种培养复发膀胱癌活检样本类器官的培养基及其培养方法与流程
1.本发明涉及细胞培养领域,具体的涉及一种复发性膀胱癌类器官的培养基及其培养方法。
背景技术:
2.膀胱癌是影响人类健康和生存,加重居民经济负担的重要瘤种。目前膀胱癌新发病例数全球每年约57万余例,位居所有肿瘤第12位;全球每年因膀胱癌致死病例数约21万余例,位居所有肿瘤第14位。经过各种手段综合治疗后的膀胱癌患者5年生存率高达77%,其中膀胱原位癌、局部、区域和远处转移患者的5年生存率分别为96%,69%,37%和6%。影响膀胱癌患者生存和预后的最重要因素是初次治疗后的肿瘤复发,膀胱癌的复发与初诊肿瘤分期有关:原位癌或非浸润性癌的5年复发率约为65%,进展期患者复发率高达73%。膀胱癌复发后的治疗相较初诊时难度增加较大,且往往治疗效果欠佳。
3.如何进一步改善复发性膀胱癌的治疗效果是膀胱癌治疗领域的重点和难点,其中肿瘤个体化治疗(精准治疗)是重要的潜在方向。肿瘤类器官作为新兴的肿瘤体外模型,有望为复发性膀胱癌精准治疗提供可靠帮助。
4.肿瘤类器官(tumor organoid)则一般是指由肿瘤患者肿瘤组织体外培养而来的类器官。肿瘤类器官能在病理形态、基因变异、染色体稳定性和肿瘤异质性等方面忠实模拟对应患者体内肿瘤,因此肿瘤类器官是指导肿瘤精准治疗的绝佳工具。目前原发膀胱癌类器官培养体系已成功建立,美国哥伦比亚大学医学中心的suk hyung lee等成功培养原发膀胱癌类器官并证明其是模拟肿瘤进化和预测药物疗效的可靠工具。然而迄今为止原发膀胱癌类器官的培养成功率尚且不高,培养经验最丰富的研究者成功率可达70%左右,一般技术人员的成功率只有30%左右。导致培养成功率较低的原因很多,培养基缺陷是其中最关键的原因。
5.复发性肿瘤的肿瘤类器官培养难度较原发肿瘤更大,若采用原发肿瘤类器官培养基培养成功率极低,这是类器官学术界和产业界共识性难题。因此复发性膀胱癌的肿瘤类器官培养是一大挑战,目前尚未见到相关成功研究被报道。这对肿瘤类器官指导复发性膀胱癌精准治疗造成明显障碍。
6.本发明要解决的技术问题是在充分了解复发性膀胱癌分子生物学和以往丰富的类器官培养经验基础上,开发了针对复发性膀胱癌高度异质性的多种不同组分培养基,解决了复发性膀胱癌肿瘤类器官的培养成功率低下的难题,为肿瘤类器官用于指导复发性膀胱癌精准治疗打下了坚实基础。
技术实现要素:
7.本发明的目的在于,提供一种适宜复发性膀胱癌类器官培养的培养基及其培养方法,进而获得复发性膀胱癌类器官,以便为复发性膀胱癌的病程发展以及抗癌药物的筛选提供有利条件。
8.为解决上述技术问题,本发明提供一种复发性膀胱癌的类器官培养基,所述培养基成分包括如下成分:
9.高糖dmem培养基,f12k培养基,抗坏血酸,l-谷氨酸,亚硒酸钠,乙醇胺盐酸盐,偏钒酸铵,四水合氯化锰,n2,b27,谷氨酰胺补剂,hepes,烟酰胺,normocin
tm
,n-乙酰半胱氨酸,r-spondin 1,noggin。
10.优选的,所述培养基中高糖dmem培养基和f12k培养基的比例为1-2:1。
11.优选的,所述培养基中l-谷氨酸的浓度为1-100mg/l。
12.优选的,所述培养基中亚硒酸钠的浓度为0.002-0.5mg/l。
13.优选的,所述培养基中乙醇胺盐酸盐的浓度为2-200mg/l。
14.优选的,所述培养基中偏钒酸铵的浓度为1
×
10-4-20
×
10-4
mg/l。
15.优选的,所述培养基中四水合氯化锰的浓度为5
×
10-5-50
×
10-5
mg/l。
16.优选的,所述培养基中r-spondin 1的浓度为50-1000ng/ml。
17.优选的,所述培养基中noggin的浓度为10-200ng/ml。
18.优选的,所述培养基中n2:b27的规格为0.1-2。
19.优选的,所述培养基中谷氨酰胺补剂规格为1
×
。
20.优选的,所述培养基中hepes的规格为1
×
。
21.优选的,所述培养基中normocin
tm
的规格为1
×
。
22.优选的,所述培养基中烟酰胺的浓度为1-100mm。
23.优选的,所述培养基中n-乙酰半胱氨酸的浓度为0.1-10mm。
24.优选的,所述培养基中还包括a83-01,进一步优选的,所述a83-01浓度为0.1-50μm。
25.优选的,所述培养基中还包括hgf,进一步优选的,所述hgf浓度为5-500ng/ml。
26.优选的,所述培养基中还包括chir99021,进一步优选的,所述chir99021浓度为1-100μm。
27.优选的,所述培养基中还包括dmso,进一步优选的,所述dmso浓度为培养基体积比的0.01-2%。
28.本发明另一方面,提供了一种培养基培养复发性膀胱癌细胞获得膀胱癌类器官的培养方法,包括使用上述培养基以及优选的组分选择性的添加,能够对多种的复发性膀胱癌实现类器官培养。
29.具体的,所述方法如下:
30.1.获得临床复发膀胱癌活检样本(直径3-5mm),4℃保存于专用保存液中,24小时内低温转移至操作室;
31.2.样本冰pbs清洗3-5次,低温切成1mm碎片,酶解消化;
32.3.样本消化完全后,添加与消化液同体积的冰pbs,反复吹打直至不见碎片组织,细胞筛网过滤;
33.4.低温离心去除上清,冰浴加入红细胞裂解液去除红细胞;
34.5.待裂解操作完成后,低温离心去除上清,冰pbs重悬,重复3-5次;
35.6.低温离心去除上清,依据获得细胞情况,1-5ml冰pbs重悬后显微镜下计数细胞;
36.7.低温离心去除上清,依据细胞计数加入适量冰matrigel重悬接种于24孔板,加
入膀胱癌培养液,每3天更换一次相应培养液;
37.8.肿瘤类器官培养12-18天后,每孔添加1ml冰pbs,反复吹打,移入15ml离心管;
38.9.低温离心去除上清,冰pbs重悬,重复3-5次,直至matrigel全部清除;
39.10.离心结束后,冰matrigel重悬,1:3接种扩增,待肿瘤类器官稳定传代后,重复步骤9,一半类器官做药物敏感性实验,一半类器官用细胞冻存液冻存。
40.优选的,步骤2中,所述酶解消化条件为:37℃,胶原酶消化30-60min;
41.优选的,步骤3中,细胞筛网过滤操作中,筛网孔径为100μm;
42.优选的,步骤4-9中,低温离心去除上清的操作中,离心转速为70-300g,离心时间为5-10min;
43.优选的,步骤7中,matrigel重悬调整细胞浓度,1000-2000/50μl接种入24孔板,待matrigel凝固后加入相应的培养基。
44.第三方面,本发明公开了一种利用上述培养基进行膀胱癌类器官模型的制备,通过制备得到的膀胱癌类器官模型,能够更直观的展示膀胱癌原发病理机制以及癌细胞的侵袭机制。并且,所述模型还能够用于筛选治疗膀胱癌的药物。
45.本发明和现有技术相比,具有以下有益效果:
46.本发明公开的培养基可以进行组分的调整,能够对异质性差异巨大的复发性膀胱癌的类器官进行培养,并且培养基成本低,来源稳定可靠,为后续了解膀胱癌发病机制以及筛选药物奠定了基础。
附图说明
47.图1为不同培养基培养复发性膀胱癌类器官成功率比较。
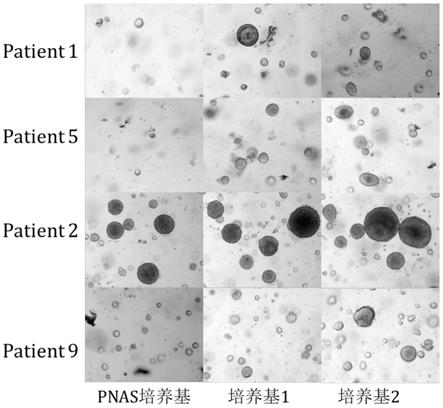
48.图2为pnas培养基和两种优化后的改良培养基培养复发性膀胱癌获得的类器官。
具体实施方式
49.下面将结合示意图对本发明公开的培养基以及培养方法进行更详细的描述,其中表示了本发明的优选实施例,应该理解本领域技术人员可以修改在此描述的本发明,而仍然实现本发明的有利效果。因此,下列描述应当被理解为对于本领域技术人员的广泛知道,而并不作为对本发明的限制。
50.对于培养基组分,可通过市售获得,规格和来源具体如下:
51.高糖dmem培养基,f12k培养基,抗坏血酸(a103539,aladdin),l-谷氨酸(g6013,sigma),亚硒酸钠(s5261,sigma),乙醇胺盐酸盐(e120635,aladdin),偏钒酸铵(a111829,aladdin),四水合氯化锰(m112543,aladdin),n2(gibco),b27(gibco),谷氨酰胺补剂(gibco),hepes(gibco),烟酰胺(sigma),normocin
tm
(invivogen),n-乙酰半胱氨酸(sigma),r-spondin 1(sinobiological),noggin(sinobiological),a83-01(tocris),egf(prerotech),fgf10(prerotech),肝素(sigma),hgf(prerotech),dmso(sigma),chir99021(tocris)。
52.实施例改良培养基
53.为了实现对多种异质性复发性膀胱癌的类器官培养,并且寻找能够替代advance dmem/f12培养基的其他培养基组分以期能够降低培养基整体成本,本发明对培养复发性膀
胱癌类器官培养基进行筛选和优化,最终确定了如下组分:
54.高糖dmem/f12k培养基(1-2:1),抗坏血酸1-100mg/l,l-谷氨酸1-100mg/l,亚硒酸钠(0.002-0.5mg/l),乙醇胺盐酸盐(2-200mg/l),偏钒酸铵(1
×
10-4-20
×
10-4
mg/l),四水合氯化锰(5
×
10-5-50
×
10-5
mg/l)、r-spondin1(50-1000ng/ml),noggin(10-200ng/ml),n2:b27(0.1-2),谷氨酰胺补剂(1
×
),hepes(1
×
),烟酰胺(1-100mm),normocin
tm
(1
×
),n-乙酰半胱氨酸(0.1-10mm);a83-01(0.1-50μm),egf(1-200ng/ml),fgf10(1-100ng/ml),肝素(10-200iu/ml);hgf(50-500ng/ml),dmso(0.01-2%),chir99021(1-100μm)。
55.实施例1、改良培养基1
56.dmem/f12k培养基(1:1),抗坏血酸(10mg/l),l-谷氨酸(50mg/l),亚硒酸钠(0.05mg/l),乙醇胺盐酸盐(20mg/l),偏钒酸铵(5
×
10-4
mg/l),四水合氯化锰(7
×
10-5
mg/l),r-spondin 1(200ng/ml),noggin(20ng/ml),n2:b27(1:1),谷氨酰胺补剂(1
×
),hepes(1
×
),烟酰胺(20mm),normocin
tm
(1
×
),n-乙酰半胱氨酸(2mm),a83-01(10μm),egf(100ng/ml),fgf10(20ng/ml),肝素(100iu/ml)。
57.实施例2、改良培养基2。
58.dmem/f12k培养基(2:1),抗坏血酸(2mg/l),l-谷氨酸(100mg/l),亚硒酸钠(0.1mg/l),乙醇胺盐酸盐(50mg/l),偏钒酸铵(20
×
10-4
mg/l),四水合氯化锰(15
×
10-5
mg/l);r-spondin 1(500ng/ml),noggin(50ng/ml),n2:b27(1:2),谷氨酰胺补剂(1
×
),hepes(1
×
),烟酰胺(5mm),normocin
tm
(1
×
),n-乙酰半胱氨酸(2mm),hgf(100ng/ml),dmso(1%,v/v),chir99021(50μm)。
59.实施例3、两种改良培养基和原发膀胱癌(pnas)培养复发性膀胱癌类器官比较
60.为了验证改良后的培养基对类器官的培养效果,将上述实施例1-2中改良的培养基与现有技术中的pnas培养基进行比较,除培养基组成不同外,其他培养条件完全一致,观察复发膀胱癌类器官的生长状况。
61.其中,原发膀胱癌(pnas)培养基成分组成如下:
62.advance dmem/f12培养基,b27(1
×
),烟酰胺10mm,n-乙酰半胱氨酸(1.25mm),a83-01(5μm),fgf2(12.5ng/ml),fgf7(25ng/ml),fgf10(100ng/ml),y27632(10μm)。
63.取9例复发性膀胱癌活检样本(patient1-9),分别用改良后的培养基(1,2)和pnas培养基培养12-18天,具体操作如下:
64.复发膀胱癌活检样本(直径3-5mm),4℃保存于专用保存液中,24小时内低温转移至操作室;
65.1.样本冰pbs清洗3-5次,每次5min;
66.2.样本低温切成1mm碎片入37℃预热胶原酶消化液中,消化30-60min;
67.3.样本消化完全后,添加与消化液同体积的冰pbs,反复吹打直至不见碎片组织,100μm细胞筛网过滤;
68.4. 100g低温离心5-10min,去除上清,无菌红细胞裂解1ml冰上5min,5ml冰pbs终止裂解;
69.5. 70g低温离心5-10min,去除上清,冰pbs重悬,此过程重复3-5次;
70.6. 200g低温离心10min,去除上清,依据获得细胞情况,1-5ml冰pbs重悬后显微镜下计数细胞;
71.7. 300g低温离心10min,去除上清,依据细胞计数加入适量冰matrigel重悬接种于24孔板,加入膀胱癌培养液,每3天更换一次相应培养液;
72.8.肿瘤类器官培养9-18天后,每孔添加1ml冰pbs,反复吹打,移入15ml离心管;
73.9. 300g低温离心10min,去上清,冰pbs重悬,此步骤重复3-5次,直至matrigel全部清除
74.10.离心结束后,冰matrigel重悬,1:3接种扩增,待肿瘤类器官稳定传代后,重复步骤10,一半类器官做药物敏感性实验,一半类器官用细胞冻存液冻存。
75.结果
76.9例复发膀胱癌活检样本中,培养基1和2成功培养6例(p1-3,p5,p7,p9)和7例(p1-2,p4-5,p7-9)复发膀胱癌类器官,相同培养时间段,pnas培养基成功培养2例(p2,p9)复发膀胱癌类器官。在复发膀胱癌培养基(1,2)中,活检样本一般培养9-12天即可首次传代,在pnas培养基中,活检样本需要14-18天才可以进行首次传代。复发膀胱癌培养基(1,2)的培养成功率分别为66.7%(6/9)和77.8%(7/9),pnas培养基成功率则为22.2%(2/9)。
77.已报道的原发膀胱癌培养基不太适合复发膀胱癌类器官的培养,本发明膀胱癌培养基针对复发膀胱癌有较高的类器官培养成功率和相对较短的类器官培养时间(图1,2)。
78.显然,本领域的技术人员可以对本发明进行各种改动和变型而不脱离本发明的精神和范围。这样,倘若本发明的这些修改和变型属于本发明权利要求及其等同技术的范围之内,则本发明也意图包含这些改动和变型在内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1