一种含7-氨基香豆素结构基团的荧光化合物
1.本发明属于荧光化合物技术领域,具体涉及一种含7-氨基香豆素结构基团的荧光化合物。
背景技术:
2.p-糖蛋白(p-glycoprotein,p-gp)是一种分子量170kd的跨膜糖蛋白,它具有能量依赖性"药泵"功能,使细胞内药物泵出细胞外,减低了细胞内的药物浓度,使细胞产生耐药性。p-gp的存在影响了大量治疗药物的吸收分布,包括抗癌药物、抗病毒药物、抗组胺药、抗癫痫药和镇痛药。
3.目前,对p-gp的成像主要通过正电子发射计算机断层扫描(positron emissiontomography,pet)技术。其中用于研究p-gp功能的pet示踪剂是用同位素标记的p-gp底物,如[
11
c]维拉帕米,[
11
c]洛培酰胺,[
11
c]秋水仙碱,[
11
c]卡维地洛,[
64
cu]配合物,[
68
ga]配合物和[
99m
tc]配合物等,由于其低基线脑吸收,它们仅被用于监测帕金森和阿尔兹海默病患者p-gp的下降,不能用于观察患者p-gp的增加。少量的同位素标记的p-gp抑制剂,如[
11
c]elacridar、[
11
c]laniquidar和[
11
c]tarquidar也被研究用于p-gp表达成像,但其实际效果仍待进一步考察。
[0004]
此外,pet技术检查费用相对较高,并且受检者安全保障、同期使用药物对pet的影响等对实际操作与结果可信性带来困难。
技术实现要素:
[0005]
针对现有技术中的不足与难题,本发明旨在提供一种含7-氨基香豆素结构基团的荧光化合物,开发了可视性p-gp示踪剂,对肿瘤、癫痫等疾病的p-gp组织高表达区定位、细胞内p-gp定位及其研究的可视性等问题提供了新的视角和选择。采用计算机辅助药物设计、荧光量子产率测定、细胞毒性实验、细胞和组织成像评价等方法,证实了化合物出色的p-gp共定位能力和安全性。
[0006]
本发明通过以下技术方案予以实现:
[0007]
本发明提供一种含7-氨基香豆素结构基团的荧光化合物,其为7-氨基香豆素报告基团通过2-甲酰胺-4,5-二甲氧基苯甲酰胺连接2-(6,7-二甲氧基-3,4-二氢-1h-异喹啉-2-基)苯乙基结合基团形成的7-氨基香豆素类荧光化合物,其结构式如下式(1)所示:
[0008][0009]
所述7-氨基香豆素类荧光化合物用于p-gp特异性荧光探针。
[0010]
与现有技术相比,本发明有益效果包括:
[0011]
1、本发明开发了一种7-氨基香豆素类荧光化合物作为p-gp特异性荧光探针,这些荧光探针能够可靠地用于p-gp的定位示踪,具有特异性高、灵敏度高、安全性好的优点;对肿瘤、癫痫等疾病的p-gp组织高表达区定位、细胞内p-gp定位及其研究的可视性等问题提供了新的视角和选择。
[0012]
2、本发明采用p-gp特异性示踪剂荧光显像,与目前使用的pet示踪剂相比,无放射性伤害,安全性高,仅需荧光成像仪辅助操作,且结果分析简便直观。
附图说明
[0013]
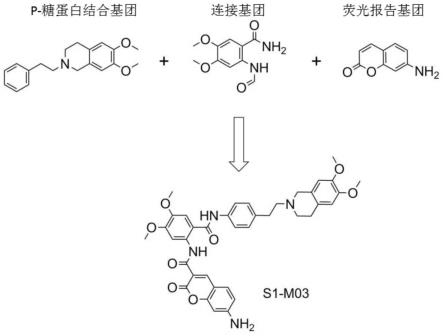
图1为本发明荧光化合物的设计图;
[0014]
图2为本发明荧光化合物s1-m03合成路线图;
[0015]
图3为本发明荧光化合物s1-m03紫外吸收曲线图;
[0016]
图4为本发明荧光化合物s1-m03的荧光强度曲线图;
[0017]
图5为本发明荧光化合物s1-m03的细胞存活曲线图;
[0018]
图6为本发明荧光化合物s1-m03与p-gp共定位成像;
[0019]
图7为本发明荧光化合物s1-m03肝脏切片染色。
具体实施方式
[0020]
下面结合附图,对本发明作进一步地说明。
[0021]
实施例1荧光化合物的设计与合成
[0022]
如图1所示,s1-m03为7-氨基香豆素报告基团通过2-甲酰胺-4,5-二甲氧基苯甲酰胺连接2-(6,7-二甲氧基-3,4-二氢-1h-异喹啉-2-基)苯乙基结合基团形成的7-氨基香豆素类荧光化合物。
[0023]
为确定设计的小分子是否能与p-gp结合及其在实际应用中的可能性,我们采用加拿大化学计算集团公司开发的化学计算及分子模拟软件moe进行了理化性质和分子对接计算。
[0024]
结果显示,s1-m03具有良好的预测结合能力及适宜的理化性质,具体结果如下表1所示,荧光化合物s1-m03对接评分为-16.2382kcal/mol,表现出较高的p-gp结合能力,且具有较好的理化性质,其log p(o/w)为4.49,分子量为678.74,适合动物应用。
[0025]
表1 s1-m03的理化性质及对接得分
[0026]
compoundlogp(o/w)mol.weights(kcal/mol)s1-m034.49678.74-16.2382
[0027]
7-氨基香豆素荧光化合物以对硝基苯乙基溴、盐酸
‑‑
1,2,3,4-四氢-6,7-二甲氧基异喹啉、4,5-二甲氧基-2-硝基-苯甲酸、2-羟基-4-甲基-苯甲醛、2,2-二甲基-1,3-二恶烷-4,6-二酮等为原料,经多步有机反应生成。具体合成路线如图2所示。
[0028]
实施例2荧光化合物s1-m03的相关光学性质测定
[0029]
化学合成s1-m03后进行了荧光性质测定
[0030]
(一)紫外吸光度的测量
[0031]
标准物质香豆素-153(coumarin-153,c-153)溶于无水乙醇中,化合物s1-m03溶于dmso中,样品浓度均为30μm。检测吸光度用日本shimadzu公司生产的紫外-可见光分光光度计uv-2450检测,结果如图3所示,s1-m03的最大吸收波长为410-413nm,吸光度为0.200。
[0032]
(二)荧光光谱的测量
[0033]
首先用上述测量紫外吸光度的最大吸收波长作为固定的发射波长,扫描出激发曲线,得到最大激发波长,再用最大激发波长作为固定激发波长,扫描出发射曲线,得到最大发射波长。化合物的激发曲线和发射曲线用日本hitachi公司生产的荧光光谱仪f-7000fl spectrophotometer检测。调整ex slit:10.0nm or 5.0nm,em slit:10.0nm or 5.0nm,pmt voltage:400v,结果如图4所示,s1-m03的最大激发波长为428nm,最大发射波长为494nm。
[0034]
(三)绝对量子产率的测量
[0035]
化合物的绝对量子产率用日本horiba公司生产的稳态-瞬态荧光光谱仪fluoromax-4-tcspc检测,选择合适的激发波长范围和发射波长范围拟合量子产率曲线,得到绝对量子产率,由绝对量子产率可以计算出化合物相对于c-153(香豆素153)的量子产率。其中对照品c-153用无水乙醇校正,荧光化合物用dmso校正,结果如表2所示。
[0036]
表2 s1-m03的量子产率
[0037][0038]
实施例3荧光化合物的细胞毒性检测
[0039]
通过噻唑蓝(mtt)实验进行了化合物细胞毒性检测。
[0040]
1、取对数生长期细胞,离心收集后,用完全培养基重悬,制成单细胞悬液,调整细胞浓度至1.5
×
10^4个/ml,96孔板每孔加入200ul细胞悬液。
[0041]
2、实验组分别于铺板后24h分别加入化合物,浓度梯度为100nm,200nm,1μm,2μm,10μm。37℃,5%co2条件下继续培养2-3天。
[0042]
3、吸除培养液,加5mg/ml mtt 10ul,再继续培养4小时,吸除mtt,加入dmso 100ul,于492nm波长下检测吸光度。同时设置调零孔(培养基、mtt、二甲基亚砜)。
[0043]
4、结果如图5所示,在含100nm,200nm,1μm,2μm,10μm浓度的s1-m03培养基溶液中
细胞存活率皆在75%以上,安全性较高。
[0044]
实施例4荧光化合物s1-m03的应用
[0045]
在具体实施中,荧光化合物s1-m03作为p-糖蛋白示踪剂。
[0046]
(一)s1-m03在llc-pk1-mdr1-apple细胞内与p-糖蛋白的共定位情况,如图6所示。
[0047]
1、llc-pk1-mdr1-apple细胞为转染mdr1-apple(apple为红色荧光标记)后的细胞。实验前两天将llc-pk1-mdr1-apple细胞种植于24孔板的爬片上;
[0048]
2、给药前用pbs将细胞洗1遍,每孔加入150μl的化合物(5μm);
[0049]
3、放入孵箱内培养1h后,用pbs将细胞洗2遍,取出爬片,将爬片覆盖在滴有抗荧光淬灭封片剂的载玻片上,指甲油固定,在488nm(绿色),568nm(红色)通道下激发,在日本nicon公司生产的激光扫描共聚焦显微镜a1r hd25下60倍油浸物镜成像。
[0050]
4、结果显示,s1-m03与p-糖蛋白荧光位置一致,s1-m03具有定位p-糖蛋白的能力。
[0051]
(二)检测荧光化合物s1-m03化合物在离体肝脏切片中与p-糖蛋白的结合情况,如图7所示。
[0052]
1、将肝脏冠状面进行冰冻切片,切片厚度15μm,切片粘附于载玻片上;
[0053]
2、用组化笔在组织周围画圈,实验组和对照组分别滴加化合物(5μm);
[0054]
3、孵育30min后用tbs洗两遍,在荧光倒置显微镜ti(日本尼康)10倍物镜下拍摄5个切片视野(图7a仅为一个代表性视野),使用的滤光片为ecfp。
[0055]
4、使用image pro plus 6.0对拍摄的荧光图片计算荧光化合物结合面积占总面积的比值,用graphpad prism6.01统计化合物在对照组和mdr1组小鼠肝脏组织切片结合面积比,数据采用multiple t test-one per row方法分析,mean
±
sem处理,结果显示,两组进行统计分析后,p《0.0001,可认为s1-m03在人源p-糖蛋白高表达组(mdr1++组)中染色荧光明显多于对照组,即s1-m03在肝脏中可特异性靶向p-糖蛋白。
[0056]
综上所述,化合物s1-m03对接评分为-16.2382kcal/mol,表现出较高的p-糖蛋白结合能力,且具有较好的理化性质,其log p(o/w)为4.49,分子量为678.74,适合动物活体应用。化学合成s1-m03后,进行了荧光性质测定和细胞毒性检测。在llc-pk1-mdr1-apple细胞中,化合物与p-糖蛋白共定位效果良好,且在组织水平上,高表达p-糖蛋白组中化合物的积累量均大于对照组,说明化合物特异性靶向p-糖蛋白,进一步验证了荧光探针对p-糖蛋白的定位能力。
[0057]
以上所述仅表达了本发明的优选实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形、改进及替代,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1