一种用于胃癌的诊断和预后监测的血浆外泌体circRNA标志物及其应用
一种用于胃癌的诊断和预后监测的血浆外泌体circrna标志物及其应用
技术领域
1.本发明属于分子诊断技术领域,具体涉及一种用于胃癌的诊断和预后监测的血浆外泌体circrna标志物及其应用。
背景技术:
2.胃癌(gastric cancer,gc)是世界范围内最常见的一种恶性肿瘤,胃癌的发生发展是一个多因素、多细胞、多步骤的过程,由于胃癌早期缺乏特异性症状,绝大多数确诊断病例处于晚期,预后较差,存在广泛的转移和高复发。且现有的治疗方法如化疗、放疗不仅副作用强且易发生耐药。因此,进一步探寻有助于胃癌早期诊断和预后判断且无创的相关分子标志物是目前亟需解决的重要问题。
3.环状rna(circrna)是一类由前体mrna反向剪接产生的闭合环状非编码rna分子,随着rna深度测序技术和生物信息学的最新进展,已发现大量circrna在哺乳动物细胞中表达丰富。而circrna在真核生物中具有不同物种的保守性、高稳定性、在组织和发育阶段特异性表达等特点,目前研究证明circrna可作为mirna海绵,与蛋白结合、翻译蛋白、调节亲本基因转录等功能,并能被运输到体液中,具有作为生物标志物的巨大潜力。
4.外泌体(exosome)是一类直径30~100nm的细胞外囊泡,由多种细胞分泌,几乎存在于所有的体液当中,通过其携带的蛋白质、脂质、核酸核代谢产物等来发挥细胞间通讯功能,参与免疫应答、病毒感染、代谢和心血管疾病、神经退行性疾病以及癌症进展等多种生理和病理过程。研究证实circrnas富含在外泌体中,通过外泌体开始循环并到达受体细胞,从而实现其各种生物学功能,circrna作为一种稳定性较好生物标志物因其能在外泌体中大量富集,因此研究循环体液中外泌体circrna标志物对疾病的诊断具有重要意义。
5.目前,临床上现有的胃癌诊断标志物如cea、ca199、ca724等缺乏特异性,对临床真正起到辅助诊断的肿瘤标志物少,所以急需开发一种快速、准确的检测血浆中外泌体circrna的方法。
技术实现要素:
6.有鉴于此,本发明的目的在于提供一种用于胃癌的诊断和预后监测的血浆外泌体circrna标志物及其应用,所述血浆外泌体circrna标志物能够对胃癌进行有效的诊断和预后监测,并在一定程度上能够鉴别萎缩性胃炎患者,为临床的早期诊断和治疗靶点提供了重要依据。
7.为了实现上述发明目的,本发明提供以下技术方案:
8.本发明提供了一种血浆外泌体circrna的提取试剂盒,包括提取血浆外泌体的试剂和提取外泌体circrna的试剂;
9.所述提取血浆外泌体的试剂包括exoqiuck plasma prep and exosome precipitationkit;
10.所述提取外泌体circrna的试剂包括单独包装的:mirneasy serum/plasmakit、氯仿和无水乙醇。
11.本发明提供了一种利用上述提取试剂盒提取得到的用于胃癌的诊断和预后监测的血浆外泌体circrna标志物,所述血浆外泌体circrna标志物包括hsa_circ_0006853,所述hsa_circ_0006853的核酸序列如seq id no.1所示。
12.本发明还提供了一种检测上述血浆外泌体circrna标志物的试剂在制备胃癌诊断工具中的应用。
13.优选的,所述试剂包括针对hsa_circ_0006853设计的特异性引物对。
14.优选的,所述特异性引物对包括seq id no.2所示的上游引物和seq id no.3所示的下游引物。
15.本发明还提供了一种胃癌诊断试剂盒,包括seq id no.2所示的上游引物和seq id no.3所示的下游引物。
16.优选的,还包括构建qrt-pcr体系的其他试剂。
17.优选的,还包括内参基因β-actin的引物对。
18.优选的,所述内参基因β-actin的引物对,上游引物如seq id no.4所示,下游引物如seq id no.5所示。
19.优选的,还包括反转录试剂。
20.有益效果:本发明提供了一种用于胃癌的诊断和预后监测的血浆外泌体circrna标志物,以及血浆外泌体circrna的提取试剂盒,能够从血浆中方便、准确的提取和检测外泌体circrna,有利于实验室及临床血浆外泌体circrna的分析和应用。本发明还提供了hsa_circ_0006853的试剂盒,可以快速检测hsa_circ_0006853在内的多种circrna,为胃癌的早期诊断和预后判断提供了一种有价值的标志物检测方法,也为分析更多的血浆外泌体circrna应用于肿瘤标志物提供帮助。
附图说明
21.图1为本发明实施例提供的通过nta(a)、电镜(b)、以及western blot鉴定(c)所分离的血浆外泌体粒径和纯度示意图;
22.图2为本发明实施例提供的hsa_circ_0006853和actin分子进行实时荧光定量pcr的扩增曲线及融解曲线图;
23.图3为本发明实施例提供的hsa_circ_0006853进行实时荧光定量pcr扩增后产物琼脂糖电泳和测序鉴定示意图;
24.图4为本发明实施例提供的hsa_circ_0006853进行成环鉴定时rnaser实验以及gdna实验示意图;
25.图5为本发明实施例提供的实时荧光定量pcr比较胃癌患者、萎缩性胃炎患者、健康对照者血浆外泌体hsa_circ_0006853差异表达和术前术后的示意图;
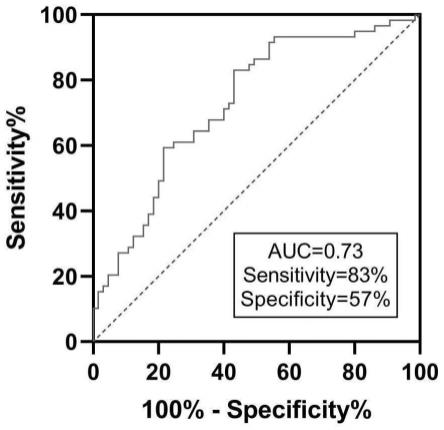
26.图6为本发明实施例提供的roc曲线分析血浆外泌体hsa_circ_0006853对胃癌诊断的特异性和灵敏性示意图。
具体实施方式
27.本发明提供了一种血浆外泌体circrna的提取试剂盒,包括提取血浆外泌体的试剂和提取外泌体circrna的试剂;
28.所述提取血浆外泌体的试剂包括exoqiuck plasma prep and exosome precipitation kit;
29.所述提取外泌体circrna的试剂包括单独包装的:mirneasy serum/plasma kit、氯仿和无水乙醇。
30.本发明对所述提取血浆外泌体的试剂和提取外泌体circrna的试剂的来源并没有特殊限定,可利用本领域的常规市售试剂即可。如在本发明实施例中,以exoqiuck plasma prep and exosome precipitation kit作为提取血浆外泌体的试剂,购自sbi公司,货号exoq5tm-1;以mirneasy serum/plasma kit、氯仿和无水乙醇作为提取外泌体circrna的试剂,且mirneasy serum/plasma kit购自qiagen,货号为217184。
31.利用本发明所述提取试剂盒,能够提取血浆外泌体中包括hsa_circ_0006853在内的多种circrna。
32.本发明还提供了利用上述提取试剂盒提取血浆外泌体circrna的方法,具体包括:血浆外泌体的分离提取和外泌体circrna的提取。
33.本发明所述血浆外泌体的分离提取,优选包括:将血浆与thrombin混合后室温静置,离心弃沉淀,将上清与exoqiuck plasma prep and exosome precipitation kit混合后静置,离心弃上清,沉淀即为血浆外泌体。
34.本发明将所述血浆外泌体以灭菌1x pbs重悬后进行外泌体circrna的提取,优选包括:将上述的外泌体与qiazol裂解液(mirneasy serum/plasma kit试剂盒中自带)混合裂解后,再与外泌体等体积的氯仿混合振荡;离心后将收集得到的上层水相与无水乙醇混合后,混合液到spin colum中离心,弃滤液,回收collection tube,重复上一步骤,将剩余的混合液离心过柱;弃滤液,回收collection tube,加rwt缓冲液,离心;弃滤液,回收collection tube,加rpe缓冲液,离心;弃滤液,回收collection tube,加80%乙醇,离心;弃滤液及收集管,将spin colum置于新的2ml collection tube中,室温全速离心5min使膜干燥;弃collection tube,将spin colum放置新的1.5ml collection tube中,向膜中间部位滴加rnase-free water,小心盖上盖子,室温静置;离心1min,将洗脱得到的rna溶液再次滴加至膜中间,室温静置3-5min后再次离心1min,洗脱得到外泌体总rna。本发明将得到的外泌体总rna置于冰上,待立即使用。
35.本发明还提供了一种利用上述提取试剂盒提取得到的用于胃癌的诊断和预后检测的血浆外泌体circrna标志物,所述血浆外泌体circrna标志物包括hsa_circ_0006853,所述hsa_circ_0006853的核酸序列如seq id no.1所示:gggcccggcg gatgcctcct ttgccggagc ttggaacaga ctcacggcca gcgaagtgagttcaatggct gaggtgag。
36.本发明还提供了一种检测上述血浆外泌体circrna标志物的试剂在制备胃癌诊断工具中的应用。
37.本发明所述试剂优选包括针对hsa_circ_0006853设计的特异性引物对,所述特异性引物对包括seq id no.2所示的上游引物:caatggctga ggtgaggggc c和seq id no.3所示的下游引物:ctgttccaag ctccggcaaa gg。
38.本发明还提供了一种胃癌诊断试剂盒,包括seq id no.2所示的上游引物和seq id no.3所示的下游引物。
39.本发明所述试剂盒中优选还包括构建qrt-pcr体系的其他试剂,如aceq qpcr sybr green mastermix,购自vazyme公司,货号q111-02。
40.本发明所述试剂盒中优选还包括内参基因β-actin的引物对,所述内参基因β-actin的引物对,上游引物优选如seq id no.4所示:cacgaaacta ccttcaactc c,下游引物优选如seq id no.5所示:catactcctg cttgctgatc。
41.本发明所述试剂盒中优选还包括反转录试剂,如本发明实施例中使用的hiscript iii strand cdna synthesis kit,购自vazyme公司,货号r312-01/02。
42.下面结合实施例对本发明提供的一种用于胃癌的诊断和预后监测的血浆外泌体circrna标志物及其应用进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
43.实施例1
44.血浆外泌体circrna的提取
45.(1)血浆的采集与制备
46.1)以edta抗凝采血管采集肘静脉血8ml,采血后立即轻柔颠倒混匀5次以充分混匀;
47.2)室温静置30min中后,以水平离心机3000rpm/min离心10min初步分离得到上层血浆;
48.3)使用移液器将血浆转移至rnase free进口ep管,再次以水平离心机3000g/min离心15min以去除残余细胞碎片;
49.4)使用移液器将离心后的上层血浆转移并分装至新的rnase free进口ep管(260μl/管);-80℃保存备用或4℃放置立即使用。
50.(2)血浆外泌体的分离提取
51.1)将血浆从-80℃取出置4℃化冻,使用移液器吸取250μl至新的rnase free进口ep管,随后加入2μl的thrombin立即轻柔吹打混匀,室温静置5min;
52.3)室温10000rpm/min离心5min;
53.4)避免损失过多的血浆,使用移液枪以旋转的方式挑去絮状的纤维蛋白沉淀,随后加入63μl的exoqiuck plasma prep and exosome precipitation kit;
54.5)4℃静置30min,随后在4℃下以1500g,离心30min;
55.6)弃上清,再次4℃下以1500g,离心5min以去除残留液体;
56.7)以200μl灭菌1x pbs重悬管底的外泌体沉淀,4℃放置10min以溶解外泌体,待进一步使用。外泌体的表征鉴定如图1所示。
57.(3)外泌体circrna的提取
58.1)将上述的外泌体加入1ml的qiazol裂解液,振荡30s充分裂解外泌体,然后室温静置5min,加入与外泌体等体积的氯仿,剧烈涡旋振荡15s,并放置室温平衡2-3min;
59.2)4℃,12000g,离心15min,吸取上层水相750μl至新ep管,(注意:不要吸到白色的中间层),随后加入1.5倍体积预冷的无水乙醇,移液枪上下吹打混匀;
60.3)吸700μl上一步的混合液到spin colum(已放置2ml的collection tube中),室
温离心,12000g,15s;
61.4)弃滤液,回收collection tube,重复上一步骤,将剩余的混合液离心过柱;
62.5)弃滤液,回收collection tube,加700μl,rwt缓冲液,室温离心,12000g,15s;
63.6)弃滤液,回收collection tube,加500μlrpe缓冲液,室温离心,12000g,15s;
64.7)弃滤液,回收collection tube,加500μl,80%乙醇,室温离心,12000g,2min;
65.8)弃滤液及收集管,将spin colum置于新的2ml collection tube中(试剂盒提供),室温全速离心5min使膜干燥;
66.9)弃collection tube,将spin colum放置新的1.5ml collection tube中(试剂盒提供),向膜中间部位滴加14μl rnase-free water,小心盖上盖子,室温静置3-5min;
67.10)室温全速离心1min,将洗脱得到的rna溶液再次滴加至膜中间,室温静置3-5min后再次全速离心1min,洗脱得到外泌体总rna;
68.11)得到的rna溶液置冰上待立即使用。
69.实施例2
70.血浆外泌体hsa_circ_0006853的检测和测定
71.(1)cdna的制备
72.20μl反转录体系:10x rt mix 2μl、random hexamers(50ng/nl)1μl、hiscript enzyme mix 2μl、total rna≤1ug和余量的rnase free ddh20。
73.反转录程序:37℃15min,85℃5s,4℃保存。
74.反应产物可置于4℃立即用于qpcr反应,或放置-20℃半年内使用,或-80℃保存避免反复冻融。
75.cdna可根据基因在样本中的表达量情况以rnase free ddh2o适当稀释或直接用于qpcr反应体系。
76.(2)实时荧光定量pcr
77.20μl qpcr反应体系:2xaceq qpcr sybr green mastermix 10μl、forward primer(10μm)0.4μl、reverse primer(10μm)0.4μl、cdna 2μl和余量的rnase free ddh2o。
78.于thermofisher quantstudio 3qs3荧光定量pcr仪中进行实时荧光定量pcr反应:95℃预变性5min;循环反应95℃15s,60℃30s(采集荧光),40循环;熔解曲线:95℃15s,60℃30s,95℃15s(采集荧光)。
79.引物特异性验证:本发明实施例提供的实时荧光定量pcr检测hsa_circ_0006853和β-actin的扩增曲线及熔解曲线图,如图2所示,其中a为扩增曲线,b为熔解曲线。
80.hsa_circ_0006853扩增后pcr产物鉴定:琼脂糖凝胶电泳分析产物单一性,如图4的a所示;t-a克隆质粒后测序验证,如图3的b所示。
81.成环鉴定:本发明实施例提供的rnaser消化实验和gdna实验对hsa_circ_0006853进行成环鉴定以验证提供的hsa_circ_0006853引物的扩增产物确实是一个环状rna,如图4中的a和b所示。
82.实施例3
83.胃癌血浆外泌体hsa_circ_0006853作为诊断标志物价值
84.(1)本发明纳入59例2021年7月-2022年1月在镇江市第一人民医院和江苏大学附属医院(镇江市江滨医院)及江苏大学附属澳洋医院胃肠外科就诊的胃癌患者,收集其年
龄、性别、肿瘤大小、位置、分化程度、淋巴结转移、远端转移、神经受累、tnm分期、组织学分型、cea、ca199、ca242等基本资料,采集术前和术后肘静脉并检测血浆外泌体hsa_circ_0006853水平。同时纳入同期健康体检者65例和44例萎缩性胃炎患者按年龄和性别匹配。三组样本同时收取、采样、分装、保存条件均一致,进行血浆外泌体hsa_circ_0006853含量检测和分析。
85.(2)数据分析:本实验数据采用相对定量的分析方法,以β-actin为内参基因(引物序列如seq id no.4和seq id no.5所示),以
△
ct=ct
hsa-circ_0006853-ct
β-actin
表示个样本检测数值,比较不同组别的差异以及术前和术后的差异,并以graphpad prism8.2.0和spss 20.0进行分析。
86.(3)结果:
87.胃癌患者与萎缩性胃炎患者、健康体检者血浆外泌体hsa_circ_0006853表达水平(a)以及胃癌患者术前和术后表达水平(b)的比较结果如图5所示,hsa-circ_0006853在胃癌患者的血浆外泌体中(gc-ex组)高表达,且在健康体检者(normal-ex)、萎缩性胃炎患者(gastritis-ex)、胃癌患者的血浆外泌体中表达水平依次升高。而在胃癌肿瘤组织切除后,hsa_circ_0006853的表达水平下降。血浆外泌体hsa_circ_0006853对胃癌诊断的特异度和灵敏度结果如图6所示,在诊断效能上,hsa_circ_0006853的auc面积为0.73,灵敏度和特异度分别为83%和57%。以上结果表明外泌体hsa_circ_0006853在胃癌的诊断和鉴别上是一个有潜力的生物标志物,并且是一个有效的预后监测指标。
88.综上可知,血浆外泌体hsa_circ_0006853能够对胃癌的早期诊断和鉴别诊断提供具有潜在价值的新型生物标志物。提供的血浆外泌体circrna检测方法可为临床实验室挖掘更多的血浆外泌体circrna标志物应用于肿瘤诊断提供参考和帮助。
89.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1