三(1,2-苯基)二胺衍生物有机光电材料及其应用的制作方法
三(1,2-苯基)二胺衍生物有机光电材料及其应用
技术领域
1.本发明属于有机电致发光材料技术领域,具体涉及多种三(1,2-苯基)二胺衍生物有机光电材料,及其在有机电致发光材料或元件中的应用。
背景技术:
2.有机电致发光是一种新型光电信息技术。作为一种自发光的电子元件,有机电致发光二极管(organic light emission diodes,oled)显示及照明元件的发光机理是在直流电场的作用下,借助有机半导体功能材料将电能直接转化为光能。oled发光色彩可为单独的红、绿、蓝、黄光或者是组合白光。oled发光显示技术的最大特点在于超薄、响应速度快、超轻量、面发光及柔性显示,可用于制造单色或全色显示器,还可以制作照明、显示产品或液晶显示器的背光源。
3.有机电致发光元件(有机el元件),根据发光原理的不同,可分为荧光型与磷光型两类。向有机el元件施加电压,注入来自阳极的空穴与来自阴极的电子,其在发光层中再次结合形成激子,激子辐射跃迁产生发光现象。依据电子自旋统计法,单线态激子与三重态激子以25:75的比例生成。荧光型有机电致发光材料因为利用了单线态激子来发光,故其内部量子效率只能达到25%。磷光型有机电致发光材料由重金属元素构成,通过系间窜越可以同时利用单线态和三线态能量,内量子效率可以达到100%。
4.热活性延迟荧光(thermally activated delayed fluorescence,tadf)材料是继有机荧光材料和有机磷光材料之后发展的第三代有机发光材料。该类材料一般具有较小的单线态-三线态能级差(δest),三线态激子可以通过反系间窜越转变成单线态激子发光,可以充分利用电激发下形成的单线态激子和三线态激子,器件的内量子效率可以达到100%,同时材料结构可控,性质稳定,价格便宜无需铱、铂等贵重金属,在oleds领域的应用前景广阔。目前的研究结果表明:tadf材料一般由给电子基团-吸电子基团通过π健连接而成,通过分子内电荷传输形成激子,材料的工作寿命还达不到应用要求,尤其在蓝光产业化方面仍以传统荧光材料为主,如何设计开发高性能蓝光荧光材料一直是行业内的热点。
5.三(1,2-苯基)二胺由于其特有的刚性和空间立体结构,可以有效的抑制π-π堆积,减少因分子聚集而引起的猝灭和分子振动,分子结构更加稳定。分子中的氮原子有别于c、si、p原子的吸电子特性,三(1,2-苯基)二胺母核结构中由于两个n原子的存在而具有胺基性质,在激发态下可以有效传递空穴,进一步连接给电子基团构筑成具有空穴传输性能的材料,该类材料具有合适的分子前线轨道能级和较高的三线态能量(t1),可用作空穴传输材料和发光材料,具有广泛的应用市场前景。
技术实现要素:
6.本发明的目的在于提供一系列三(1,2-苯基)二胺衍生物,所述衍生物在三(1,2-苯基)二胺母核基础上进一步引入胺基、咔唑基等给电子基团,所构筑的化合物具有典型的给电子特性。本发明提供的三(1,2-苯基)二胺衍生物作为空穴传输材料或发光层材料应用
到有机电致发光器件中,能够显著改善有机电致发光器件的器件性能。
7.一方面,本发明涉及三(1,2-苯基)二胺衍生物,其结构通式如式(i)所示:
[0008][0009]
其中,取代基l为单键或芳基,取代基d为给电子基团;
[0010]
所述给电子基团选自取代或未被取代的胺基、取代或未被取代的咔唑基、取代或未被取代的吩噁嗪基、取代或未被取代的吖啶基、取代或未被取代的10h螺[吖啶-9,9
’‑
芴]基、取代或未被取代的10h螺[吖啶-9,9
’‑
呫吨]基、取代或未被取代的5-苯基-5,10-二氢吩嗪基、取代或未被取代的10h-吩噻嗪基中的任一种。
[0011]
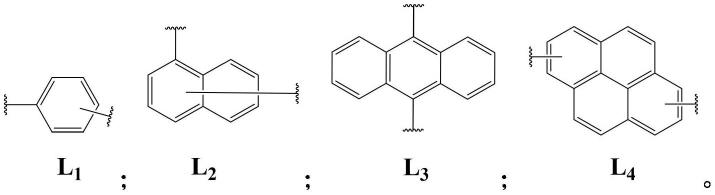
进一步地,本发明提供的三(1,2-苯基)二胺衍生物中,所述取代基l为l1~l4中的任一种:
[0012][0013]
进一步地,本发明提供的三(1,2-苯基)二胺衍生物中,其特征在于,所述取代基d为d1~d7中的任一种:
[0014]
[0015]
其中,ar1或ar2为芳基、杂芳基中的任一种;r1或r2为芳基、烷基、杂芳基中的任一种;x为氧原子、硫原子、c-m1m2或n-m3中的一种,所述m1或m2为氢原子、甲基、苯基、联苯基中的任一种,所述m3为苯基;y为碳原子、氮原子、氧原子中的任一种。
[0016]
进一步优选地,本发明提供的三(1,2-苯基)二胺衍生物中,所述ar1或ar2为苯基、联苯基、咔唑基、呋喃基中的任一种,所述r1或r2为甲基、乙基、叔丁基、苯基、联苯基、咔唑基、呋喃基中的任一种。
[0017]
进一步地,本发明提供了所述三(1,2-苯基)二胺衍生物的具体结构,其为化合物1~50中的任一种:
[0018]
[0019]
[0020]
[0021][0022]
另一方面,本发明涉及一种有机电致发光材料,其含有本发明所述的三(1,2-苯基)二胺衍生物。
[0023]
另一方面,本发明涉及一种有机电致发光元件,其由本发明所述的有机电致发光材料制成。
[0024]
作为一种优选的实施方式,所述的有机电致发光元件,包括阳极和阴极,以及位于所述阳极和阴极之间的至少一个有机层,所述有机层包括空穴传输层、发光层、电子传输层,所述空穴传输层或发光层含有所述的有机电致发光材料。
[0025]
作为一种优选的实施方式,所述的有机电致发光元件,所述发光层为磷光器件、荧光器件、热活性延迟荧光器件中的任一种。
[0026]
另一方面,本发明还给出了所述有机电致发光材料,或所述有机电致发光元件在有机电致发光显示中的应用。
[0027]
本发明与现有技术相比具有以下有益效果或者优点:
[0028]
本发明提供了多种三(1,2-苯基)二胺衍生物,并给出了所述三(1,2-苯基)二胺衍
生物的合成方法。本发明在三(1,2-苯基)二胺母核基础上进一步引入胺基、咔唑基等给电子基团,所构筑的化合物具有典型的给电子特性,具有合适的homo/lumo值和较高的三线态能量值,可以用于制备高性能有机el元件。同时,本发明所述空间立体结构三(1,2-苯基)二胺衍生物具有较高的热稳定性,可显著提高发光器件的发光稳定性,可作为空穴传输材料和发光层材料使用,在oled发光器件及显示装置上具有广阔的应用前景。
附图说明
[0029]
下面通过附图结合实施例具体描述本发明,其中附图所示内容仅用于对本发明的解释说明,而不构成对本发明任何意义上的限制。
[0030]
图1是本发明实施例所述有机电致发光元件的结构示意图。
[0031]
附图标记说明:1、衬底,2、阳极层,3、空穴注入层,4、第一空穴传输层,5、第二空穴传输层,6、发光层,7、空穴阻挡层,8、电子传输层,9、电子注入层,10、阴极层。
具体实施方式
[0032]
以下结合具体实施例,对本发明的具体实施方案做详细的阐述。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围,本发明的保护范围以权利要求为准,包括在此基础上所做出的显而易见的变化或变动等。
[0033]
下述各实施例中所述实验方法和检测方法,如无特殊说明,均为常规方法;所述试剂和材料,如无特殊说明,均可在市场上购买得到。
[0034]
实施例1
[0035]
本实施例提供了所述三(1,2-苯基)二胺衍生物涉及的具体化合物与对应中间体的具体合成方法。
[0036]
(1)中间体1的合成
[0037][0038]
在三口瓶中依次加入300g中间体1-1,1330.0g中间体1-2,929.6g叔丁醇钠,8l甲苯,通入氮气置换反应瓶中的空气后加入38.2g碘化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1-1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得149.8g中间体1,收率27.8%。
[0039]
(2)中间体1的合成
[0040]
[0041]
在三口瓶中依次加入60g中间体1,120.5g中间体2-1,62.0g醋酸钾,1l甲苯,通入氮气置换反应瓶中的空气后加入4.6g[1,1
’‑
双(二苯基膦基)二茂铁]二氯化钯,将反应液升温至110℃回流搅拌反应6h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得76.3g中间体2,收率63.2%。
[0042]
(3)化合物1的合成
[0043][0044]
在三口瓶中依次加入10g中间体2,9.3g化合物1-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得9.3g化合物1,收率71.6%。
[0045]1h nmr(400mhz,cdcl3)δ8.19(d,j=7.2hz,2h),7.91-7.94(m,6h),7.50(t,j=7.2hz,2h),7.33(d,j=7.6hz,1h),7.23(s,1h),7.21(m,3h),7.14(d,j=7.6hz,4h),6.95(d,j=7.6hz,4h)。
[0046]
(4)化合物6的合成
[0047][0048]
在三口瓶中依次加入10g中间体1,5.5g中间体6-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得9.6g化合物6,收率76.2%。
[0049]1h nmr(400mhz,cdcl3)δ8.19(d,j=7.2hz,2h),7.94(d,j=7.2hz,2h),7.50(d,j=7.2hz,2h),7.35(d,j=7.6hz,1h),7.28(d,j=7.6hz,1h),7.20(d,j=7.2hz,2h),7.14(d,j=7.6hz,4h),7.12(s,1h),6.95(d,j=7.6hz,4h)。
[0050]
(5)化合物17的合成
[0051][0052]
在三口瓶中依次加入10g中间体1,13.9g中间体17-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得16.5g化合物17,收率81.9%。
[0053]1h nmr(400mhz,cdcl3)δ8.09(d,j=6.4hz,2h),8.06(d,j=6.4hz,2h),7.99(d,j=6.4hz,2h),7.63(t,j=6.4hz,2h),7.60(t,j=6.4hz,2h),7.55(m,6h),7.37(m,6h),7.14(d,j=7.6hz,4h),7.10(d,j=7.6hz,1h),6.95(d,j=7.6hz,4h),6.80(m,2h)。
[0054]
(6)化合物18的合成
[0055][0056]
在三口瓶中依次加入10g中间体2,9.3g化合物18-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得10.0g化合物18,收率76.3%。
[0057]1h nmr(400mhz,cdcl3)δ7.55(d,j=7.2hz,2h),7.37(d,j=7.2hz,2h),7.33(d,j=7.6hz,1h),7.21-7.24(m,6h),7.14(d,j=7.6hz,4h),7.08(d,j=7.2hz,4h),7.00(t,j=7.2hz,2h),6.95(d,j=7.6hz,4h)。
[0058]
(7)化合物22的合成
[0059][0060]
在三口瓶中依次加入10g中间体2,11.9g化合物22-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得10.1g化合物22,收率65.8%。
[0061]1h nmr(400mhz,cdcl3)δ8.22(s,1h),7.98(d,j=7.2hz,1h),7.54-7.56(m,4h),
7.39(t,j=7.2hz,1h),7.37(d,j=7.2hz,2h),7.33(d,j=7.6hz,1h),7.31(t,j=7.2hz,1h),7.21-7.24(m,4h),7.14(d,j=7.2hz,4h),7.00(d,j=7.2hz,1h),6.97(d,j=7.6hz,1h),6.95(d,j=7.2hz,4h)。
[0062]
(8)化合物23的合成
[0063][0064]
在三口瓶中依次加入10g中间体2,12.6g化合物23-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得10.2g化合物23,收率63.1%。
[0065]1h nmr(400mhz,cdcl3)δ7.90(d,j=6.8hz,1h),7.62(s,1h),7.55(m,3h),7.51(d,j=7.2hz,1h),7.38(m,3h),7.33(d,j=7.6hz,1h),7.28(t,j=6.8hz,1h),7.21-7.24(m,4h),7.14(d,j=7.2hz,4h),7.08(d,j=6.8hz,2h),7.06(d,j=7.2hz,1h),7.00(d,j=6.8hz,1h),6.95(d,j=7.2hz,4h),1.69(s,6h)。
[0066]
(9)化合物24的合成
[0067][0068]
在三口瓶中依次加入10g中间体2,14.0g化合物24-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得11.9g化合物24,收率68.3%。
[0069]1h nmr(400mhz,cdcl3)δ7.62(d,j=6.8hz,2h),7.58(d,j=6.8hz,1h),7.54(m,4h),7.50(d,j=6.8hz,2h),7.37(d,j=6.8hz,2h),7.33-7.35(m,5h),7.21-7.24(m,4h),7.16(t,j=7.2hz,1h),7.14(d,j=7.2hz,4h),7.08(d,j=6.8hz,2h),7.00(t,j=6.8hz,1h),6.95(d,j=7.2hz,4h)。
[0070]
(10)化合物28的合成
[0071][0072]
在三口瓶中依次加入10g中间体1,17.2g中间体28-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得12.3g化合物28,收率52.9%。
[0073]1h nmr(400mhz,cdcl3)δ7.89(d,j=6.8hz,3h),7.62(s,2h),7.51(m,4h),7.45(d,j=6.8hz,2h),7.38(t,j=6.8hz,2h),7.26-7.28(m,6h),7.14(d,j=7.2hz,4h),7.10(d,j=7.2hz,4h),7.06(d,j=6.8hz,2h),6.95(d,j=7.2hz,4h),6.80(m,2h),1.69(s,6h)。
[0074]
(11)化合物29的合成
[0075][0076]
在三口瓶中依次加入10g中间体1,9.4g中间体29-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得13.5g化合物29,收率83.7%。
[0077]1h nmr(400mhz,cdcl3)δ7.90(d,j=6.8hz,1h),7.62(s,1h),7.55(d,j=6.8hz,1h),7.51(d,j=6.8hz,1h),7.38(t,j=6.8hz,1h),7.28(t,j=6.8hz,1h),7.24(t,j=6.8hz,2h),7.14(d,j=7.2hz,4h),7.10(d,j=7.2hz,1h),7.08(d,j=6.8hz,2h),7.06(d,j=6.8hz,1h),7.00(d,j=6.8hz,1h),6.95(d,j=7.2hz,4h),6.80(m,2h),1.69(s,6h)。
[0078]
(12)化合物30的合成
[0079][0080]
在三口瓶中依次加入10g中间体1,11.9g中间体30-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应
4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得14.0g化合物30,收率76.2%。
[0081]1h nmr(400mhz,cdcl3)δ7.90(d,j=6.8hz,1h),7.75(d,j=6.4hz,2h),7.62(s,1h),7.55(m,3h),7.51(d,j=6.8hz,1h),7.49(d,j=6.4hz,2h),7.41(t,j=6.4hz,1h),7.37(m,3h),7.28(t,j=6.8hz,1h),7.14(d,j=7.2hz,4h),7.10(d,j=7.2hz,1h),7.06(d,j=6.8hz,1h),6.95(d,j=7.2hz,4h),6.80(m,2h),1.69(s,6h)。
[0082]
(13)化合物33的合成
[0083][0084]
在三口瓶中依次加入10g中间体1,6.9g中间体33-1,4.3g叔丁醇钠,67mg醋酸钯,200ml甲苯,通入氮气置换反应瓶中的空气后加入2.0ml 10%的三叔丁基膦的甲苯溶液,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得8.8g化合物33,收率63.7%。
[0085]1h nmr(400mhz,cdcl3)δ7.19(t,j=7.2hz,2h),7.17(d,j=7.2hz,2h),7.14(m,6h),7.10(d,j=7.6hz,1h),6.95(m,6h),6.80(m,2h),1.69(s,6h)。
[0086]
(14)化合物37的合成
[0087][0088]
在三口瓶中依次加入10g中间体2,14.0g化合物37-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得11.2g化合物37,收率64.9%。
[0089]1h nmr(400mhz,cdcl3)δ7.90(d,j=6.8hz,2h),7.55(m,4h),7.37(m,4h),7.33(d,j=7.6hz,1h),7.28(t,j=6.8hz,2h),7.23(s,1h),7.21(d,j=7.6hz,1h),7.17-7.19(m,4h),7.14(m,6h),6.95(m,6h)。
[0090]
(15)化合物38的合成
[0091]
[0092]
在三口瓶中依次加入10g中间体2,10.4g化合物38-1,7.2g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.3g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体2完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得10.0g化合物38,收率71.2%。
[0093]1h nmr(400mhz,cdcl3)δ7.55(d,j=6.8hz,2h),7.37(d,j=6.8hz,2h),7.33(d,j=7.6hz,1h),7.23(s,1h),7.17-7.21(m,5h),7.14(m,6h),6.95(m,6h),1.69(s,6h)。
[0094]
(16)化合物44的合成
[0095][0096]
在三口瓶中依次加入10g中间体1,9.4g化合物44-1,8.3g碳酸钾,200ml甲苯,40ml乙醇,20ml水。通入氮气置换反应瓶中的空气后加入0.34g四(三苯基膦)钯,将反应液升温至80℃回流搅拌反应6h,tlc监测原料中间体1完全消耗后停止加热,降至室温后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得10.9g化合物44,收率73.5%。
[0097]1h nmr(400mhz,cdcl3)δ7.94-7.99(m,4h),7.89(s,1h),7.62(t,j=6.8hz,2h),7.58(t,j=6.8hz,1h),7.50(d,j=6.8hz,2h),7.33(d,j=7.6hz,1h),7.23(s,1h),7.21(d,j=7.6hz,1h),7.16(m,2h),7.14(d,j=7.2hz,4h),6.95(d,j=7.2hz,4h)。
[0098]
(17)化合物46的合成
[0099][0100]
在三口瓶中依次加入10g中间体1,10.9g中间体46-1,4.3g叔丁醇钠,200ml甲苯,通入氮气置换反应瓶中的空气后加入0.4g溴化亚铜,将反应液升温至110℃回流搅拌反应4h,tlc监测原料中间体1完全消耗后停止加热,降至室温19后将反应液水洗至中性,有机相用无水硫酸钠干燥后过硅胶柱纯化得13.4g化合物46,收率76.2%。
[0101]1h nmr(400mhz,cdcl3)δ7.62(t,j=6.8hz,2h),7.58(m,3h),7.55(m,3h),7.50(m,4h),7.40(s,1h),7.35(d,j=7.6hz,1h),7.28(d,j=7.6hz,1h),7.16(t,j=7.2hz,2h),7.14(d,j=7.2hz,4h),7.12(s,1h),6.95(d,j=7.2hz,4h)。
[0102]
实施例2
[0103]
本实施例对本发明涉及的部分化合物及现有材料分别进行t1能量以及homo、lumo能级测试。
[0104]
最高分子占有轨道(homo)和最低分子未占有轨道(lumo)三线态能量(t1)为模拟
计算所得数据,试验结果如表1所示。
[0105]
表1,三(1,2-苯基)二胺衍生物及现有材料的性能测试
[0106][0107][0108]
由表1可得,本发明的三(1,2-苯基)二胺衍生物具有较高的三线态能量和较合适的homo/lumo,在oled器件中有利于载流子的传输和能量的转移,这些化合物可以作为空穴传输材料使用,也可以作为发光材料使用。在没有特定限制的情况下,上述有机电致发光器件可以是磷光器件、荧光器件,也可以是热活性延迟荧光(tadf)材料器件。因此,本发明以三(1,2-苯基)二胺为给体的化合物在应用于oled器件后,可以有效地提高器件的发光效率
及使用寿命等性能。
[0109]
实施例3
[0110]
本实施例以本发明提供的部分三(1,2-苯基)二胺衍生物为例,将其作为发光材料或空穴传输材料应用到有机电致发光器件中,以验证其所取得的优异效果。
[0111]
具体通过器件实施例1~15和对比例1的器件性能详细说明本发明的oled材料应用在器件中的优异效果。本发明器件实施例1~15和对比例1的制作工艺完全相同,并且采用了相同的玻璃基板和电极材料,电极材料膜厚也保持一致,所不同的是发光层或第二空穴传输层做了调整,具体如下。
[0112]
器件实施例1
[0113]
本实施例提供了一种有机电致发光器件,其结构具体如图1所示,包括依次层叠设置的衬底1、阳极层2、空穴注入层3、第一空穴传输层4、第二空穴传输层5、发光层6、空穴阻挡层7、电子传输层8、电子注入层9和阴极层10。
[0114]
其中,阳极层2材料选择具有高公函数的铟锡氧化物(ito),空穴注入层3材料选择hat-cn,厚度为5nm;第一空穴传输层4材料选择npb,厚度为60nm;第二空穴传输层5材料选择ht-2,厚度为15nm;发光层6使用化合物1作为发光材料,以bh1作为主体材料,掺杂质量比为3%,厚度为30nm;空穴阻挡层7的材料选择hb1,厚度为10nm;电子传输层8的材料选择et-1,厚度为35nm;电子注入层9的材料选择liq,厚度为2nm;阴极层的材料选择al,厚度为100nm。
[0115]
器件中各功能层所使用基本材料结构式如下:
[0116]
[0117][0118]
上述有机电致发光器件的具体制备步骤如下:
[0119]
1)清洗透明玻璃基板上的ito阳极,分别用去离子水、丙酮、乙醇各超声清洗20分钟,然后进行氧气氛围下等离子(plasma)处理5分钟;
[0120]
2)在ito阳极层上,通过真空蒸镀方式蒸镀空穴注入层材料hat-cn,厚度为5nm,这层作为空穴注入层;
[0121]
3)在空穴注入层上通过真空蒸镀方式蒸镀空穴传输材料npb,厚度为60nm,该层作为第一空穴传输层;
[0122]
4)在第一空穴传输层npb上通过真空蒸镀方式蒸镀空穴传输材料ht-2,厚度为15nm,这层作为第二空穴传输层;
[0123]
5)在第二空穴传输层上,通过真空蒸镀方式共蒸镀发光层,使用化合物1作为发光材料,bh1作为主体材料,掺杂质量比为3%,厚度为30nm;
[0124]
6)在发光层之上,通过真空蒸镀的方式蒸镀空穴阻挡材料hb1,厚度为10nm,这一层作为空穴阻挡层;
[0125]
7)在空穴阻挡层上,通过真空蒸镀的方式蒸镀电子传输材料et-1,厚度为35nm,这一层作为电子传输层;
[0126]
8)在电子传输层上,通过真空蒸镀的方式蒸镀电子注入材料liq,厚度为2nm,这一层作为电子注入层;
[0127]
9)在电子注入层上,通过真空蒸镀的方式蒸镀阴极al,厚度为100nm,该层作为阴极导电电极使用。
[0128]
器件实施例2
[0129]
与器件实施例1相同,不同之处:将化合物22作为发光材料替代化合物1。
[0130]
器件实施例3
[0131]
与器件实施例1相同,不同之处:将化合物23作为发光材料替代化合物1。
[0132]
器件实施例4
[0133]
与器件实施例1相同,不同之处:将化合物24作为发光材料替代化合物1。
[0134]
器件实施例5
[0135]
与器件实施例1相同,不同之处:将化合物29作为发光材料替代化合物1。
[0136]
器件实施例6
[0137]
与器件实施例1相同,不同之处:将化合物30作为发光材料替代化合物1。
[0138]
器件实施例7
[0139]
与器件实施例1相同,不同之处:将化合物33作为发光材料替代化合物1。
[0140]
器件实施例8
[0141]
与器件实施例1相同,不同之处:将化合物6作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0142]
器件实施例9
[0143]
与器件实施例1相同,不同之处:将化合物17作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0144]
器件实施例10
[0145]
与器件实施例1相同,不同之处:将化合物18作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0146]
器件实施例11
[0147]
与器件实施例1相同,不同之处:将化合物28作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0148]
器件实施例12
[0149]
与器件实施例1相同,不同之处:将化合物37作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0150]
器件实施例13
[0151]
与器件实施例1相同,不同之处:将化合物38作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0152]
器件实施例14
[0153]
与器件实施例1相同,不同之处:将化合物44作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0154]
器件实施例15
[0155]
与器件实施例1相同,不同之处:将化合物46作为空穴传输层替代ht-2,bd01作为发光材料替代化合物1。
[0156]
对比例1
[0157]
与器件实施例1相同,不同之处:bd01作为发光材料替代化合物1。
[0158]
本发明器件实施例1~15、对比实施例1所制备的不同器件构成成分,如表2所示。
[0159]
表2,各组有机电致发光器件构成成分对比表
[0160]
[0161][0162]
将表2所述各组有机电致发光器件用驱动电路将阴极和阳极连接起来,通过标准的方法,采用keithley2400电源结合pr670光度计测试oled器件的电压-效率-电流密度关系。测试结果如表3所示:
[0163]
表3,各器件实施例有机电致发光器件性能结果
[0164]
[0165][0166]
由表3可得,本发明提供的化合物作为发光材料和第二空穴传输层材料应用到oled发光器中,性能优良。如器件实施例6中的化合物30作为发光材料与对比例1bd01相比,发光效率和亮度都得到了显著的提高,发光效率提高了19.3%,6v电压下亮度提高了29.2%;器件实施例11中的化合物28作为第二空穴传输层材料与对比例1中的ht-2相比,发光效率提高了17.4%,6v电压下亮度提高了28.4%。综上所述,选用本发明的化合物作为oled器件的发光材料或空穴传输材料,对比现有材料应用的oled发光器件,器件的发光效率、亮度等光电性能均有良好的表现,在oled器件的应用上具有很大的应用价值和商业前景,具有良好的产业化前景。
[0167]
如上所述,即可较好地实现本发明,上述的实施例仅仅是对本发明的优选实施方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种改变和改进,均应落入本发明确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1