磺化苯代聚苯基离聚物及其制备方法、质子交换膜
1.本技术属于离聚物合成技术领域,尤其涉及一种磺化苯代聚苯基离聚物及其制备方法、质子交换膜。
背景技术:
2.质子交换膜(proton exchange membrane,pem)是一种选择性固态离子传输介质,广泛用于电化学储能器件中,如燃料电池、水电解、液流电池等。目前广泛使用的质子交换膜材料为全氟磺酸树脂(perfluorosulfonic acid resin,pfsa),因为其具有高电导率、强拉伸机械性能,但由于自身结构因素,其表现出合成复杂、成本高昂、热稳定性差、气体渗透率高等缺点。为此,新型质子交换膜材料被广泛研究,磺化聚苯基pem具有良好的热稳定性、低气体渗透率等优点,有望取代商业化pfsa。
3.离聚物(ionomer)是指碳氢分子链中含有离子基团的聚合物,其离子基团之间通过离子相互作用可形成交联网络,因而具备许多独特的优良性能。目前,磺化聚苯基离聚物膜材料被广泛研究,由于聚苯基材料主链由苯环构成,导致聚合物结构刚性强,难以获得高分子量聚合物,从而导致该类离聚物成膜性和耐久性差。litt等人(ecs transactions,2010,33,1,695-710)利用cu催化乌尔曼反应制备磺化聚对苯,由于cu催化乌尔曼反应对于苯环电子云密度有较高要求,因此其只能得到高离子交换容量且可溶于水的聚苯磺酸,其结构如下:
[0004][0005]
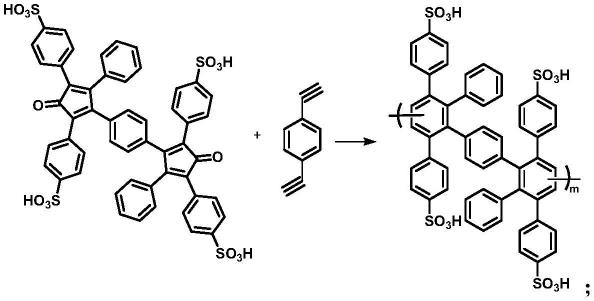
holdcroft等人(j.am.chem.soc.2015,137,12223-12226)设计了新型磺化单体并与1,4-苯二炔通过狄尔斯-阿尔德环化聚合反应合成磺化苯代聚苯基离聚物,该合成方法反应如下:
[0006][0007]
因磺化单体分子量高,因此上述方法制备得到的离子交换膜理论容量小于3.7meq g-1
,且因单体制备复杂,因而结构改性较困难,不利于新材料的研发。
技术实现要素:
[0008]
本技术的目的在于提供一种磺化苯代聚苯基离聚物及其制备方法、质子交换膜,旨在解决如何简单、低成本制备磺化苯代聚苯基离聚物的问题。
[0009]
为实现上述申请目的,本技术采用的技术方案如下:
[0010]
第一方面,本技术提供一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0011]
获取含有式ia或式ib所示的结构单元的前驱体聚合物;
[0012]
将所述前驱体聚合物与式iia或式iib所示的第一单体进行羟醛缩合反应,然后与式iiia或式iiib所示的第二单体进行狄尔斯-阿尔德反应,得到磺化苯代聚苯基离聚物;
[0013][0014]
其中,
[0015]
r1、r2、r3、r4、r5、r6分别独立选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,且r1、r2、r3、r4中至少有一个为-so3h,n为0~10的整数;
[0016]
当所述前驱体聚合物含有式ia所示的结构单元时,所述第一单体为式iia,当所述前驱体聚合物含有式ib所示的结构单元时,所述第一单体为式iib。
[0017]
第二方面,本技术提供一种磺化苯代聚苯基离聚物,所述磺化苯代聚苯基离聚物由本技术上述制备方法制备得到。
[0018]
第三方面,本技术提供一种质子交换膜,所述质子交换膜的材料包括本技术上述制备方法制备得到的所述磺化苯代聚苯基离聚物。
[0019]
本技术第一方面提供的磺化苯代聚苯基离聚物的制备方法,先获取含有式ia或式ib所示的结构单元的前驱体聚合物,然后利用羟醛缩合反应和狄尔斯-阿尔德环化反应完成苯代化反应,因前驱体聚合物的主链含有苯偶酰或二苯丙酮的结构单元,且溶解性优良,因此为前驱体聚合物与第一单体的羟醛缩合反应以及与第二单体的狄尔斯-阿尔德环化反应提供了条件,从而完成苯代化以得到高分子磺化苯代聚苯基离聚物,该过程使用的第一单体和第二单体简单,易于进行分子结构调控,为磺化苯代聚苯基离聚物产物的相关结构优化与调控提供更大的空间;因此,本技术的制备方法具有合成简单、成本低廉、得到的离聚物分子量高、易于调控等特点,具有广阔的应用前景。
[0020]
本技术第二方面提供的磺化苯代聚苯基离聚物由本技术特有的磺化苯代聚苯基离聚物的制备方法制备得到,因此,基于该制备方法特点,本技术的磺化苯代聚苯基离聚物不仅获取成本低廉,而且相关结构容易优化和调控,可用作质子交换膜具有很好的应用前景。
[0021]
本技术第三方面提供的质子交换膜的材料包括本技术上述特有的磺化苯代聚苯
基离聚物的制备方法制备得到的磺化苯代聚苯基离聚物;基于该制备方法得到的磺化苯代聚苯基离聚物的特点,本技术的质子交换膜不仅成本低廉,而且可以有效控制离聚物的离子交换膜容量,因此在燃料电池、电解池、液流电池等电化学能源转换装置中具有很好的应用前景。
具体实施方式
[0022]
为了使本技术要解决的技术问题、技术方案及有益效果更加清楚明白,以下结合实施例,对本技术进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本技术,并不用于限定本技术。
[0023]
本技术中,术语“和/或”,描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b的情况。其中a,b可以是单数或者复数。字符“/”一般表示前后关联对象是一种“或”的关系。
[0024]
本技术中,“至少一种”是指一种或者多种,“多种”是指两种或两种以上。“以下至少一项(个)”或其类似表达,是指的这些项中的任意组合,包括单项(个)或复数项(个)的任意组合。
[0025]
应理解,在本技术的各种实施例中,上述各过程的序号的大小并不意味着执行顺序的先后,部分或全部步骤可以并行执行或先后执行,各过程的执行顺序应以其功能和内在逻辑确定,而不应对本技术实施例的实施过程构成任何限定。
[0026]
在本技术实施例中使用的术语是仅仅出于描述特定实施例的目的,而非旨在限制本技术。在本技术实施例和所附权利要求书中所使用的单数形式的“一种”、“所述”和“该”也旨在包括多数形式,除非上下文清楚地表示其他含义。
[0027]
术语“第一”、“第二”仅用于描述目的,用来将目的如物质彼此区分开,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。例如,在不脱离本技术实施例范围的情况下,第一xx也可以被称为第二xx,类似地,第二xx也可以被称为第一xx。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。
[0028]
本技术实施例第一方面提供一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0029]
s01:获取含有式ia所示的结构单元的前驱体聚合物;
[0030]
s02:将含有式ia所示的结构单元的前驱体聚合物与式iia所示的第一单体进行羟醛缩合反应,然后与式iiia或式iiib所示的第二单体进行狄尔斯-阿尔德反应,得到磺化苯代聚苯基离聚物;
[0031][0032]
或者,
[0033]
s01:获取含有式ib所示的结构单元的前驱体聚合物;
[0034]
s02:将含有式ib所示的结构单元的前驱体聚合物与式iib所示的第一单体进行羟醛缩合反应,然后与式iiia或式iiib所示的第二单体进行狄尔斯-阿尔德反应,得到磺化苯代聚苯基离聚物;
[0035][0036]
上述结构中,r1、r2、r3、r4、r5、r6分别独立选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,且r1、r2、r3、r4中至少有一个为-so3h,n为0~10的整数。
[0037]
上述磺化苯代聚苯基离聚物的制备方法,前驱体聚合物含有苯偶酰(参见式ia所示的结构单元)或二苯基丙酮(参见式ib所示的结构单元)功能基团,易溶解,因此为与第一单体的羟醛缩合反应以及与第二单体的狄尔斯-阿尔德环化反应从而完成苯代化提供了条件,而上述过程使用的第一单体和第二单体简单,易于进行分子结构调控,为磺化苯代聚苯基离聚物产物的相关结构优化与调控提供更大的空间。
[0038]
具体地,含有式ia所示的结构单元的前驱体聚合物与式iia所示的第一单体进行羟醛缩合反应完成第一步苯代化后,使得初始聚合物产物含有如下iva所示的结构单元:
[0039][0040]
或者,含有式ib所示的结构单元的前驱体聚合物与式iib所示的第一单体进行羟醛缩合反应完成第一步苯代化后,使得初始聚合物产物含有如下ivb所示的结构单元:
[0041][0042]
而含有上述iva或ivb所示的结构单元的初始聚合物产物利用狄尔斯-阿尔德环化反应式与iiia或iiib所示的第二单体完成第二步苯代化反应,得到最终的磺化苯代聚苯基离聚物;
[0043]
如使用iiia单体,磺化苯代聚苯基离聚物含有结构单元:
[0044]
如使用iiib单体,磺化苯代聚苯基离聚物含有结构单元:
[0045]
需要说明的是,上述化学结构中,r1、r2、r3、r4、r5、r6分别独立选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,即r1选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,r2选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,r3选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,r4选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基
中的至少一种,r5选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种,r6选自h、-so3h、-(cf2)ncf3、-cooh、-no2和苯基中的至少一种;其中的-(cf2)ncf3中n为0~10的整数,即-(cf2)ncf3可以是-cf3、-cf2cf3、-(cf2)2cf3、-(cf2)3cf3、-(cf2)5cf3、-(cf2)6cf3、-(cf2)
10
cf3等。
[0046]
本技术上述结构中的r1、r2、r3、r4中至少有一个为-so3h;即可以在前驱体聚合物中的ia或ib所示的结构单元中,通过r1和/或r2引入-so3h,也可以在iia或iib所示的第一单体中,通过r3和/或r4引入-so3h;这样,羟醛缩合反应得到的产物含有磺基,为离聚物的磺化提供基础。当然,进一步地,还可以在iiia或iiib所示的第二单体中,通过r5,或者通过r5和/或r6引入-so3h。因此,磺酸的引入途径有多种,从而可以有效控制离聚物的离子交换膜容量。
[0047]
在一些实施例中,式ia或式ib所示的结构单元中,r1和r2为-so3h;或者,式iia或式iib所示的第一单体中,r3和r4为-so3h。例如,当前驱体聚合物含有式ia所示的结构单元时,iia所示的第一单体中r3和r4为-so3h;或者,当前驱体聚合物含有式ib所示的结构单元时,iib所示的第一单体中r3和r4为-so3h,即通过第一单体的羟醛缩合反应,从而在前驱体聚合物上引入磺酸。进一步地,iiia所示的第二单体中的r5为-so3h,或者iiib所示的第二单体中的r5和r6为-so3h,即通过第二单体的狄尔斯-阿尔德环化反应,从而在前驱体聚合物上引入磺酸。因第一单体和第二单体的结构简单,易于进行分子结构调控,为相关产物的结构优化与调控提供更大的空间,而且单体中磺酸的引入,可以更有效控制离聚物的离子交换膜容量,因此本技术的磺化苯代聚苯基离聚物的制备方法具有分子量高、合成简单、成本低廉、离子交换膜容量易控制等特点。
[0048]
在一实施例中,含有式ia或式ib所示的结构单元的前驱体聚合物可以通过偶合反应制备得到,即采用偶合反应机理制备含有苯偶酰或二苯基丙酮功能基团的前驱体聚合物,具体地,上述前驱体聚合物通过钯催化铃木反应、镍催化乌尔曼偶合反应、或铜催化乌尔曼偶合反应制备得到。
[0049]
例如,将原料(如4,4
’‑
二溴苯偶酰、4,4
’‑
二碘苯偶酰、4,4'-二溴二苄基酮、4,4'-二碘二苄基酮、4-溴-4
’‑
硼酸苯偶酰等苯偶酰类原料或二苯基丙酮类原料)进行钯催化铃木反应,从而可以得到含有式ia或式ib所示的结构单元的前驱体聚合物。其中,钯催化铃木反应使用的钯催化剂可为pdcl2,pd(pph3)4,pd(oac)2中的一种。
[0050]
例如,将原料(如4,4
’‑
二氯苯偶酰、4,4'-二氯二苄基酮等苯偶酰类原料或二苯基丙酮类原料)进行镍催化乌尔曼偶合反应,从而可以得到含有式ia或式ib所示的结构单元的前驱体聚合物。其中,镍催化乌尔曼偶合反应使用的镍催化剂可为nibr2,nicl2,ni(oac)2,ni(cod)2中的一种。
[0051]
例如,将原料(如4,4
’‑
二溴苯偶酰、4,4'-二溴二苄基酮等苯偶酰类原料或二苯基丙酮类原料)进行铜催化乌尔曼偶合反应,从而可以得到含有式ia或式ib所示的结构单元的前驱体聚合物。其中,铜催化乌尔曼偶合反应使用的铜催化剂可为铜粉。
[0052]
进一步地,前驱体聚合物可以在40~150℃的反应温度条件下制备得到,如40℃、60℃、100℃、120℃、150℃等;即钯催化铃木反应、镍催化乌尔曼偶合反应、或铜催化乌尔曼偶合反应中,苯偶酰类原料或二苯基丙酮类原料均可以在40~150℃实现聚合反应得到前驱体聚合物。
[0053]
进一步地,如果得到式ib所示的结构单元的前驱体聚合物,则可以在碱性条件下
进行钯催化铃木反应、镍催化乌尔曼偶合反应、或铜催化乌尔曼偶合反应制备得到,该碱性条件可以通过k2co3、na2co3、lioh、naoh、koh中的至少一种提供。
[0054]
本技术实施例从分子设计角度,优先获取主链含有苯偶酰或二苯丙酮单元且溶解性优良的前驱体聚合物,其中的苯偶酰或二苯丙酮单元为羟醛缩合反应与狄尔斯-阿尔德环化反应苯代化提供了条件,从而制备高分子磺化苯代聚苯基离聚物。
[0055]
在一实施例中,前驱体聚合物与式iia或式iib所示的第一单体进行羟醛缩合反应中,是在第一碱性条件下进行羟醛缩合反应。具体地,第一碱性条件由k2co3、na2co3、lioh、naoh、koh中的至少一种提供,羟醛缩合反应的温度为100~220℃,如可以是100℃、120℃、150℃、180℃、220℃等。
[0056]
在一实施例中,上述羟醛缩合反应得到含有式iva或式ivb所示的结构单元的初始聚合物产物与式iiia或式iiib所示的第二单体进行狄尔斯-阿尔德反应中,是在第二碱性条件下进行狄尔斯-阿尔德反应。
[0057]
具体地,第二碱性条件由k2co3、na2co3、lioh、naoh、koh中的至少一种提供,狄尔斯-阿尔德反应的温度为130~250℃,如可以是130℃、150℃、200℃、220℃、250℃等。
[0058]
在一实施例中,上述羟醛缩合反应和狄尔斯-阿尔德反应均在有机溶剂中进行,具体地,在含苯的芳香类有机溶剂中进行,例如羟醛缩合反应在硝基苯溶剂中进行,狄尔斯-阿尔德反应在等体积比的甲苯和硝基苯的混合溶剂中进行。上述含苯的芳香类有机溶剂可以更好地进行羟醛缩合反应和狄尔斯-阿尔德反应。
[0059]
本技术实施例第二方面提供一种磺化苯代聚苯基离聚物,该磺化苯代聚苯基离聚物由本技术实施例上述磺化苯代聚苯基离聚物的制备方法制备得到。
[0060]
因此,基于本技术实施例的磺化苯代聚苯基离聚物的制备方法的特点,该特有的磺化苯代聚苯基离聚物的制备方法得到的磺化苯代聚苯基离聚物不仅获取成本低廉,而且相关结构容易优化和调控,因此被申请实施例的磺化苯代聚苯基离聚物具有合成简单、成本低廉、得到的离聚物分子量高、易于调控等特点,可用作质子交换膜具有很好的应用前景,例如可以用于燃料电池、电解池、液流电池等电化学能源转换装置中。
[0061]
本技术实施例第三方面还提供一种质子交换膜,该质子交换膜的材料包括本技术实施例上述磺化苯代聚苯基离聚物的制备方法制备得到的磺化苯代聚苯基离聚物。
[0062]
基于本技术实施例该磺化苯代聚苯基离聚物的制备方法的特点,本技术实施例的质子交换膜不仅成本低廉,而且可以有效控制离聚物的离子交换膜容量,因此在燃料电池、电解池、液流电池等电化学能源转换装置中具有很好的应用前景。
[0063]
下面结合具体实施例进行说明。
[0064]
实施例1
[0065]
一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0066]
(1)前驱体聚合物制备:在100ml带有磁子、进气口、冷凝管的三口瓶中加入1.0g 4,4
’‑
二溴苯偶酰,5g铜粉催化剂和33ml n-甲基吡咯烷酮(nmp)溶剂,在n2保护条件下150℃反应24h,待温度冷却至室温后,出料至1m hno3水溶液中除去催化剂,用0.5m hno3水溶液洗涤3次后,用超纯水洗涤产物至溶液为中性,过滤并收产物,在80℃条件下真空烘干24h,得到前驱体聚合物0.56g,产率100%。
[0067]
(2)羟醛缩合反应:在100ml带有磁子、进气口、dean-stark装置的三口瓶中加入
0.5g上述前驱体聚合物,20ml硝基苯,1.0g koh和1.2g双(4-磺酸苯基)丙酮,在n2保护条件下,180℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到初始聚合物1.4g,产率95%。
[0068]
(3)狄尔斯-阿尔德反应:在100ml带有磁子、dean-stark装置,进气口的三口瓶中加入0.5g上述初始聚合物,10ml硝基苯,0.21g 4-磺酸苯乙炔,0.78g k2co3,10ml甲苯,在n2保护条件下,200℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到最终的磺化苯代聚苯基离聚物0.6g,产率96%。
[0069]
合成路线如下:
[0070][0071]
实施例2
[0072]
一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0073]
(1)前驱体聚合物制备:在100ml带有磁子、进气口、冷凝管的三口瓶中加入1.0g 3,3
’‑
三氟甲基-4,4
’‑
二溴苯偶酰,3.8g铜粉催化剂和33ml nmp溶剂,在n2保护条件下150℃反应24h,待温度冷却至室温,出料至1m hno3水溶液中除去催化剂,用0.5m hno3水溶液洗涤3次后,用超纯水洗涤产物至溶液为中性,过滤并收集产物,在80℃条件下真空烘干24h,得到前驱体聚合物0.66g,产率97%。
[0074]
(2)羟醛缩合反应:在100ml带有磁子、进气口、dean-stark装置的三口瓶中加入0.5g上述前驱体聚合物,20ml硝基苯,0.5g koh和0.65g双(4-磺酸苯基)丙酮,在n2保护条件下,180℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到初始聚合物0.9g,产率94%。
[0075]
(3)狄尔斯-阿尔德反应:在100ml带有磁子、dean-stark装置,进气口的三口瓶中加入0.5g上述初始聚合物,10ml硝基苯,0.16g 4-磺酸苯乙炔,0.63g k2co3,10ml甲苯,在n2保护条件下,200℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到最终的磺化苯代聚苯基离聚物0.6g,产率98%。
[0076]
合成路线如下:
[0077][0078]
实施例3
[0079]
一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0080]
(1)前驱体聚合物制备:在100ml带有磁子、进气口、冷凝管的三口瓶中加入1.0g 3,3
’‑
甲基-4,4
’‑
二氯苯偶酰,0.64g联吡啶,1.07g ni(cod)2和15ml nmp溶剂,在n2保护条件下80℃反应4h,待温度冷却至室温,出料至1m hcl水溶液中除去催化剂,用1.0m hcl水溶液洗涤3次后,用超纯水洗涤产物至溶液为中性,过滤并收集产物,在80℃条件下真空烘干24h,得到前驱体聚合物0.75g,产率98%。
[0081]
(2)羟醛缩合反应:在100ml带有磁子、进气口、dean-stark装置的三口瓶中加入0.5g上述前驱体聚合物,20ml硝基苯,0.7g koh和0.94g双(4-磺酸苯基)丙酮,在n2保护条件下,180℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到初始聚合物1.18g,产率98%。
[0082]
(3)狄尔斯-阿尔德反应:在100ml带有磁子、dean-stark装置,进气口的三口瓶中加入0.5g上述初始聚合物,10ml硝基苯,0.11g苯乙炔,0.4g k2co3,10ml甲苯,在n2保护条件下,200℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到最终的磺化苯代聚苯基离聚物0.58g,产率97%。
[0083]
合成路线如下:
[0084][0085]
实施例4
[0086]
一种磺化苯代聚苯基离聚物的制备方法,包括如下步骤:
[0087]
(1)前驱体聚合物制备:在100ml带有磁子、进气口、冷凝管的三口瓶中加入1.0g双(4-溴-2-全氟己基苯基)丙酮,0.64g双(频哪醇合)二硼,0.34g pd(pph3)4,0.41g k2co3,15ml dmf,在n2保护条件下100℃反应24h,待温度冷却至室温,加入30ml dmf稀释,然后过滤移除催化剂,收集滤液并倒入水中有聚合物析出,手机聚合物并用水洗涤3次,收集产物,在80℃条件下真空烘干24h,得到前驱体聚合物0.82g,产率98%。
[0088]
(2)羟醛缩合反应:在100ml带有磁子、进气口、dean-stark装置的三口瓶中加入0.5g上述前驱体聚合物,20ml硝基苯,0.27g 3,3
’‑
磺酸苯偶酰,0.3g koh,在n2保护条件下,180℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到初始聚合物0.68g,产率97%。
[0089]
(3)狄尔斯-阿尔德反应:在100ml带有磁子、dean-stark装置,进气口的三口瓶中加入0.5g上述初始聚合物,10ml硝基苯,0.09g苯乙炔,0.07g k2co3,10ml甲苯,在n2保护条件下,200℃反应48h,待温度冷却至室温,该溶液出料至乙酸乙酯中,然后用乙酸乙酯洗涤聚合3次,超纯水洗涤产物至中性,过滤并收集产物,在80℃条件下真空烘干24h,得到最终的磺化苯代聚苯基离聚物0.73g,产率99%。
[0090]
合成路线如下:
[0091][0092]
以上所述仅为本技术的较佳实施例而已,并不用以限制本技术,凡在本技术的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本技术的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1