一种检测TLR10rs11096957基因型的方法及其在评估移植肝功能中的应用
一种检测tlr10 rs11096957基因型的方法及其在评估移植肝功能中的应用
技术领域
1.本发明涉及基因检测技术领域,具体涉及一种检测tlr10rs11096957基因型的方法及其在评估移植肝功能中的应用。
背景技术:
2.肝脏移植是目前公认的治疗各种终末期肝病的最佳治疗手段,可明显提高终末期肝病病人的存活时间。肝功能是肝移植术后随访的主要项目,其核心指标的变化趋势或稳定程度可以帮助医务人员判断肝移植预后的综合情况。对肝功能实施严密的监测能够及时发现随访期间可能会出现的并发症(例如急性排异、药物性损伤)等情况。总胆红素(total bilirubin,tbil)和直接胆红素(direct bilirubin,dbil)是评价肝功能的两个指标,其随时间的变化是评估移植后肝功能进程的推荐手段。肝移植患者需要使用免疫抑制剂来降低移植排斥,以提高移植肝的存活率。而免疫抑制剂作用不足可能增加排斥反应的风险,过强有可能引起不良反应的发生,包括肝毒性等,这些因素都会影响移植后tbil和dbil的变化,使得移植后肝功能在个体间具有很大的差异。
3.遗传因素是造成移植肝功能的个体差异的重要因素之一,而单核苷酸多态性(single nucleotide polymorphisms,snp)是最常见的遗传变异形式,90%的个体差异是由snp造成的。
4.toll样受体(toll-like receptors,tlrs)是参与天然免疫的一类重要蛋白质分子,是微生物入侵后预警免疫系统必需的天然免疫受体,在机体抗感染免疫激活机体天然免疫中发挥重要作用。并且tlrs通过调控单核/巨噬细胞、树突状细胞等抗原提呈细胞的活化,cd80等第二信号的表达,在天然免疫和获得性免疫之间起着重要的桥梁作用。此外,新近的研究表明,tlrs还参与某些自身免疫性疾病及机体的移植免疫,动物实验和临床研究也报道了tlrs与同种异体排斥反应程度相关联,其过度的免疫应答反应可以引发移植物排斥反应。因此tlrs信号通路参与移植免疫的研究已成为器官移植领域研究的热点之一。
5.目前,在哺乳动物及人类中已经发现的人tlrs家族成员有13种,即tlr1-tlr13。其分布十分广泛,主要分布于单核细胞、巨噬细胞、树突状细胞、多形核细胞、b细胞、t细胞、嗜碱性粒细胞及nk细胞等淋巴细胞。tlr10是tlrs家族的一个重要成员,主要表达在免疫相关的组织和细胞,包括脾、淋巴结、人类b细胞等。不同于其他tlrs家族成员,tlr10具有抑炎作用,对其他tlr信号、炎症因子的产生、单核细胞和b细胞的活化具有抑制作用。
6.已有文献研究报道了tlr10可能与一些肿瘤、免疫疾病和感染疾病相关,如膀胱癌、iga肝病、克罗恩病、哮喘、肺曲霉菌病、关节炎等等。也有在同种异体造血干细胞移植患者中的研究中发现tlr10与急性移植物抗宿主疾病的发病相关。tlr10基因多态性与许多免疫性疾病的发病密切相关,而且tlrs与器官移植免疫的相关性已经得到公认,tlr10基因多态性对于评估肝移植患者移植肝功能具有重要意义。
7.目前仍无预测肝移植患者移植肝功能的可靠手段。鉴于它对移植肝存活率的影
响,对其预测无疑具有很大的临床及经济学价值。
技术实现要素:
8.为了克服现有技术中的缺陷,本发明提供了一种检测tlr10 rs11096957基因型的方法,进而为制备用于评估肝移植患者移植肝功能以及评价患者在肝移植后是否需要重点监测肝脏病理变化、调整治疗方案的产品提供策略。本发明是基于时间飞行质谱(maldi-tof)技术对tlr10 rs11096957基因型进行检测的,该方法的技术原理如下:首先通过pcr扩增含有snp的基因组片段,然后通过序列特异性引物实现单碱基延伸,随后样品分析物与芯片基质共结晶后在真空管中受瞬时纳秒(10-9
s)强激光激发;核酸分子因此解吸附成为单电荷离子,由于电场中离子飞行时间与离子质量成反比,通过检测核酸分子在真空管中的飞行时间而获得样品分析物的精确分子量,从而检测出snp位点信息。
9.为实现上述目的,本发明采用如下技术方案:
10.本发明的第一方面是提供一种检测tlr10 rs11096957基因型的方法,其包括如下步骤:
11.步骤一,提取肝移植患者全血基因组dna,调整浓度后进行pcr扩增;
12.步骤二,扩增的pcr产物经sap处理后,进行单碱基延伸反应;
13.步骤三,纯化单碱基延伸反应产物,用飞行时间质谱仪进行检测,进行基因分型。
14.进一步地,基因组dna的浓度被调整为20-50ng/μl。
15.进一步地,步骤一中pcr扩增所采用的引物的序列为seq id no.:1和seq id no.:2。
16.进一步地,步骤二中单碱基延伸反应所采用的单碱基延伸引物的序列为seq id no.:3。
17.本发明的第二方面是提供上述方法采用的试剂在制备用于评估肝移植患者移植肝功能的产品中的应用,该产品包括上述方法采用的试剂以及使用说明书。
18.进一步地,上述使用说明书包括如下指示:
19.a.采用上述方法检测tlr10 rs11096957基因型;
20.b.基于分型检测结果根据评估标准对患者肝功能进行评估;该分型检测结果选自tg型、tt型和gg型中的一种;该评估标准为:携带tg/tt型的肝移植患者移植后肝功能的恢复较携带gg型的患者更慢。
21.进一步地,上述产品为试剂盒。
22.本发明的第三方面是提供上述方法采用的试剂在制备用于评价肝移植患者在移植后是否需要重点监测肝脏病理变化的产品中的应用,该产品包括上述方法采用的试剂以及使用说明书。
23.进一步地,上述使用说明书包括如下指示:
24.a.采用上述方法检测tlr10 rs11096957基因型;
25.b.基于分型检测结果根据评价标准对肝移植患者在移植后是否需要重点监测肝脏病理变化进行评价;该分型检测结果选自tg型、tt型和gg型中的一种;评价标准为:携带tg/tt型的患者需要重点监测肝脏病理变化,调整治疗方案;携带gg型的患者不需要重点监测肝脏病理变化,调整治疗方案。
inhibitor,cni)、霉酚酸(mycophenolic acid,mpa)和糖皮质激素。钙调磷酸酶抑制剂为他克莫司(tac,普乐可复,astellas,ireland),霉酚酸包括霉酚酸酯(mmf,骁悉,roche,shangha,china)和霉酚酸钠(mps,米芙,novartis,basel,switzerland),糖皮质激素为强的松或甲强龙。
44.tac的起始剂量为0.1-0.15mg/kg/d,早晚各口服一次。之后通过tdm及剂量调整将tac谷浓度维持在:第一个月内8-10ng/ml,第1-3个月6-8ng/ml,此后维持在4-6ng/ml,特殊情况下可根据临床需要调整个体目标浓度值。
45.mmf或mps从术后第一天开始给药,每天2次。mmf给药剂量按照体重梯度调整,对于体重<50kg,50~70kg,>70kg的患者,初始剂量分别为1.0g/天、1.5g/天和2.0g/天,并在1个月后分别减量至0.75g/天、1.0g/天和1.5g/天。mps的给药剂量按照0.18g mps=0.25g mmf换算。
46.糖皮质激素从手术当天开始给药。手术当天静脉注射1g甲强龙,之后连续3天每天静脉注射500mg。术后第四天开始改用强的松80mg口服,按每天10mg/天递减至20mg(第10天),3个月后再次减量至10mg/天。
47.3.移植肝功能指标
48.移植肝功能使用移植术后术后tbil和dbil变化评估,收集术后基础值、1-12个月tbil和dbil进行统计。基础值定义为移植初期tbil和dbil值。
49.4.基因型检测
50.所有入选肝移植患者,采集外周静脉血2ml,edta抗凝,-20℃冰箱保存用于基因型检测。
51.肝移植患者基因分型方法采用massarray时间飞行质谱。用dna提取试剂盒提取全血基因组dna,并调整浓度为20-50ng/μl。探针及引物由上海生物工程公司合成。dna模板进行pcr循环,pcr产物进行sap处理及延伸反应。延伸产物纯化后,将检测样品从384孔反应板转移到表面覆盖基质的massarray spectrochip芯片,将样品转移到spectrochip芯片后,即可放入质谱仪进行检测,typer软件分析实验结果,获得分型数据。
52.具体步骤如下:
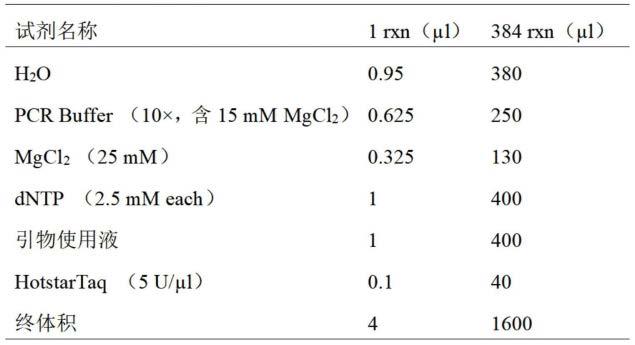
53.(1)多重pcr反应:查找目的基因序列,针对突变位点,设计并合成pcr引物(acgttggatgggcaaaagccaatttgtaag(seq id no.:1)和acgttggatgaggtcgtcccagagtaaatc(seq id no.:2)),在384孔板各孔中分别加入1μl dna和4μl pcr反应液,封膜、短暂离心后,放入pcr仪,运行pcr反应程序。pcr反应程序为:94℃15min,45个循环(94℃20sec,56℃30sec,72℃1min),72℃3min。
54.表1 pcr反应液成分
[0055][0056]
(2)sap处理:在384孔板各孔中分别加入2μl sap反应液,封膜、离心后,放入pcr仪,运行sap反应程序。sap反应程序:37℃40min,85℃5min。
[0057]
表2 sap反应体系
[0058][0059]
(3)延伸反应:设计单碱基延伸引物tctgcaacgaaatcttagtttagaa(seq id no.:3);在384孔板各孔中分别加入2μl iplex反应液,封膜、离心后,放入pcr仪,运行extension反应程序。延伸反应条件为:94℃30sec,40个循环(94℃5sec,5个小循环(52℃5sec,80℃5sec)),72℃3min。
[0060]
表3延伸反应体系
[0061][0062]
(4)产物纯化:将反应结束的384孔板1,000rpm离心1min,每孔加入25μl去离子水,倒置在384孔树脂板上,然后反置将树脂板扣在384孔板上,敲击使树脂落入384孔板,封膜后翻转384孔板20min,3,500rpm离心5min;
[0063]
(5)质谱检测:将检测样品从384孔反应板转移到表面覆盖基质的massarray spectrochip芯片,放入massarray analyzer compact质谱仪进行检测,typer软件分析实验结果,获得分型数据(其中tt、tg和gg的分型图分别如图1-3)。
[0064]
5.关联性研究的统计分析
[0065]
基因多态性对tbil和dbil变化趋势的影响采用混合线性模型进行重复测量数据的分析,将数据集重组为mixed可分析结构,重复测量方差结构选择复合对称结构;采用多因素混合线性模型对snp进行多因素统计分析,将年龄、性别、体重、诱导免疫治疗等临床混杂因素作为混杂因素纳入模型。
[0066]
6.统计结果
[0067]
为了考察tlr10 rs11096957基因多态性对移植后肝功能的影响,我们采用线性混合模型分析了snp与肝移植患者移植后1年内tbil和dbil变化趋势之间的关系。分析发现snp对tbil和dbil变化趋势有显著影响,tg/tt基因型的患者tbil和dbil明显比gg基因型下降更慢(tbil:-55.8%vs.-75.0%,p=0.001,图4a,表4;dbil:-66.4%vs.-87.8%,p=0.002,图4b,表5)。
[0068]
表4 tlr10 rs11096957基因多态性对移植后tbil的影响
[0069][0070]
表5 tlr10 rs11096957基因多态性对移植后dbil的影响
[0071]
[0072][0073]
多因素分析纳入了年龄、性别、体重、诱导免疫治疗等临床混杂因素,考察纳入这些因素后rs11096957基因多态性对移植后肝功能的影响,结果见表6-7,结果与单因素分析一致,rs11096957基因多态性影响tbil和dbil变化趋势,gg基因型的患者tbil和dbil下降的速度快于tg/tt基因型(tbil:p=0.003;dbil:p=0.005)。
[0074]
表6 tlr10 rs11096957基因多态性对移植后tbil影响的多因素分析
[0075][0076]
表7 tlr10 rs11096957基因多态性对移植后dbil影响的多因素分析
[0077][0078][0079]
7.结论
[0080]
上述结果可以看出,以肝移植患者为研究对象,携带tg/tt型的患者移植后1年内
tbil和dbil的下降较gg型的患者更慢。
[0081]
因此可通过检测肝移植患者的tlr10 rs11096957基因型来预测该待测患者移植后肝功能,tg/tt基因型的待测患者比gg基因型的待测患者移植肝功能恢复更慢。
[0082]
基于检测结果可以有助于风险预测,携带tg/tt型的患者需要重点监测肝脏病理变化,调整治疗方案;携带gg型的患者不需要重点监测肝脏病理变化,调整治疗方案。
[0083]
以上对本发明的具体实施例进行了详细描述,但其只作为范例,本发明并不限制于以上描述的具体实施例。对于本领域技术人员而言,任何对本发明进行等同修改和替代也都在本发明的范畴之中。因此,在不脱离本发明精神和范围下所作的均等变换和修改,都应涵盖在本发明的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1