一种激活肿瘤免疫的基因修饰干细胞制备方法与流程
1.本发明属于生物医药领域,具体涉及一种激活肿瘤免疫的基因修饰干细胞制备方法。
背景技术:
2.肿瘤(tumour)是指机体在各种致瘤因子作用下,局部组织细胞增生所形成的新生物,因为这种新生物多呈占位性块状突起,也称赘生物。根据新生物的细胞特性及对机体的危害性程度,又将肿瘤分为良性肿瘤和恶性肿瘤两大类。恶性肿瘤可分为癌和肉瘤,癌是指来源于上皮组织的恶性肿瘤。肉瘤是指间叶组织,包括纤维结缔组织、脂肪、肌肉、脉管、骨和软骨组织等,发生的恶性肿瘤。研究发现,肿瘤细胞会出现不同于正常细胞的代谢变化,同时肿瘤细胞自身可通过糖酵解和氧化磷酸化之间的转换来适应代谢环境的改变。针对t细胞表面的免疫检查点开发抗体一直是肿瘤免疫治疗的热点之一,但是除了ctla-4、pd-1这类细胞表面抑制性受体之外,t细胞表面还有一类激活性受体分子,同样在机体的免疫应答中具有重要作用,ox40就是其中之一。
3.ox40(又称cd134、tnfrsf4、act35)属肿瘤坏死因子受体超家族(tnfrsf),是分子量约50kda的ⅰ型跨膜糖蛋白,共含有277个氨基酸(胞浆49个氨基酸、胞外186个氨基酸)。ox40是一个相对保守的分子,其胞外段的配体结合区主要由三个完整的半胱氨酸富集区crd1、crd2、crd3和一个不完整的半胱氨酸富集区crd4组成。
4.在体内,ox40主要是在活化的cd4
+
t、cd8
+
t细胞表面诱导性表达,而初始t细胞及未致敏的记忆t细胞都不表达ox40。此外,ox40还表达于调节t细胞、nk细胞、nkt细胞和中性粒细胞。tcr信号可以诱导ox40表达,但其在t细胞表面的高表达仍需要额外的共刺激信号和相关细胞因子的协助,例如cd28-b7.1/2、il-2和tnf等。t细胞在抗原刺激24小时后开始表达ox40,并在48-72小时后表达量达到峰值。ox40的表达时长取决于tcr信号及相关的共刺激信号的强弱,通常持续5-6天。ox40在记忆t细胞上的表达要比效应t细胞迅速的多,通常在激活后1-4小时内。在体外培养的细胞系中,仅有少数细胞系能够表达ox40,且全部都是htlv-1感染的人t淋巴细胞,其中绝大部分是cd4
+
t细胞,例如,hut-102、mt-2、atl-43t和pha刺激的pbmc,未刺激的pbmc则不能表达。除上述细胞外,目前暂未发现其他细胞能够表达ox40。
5.专利cn201880050094.x公开了用于癌症治疗的treg消耗性抗体分子,如treg消耗性抗4-1bb抗体或treg消耗性ox-40抗体,可特异性结合属于肿瘤坏死因子受体超家族(tnfrsf)的靶标。专利cn201910303942.x则公开了一种重组的抗ox40(cd134)抗体及其用途,所述抗体能够与哺乳动物ox40特异性结合,优选地具有对人和/或灵长类动物ox40蛋白的高亲和性、在一定浓度下可刺激t细胞的活化及增殖等效果。
6.使用ox40激动剂抗体增强ox40信号可通过激活增强t细胞介导的抗肿瘤免疫,增强效应种属特异性t细胞免疫应答,增强细胞因子il-2、il-5和ifn-g的产生,并增强抗原激发后肿瘤特异性记忆t细胞的生成,有助于肿瘤消退和延长生存期,ox40激动剂可能增加t
细胞浸润肿瘤,并增强常规cd4和cd8t细胞的抗肿瘤免疫应答,从而改善几种临床前癌症模型的生存率,包括b16黑色素瘤、lewis肺癌、结肠癌、乳腺癌和4t-1乳腺癌。因此,ox40/ox40l通路激动剂能被用于癌症免疫治疗。然而治疗性单克隆抗体药物虽然具有先进的抗癌功能,但是抗体的免疫原性、肿瘤靶点长期使用的耐受性以及单纯性阻断信号转导通路的长期效果等问题仍有待进一步研究,多数单抗很难实现对肿瘤细胞的长期有效抑制和杀伤作用。
7.基于此,亟需一种新的方法解决上述单抗的不足,用于制备激活肿瘤免疫的药物。
技术实现要素:
8.针对上述不足,本发明提供了一种激活肿瘤免疫的间充质干细胞及其应用。本发明通过采用基因工程手段使间充质干细胞表达ox-40单抗融合蛋白,可增强效应t细胞的活化和增殖,特异性结合高ox-40表达的treg细胞,从而抑制肿瘤细胞免疫逃逸,达到治疗肿瘤相关疾病的目的。
9.为了实现上述发明目的,本发明的技术方案如下:
10.一方面,本发明提供了一种抗ox-40单克隆抗体融合蛋白(以下简称“ox-40单抗融合蛋白”或“融合蛋白”)的编码核苷酸,所述的编码核苷酸包含编码ox-40抗体的核苷酸。
11.具体地,所述的编码ox-40抗体的核苷酸包含编码ox-40抗体轻链可变区vl的seq id no:3或seq id no:5所示的核苷酸序列、和编码ox-40抗体重链可变区vh的seq id no:4或seq id no:6所示的核苷酸序列。
12.所述的seq id no:3所示的核苷酸序列为:
13.gacatccaaatgactcagagtccaagttctttgtccgcctcagttggcgacagagtaacgatcacttgcagagccagccaagatatcagtaactacttgaattggtaccaacagaaacctgggaaggcaccgaaacttctgatctactacacatctaaacttcattcaggcgtcccttcacgcttctctggttccggctctggaactgactacacactgacaatttcaagtctccagcccgaagattttgcaacatattattgtcaacagggctccgcgctcccatggacgtttggacaaggaacgaaggtagaaatcaag;
14.所述的seq id no:4所示的核苷酸序列为:
15.caagttcaacttcaggaatcaggtcccggcttggttaagccttcacagacactctccctgacttgtgcagtgtatggcggttcttttagtagtgggtattggaattggataaggaagcatccaggaaaaggtcttgagtacatcgggtatatcagttacaatgggatcacctatcacaacccgagcctgaagtcccgaataactattaacagggacacctctaaaaaccagtatagccttcaattgaatagtgttacgccagaggatactgctgtgtactactgtgctagatacaaatacgactatgatggaggacatgcgatggactactggggacagggaaccctggtgaccgtctcctcc;
16.所述的seq id no:5所示的核苷酸序列为:
17.gacatacaaatgacccagagtcctagctcactatcggcgtctgtcggtgaccgggtgaccatcacatgtcgagcctcgcaggacatatcgaactaccttaactggtaccagcagaaacctgggaaagcaccaaagcttttaatctactatacttcgaagcttcattctggtgtcccatcgcgtttcagcggatctggttccgggacagactacaccctgaccatatcaagcctgcaacccgaagattttgcgacttactactgccaacagggatcagctcttccatggacgttcgggcaaggcacaaaggtcgagattaaa;
18.所述的seq id no:6所示的核苷酸序列为:
19.caggtccaattgcaggagtcaggacctgggctcgtcaagccgtcacagactttatctttgacatgcgc
agtgtatgggggatcgttctcaagcggttactggaactggattagaaagcatccggggaaggggctagagtacattgggtatatctcgtataacggaatcacgtaccacaatccctcgttgaagagcaggattaccatcaacagggacacgtcaaaaaatcagtacagtcttcaactgaattcagtaactcccgaggatacggcggtatattactgtgcccgatacaaatatgactacgacggaggtcatgcgatggactactgggggcagggtacgctggttacggttagctcg。
20.进一步具体地,所述的编码ox-40抗体的核苷酸还包含编码信号肽的seq id no:1所示的核苷酸序列、编码接头的seq id no:2所示的核苷酸序列。
21.具体地,所述的编码核苷酸还包含编码人免疫球蛋白igg1的fc片段的核苷酸,所述的编码igg1的fc片段的核苷酸为seq id no:7所示的核苷酸序列。
22.进一步具体地,所述的编码核苷酸为seq id no:8或seq id no:9所示的序列。
23.具体地,所述的编码核苷酸编码ox-40单抗融合蛋白,所述的ox-40单抗融合蛋白包含ox-40抗体和人免疫球蛋白igg1的fc片段。
24.进一步具体地,所述的ox-40抗体包含seq id no:10所示的氨基酸序列的信号肽、seq id no:11所示的氨基酸序列的接头、seq id no:12所示的氨基酸序列的ox-40抗体轻链可变区vl、和seq id no:13所示的氨基酸序列的ox-40抗体重链可变区vh。
25.进一步具体地,所述的人免疫球蛋白igg1的fc片段为seq id no:14所示的氨基酸序列。
26.进一步具体地,所述的ox-40单抗融合蛋白的氨基酸序列为seq id no:15所示的氨基酸序列。
27.所述的ox-40单抗作为ox40激动剂,具有激活t细胞(包括cd4、cd8等t细胞亚群)功能,增强细胞因子il-2、ifn-g等的产生,从而提高抗肿瘤活性的作用。
28.又一方面,本发明提供了一种包含上述编码核苷酸的载体。
29.具体地,所述的载体包括但不限于质粒、病毒、噬菌体。
30.又一方面,本发明提供了一种包含上述编码核苷酸或上述载体的宿主细胞。
31.具体地,所述的宿主细胞包括但不限于微生物、植物或动物细胞,优选为间充质干细胞。
32.具体地,所述的核苷酸或载体通过基因工程技术导入所述的宿主细胞。
33.进一步具体地,所述的基因工程技术包括但不限于病毒转染、脂质体转染、电转移、基因编辑或mrna转染的技术,优选为采用慢病毒载体系统。
34.又一方面,本发明提供了生产上述ox-40单抗融合蛋白的方法,所述的方法包括在使得所述融合蛋白表达的情况下,培养上述宿主细胞。
35.又一方面,本发明提供了一种间充质干细胞,所述的间充质干细胞包含上述编码核苷酸或上述载体。
36.具体地,所述的间充质干细胞为骨髓组织、脂肪组织、脐带组织或胎盘组织来源的间充质干细胞。
37.又一方面,本发明提供了一种上述间充质干细胞的制备方法,所述的制备方法包括以下步骤:
38.(1)构建包含上述ox-40单抗融合蛋白编码核苷酸序列的慢病毒表达载体;
39.(2)将步骤(1)得到的慢病毒表达载体感染宿主细胞,包装得到成熟慢病毒;
40.(3)收获步骤(2)得到的成熟慢病毒,感染间充质干细胞,筛选感染成功的细胞。
41.在本发明某些实施例中,首先利用慢病毒载体系统构建ox-40单抗融合蛋白的慢病毒表达质粒,其中,ox-40单抗融合蛋白是ox-40抗体与igg1的重链fc片段组成的融合蛋白,ox-40单抗融合蛋白编码基因的3'-末端先后连接ires序列和egfp基因,形成ox-40:fc-i-egpf序列,共同处于lv-egfp慢病毒载体中cmv启动子的下游;其次,将慢病毒表达质粒与慢病毒框架质粒pgag/pol、prev、pvsv-g混合,通过ltx脂质体导入hek293t细胞中完成基因转录后,慢病毒载体被成功包装并释放到hek293t细胞培养基的上清中,然后收集含有重组慢病毒载体的上清液;最终,用收获的上清中的重组慢病毒感染间充质干细胞,24h后加入嘌呤霉素筛选得到感染成功的间充质干细胞。通过间充质干细胞核糖体表达ox-40单抗融合蛋白,并在信号肽的指导下分泌到细胞外,特异性结合高ox-40的treg细胞,从而抑制肿瘤细胞免疫逃逸,达到治疗肿瘤相关疾病的目的。
42.又一方面,本发明提供了一种药物组合物,所述的药物组合物包含上述编码核苷酸、载体、宿主细胞和/或间充质干细胞。
43.具体地,所述的药物组合物还包含任选的药学上可接受的载体。
44.进一步具体地,所述的药学上可接受的载体包括但不限于:稀释剂、赋形剂、填充剂、润湿剂、崩解剂、矫味剂和粘合剂。
45.具体地,所述的药物组合物可以单独、依次或者同时与其他药物联合施用,联合施用的其他药物非限制性的选自青霉素、阿莫西林、苄青霉素、氨苄青霉素、阿奇霉素、红霉素、克拉霉素、头孢羟氨苄、头孢克肟、四环素、米诺环素、利福平、利福布汀、氨苯磺胺、氨基糖甙、杆菌肽、多粘菌素b、奥硝唑、视黄醇、视黄醛、异维甲酸、维胺酯、阿达帕、他扎罗汀、雌激素、孕激素、糖皮质激素、抗雄性激素、维生素d3类似物如卡泊三醇和他卡西醇、糖皮质激素类药物如泼尼松和甲泼尼松、他克莫司、吡美莫司、环孢素a、霉酚酸酯、白三烯b4抑制剂、il-1抑制剂、il-2抑制剂、il-1β抑制剂,il-6抑制剂、il-8抑制剂、il-12抑制剂、il-23抑制剂、il-17抑制剂、tnf抑制剂、gm-csf抑制剂、cd19抑制剂、cd20抑制剂。联合治疗的方法还包括与光动力疗法、激光疗法、果酸疗法的联合施用。
46.又一方面,本发明提供了上述编码核苷酸、载体、宿主细胞和/或间充质干细胞在制备用于预防和/或治疗肿瘤的药物、试剂盒和/或医疗装置中的应用。
47.与现有技术相比,本发明的积极和有益效果在于:
48.本发明所得到的经修饰的间充质干细胞能够表达ox-40单抗融合蛋白,利用间充质干细胞对肿瘤部位的靶向作用及免疫调节能力和损伤部位的修复能力,通过基因修饰的方法,使间充质干细胞特异表达ox-40单抗融合蛋白至肿瘤部位而发挥作用。所述的ox-40单抗融合蛋白作为ox40/ox40l通路激动剂可增强效应t细胞的活化和增殖,特异性结合ox-40高表达的t淋巴细胞,特异激活cd4
+
t、cd8
+
t细胞,从而抑制肿瘤细胞免疫逃逸,达到治疗肿瘤相关疾病的目的。本发明为肿瘤等疾病的治疗提供了较为理想的新方法。
附图说明
49.图1为lv-ox40:fc-i-egfp质粒信息示意图。
50.图2为流式细胞法检测基因修饰干细胞表达绿色荧光蛋白结果图。
51.图3为elisa检测细胞分泌的融合蛋白igg1蛋白含量结果图。
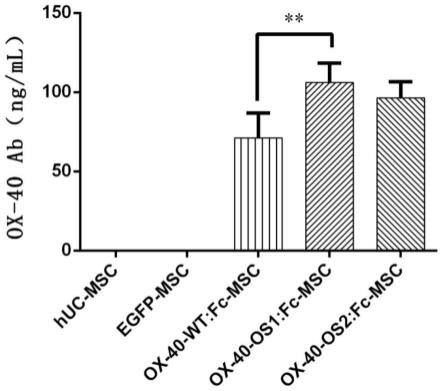
52.图4为通过与ox-40蛋白结合实验检测基因修饰干细胞细胞分泌的ox40单抗含量
结果图。
53.图5为检测基因修饰干细胞激活外周血淋巴细胞分泌ifn-γ的实验结果图。
具体实施方式
54.下面结合具体实施例,对本发明作进一步详细的阐述,下述实施例不用于限制本发明,仅用于说明本发明。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
55.术语
56.为了更容易理解本发明,以下具体定义了某些技术和科学用语。除非在本文中另有明确定义,本文使用的所有的其他技术和科学术语都具有本公开所属领域的一般技术人员通常理解的含义。
57.本发明所用氨基酸三字母代码和单字母代码如j.biol.chem,243,p3558(1968,iupac-iub委员会)中所述。
58.与重组dna、寡核苷酸合成、组织培养和转化(例如电穿孔、脂质体转染)、酶促反应和纯化技术结合使用的示例性技术是本领域已知的。许多这样的技术和程序描述于,例如,sambrook等人,molecular cloning:a laboratory manual(第2版,cold spring harbor laboratory press,cold spring harbor,n.y.(1989)),以及其他许多地方。
59.本发明所述的“表达载体”是指包含重组多核苷酸的载体,其包含有效连接要表达的核苷酸序列的表达控制序列。表达载体包含用于表达的顺式作用元件;用于表达的其它元件可以由宿主细胞提供或在体外表达系统中。表达载体包括本领域已知的所有那些,包括被掺入重组多核苷酸的粘粒、质粒(例如,裸的或包含在脂质体中)和病毒(例如,慢病毒、逆转录病毒、腺病毒和腺伴随病毒)。
60.本发明所述的“宿主细胞”是可用于表达核酸,例如本发明的核酸的细胞。宿主细胞可以是原核生物,例如,大肠杆菌(e.coli),或其可以是真核生物,例如,单细胞真核生物(例如,酵母或其他真菌)、植物细胞(例如,烟草或番茄植物细胞)、动物细胞(例如,人细胞、猴细胞、仓鼠细胞、大鼠细胞、小鼠细胞或昆虫细胞)或杂交瘤。
61.本发明所述的“间充质干细胞”(mscs)来源于发育早期中胚层,具有多种细胞功能,包括受损组织的修复及再生、参与机体免疫调节、促进血管新生、炎症部位归巢和靶向作用以及抑制肿瘤生长。与成人组织相比,从脐带等组织中分离出的mscs具有更好的体外生长潜力和更高的再生能力,msc被定义为具有一些共同的基本特性,如体外可塑性粘附,表面标志cd73、cd90和cd105的表达以及体外成骨、成脂、成软骨的分化能力。除了这些典型的mscs特征之外,脐带来源的mscs可以产生和释放更多的转化生长因子-β(tgf-β)、血管内皮因子-α(vegf-α)和表皮生长因子(egf)。
62.肿瘤微环境中如成纤维细胞生长因子-2(fgf-2)、单核细胞趋化蛋白-1(mcp-1)、促炎因子白介素-6(il-6)和肿瘤坏死因子α(tnfα)的大量分泌有助于mscs聚集于肿瘤部位,而免疫细胞与肿瘤间质内的mscs的相互作用可以激活mscs的免疫调节能力。mscs可以分泌多种免疫调节剂,如一氧化氮(no)、前列腺素e2(pge2)、白细胞介素6(il-6)、白细胞介素10(il-10)、吲哚胺2,3-双加氧酶(ido)的代谢产物等,与诱导免疫耐受和t细胞th1向th2
id no:15)。所述的ox-40抗体包含seq id no:10所示的氨基酸序列的信号肽、seq id no:11所示的氨基酸序列的接头、seq id no:12所示的氨基酸序列的ox-40抗体轻链可变区vl、和seq id no:13所示的氨基酸序列的ox-40抗体重链可变区vh;所述的人免疫球蛋白igg1的fc片段为seq id no:14所示的氨基酸序列。
73.ox-40单抗融合蛋白的编码基因(seq id no:8或seq id no:9所示的序列)包括ox-40抗体的核苷酸序列和编码igg1重链fc片段的核苷酸序列,其中,所述的编码ox-40抗体的核苷酸包含编码信号肽的核苷酸seq id no:1所示的序列、编码接头的核苷酸seq id no:2所示的序列、编码ox-40抗体轻链可变区vl的核苷酸seq id no:3或seq id no:5所示的序列、和编码ox-40抗体重链可变区vh的核苷酸seq id no:4或seq id no:6所示的序列;编码igg1重链fc片段的核苷酸序列为seq id no:7所示的核苷酸序列。
74.ox-40单抗融合蛋白编码基因(seq id no:8或seq id no:9所示的序列)的3'-末端先后连接ires序列和egfp基因,形成ox-40-os1:fc-i-egfp或ox-40-os2:fc-i-egfp序列,共同处于cmv启动子下游(载体示意图见图1)。
75.具体地,seq id no:3或seq id no:5所示的编码ox-40抗体轻链可变区的核苷酸序列由seq id no:16所示的wt序列优化得到,seq id no:4或seq id no:6所示的编码ox-40抗体重链可变区的核苷酸序列由seq id no:17所示的wt序列优化得到。同时,利用所述的wt序列构建ox-40-wt:fc-i-egfp序列(该序列编码ox-40抗体轻链可变区的核苷酸序列为seq id no:16所示的wt序列,编码ox-40抗体重链可变区的核苷酸序列为seq id no:17所示的wt序列,其余序列与ox-40-os1:fc-i-egfp或ox-40-os2:fc-i-egfp序列相同)。
76.按照上述基因结构,利用常规的基因工程手段将目的基因片段插入lv-egfp质粒的相应位点,得到慢病毒表达质粒lv-ox-40-os1:fc、lv-ox-40-os2:fc和lv-ox-40-wt:fc。
77.实施例2.病毒制备及收获
78.将实施例1制备的lv-ox-40-os1:fc、lv-ox-40-os2:fc和lv-ox-40-wt:fc质粒分别与慢病毒框架质粒pgag/pol、prev、pvsv-g,通过ltx脂质体转染到hek293t细胞中,成功包装的重组慢病毒载体释放到hek293t细胞培养上清液中,收获含有重组慢病毒载体的细胞培养上清液。同时制备对照lv-egfp病毒。
79.实施例3.基因修饰间充质干细胞的制备
80.将实施例2中收获的含有重组慢病毒载体的细胞培养上清液进行超滤纯化,并加入到对数生长期的p2-p3代脐带间充质干细胞中,重组慢病毒载体感染间充质干细胞24h后换液,继续培养24小时后再次换液,加入嘌呤霉素筛选得到成功感染的间充质干细胞egfp-msc、ox-40-os1:fc-msc、ox-40-os2:fc-msc、ox-40-wt:fc-msc。
81.实施例4.流式细胞法检测基因修饰干细胞表达绿色荧光蛋白
82.将实施例3中的成功感染慢病毒的间充质干细胞接种至t75培养瓶中,待细胞培养至80%后收获细胞,通过流式细胞法检测慢病毒感染后间充质干细胞发出的绿色荧光(结果见图2),发现lv-egfp及lv-ox40-os1:fc、lv-ox-40-os2:fc、lv-ox-40-wt:fc慢病毒感染后的间充质干细胞均可在绿色荧光通道检测到阳性信号,而正常间充质干细胞无绿色荧光,表明lv-egpf及lv-ox40:fc融合蛋白的慢病毒均可成功感染间充质干细胞,感染率达到85%以上。
83.实施例5.elisa检测细胞分泌的融合蛋白igg1蛋白含量
84.采用igg1 elisa试剂盒(bms2092,thermo)检测细胞培养上清中分泌的融合蛋白igg1含量。
85.将实施例3获得的基因修饰间充质干细胞培养72小时后收获细胞上清,并将细胞培养上清加入igg1 elisa试剂盒,检测融合蛋白中igg1蛋白水平,结果发现,lv-ox-40-os1:fc、lv-ox-40-os2:fc与lv-ox-40-wt:fc慢病毒感染后的间充质干细胞(ox-40-os1:fc-msc、ox-40-os2:fc-msc和ox-40-wt:fc-msc)均高表达igg1,且表达量在27.5-35.8ng/ml之间,三组相比没有显著差异(p》0.05),而正常huc-msc及egfp-msc不表达igg1(结果见图3)。
86.实施例6.elisa检测基因修饰干细胞细胞分泌的ox-40单抗含量
87.采用ox-40重组蛋白结合ox-40抗体的方式检测细胞培养上清中ox-40抗体的表达情况。
88.将human ox40/tnfrsf4/cd134 proteinfc tag(acro,ox0-h5255)以1μg/ml的浓度包被酶标板,封闭后,以anti-ox-40antibody(sinobiological 10481-t16)为标准品加入标准品空中,将实施例3中获得的基因修饰间充质干细胞培养72h后收获的上清加入样品孔中,孵育2h后,hrp结合的抗人igg抗体(acro,ig1-s71)、hrp结合抗兔igg抗体(southernbiotech,4055-05)作为酶标抗体孵育1h,后加入tmb显色液显色10-20min,终止液终止,酶标仪检测od450nm读数。结果见图4,ox-40-os1:fc-msc、ox-40-os2:fc-msc和ox-40-wt:fc-msc均可以表达与重组ox-40蛋白结合的ox-40抗体,且ox-40-os1:fc-msc分泌的ox-40抗体浓度最高,为106.0
±
12.3ng/ml,与ox-40-wt:fc-msc相比,有显著性差异(p<0.01),而正常huc-msc及egfp-msc则不表达ox-40抗体。
89.实施例7.检测基因修饰干细胞激活外周血淋巴细胞分泌ifn-γ
90.通过检测pbmc活化后分泌的炎性因子ifn-γ来检测基因修饰间充质干细胞的活化功能,分离人pbmc细胞,加入抗-cd3抗体(biolegend,317325)(1μg/ml)和抗-cd28抗体(biolegend,302933)(1μg/ml)与实施例3获得的各组细胞(1*104/cm2接种24孔板并培养24h)共培养72h,以抗-cd3抗体(1μg/ml)、抗-cd28抗体(1μg/ml)刺激pbmc 72h为对照组,通过elisa(r&d,dif50c)检测细胞上清中ifn-γ的浓度。
91.结果发现,cd3/cd28可以刺激pbmc分泌ifn-γ,浓度为473.2
±
68.2pg/ml,正常huc-msc及egfp-msc细胞可以显著抑制活化的pbmc分泌ifn-γ,浓度为57.6
±
4.8pg/ml,而ox-40-os1:fc-msc、ox-40-os2:fc-msc和ox-40-wt:fc-msc细胞则可以显著增强pbmc中ifn-γ的释放,ifn-γ浓度分别为1462.4
±
122.8pg/ml、1209.6
±
176.1pg/ml、922.2
±
97.3pg/ml;与ox-40-wt:fc-msc细胞相比,ox-40-os1:fc-msc对pbmc中ifn-γ的释放增加58.6%(p《0.01)。
92.以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1