一种与宫颈癌相关的微卫星位点及其检测引物的制作方法
1.本发明涉及基因检测领域,尤其涉及一种与宫颈癌相关的微卫星位点及其检测引物。
背景技术:
2.微卫星是遍布于人类基因的短串联重复序列,高度可变,在真核生物基因组中无处不在。由于高度可变性,微卫星在人群中趋于变化,因此被广泛用作分子标记、连锁作图、谱系作图和基因型鉴定的目的。
3.当其发生突变、丢失的时候,主要通过dna错配修复系统(mismatch repair,mmr)来修复。如果mmr基因发生失活,引起dna错配修复功能缺陷,导致细胞修复错配碱基的功能降低或缺失,会产生微卫星不稳定(msi),这种机制广泛存在于各种癌症中。
4.msi在结肠癌中,可作为遗传性非息肉病性结直肠癌的诊断依据之一。因msi表型实体瘤会在选择性高度上调包括pd-1、pd-l1、ctla-4等多个免疫检查点的表达,故而亦是免疫检查点抑制剂的适应症,也是晚期转移性结肠癌的用药指征。
5.目前,对于宫颈癌相关的微卫星位点的研究并不多见,而进一步发掘与宫颈癌相关的微卫星位点,对于宫颈癌的临床辅助诊断具有新的意义,也对宫颈癌的进一步用药治疗提供新的思路。
技术实现要素:
6.为了解决目前宫颈癌相关微卫星位点研究不足的情况,本发明提供如下技术方案。
7.本发明公开了一种与宫颈癌相关的微卫星位点组合物,所述组合物包括:包括bat26微卫星位点的核苷酸,包括d6s2447微卫星位点的核苷酸,包括线粒体基因d-loop区微卫星位点的核苷酸,包括nr24微卫星位点的核苷酸。
8.本发明公开了一种用于检测宫颈癌相关的微卫星位点的引物组合物,所述引物组合物包括:检测bat26微卫星位点的引物,检测d6s2447微卫星位点的引物,检测线粒体基因d-loop区微卫星位点的引物,检测nr24微卫星位点的引物。
9.优选的,检测bat26微卫星位点的引物分别如seq id no:1和2所示,检测d6s2447微卫星位点的引物分别如seq id no:3和4所示,检测线粒体基因d-loop区微卫星位点的引物分别如seq id no:5和6所示,检测nr24微卫星位点的引物分别如seq id no:7和8所示。
10.优选的,所述seq id no:1和2的序列分别为ccagtat atgaaattgga和tttaaccattcaacattt。
11.优选的,所述seq id no:3和4的序列分别为actctggtagacattctaga和tgcatttctcttccttatcac。
12.优选的,所述seq id no:5和6的序列分别为cactccca tactactaat和ctgtggggggtgtctttgg。
13.优选的,所述seq id no:7和8的序列分别为tct gccttaacgt gatccc和ctgggtgacagagtgagac。
14.优选的,所述引物组合物还包括内参位点引物。
15.优选的,所述内参为qs21和qs7。
16.优选的,所述内参qs21的引物分别如seq id no:9和10所示。
17.优选的,所述seq id no:9和10的序列分别为ttgctcttgccctattaca和ctactatccgctcagaga。
18.优选的,所述内参qs7的引物分别如seq id no:11和12所示。
19.优选的,所述seq id no:11和12的序列分别为cgtaaaaaggccgcatacta和gacttgagcgtcgattttaca。
20.优选的,所述引物采用荧光基团进行标记。
21.优选的,所述荧光基团选自:fam、hex、tet、joe、tam、ned、vic、cy3、cy5、rox或tamra。
22.本发明所述的复合扩增体系中涉及到的2个试剂内参位点的设计参考为puc18+质粒,参考puc18+质粒的序列,分别设计扩增产物为120bp和330bp的pcr扩增引物,本扩增体系中所用的试剂内参模板为puc18+质粒。
23.本发明公开了一种用于检测与宫颈癌相关的微卫星位点的试剂盒,所述试剂盒包括所述的组合物和/或所述的引物组合物。
24.本发明公开了一种检测微卫星不稳定性的方法,所述方法包括以下步骤:采用所述的组合物,或所述的试剂盒,对待测dna进行荧光定量pcr和毛细管电泳,根据结果判断微卫星不稳定性的状态。
25.优选的,所述的dna来源于病理组织、石蜡包埋切片组织、肿瘤细胞或外周血中的任意一种。
26.本发明进一步提供了一种适合用于石蜡包埋切片的dna提取方法。
27.本发明进一步提供了一种用于石蜡包埋切片dna的荧光定量pcr方法。
28.优选的,所述pcr反应程序为:95℃,65-90秒;95℃变性,30-60秒;58-62℃退火,70-90秒;扩增30-40个循环;60℃终延伸,45-60分钟。
29.本发明提供了4组与宫颈癌相关的微卫星位点及其扩增引物,采用本发明的引物可以用于检测宫颈癌患者中微卫星位点的突变情况,对于宫颈癌的诊断以及进一步的治疗具有重要的意义。
附图说明
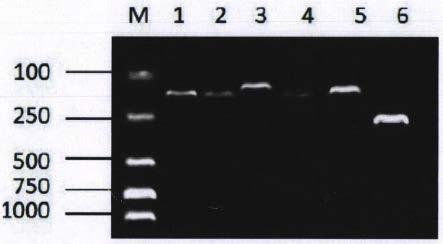
30.图1为微卫星位点及内参基因扩增产物琼脂糖电泳结果,其中,1为bat26,2为d6s2447,3为线粒体基因d-loop区,4为nr24,5为qs21,6为qs7。
31.图2为微卫星位点bat26扩增引物荧光定量pcr灵敏度检测。
32.图3为微卫星位点d6s2447扩增引物荧光定量pcr灵敏度检测。
33.图4为微卫星位点线粒体基因d-loop区扩增引物荧光定量pcr灵敏度检测。
34.图5为微卫星位点nr24扩增引物荧光定量pcr灵敏度检测。
具体实施方式
35.以下实施例进一步说明本发明的内容,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改或替换,均属于本发明的范围。
36.若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段。
37.实施例1样本来源
38.收集南方某医院近一年内经手术切除的宫颈癌组织以及癌旁正常组织,以及医院自己制备的石蜡包埋切片组织。患者年龄,35-65岁,平均年龄46岁。按照figo2000年修订的标准进行临床分期,其中,ia期8例,ib-iia期12例。手术切除宫颈癌组织17例,石蜡包埋切片组织3例。
39.实施例2样本基因组的制备
40.普通组织:将组织块剪碎、匀浆,蛋白酶k消化,酚/氯仿抽提,乙醇沉淀,te溶解。加pcr缓冲液等,溶液直接用于pcr扩增。
41.石蜡包埋组织:(1)向装有组织的ep管中加入1.0ml二甲苯溶剂,振荡器充分振荡,60℃水浴保温15min,室温离心5min,移走上清液,加入无水乙醇,振荡器充分振荡,室温离心5min(12000r/min),弃上清液。重复上述步骤一次。打开离心管盖子,37℃保温10~15min。(2)加入200μl细胞裂解液,振荡至彻底悬浮,加入40μl蛋白酶k溶液,充分混匀。56℃水浴箱放置8h,每小时颠倒混匀样品2~3次,直至组织完全溶解。(3)加入200μlpb缓冲液,充分颠倒混匀,70℃放置10min至溶液变清亮,加入250μl无水乙醇,充分振荡混匀,将离心管内溶液及絮状沉淀加入吸附柱内(吸附柱放入收集管中),12000rpm离心1min,倒掉收集管中的废液,吸附柱放回收集管,向吸附柱中加入500μlte缓冲液,12000rpm离心1min,倒掉收集管中的废液,吸附柱放回收集管,向吸附柱中加入700μl异丙醇,12000rpm离心1min,倒掉收集管中的废液,吸附柱放回收集管,向吸附柱中加入500μl无水乙醇,重复上一步骤,将吸附柱放回收集管,12000rpm离心5min,吸附柱置于室温15min,吸附柱转入一个干净的1.5ml离心管中,向吸附膜的中间部位悬空滴加150μlte洗脱液,室温放置5min,12000rpm离心1min。
42.实施例3微卫星位点扩增引物的设计
43.根据选取的微卫星位点前后的核苷酸序列,设计扩增的引物序列,微卫星位点信息及对应的扩增引物的信息如下表1所示。
44.表1:微卫星位点及设计的扩增引物信息
[0045][0046][0047]
实施例4微卫星位点扩增反应体系的建立
[0048]
将设计好的引物交给基因引物合成公司合成之后,首先以各个msi位点靶标片段为模板,分别进行单重pcr引物的反应,扩增完成后将扩增产物进行2.5%琼脂糖凝胶电泳,根据电泳结果,对pcr的体系和扩增条件作出调整;最终保证在同一扩增体系和同一扩增条件下,6对引物都能获得单一特异性条带。扩增结果采用琼脂糖凝胶检测如图1所示。
[0049]
优化获得的pcr反应程序为:95℃,80秒;95℃变性,45秒;60℃退火,60秒;扩增40个循环;60℃终延伸,40分钟。
[0050]
实施例5微卫星位点荧光pcr扩增反应体系的建立以及引物灵敏度测定
[0051]
将扩增4组微卫星位点的引物以及两对内参引物分别标记上不同的荧光素,先进行单重扩增,扩增产物置于abi3500d遗传分析仪上进行毛细管电泳检测,根据毛细管电泳检测的结果来评估每对引物的扩增效率在单重扩增的基础上,优化反应体系,再进行复合扩增。
[0052]
表2:微卫星位点扩增体系
[0053][0054][0055]
利用建立起来的荧光pcr扩增反应体系及反应条件,进一步检测所述引物的检测灵敏度,具体操作如下:
[0056]
以包含各个msi位点的多核苷酸序列作为模板,将模板进行不同的浓度的稀释获得如下各浓度:每微升拷贝数为106、105、104、103、102、101、的样品进行qpcr检测,测定该检测方法的灵敏度。各个msi位点荧光定量pcr检测的灵敏度结果分别如图2、图3、图4和图5所示。从检测结果来看,本发明申请设计的扩增引物均能够对每微升拷贝数为10的模板进行扩增,具有较高的灵敏度。
[0057]
实施例6宫颈癌样本微卫星位点的检测
[0058]
以实施例1中的提取的宫颈癌患者组织以及癌旁正常组织的dna为模板,对每个样本荧光定量pcr检测,并进一步将扩增产物置于abi3500d遗传分析仪上进行毛细管电泳检测。对于每一个样本的有效的扩增结果,其中与正常组织相比,患者组织的各个微卫星位点的扩增长度与正常组织的微卫星位点扩增长度不一致的,判定为该宫颈癌患者存在微卫星不稳定性状。
[0059]
具体判定标准如下:有3个及以上位点发生变化,则定义为msi-h(微卫星高不稳定状态),只有1个或2个位点变化的定义为msi-l(微卫星低不稳定状态),没有任何位点发生变化的定义为mss(微卫星稳定状态)。
[0060]
各个样本的微卫星检测位点的检测结果如下表3.
[0061]
表3:宫颈癌组织微卫星位点不稳定性检测结果
[0062][0063][0064]
其中:
○
表示宫颈癌样本该微卫星位点相对于正常组织未变化
[0065]
※
表示宫颈癌样本该微卫星位点相对于正常组织有变化
[0066]
从上述检测结果可以看出,在这20例宫颈癌组织样本中,其中有4个微卫星位点发生变化的样品为0个,其中有3个微卫星位点发生变化的样品为1个,其中有2个微卫星位点发生变化的样品为4个,其中有1个微卫星位点发生变化的样品为14个,没有微卫星变化发生的样本为1个。其中线粒体基因d-loop区是上述四个微卫星位点中最易发生变化的位点,在20个样本中有8个样本在该位点均存在微卫星位点的变化。
[0067]
实施例7宫颈癌样本微卫星位点的检测准确性
[0068]
将实施例1中的20例宫颈癌患者的组织样本在采用本发明的引物对进行分型测定之后,进一步采用普罗麦格的宫颈癌检测试剂盒进行比对,其中采用普罗麦格的宫颈癌检测试剂盒检测样本,有两例未检出,显示为正常,经过计算,本发明的微卫星位点检测其符合率高于普罗麦格的宫颈癌检测试剂盒。检测结果如下表4。
[0069]
表4:宫颈癌样本微卫星位点的检测准确性
[0070][0071][0072]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明技术原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1