1.本发明涉及功能菌技术领域,尤其涉及一种具有降血压作用的干酪乳杆菌及其应用。
背景技术:2.高血压作为导致多项心血管疾病的原因之一,其血压水平越高,则心脑血管疾病的发生概率越大。血压的升高与冠心病、中风等疾病高度相关。因此,有效控制血压是预防和降低心血管死亡率的重要干预手段。高血压是一种常见多发病,会导致患者多器官病变,降低他们的生活质量,严重威胁甚至损害患者的生命安全,是我国的一个重大公共卫生问题,也是成年人死亡、患病和残疾的主要原因。目前,高血压的治疗主要是长期服用降压剂,目前市面上销售的降压剂人工合成较多,抑制效果较强。然而,长期使用合成降压剂不仅会对人体肾脏等一些器官产生副作用,还会伴有疼痛、发热等症状,使人体的正常生理功能受到不同程度的损害。
3.近年研究表明食用菌中存在的功能活性成分对降低血压有积极的作用。通常来说,食用菌的降血压作用与血管紧张素转化酶(ace)有着密切的联系。ace是一种含zn
2+
的二肽羧基肽酶,在人体肾素-血管紧张素系统(ras)和激肽-激肽原酶系统(kks)中发挥调节血压的重要作用。人体肾素在血管紧张素的水解下能产生不活跃的血管紧张素ⅰ,血管紧张素ⅰ在ace的作用下,十肽血管紧张素ⅰ切断的末端c组氨酸亮氨酸二肽转化为血管紧张素ⅱ,血管紧张素ⅱ强烈的血管收缩功能导致血管收缩。
4.ace抑制肽(acei)是从食物中提取的一种具有抑制ace活性的多肽。acei之所以能够替代降压药物的潜在可能性,是因为它对正常的血压没有影响,但有抑制高血压的作用,与降压药相比,对人体没有毒副作用。γ-氨基丁酸(gaba)是一种非蛋白质组成的天然氨基酸,是哺乳动物中枢神经系统主要的抑制性神经递质。gaba通过对中枢神经系统的调节来抑制ace活性和扩张血管,从而达到降低血压的作用。因此,从天然食物中分离得到的ace抑制剂对人体生理功能影响温和,与合成降压药相比,对人体没有毒副作用,有成为替代降压药物的可能性。
5.然而,由于菌株来源不同或个体差异导致菌株产gaba的能力不同。从同一菌属的不同来源和同一来源不同菌种两方面分析,陆小雪等在辣白菜和酸奶中分离出10株产gaba菌,10株菌产gaba能力差异显著(陆小雪,解春艳,顾振新.产γ-氨基丁酸乳酸菌的分离与鉴定[j].南京农业大学学报,2009,32(1):121-125.)。根据分析表明,不同来源的菌种之间以及同一来源的不同菌种之间所产gaba含量有着明显的差异,可能是因为不同种类或不同来源的微生物对gaba的合成条件存在差异性。
[0006]
而现已筛选到的一些菌株的ace抑制率较低。如,吴霖等筛选的乳杆菌发酵乳gy-3的ace抑制活性最高为79.52%(吴霖,葛洋,张海坤,等.一株高ace抑制活性乳杆菌的筛选鉴定、培养条件优化及其基因组分析[j].微生物学通报,2019,46(11):2830-2847.)。因此,有必要进一步开发ace抑制活性高的菌株。
技术实现要素:[0007]
本发明的目的在于提供一种具有降血压作用的干酪乳杆菌及其应用。
[0008]
为了实现上述发明目的,本发明提供以下技术方案:
[0009]
本发明提供了一种干酪乳杆菌(lactobacillus casei)slk30,该菌株保藏于广东省微生物菌种保藏中心,地址广州市先烈中路100号大院59号楼5楼,保藏日期为:2022年3月9日,保藏编号为:gdmcc no:62280。
[0010]
本发明还提供了一种干酪乳杆菌slk30在制备降血压药物或功能食品中的应用。
[0011]
优选的,所述药物为血管紧张素转化酶活性抑制剂。
[0012]
优选的,所述功能食品为发酵凝乳制品。
[0013]
优选的,所述功能食品中含有血管紧张素转化酶活性抑制剂。
[0014]
优选的,所述血管紧张素转化酶活性抑制剂为γ-氨基丁酸和/或血管紧张素转化酶抑制肽。
[0015]
本发明提供的干酪乳杆菌slk30对ace抑制率和产gaba能力较为理想,为降血压益生菌株。发酵特性研究表明干酪乳杆菌slk30有较好的产酸能力,而且能达到发酵乳的酸度要求,其发酵乳的ace抑制活性也比较高,且干酪乳杆菌slk30还具有较好的耐酸耐胆盐能力,对指示菌常见致病菌金黄色葡萄球菌、大肠杆菌、伤寒沙门氏菌具有较强的抑制作用,可以作为潜在的降血压益生菌在发酵食品中应用。
附图说明
[0016]
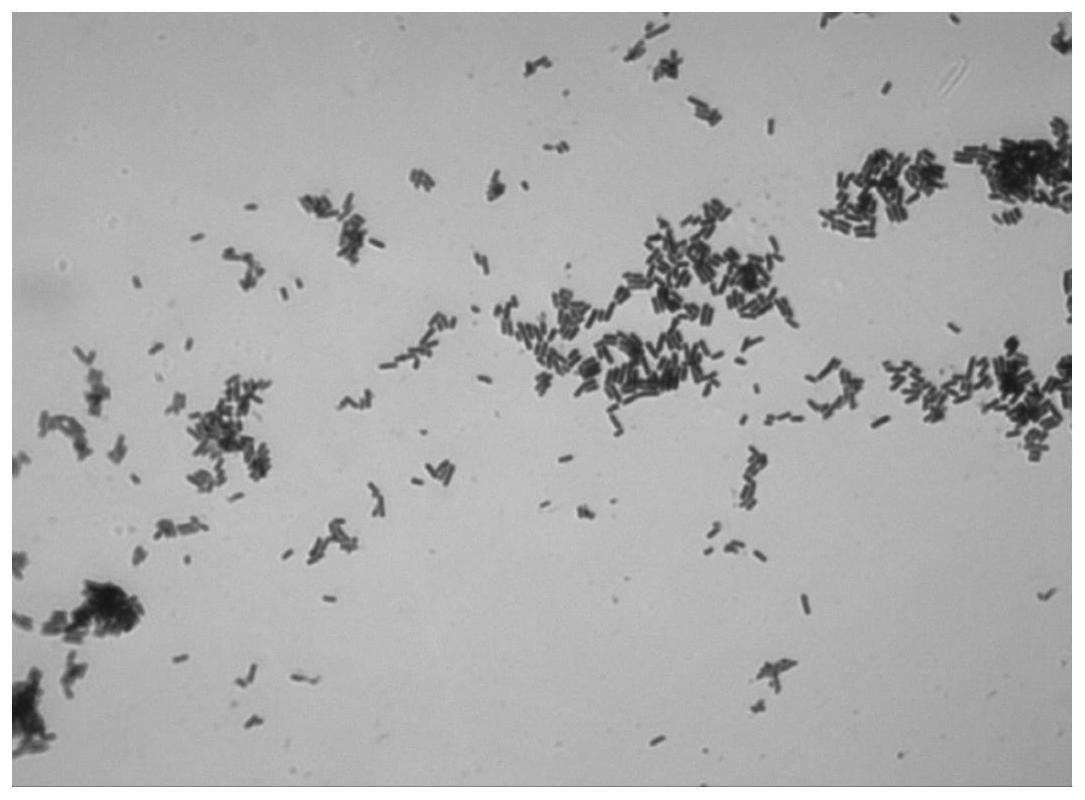
图1为干酪乳杆菌slk30菌体形态(100
×
);
[0017]
图2为实施例1中干酪乳杆菌slk30的溶血试验结果;
[0018]
图3为实施例2中采用高效液相色谱法测定gaba含量的标准工作曲线;
[0019]
图4为实施例2中干酪乳杆菌slk30发酵上清液中gaba含量测定高效液相色谱图。
[0020]
保藏说明
[0021]
干酪乳杆菌(lactobacillus casei)slk30,该菌株保藏于广东省微生物菌种保藏中心,地址广州市先烈中路100号大院59号楼5楼,保藏日期为:2022年3月9日,保藏编号为:gdmcc no:62280。
具体实施方式
[0022]
本发明实施例中所用试剂生产厂家和生产批号如表1所示
[0023]
表1实施例所用试剂生产厂家和生产批号信息
[0024][0025][0026]
表2实施例所用一起生产厂家和型号/规格信息
[0027]
仪器名称型号/规格生产厂家分析天平me204e上海梅特勒-托利多仪器有限公司生化培养箱shp-150上海精宏实验设备有限公司高速冷冻离心机biofuge stratos赛默飞世尔科技公司ph计pb-10德国赛多利斯集团超净工作台sw-cj-2f苏州安泰空气技术有限公司立式压力蒸汽灭菌器ym 50上海三申医疗器械有限公司循环水真空泵shz
‑ⅲ
上海亚荣生化仪器厂高效液相色谱仪agilent hp 1100美国hp公司滴定装置dz-1上海雷磁仪器厂牛津杯6
×8×
10mm上海申源科学仪器有限公司
[0028]
下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
[0029]
实施例1
[0030]
本发明提供的干酪乳杆菌slk30,来源于发酵饲料样本,该菌株经测序分析,将测序得到的序列在ezbiocloud database中进行核酸序列比对,结果显示菌株为干酪乳杆菌,并将其命名为干酪乳杆菌(lactobacillus casei)slk30。其微生物形态学特征为:呈圆形,乳白色半透明,表面平滑,有凸起,边缘整齐。显微镜观察成对或链状出现,属于革兰氏阳性菌株。菌体形态如图1所示。
[0031]
溶血能力测定
[0032]
按2%的接种量将干酪乳杆菌slk30接种至已灭菌的mrs肉汤培养基中,在37℃培养24h,活化至2代,使菌株活力恢复至正常,备用。
[0033]
将干酪乳杆菌slk30用一次性接种环划“mi”型接种于含5%无菌脱纤维羊血的血琼脂平板中,于37℃培养24h,观察菌落周围变化情况。结果如图2,从图2中可以看出菌落周围既无透明圈也无绿色圈,不会产生溶血作用,为γ-溶血,为安全菌株。因此,干酪乳杆菌slk30在溶血作用方面具有良好的安全性,无强致病性。
[0034]
实施例2
[0035]
产gaba能力测定
[0036]
加入1%的l-谷氨酸钠至mrs肉汤培养基中,121℃高压灭菌15min,按3%的接种量取实施例1中活化2代的干酪乳杆菌slk30接种于mrs培养液中,37℃静置培养24h后,离心(5200r/min,20min),收集发酵上清液于-40℃冰箱保存备用。
[0037]
gaba标准稀释样品浓度:0.1g/l、0.2g/l、0.4g/l、0.6g/l、0.8g/l;分别取200μl gaba标准稀释样品,分别加入600μl opa衍生试剂,混匀后加入800μl kh2po4缓冲液,涡旋混匀后经有机膜过滤,待进样。
[0038]
色谱柱:agilentc-18柱;流动相a(15mmol/l ch3cooh-ch3coona缓冲液):流动相b(甲醇)=55:45;0.8ml/min;30℃;334nm;自动进样;进样量为20μl。
[0039]
得到gaba标准稀释样品色谱图,以gaba的色谱峰面积为纵坐标、对应的质量浓度为横坐标绘制标准工作曲线,如图3所示。由图3可知,当gaba浓度在0.1~0.8g/l范围内时,线性方程为y=5889.195x+57.078,r2为0.999,说明gaba衍生物的峰面积与其质量浓度有很好的呈正比的线性关系,可用于gaba的定量分析。
[0040]
取制备的发酵上清液200μl,加入600μl opa衍生试剂,混匀后加入800μl kh2po4缓冲液,涡旋混匀后经有机膜过滤,得到发酵上清液的待进样。按照gaba标准稀释样品的色谱条件进行高效液相检测,色谱图见图4。得到发酵上清液中gaba含量为0.362g/l。可见,干酪乳杆菌slk30产gaba能力较强。
[0041]
实施例3
[0042]
对ace抑制率能力
[0043]
按3%的接种量取实施例1中活化2代的干酪乳杆菌slk30接种于灭菌的12%脱脂奶粉中,在42℃下发酵发酵34h,得到发酵乳,将发酵乳于4500g离心10min,取上清液,用1.0mol/l naoh调ph至7.5,用ace试剂盒测定干酪乳杆菌slk30对ace的抑制活性。ace抑制活性的测定方法按照ace试剂盒说明书上的方法进行测定。结果显示干酪乳杆菌slk30对ace的抑制率为89.99%,对ace的抑制活性较高。
[0044]
实施例4
[0045]
为了进一步开发干酪乳杆菌slk30的应用范围,本实施例对干酪乳杆菌slk30的产酸特性、耐酸能力、耐胆盐能力、抑菌能力进行测试,以期将其用于制备降血压的功能食品。
[0046]
发酸特性的测定
[0047]
参照国标gb4789.35-2016《食品安全国家标准食品微生物学检验乳酸菌检验》将实施例1中活化2代的干酪乳杆菌slk30按体积分数2%的接种量接入至12%灭菌脱脂乳中,在37℃发酵培养24h。将已充分混匀的发酵乳菌悬液进行10倍系列梯度稀释,分别吸取稀释
10-5
、10-6
cfu/ml的菌液接种于mrs琼脂培养基平板上,用一次性涂布器将菌液涂布均匀,再将平板倒置于37℃恒温培养箱中培养48h,对菌落形成单位(cfu/ml)进行计数。
[0048]
采用ph计法测定ph,平行2次;
[0049]
参照国标gb5009.239-2016《食品安全国家标准食品酸度的测定》测定乳酸菌发酵乳滴定酸度,平行2次。
[0050]
乳酸菌数量能够反映出乳酸菌的发酵程度和营养价值的高低,产酸能力能够很好的表现出乳酸菌活力强弱,由表3可知,干酪乳杆菌slk30活菌数为7个对数值,完全符合活菌数的要求标准。干酪乳杆菌slk30发酵终点ph值为4.65,表明干酪乳杆菌slk30具有较好的产酸能力。滴定酸度的测定结果与ph值基本上是相对应的,在发酵期间,菌株滴定酸度为94.35,满足gb 19302-2010《食品安全国家标准发酵乳》中规定酸度≥70
°
t的要求。从ace抑制活性的测定来看,干酪乳杆菌slk30的ace抑制活性比较高,为89.99%。由于gaba合成通常是通过生物体内的gad催化,将l-谷氨酸或其钠盐经α-脱羧而得来的,从表3测定的发酵乳gaba含量来看,由于没有添加外源的l-谷氨酸钠,因此,gaba含量较低,因此,在产品发酵时需要添加外源l-谷氨酸钠,以得到gaba含量高的产品。
[0051]
表3干酪乳杆菌slk30的发酵特性结果
[0052][0053]
耐酸能力测定
[0054]
将干酪乳杆菌slk30活化2代的菌液离心(12000g,10min),收集菌体,用灭菌水将菌体洗涤震荡,制成菌悬液,用酶标仪测定波长560nm处的浊度,使其od
595nm
为0.8,于4℃冰箱冷藏,备用。
[0055]
吸取ph=2.0,ph=2.5和ph=3.0的酸液各100μl,其中使用前,向ph=3.0的酸液中加入0.3%的胃蛋白酶,作为模拟胃液。然后分别加入150μl的菌悬液,每个样品平行测定3次,37℃培养16h;分别在0h和16h测定od
610nm
值,计算其存活率(%),存活率计算公式如下:
[0056]
存活率(%)=(16h od
610nm
/0h od
610nm
)
×
100%
[0057]
由表4可知,干酪乳杆菌slk30在不同测试的ph水平下均具有高的存活率。通常情况下,人体胃液ph范围为3.0左右,干酪乳杆菌slk30在此ph内若能有较高的存活率,则表明菌株对胃酸有一定的耐受性,适合在酸性环境中生存。
[0058]
表4干酪乳杆菌slk30耐酸能力实验结果
[0059][0060]
耐胆盐能力测定
[0061]
吸取菌悬液150μl分别加入牛胆盐浓度为0.0%、0.3%、0.5%和1.0%的胆盐-mrs液体培养基中,每个样品平行测定3次,37℃培养16h;分别在0h和16h测定其od
610nm
值,计算其存活率(%),计算公式如下:
[0062]
存活率(%)=(16hod
610nm
/0hod
610nm
)
×
100%
[0063]
结果如表5。人体肠道中的胆盐浓度一般在0.03%~0.3%浓度范围内波动,乳酸菌在胆盐浓度内若能有较高的存活率,则表明菌株对胆盐有一定的耐受性。从表5可知,干酪乳杆菌slk30在不同胆盐浓度中均有良好的耐受性,在0.3%胆盐环境中培养16h后存活率为119.14%;在0.5%胆盐浓度中培养16h后存活率为100.24%。因此,干酪乳杆菌slk30对胆盐均具有较强的耐受性。
[0064]
表5干酪乳杆菌slk30耐胆盐能力实验结果
[0065][0066]
抑菌能力测定
[0067]
用移液枪准确吸取10ml无菌的质量浓度为2%的琼脂溶液至一次性的培养皿中,待完全凝固后,用镊子取4个已灭菌的牛津杯等距离放置于琼脂平板上。吸取致病菌指示菌悬液200μl加入到已分装于锥形瓶中的20ml无菌营养琼脂培养基(50℃)中,混合均匀后迅速倒入培养皿中,使其凝固30min后用镊子取出牛津杯,将培养皿在4℃下放置0.5h后吸取150μl干酪乳杆菌slk30离心上清液注入平板圆孔中,于37℃培养24h,平行2次,24h后用游标卡尺测量抑菌圈4个不同位置的直径(mm)如表6。
[0068]
如表6所示,干酪乳杆菌slk30对三种致病菌的抑菌效果较好,其发酵上清液的抑菌圈直径均大于15.00mm,显示出极佳的抑菌性能,这可能是乳酸菌发酵上清液在发酵过程中产生了有机酸、细菌素、过氧化氢等原因导致的。
[0069]
表6干酪乳杆菌slk30抑菌能力实验结果
[0070][0071]
由以上实施例可知,本发明提供了干酪乳杆菌slk30经溶血实验安全性评价,该菌为安全菌株,且产gaba和ace抑制率较为理想,为降血压益生菌株,发酵特性研究表明干酪乳杆菌slk30有较好的产酸能力,而且能达到发酵乳的酸度要求,其发酵乳的ace抑制活性也比较高,且干酪乳杆菌slk30还具有较好的耐酸耐胆盐能力,对指示菌金黄色葡萄球菌、大肠杆菌和伤寒沙门氏菌具有较强的抑制作用,可以作为潜在的降血压益生菌在发酵食品中应用。
[0072]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
