一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒
1.本发明涉及一种试剂盒,特别是涉及一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒,属于试剂盒技术领域。
背景技术:
2.禽腹泻病是导致家禽死亡的主要原因之一,严重危害家禽健康,影响饲料报酬,制约着家禽养殖业的健康发展;
3.其中沙门氏菌、产气荚膜梭菌和大肠杆菌是引起家禽细菌性腹泻病的主要病原,这3种细菌引起的腹泻病存在着相似的临床症状,临床上主要表现为食欲不振、精神萎靡、背羽粗乱、拉白色或红色稀便等症状,影响家禽的正常生长发育。禽细菌性腹泻一年四季都有可能发生,临床上难以分辨,即可单一感染,也可相互混合感染,给病原的诊断造成了很大的困难。
4.目前禽沙门氏菌、产气荚膜梭菌和大肠杆菌的诊断方法主要包括细菌分离、普通pcr和16s测序等,但这些方法都存在局限性:细菌分离培养操作繁琐、花费时间较长,普通pcr需要凝胶电泳分析,操作繁琐,且灵敏度相对较低,16s测序耗时较长并需要比对分析等,为此设计一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒来解决上述问题。
技术实现要素:
5.本发明的主要目的是为了提供一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒,荧光pcr的灵敏度和试验速度较传统pcr大大提升,并且可以同时特异性检测多种病原。
6.本发明的目的可以通过采用如下技术方案达到:
7.一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒,包括pcr mix、浓度为250nm的primer f/r、浓度为250nm的probe。
8.优选的,所述primer f/r包含有inva-f/r、plc-f/r、phoa-f/r。
9.优选的,
10.inva-f/r扩增得到的目的基因的序列为:gttcgtcattccattacctacctatctggttgatttcctgatcgcactgaatatcgtactggcgatattggtgtttatgggg;
11.其中inva-f/r的识别标记为seq id no.10;
12.plc-f/r扩增得到的目的基因的序列为:atggcaaagaggaaactataaacaagctacattctatcttggagaggctatgcactattttggagatatagatactccatatcatcctgctaatgttactgccgttg;
13.其中plc-f/r的识别标记为seq id no.11;
14.phoa-f/r扩增得到的目的基因的序列为:ctaggactgtttgctgacggcaatatgccagtgcgctggcaaggaccgaaagcaacgtaccacggcaatatcgacaagcccgcagttacctgtacgccta;
15.其中phoa-f/r的识别标记为seq id no.12。
16.优选的,inva-f/r的上游引物为gttcgtcattccattacc;
17.其中inva-f/r的上游引物识别标记为seq id no.1;
18.inva-f/r的下游引物为cccataaacaccaatatcg;
19.其中inva-f/r的下游引物识别标记为seq id no.2。
20.优选的,plc-f/r的上游引物为atggcaaagaggaaacta;
21.其中plc-f/r的上游引物识别标记为seq id no.4;
22.plc-f/r的下游引物为caacggcagtaacattag;
23.其中plc-f/r的下游引物识别标记为seq id no.5。
24.优选的,phoa-f/r的上游引物为ctaggactgtttgctgac;
25.其中phoa-f/r的上游引物识别标记为seq id no.7;
26.phoa-f/r的下游引物为taggcgtacaggtaactg;
27.其中phoa-f/r的下游引物识别标记为seq id no.8。
28.优选的,probe包含有inva-probe、plc-probe、phoa-probe。
29.优选的,所述inva-probe的基因的序列为tcctgatcgcactgaatatcgtactg;
30.其中inva-probe的识别标记为seq id no.3;
31.plc-probe的基因的序列为ctacattctatcttggagaggctatgc;
32.其中plc-probe的识别标记为seq id no.6;
33.phoa-probe的基因的序列为ctggcaaggaccgaaagcaac;
34.其中phoa-probe的识别标记为seq id no.9。
35.优选的,inva-probe的5'端连接有6-fam,3'端连接有bhq1;plc-probe的5'端连接有rox,3'端连接有bhq2;phoa-probe的5'端连接有vic,3'端连接有bhq2。
36.本发明的有益技术效果:
37.本发明提供的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒,荧光pcr的灵敏度和试验速度较传统pcr大大提升,并且可以同时特异性检测多种病原。
附图说明
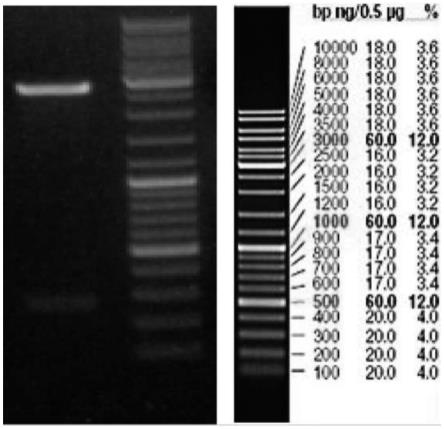
38.图1为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的puc57/inva-plc
–
phoa质粒的酶切分析图;
39.图2为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的inva-f/r/p标准方程图;
40.图3为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的plc-f/r/p标准方程图;
41.图4为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的phoa-f/r/p标准方程图;
42.图5为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的沙门氏菌灵敏度检测分析图;
43.图6为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的大肠杆菌灵敏度检测分析图;
44.图7为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的产气荚膜梭菌灵敏度检测分析图;
45.图8为按照本发明的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒的一优选实施例的特异性检测分析图。
具体实施方式
46.为使本领域技术人员更加清楚和明确本发明的技术方案,下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
47.本实施例提供的一种用于检测禽沙门氏菌、产气荚膜梭菌和大肠杆菌试剂盒,包括pcr mix、浓度为250nm的primer f/r、浓度为250nm的probe。
48.按下述扩增反应体系(如表1所示)和反应程序进行反应:
49.表1
[0050][0051]
其中,引物探针混合物中,各组分均为0.5μl,工作浓度为250nm;
[0052]
阳性标准品为puc57/inva-plc-phoa;
[0053]
阴性标准品为不含沙门氏菌、产气荚膜梭菌和大肠杆菌核酸的生理盐水。
[0054]
反应程序为:95℃30s;95℃5s,59℃30s,45个循环,在每一循环退火结束时收集荧光信号;
[0055]
通过荧光定量pcr仪自带软件读取相应的ct值。具体成立条件和判定标准如表2所示(注:ct值>35,判定为可疑,若重复试验,扩增曲线有明显起峰判定为阳性,否则为阴性,“+”表示重复试验为阳性,
“‑”
表示重复试验为阴性)。
[0056]
表2:
[0057]
[0058][0059]
在本实施例中,所述primer f/r包含有inva-f/r、plc-f/r、phoa-f/r。
[0060]
在本实施例中,inva-f/r扩增得到的目的基因的序列为:gttcgtcattccattacctacctatctggttgatttcctgatcgcactgaatatcgtactggcgatattggtgtttatgggg;
[0061]
其中inva-f/r的识别标记为seq id no.10;
[0062]
plc-f/r扩增得到的目的基因的序列为:atggcaaagaggaaactataaacaagctacattctatcttggagaggctatgcactattttggagatatagatactccatatcatcctgctaatgttactgccgttg;
[0063]
其中plc-f/r的识别标记为seq id no.11;
[0064]
phoa-f/r扩增得到的目的基因的序列为:ctaggactgtttgctgacggcaatatgccagtgcgctggcaaggaccgaaagcaacgtaccacggcaatatcgacaagcccgcagttacctgtacgccta;
[0065]
如图2-4所示,三组引物组inva-f/r/p、plc-f/r/p和phoa-f/r/p对应的标准曲线的相关系数r2均大于0.99,扩增效率均在96%~99%的范围内。起始模板数与ct值之间均呈现良好线性关系,针对inva-f/r/p,6.69
×
100~6.69
×
108copies/μl浓度的pcr扩增曲线均有效,r2为0.99731,扩增效率为99%,标准方程为y=-3.35x+41.58,检出限为66.9copies/μl;针对plc-f/r/p,6.69
×
100~6.69
×
108copies/μl浓度的pcr扩增曲线均有效,r2为0.9966,扩增效率为96%,标准方程为y=-3.41x+40.53,检出限为66.9copies/μl;针对phoa-f/r/p,6.69
×
100~6.69
×
108copies/μl浓度的pcr扩增曲线均有效,r2为0.99703,扩增效率为96%,标准方程为y=-3.41x+40.64,检出限为66.9copies/μl。
[0066]
其中phoa-f/r的识别标记为seq id no.12。
[0067]
在本实施例中,inva-f/r的上游引物为gttcgtcattccattacc;
[0068]
其中inva-f/r的上游引物识别标记为seq id no.1;
[0069]
inva-f/r的下游引物为cccataaacaccaatatcg;
[0070]
其中inva-f/r的下游引物识别标记为seq id no.2。
[0071]
在本实施例中,plc-f/r的上游引物为atggcaaagaggaaacta;
[0072]
其中plc-f/r的上游引物识别标记为seq id no.4;
[0073]
plc-f/r的下游引物为caacggcagtaacattag;
[0074]
其中plc-f/r的下游引物识别标记为seq id no.5。
[0075]
在本实施例中,phoa-f/r的上游引物为ctaggactgtttgctgac;
[0076]
其中phoa-f/r的上游引物识别标记为seq id no.7;
[0077]
phoa-f/r的下游引物为taggcgtacaggtaactg;
[0078]
其中phoa-f/r的下游引物识别标记为seq id no.8。
[0079]
在本实施例中,probe包含有inva-probe、plc-probe、phoa-probe。
[0080]
在本实施例中,所述inva-probe的基因的序列为tcctgatcgcactgaatatcgtactg;
[0081]
其中inva-probe的识别标记为seq id no.3;
[0082]
plc-probe的基因的序列为ctacattctatcttggagaggctatgc;
[0083]
其中plc-probe的识别标记为seq id no.6;
[0084]
phoa-probe的基因的序列为ctggcaaggaccgaaagcaac;
[0085]
其中phoa-probe的识别标记为seq id no.9。
[0086]
在本实施例中,inva-probe的5'端连接有6-fam,3'端连接有bhq1;plc-probe的5'端连接有rox,3'端连接有bhq2;phoa-probe的5'端连接有vic,3'端连接有bhq2。
[0087]
如图5-7所示,将阳性标准品(puc57/inva-plc-phoa)进行10倍梯度稀释,得到浓度在6.69
×
100~6.69
×
108copies/μl的阳性标准品溶液。以上述阳性标准品溶液作为检测对象,检测上述方法的灵敏度。
[0088]
以拷贝数衡量灵敏度。上述方法对沙门氏菌、大肠杆菌、产气荚膜梭菌3的最低检测限均为66.9copies/μl,以拷贝数衡量灵敏度。上述方法对沙门氏菌、大肠杆菌、产气荚膜梭菌3的最低检测限均为66.9copies/μl;
[0089]
如图8所示,用优化后的三重荧光pcr检测方法对实验室保存的禽沙门氏菌、大肠杆菌、产气荚膜梭菌、巴氏杆菌、新城疫病毒、鸭疫里默氏杆菌、丁酸梭菌、枯草芽孢杆菌、粪肠球菌、戊糖片球菌进行检测,并用ddh2o作为阴性对照,标准质粒作为阳性对照以验证检测方法的特异性,结果显示,仅有沙门氏菌、大肠杆菌、产气荚膜梭菌能检测出ct值,其他病毒或细菌均无ct值,表明该方法具有良好的特异性。
[0090]
将阳性标准品(puc57/inva-plc-phoa)进行稀释,得到浓度分别为6.69
×
104、6.69
×
106、6.69
×
108copies/μl的阳性标准品溶液,以depc水作为阴性对照。以上述阳性标准品溶液和阴性对照作为检测对象,检测上述方法的重复性。每个浓度重复9次
[0091]
结果显示,三个梯度的组内重复性十分良好,组内变异系数不大于3.0%(其中,6.69
×
104copies/μl的组内变异系数依次为1.02%、0.6%、0.55%;6.69
×
106copies/μl的组内变异系数依次为1.51%、1.24%、1.53%;6.69
×
108copies/μl的组内变异系数依次
为2.26%、2.84%、1.29%);如表3所示;
[0092][0093][0094]
以上,仅为本发明进一步的实施例,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明所公开的范围内,根据本发明的技术方案及其构思加以等同替换或改变,都属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1