一株副干酪乳杆菌及其在制备防治皮肤病的产品中的应用的制作方法
1.本发明涉及微生物技术领域,尤其涉及一株副干酪乳杆菌及其在制备防治皮肤病的产品中的应用。
背景技术:
2.皮肤具备着近乎完美的生理保护功能:如屏障作用、感觉作用、调节体温、吸收作用、分泌和排泄作用等,在维护机体的健康上,起到十分重要的作用。当皮肤的生理功能受到损害,就会引起皮肤病。
3.皮肤表面有多种微生物与皮肤环境一起形成的皮肤微生态。如果皮肤不健康,有可能出现菌群失调,继而导致某些菌株大量繁殖,或者导致外来致病菌大量侵入而引发疾病。比如:某些菌类获得有利生存条件在皮肤上大量繁殖、皮肤接触到外来毒力较强的菌株、代谢失调营养不良而患有慢性疾病的人让细菌容易入侵、皮肤过度洗护带来的皮肤菌群环境破坏等,在这些情况下,皮肤微生态较为脆弱,从而皮肤病原菌入侵或者过度繁殖易诱导皮肤疾病。
4.臭汗症是一种发生在特定皮肤部位的皮肤疾病,它是指汗液中具有特殊臭味的现象,主要包括足臭和腋臭,与特定部位菌群的代谢过程密切相关,臭汗症相关菌群旺盛地代谢导致了臭汗症的发生。研究发现益生菌灭活上清液能够显著降低臭汗症相关病原菌的生长及其代谢物异戊酸的产生,从而人们可以通过添加益生菌制剂直接接触病原菌抑制其生长的方式,来改善臭汗症。
5.鼻窦炎是耳鼻咽喉科学中的常见疾病。研究表明铜绿假单胞菌(pseudo monas aeruginosa)是鼻窦炎的重要病原菌,而清酒乳杆菌(lactobacillus sa kei)对于维持鼻腔正常功能有积极作用。因此,可以通过降低铜绿假单胞菌和清酒乳酸菌的相对比例来治疗鼻窦炎。
6.皮肤炎症是一种常见的皮肤疾病,它是皮肤对于外界刺激的一种防御反应,表现为红、肿、热、痛和功能障碍。皮肤微生态中包含多种细菌,细菌也会诱发炎症,属于生物性的炎症:部分细菌繁殖的时候会产生一些毒素,会导致细胞或者组织损伤,部分病原菌死亡之后,还可能会诱发一系列免疫反应,尸体也会释放出很多导致免疫反应的物质,导致的炎症。皮肤表面病原菌紊乱引发炎症的因素是多重的。
7.皮肤部分菌株过度增殖或者皮肤病原菌的入侵、皮肤炎症以及其它的因素对皮肤长期造成损伤容易使得皮肤屏障受损,从而失去皮肤原有的生理保护功能,继而病原菌的入侵和增殖更不受控制,形成恶性循环,导致皮肤炎症难以愈合。只有将细菌等微生物都调节回复到健康皮肤水平,让整个面部的微生态系统回复到平衡状态,皮肤才能在一个适宜它生长的环境下进行自我修复。不解决生态紊乱问题,单独治疗皮肤屏障或者炎症等问题是治标不治本。
8.在经济持续发展过程中,人们的生活节奏不断加快,无形中压力也在不断增长,导致众多年轻人肌肤出现了问题。随着人们对美和健康的需求越来越高,研发人员在抑制皮
肤病原菌生长、调节皮肤微生态平衡、皮肤抗炎和皮肤屏障修复等皮肤疾病治疗相关领域做出了诸多努力。从开始的“抗生素+激素”、“中草药精华+抗生素”、“天然原料+引发剂”等治疗方案发展到如今的利用益生菌生物活性物质、调节皮肤微生态的方案,研发人员在皮肤治疗领域取得了显著的进步。副干酪乳杆菌(lactobacillus paracasei)属于乳杆菌属中的干酪乳杆菌群,广泛存在于奶酪、泡菜等发酵食品。它具有干酪乳杆菌属调节肠道和增强免疫力等益生功能,代谢产生的细菌素具有优良的抑菌性能。副干酪乳杆菌作为一种常用于肠道的益生菌,可能具备防治皮肤病的潜力,但目前其直接作用于皮肤微生态方面的研究少有报导。此外,由于皮肤表面的微生态复杂、皮肤疾病的诱发因素复杂,目前的技术及产品未能满足常见的皮肤疾病的治疗需求,有必要进一步研发更有效的护肤产品,因此有必要筛选更优的益生菌菌株。
技术实现要素:
9.有鉴于此,本发明要解决的技术问题在于提供一株副干酪乳杆菌及其在制备防治皮肤病的产品中的应用。
10.本发明提供了一株副干酪乳杆菌,其保藏编号为cctcc no:m 20211555。
11.具体地,该菌株为革兰氏阳性,显微镜下呈杆状;在mrs平板上生长可形成表面光滑边缘整齐的白色圆形不透明菌落。
12.本发明还提供了保藏编号为cctcc no:m 20211555的副干酪乳杆菌在制备防治皮肤病的产品中的应用。
13.所述防治疗皮肤病包括:抗皮肤病原菌、治疗鼻窦炎、治疗臭汗症、抗皮肤炎症和/或修复皮肤屏障。
14.所述皮肤病原菌包括痤疮丙酸杆菌和白色念珠菌中的至少一种。
15.一些实施例中,本发明提供的副干酪乳杆菌gforu-9具有抑制痤疮丙酸杆菌(propionibacterium acnes)和白色念珠菌(candida albicans)的生长的作用,抑制率为21.5%~29.0%。
16.所述治疗鼻窦炎包括改变鼻腔中相关菌群的相对比值。所述改变鼻腔中鼻腔中相关菌群的相对比值包括降低铜绿假单胞菌和清酒乳杆菌的相对比值。
17.本发明中所述的菌群相对比值,在本发明的实施例中用特定菌種间的相对浓度比值来表征。
18.所述治疗臭汗症包括抑制臭汗症病原菌生长和/或降低异戊酸的产生;所述臭汗症病原菌包括金黄色葡萄球菌(staphylococcus aureus)、表皮葡萄球菌(staphylococcus epidermidis)、人葡萄球菌(staphylococcus hominis)、溶血葡萄球菌(staphylococcus haemolyticus)、干燥棒状杆菌(corynebacter ium xerosis)中的至少一种。
19.一些实施例中,本发明提供的菌株对所述臭汗症病原菌的抑制率达32.4%~70.6%。
20.一些实施例中,本发明提供的副干酪乳杆菌gforu-9抑制臭汗症相关菌群产生异戊酸,异戊酸降低率为64.26%。
21.所述抗皮肤炎症包括抑制no释放和/或下调炎症因子的表达水平;所述下调炎症因子的表达水平包括下调il-8、il-22、cox-2和trpv1中的至少一种基因的表达水平。
22.一些实施例中,本发明提供的副干酪乳杆菌gforu-9下调hacat细胞受金黄色葡萄球菌刺激而表达的炎症因子,基因表达量下调12.83%~56.05%;还能够降低脂多糖(lps)诱导小鼠巨噬细胞raw264.7的一氧化氮(no)生成量,降低率为29.59%~54.76%。
23.所述修复皮肤屏障包括上调屏障修护相关基因flg和lor的表达。
24.一些实施例中,所述屏障修护相关基因表达量上调倍率为1.27~1.65倍。
25.本发明还提供了一种防治皮肤病的产品,其原料包括所述的副干酪乳杆菌;所述产品包括医药品、食品、保养品或化妆品。
26.本发明所述产品的原料包括所述副干酪乳杆菌gforu-9菌株的活菌、灭活菌、裂解物、提取物、培养上清液、衍生物中至少一种;所述衍生物包括:代谢产物、代谢生物产物、益生素、细胞壁及其成分、胞外多糖和含有免疫原性成分的化合物中至少一种。
27.优选地,本发明所述的产品的原料为所述副干酪乳杆菌gforu-9菌株的上清液或灭活菌体。
28.所述的产品包括医食品、药品、保养品或化妆品。
29.本发明从3步健康女孩粪便中分离并鉴定出副干酪乳杆菌gforu-9菌株,其具备防治皮肤病的作用,包括抗皮肤病原菌、治疗鼻窦炎、治疗臭汗症、抗皮肤炎症和/或修复皮肤屏障。本发明提供副干酪乳杆菌gforu-9菌株在食品、药品、保养品、化妆品等领域具有较大的市场潜力。
30.生物保藏证明
31.副干酪乳杆菌gforu-9 lactobacillus paracasei gforu-9,于2021年12月06日保藏在中国典型培养物保藏中心,地址为:中国.武汉.武汉大学,保藏编号为cctcc no:m 20211555。
附图说明
32.图1示gforu-9抑制臭汗症相关病原菌生长;
33.图2示gforu-9上清液下调炎症因子相关基因表达。
具体实施方式
34.本发明提供了一株副干酪乳杆菌gforu-9及其在制备防治皮肤病的产品中的应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
35.本发明采用的试材皆为普通市售品,皆可于市场购得。
36.下面结合实施例,进一步阐述本发明:
37.实施例1 gforu-9的分离
38.于3岁健康女孩的粪便中采样。将样品适当处理后于生理盐水中震荡混匀,取上清划线于mrs固体平板,37℃恒温培养24~48h后,挑取白色菌落反复接种筛选,直至得到均匀的单个菌落,命名为gforu-9。
39.革兰氏染色镜检:菌株gforu-9为革兰氏染色阳性,显微镜下呈杆状;在mrs平板上生长,可形成白色、表面光滑圆润不透明圆形小菌落,边缘整齐;在mrs液体培养基中呈均匀浑浊生长,久置菌体呈白色沉淀。
40.实施例2 gforu-9的核酸鉴定
41.1、16s rrna基因序列分析:
42.挑取单菌落置mrs液体培养基中,37℃培养过夜后,离心收集菌体,按照dna提取试剂盒步骤进行操作扩增菌体的序列。引物为细菌通用引物27f,1492r;pcr扩增体系为50μl体系,95℃预变性5min;94℃ 15s,57℃ 15s,72℃ 40s,35个循环;72℃延伸10min。扩增后测定核酸的碱基序列。
43.2、结果
44.pcr产物测序结果与genbank中已发表的标准序列进行同源性比较(bl astn)后得出gforu-9菌株为副干酪乳杆菌(lactobacillus paracasei)。
45.实施例3 gforu-9抑制臭汗症病原菌生长实验-菌液浓度变化
46.1、副干酪乳杆菌gforu-9菌液制备:
47.将活化的副干酪乳杆菌gforu-9菌液以mrs液体培养基培养于37℃培养箱静置培养16~18h,检测并调整至od
600
=2.0,121℃,30min灭活,离心取上清液,0.22μm滤膜过滤,得gforu-9灭活上清液样品。
48.2、病原菌菌液制备:
49.将5种病原菌:金黄色葡萄球菌cgmcc 1.8721、表皮葡萄球菌cgmcc 1.4260、人葡萄球菌cgmcc 1.493、溶血葡萄球菌cgmcc 1.540和干燥棒状杆菌cgmcc 1.1919分别用bhi培养基37℃培养18h,检测并调整至od
600
=0.2。
50.3、抑制臭汗症病原菌实验
51.将灭活上清液以10%(v/v)的比例分别加入病原菌中,37℃培养2h,以菌液浓度(od600)降低的百分比为指标评价gforu-9灭活上清液对病原菌的抑制作用。
52.结果见表1:
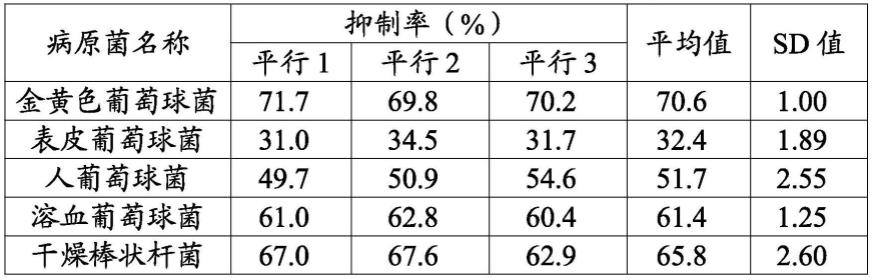
53.表1 gforu-9对臭汗症病原菌抑制率
[0054][0055]
结果如表1所示,gforu-9对金黄色葡萄球菌、表皮葡萄球菌、人葡萄球菌、溶血葡萄球菌和干燥棒状杆菌等臭汗症病原菌均具有抑制作用。
[0056]
gforu-9对臭汗症病原菌抑制率的结果见图1。
[0057]
实施例4 gforu-9降低异戊酸的产生实验
[0058]
1、副干酪乳杆菌gforu-9菌液制备:
[0059]
将活化的副干酪乳杆菌gforu-9菌液用mrs液体培养基培养于37℃培养箱静置培养16~18h,检测并调整至od
600
=2.0,121℃,30min灭活,离心取上清液,0.22μm滤膜过滤,得gforu-9灭活上清液样品。
[0060]
2、葡萄球菌混合菌液制备:
[0061]
将4种葡萄球菌:金黄色葡萄球菌、表皮葡萄球菌、人葡萄球菌和溶血葡萄球菌分别用bhi培养基37℃培养18h,检测并调整至od
600
=0.2,然后将四种菌液等体积混合制得葡萄球菌混合菌液。
[0062]
3、副干酪乳杆菌gforu-9上清液添加及异戊酸含量检测
[0063]
将gforu-9灭活上清液以10%(v/v)的比例加入葡萄球菌混合菌液中,未添加该上清液的实验组为对照,分别37℃培养2h,然后用气相色谱法测定样品和对照的异戊酸含量,并计算添加上清液后异戊酸含量降低率。
[0064]
结果见表2:
[0065]
表2 gforu-9添加对异戊酸产生的降低率
[0066][0067]
结果如表2所示,gforu-9具有降低葡萄球菌产生异戊酸的作用,降低率为64.26%。
[0068]
实施例5gforu-9抑制皮肤病原菌实验-菌液浓度变化
[0069]
1、副干酪乳杆菌gforu-9菌液制备:
[0070]
将活化的副干酪乳杆菌gforu-9菌液用mrs液体培养基培养于37℃培养箱静置培养16~18h,检测并调整至od
600
=2.0,121℃,30min灭活,离心取上清液,0.22μm滤膜过滤,得gforu-9上清液样品。
[0071]
2、病原菌菌液制备:
[0072]
将痤疮丙酸杆菌cgmcc 1.5003和白色念珠菌cgmcc 2.4550分别用bhi培养基37℃培养18h,检测并调整至od
600
=0.2。
[0073]
3、抑制病原菌实验
[0074]
将灭活上清液以10%(v/v)的比例加入病原菌中,37℃培养12~16h,以菌液浓度(od600)降低百分比为指标评价gforu-9对病原菌生长的抑制作用。
[0075]
结果见表3:
[0076]
表3 gforu-9对皮肤病原菌抑制率
[0077][0078]
结果如表3所示,gforu-9对痤疮丙酸杆菌和白色念珠菌等常见皮肤病原菌均具有抑制作用。
[0079]
实施例6 gforu-9改变菌群比例治疗鼻窦炎的作用
[0080]
1、副干酪乳杆菌gforu-9菌液制备:
[0081]
将活化的副干酪乳杆菌gforu-9菌液以mrs液体培养基培养于37℃培养箱静置培养16~18h,检测并调整至od
600
=2.0,121℃,30min灭活,离心取上清液,0.22μm滤膜过滤,得gforu-9灭活上清液样品。
[0082]
2、鼻腔菌群菌液制备:
[0083]
分别将铜绿假单胞菌cgmcc1.1785用bhi培养基、清酒乳杆菌用mrs培养基于37℃培养18h,检测并调整至od
600
=0.2。
[0084]
3、添加上清液影响皮肤菌群生长实验
[0085]
将灭活上清液以10%(v/v)的比例分别加入两种菌液中,37℃培养3h,以铜绿假单胞菌/清酒乳杆菌相对浓度(od
600
的比值)为指标评价gforu-9对鼻腔菌群生长影响。
[0086]
相对浓度比值的计算公式为:a菌和b菌的相对浓度比值=(实验组a菌的浓度/对照组a菌的浓度)/(实验组b菌的浓度/对照组b菌的浓度)。
[0087]
4、结果。结果如表4所示:gforu-9对铜绿假单胞菌有显著抑制作用,而对清酒乳杆菌有一定促进增殖作用。gforu-9能够明显降低铜绿假单胞菌和清酒乳杆菌的相对浓度比值,降低铜绿假单胞菌和清酒乳杆菌的相对比例,从而有效治疗鼻窦炎。
[0088]
表4 gforu-9对铜绿假单胞菌/清酒乳杆菌比值影响
[0089][0090]
实施例7 gforu-9降低raw264.7细胞no生成量
[0091]
1、gforu-9菌液制备
[0092]
将gforu-9用mrs培养基培养过夜,检测od600,调整菌液浓度至od600=0.2,离心后,菌体121℃高压灭菌30min得gforu-9灭活菌体,离心发酵液用0.22μm滤膜过滤得gforu-9上清液。
[0093]
2、raw264.7细胞制备
[0094]
将raw264.7细胞消化后以2
×
105个/孔的密度接种至24孔板,5%二氧化碳培养箱37℃培养过夜。
[0095]
3、gforu-9添加及lps刺激
[0096]
将上清液以5%(v/v)、灭活菌体为10%(v/v)的比例分别加入不同组的培养过夜的raw264.7细胞中,2h后添加0.5ml浓度为0.2μg/ml的lps溶液,诱导raw264.7细胞发炎,20h后取细胞培养上清,no含量检测试剂盒进行no含量检测。每次3个复孔,共进行三次实验。
[0097]
结果见表5:
[0098]
表5 gforu-9降低raw264.7细胞no生成量
[0099][0100]
结果显示gforu-9具有抗炎作用,能够降低lps诱导的raw264.7细胞no生成量,与对照组相比,上清液降低raw264.7细胞的no生成量54.76%,灭活菌体降低raw264.7细胞的no生成量29.59%。
[0101]
实施例8gforu-9下调hacat细胞炎症因子相关基因的表达
[0102]
1、gforu-9样品制备
[0103]
将gforu-9用mrs培养过夜,检测od
600
,调整菌液浓度至od600=0.2,离心后,菌体121℃高压灭菌30min得gforu-9灭活菌体,离心上清用0.22μm滤膜过滤得gforu-9上清液。
[0104]
2、hacat细胞制备
[0105]
将hacat细胞消化后以2
×
105个/孔的密度接种至24孔板,5%二氧化碳培养箱37℃培养过夜。
[0106]
3、金黄色葡萄球菌制备及添加
[0107]
金黄色葡萄球菌接入营养肉汤培养基,37℃摇床培养过夜,用mem无血清培养基调整菌液浓度至od
600
=6.0,然后以每孔100μl的量将金黄色葡萄球菌培养液添加入培养过夜的hacat细胞中,刺激细胞产生炎症因子,3h后弃去细胞培养基,pbs清洗5次,每孔重新加入1ml的mem无血清培养基。
[0108]
4、gforu-9样品添加
[0109]
将gforu-9灭活上清液以5%(v/v)的比例加入金黄色葡萄球菌刺激过的hacat细胞中,每组3个复孔,培养过夜。
[0110]
5、qpcr法检测细胞炎症因子mrna相对表达倍数
[0111]
将上述细胞弃去培养基后,用rna提取试剂盒提取rna,检测rna浓度及纯度,将所有样品调整至1μg,用反转录试剂盒、sybrgreen qpcr试剂盒进行rt-pcr及qpcr,计算炎症因子基因il-8、il-22、cox-2和trpv1的相对表达倍数f。
[0112]
公式:f=2-δδct
[0113]
结果见表6:
[0114]
表6 gforu-9下调炎症因子基因的表达
[0115][0116]
结果显示gforu-9能够下调金黄色葡萄球菌诱导的hacat细胞炎症因子相关基因表达,表达量降低12.83%~56.05%。因此,gforu-9具有抗炎作用。
[0117]
实施例9 gforu-9促进hacat屏障修复相关基因表达实验
[0118]
gforu-9灭活菌体及灭活上清液的制备方法同实施例8步骤1。接种人永生化角质形成细胞hacat(5
×
105个/孔)至6孔板,过夜培养至细胞贴壁。加入菌株上清液5%(v/v)或灭活菌体10%(v/v)至hacat细胞中,分别培养24h后,加入裂解液,提取细胞总rna,检测rna浓度及纯度,将所有样品调整至1μg,并反转录为cdna,进行qpcr检测flg和lor基因的表达。根据公式进行计算表达变化倍数。
[0119]
公式:f=2-δδct
[0120]
gforu-9上清液和灭活菌体调控屏障修护相关基因表达的结果分别见表7和表8:
[0121]
表7 gforu-9上清液上调屏障修护相关基因表达
[0122][0123]
表8 gforu-9灭活菌体上调屏障修护相关基因表达
[0124][0125]
结果如表7和表8所示,加入gforu-9具有促进皮肤屏障修复的作用。
[0126]
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1