一种检测试剂盒及其应用
1.本发明属于生物技术领域,具体涉及一种耶氏肺孢子菌、弓形虫和荚膜组织胞浆菌的检测引物组、检测试剂盒或芯片及应用。
背景技术:
2.肺孢子菌肺炎(pneumocystis pneumonia,pcp)是由耶氏肺孢子菌(pneumocystis jirovecii,pj) 感染引起的肺炎,是免疫缺陷患者重要的致死原因。肺孢子菌肺炎临床表现缺乏特异性,以发热、干咳、呼吸困难最常见,其他症状包括嗜睡、恶心、呕吐、腹泻、体重下降等;患者肺部听诊可无异常或闻及干、湿性啰音,大多表现为症状与体征的严重程度不成比例。
3.弓形虫病(toxoplasmosis)是由弓形虫(toxoplasma gondii,tg)引起的一种人畜共患寄生原虫病。该虫体主要侵犯眼、脑、心等器官,寄生于有核细胞内,人体通常表现为隐性感染,不表现明显症状,因此常被漏诊和误诊。但是当人体免疫功能受损或低下时,特别是感染艾滋病的病人,可由弓形虫隐性感染转为弓形虫病急性发作,出现急性症状,严重者可造成死亡。
4.荚膜组织胞浆菌病(histoplasmosis,hp)是由荚膜组织胞浆菌(histoplasma capsulatum,hc)引起的具有传染性的深部真菌病,经呼吸道传染,也可经皮肤、胃肠道黏膜受染,其发病初往往易误诊,使病情迁延加重。由于荚膜组织胞浆菌病主要侵犯肺和单核吞噬细胞系统,临床表现各种各样,可有发热、肝脾肿大、贫血、少数有皮肤黏膜损害,可在有免疫功能降低或缺陷的aids患者继发荚膜组织胞浆菌病。
5.肺孢子菌肺炎、弓形虫病和荚膜组织胞浆菌病的患者在临床上均表现出发热、咳嗽及呼吸困难等症状,感染程度不同临床表现的严重程度不一,影像学上也很难进行区分,患者耽误治疗会引起爆发性肺炎甚至死亡,因此,在临床上明确诊断感染病原体对于指导临床医生用药以及患者的良好预后具有重要意义。
技术实现要素:
6.本发明依据耶氏肺孢子菌mtssu(线粒体小亚单位)基因以及弓形虫的rep-529 (529bp的重复片段)片段的保守区域和荚膜组织胞浆菌的its(internal transcribed spacer,转录间隔区)片段的保守区域设计了特异性引物、探针,构建了三重荧光定量pcr的鉴别诊断检测体系,并制备成肺孢子菌肺炎、弓形虫病和荚膜组织胞浆菌病的检测试剂盒或芯片。该检测试剂盒或芯片能同时或单独检测三种病原体,提高了疾病的诊断效率,降低医务人员的工作强度,提高了患者的治疗效果。
7.本发明提供了一种检测试剂盒或芯片,所述的检测试剂盒或芯片包含耶氏肺孢子菌、弓形虫和/或荚膜组织胞浆菌的引物和/或探针。
8.优选的,耶氏肺孢子菌的引物与探针扩增或靶向mtssu基因。进一步优选的,耶氏肺孢子菌的探针包含seq id no:3所示核苷酸序列或者包含seq id no:3经过一个或几个
核苷酸的取代、缺失和/或插入且与seq id no:3具有相同或相似功能的核苷酸序列,上游引物包含seq id no:1所示核苷酸序列或者包含seq id no:1经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:1具有相同或相似功能的核苷酸序列,下游引物包含seq id no:2所示核苷酸序列或者包含seq id no:2经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:2具有相同或相似功能的核苷酸序列。更进一步优选的,耶氏肺孢子菌的探针如seq id no:3所示,上游引物如seq id no:1所示,下游引物如seq id no:2所示。
9.优选的,弓形虫的引物与探针扩增或靶向rep-529片段的保守区域。进一步优选的,弓形虫的探针包含seq id no:6所示核苷酸序列或者包含seq id no:6经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:6具有相同或相似功能的核苷酸序列,上游引物包含seq id no:4所示核苷酸序列或者包含seq id no:4经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:4具有相同或相似功能的核苷酸序列,下游引物包含seq id no:5所示核苷酸序列或者包含seq id no:5经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:5具有相同或相似功能的核苷酸序列。更进一步优选的,弓形虫的探针如seq id no:6所示,上游引物如seq id no:4所示,下游引物如seq id no:5所示。
10.优选的,荚膜组织胞浆菌的引物与探针扩增或靶向its片段(优选seq id no:14所示)。进一步优选的,荚膜组织胞浆菌的探针包含seq id no:9所示核苷酸序列或者包含seq id no:9经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:9具有相同或相似功能的核苷酸序列,上游引物包含seq id no:7所示核苷酸序列或者包含seq id no:7经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:7具有相同或相似功能的核苷酸序列,下游引物包含seq id no:8所示核苷酸序列或者包含seq id no:8经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:8具有相同或相似功能的核苷酸序列。更进一步优选的,荚膜组织胞浆菌的探针如seq id no:9所示,上游引物如seq id no:7所示,下游引物如seq id no:8所示。
11.在本发明的一个具体实施方式中,耶氏肺孢子菌的探针包含seq id no:3,上游引物包含seq id no:1,下游引物包含seq id no:2。
12.弓形虫的探针包含seq id no:6,上游引物包含seq id no:4,下游引物包含seq id no:5。
13.荚膜组织胞浆菌的探针包含seq id no:9,上游引物包含seq id no:7,下游引物包含seq id no:8。
14.优选的,所述探针中seq id no:3、6或9的5’端包含荧光报告基团的修饰,3’端包含荧光淬灭基团的修饰。所述的荧光报告基团可以为常规使用的荧光报告基团,优选包括但不限于vic(绿色荧光蛋白)、fam(carboxy-fluorescein,羧基荧光素)、texas red(德克萨斯红)、hex(hexachlorofluorescein,六氯-6-甲基荧光素)、tamra(tetramethyl-6-carboxyrhodamine,6-羟基四甲基罗丹明)、tet(tetrachlorofluorescein,四氯-6-羧基荧光素)、joe(2,7-二甲基-4,5-二氯-6-羧基荧光素)、cy3(三氢-吲哚菁型染料)、cy5(三氢-吲哚菁型染料)、rox(6-羧基-x-罗丹明)、lc red640(红色染料640)或lc red705(红色染料705)中的任意一种。所述的荧光淬灭基团可以为常规使用的,优选包括但不限于tamra(tetramethyl-6-carboxyrhodamine,6-羟基四甲基罗丹明)、dabcyl(4-(4-恶烷氨基苯偶氮)苯甲酸)、bhq1(black hole quencher 1)、bhq2(black hole quencher 2)或bhq3
(black hole quencher 3)中的任意一种。
15.在本发明的一个具体实施方式中,耶氏肺孢子菌的探针为vic-seq id no:3-bhq1。
16.在本发明的一个具体实施方式中,弓形虫的探针为texas red-seq id no:6-bhq2。
17.在本发明的一个具体实施方式中,荚膜组织胞浆菌的探针为cy5-seq id no:9-bhq2。
18.在本发明的一个具体实施方式中,所述的检测试剂盒或芯片包含耶氏肺孢子菌的探针和引物,弓形虫的探针和引物,荚膜组织胞浆菌的探针和引物。其中,耶氏肺孢子菌的探针为vic-seq id no:3-bhq1,上游引物包含seq id no:1,下游引物包含seq id no:2;弓形虫的探针为texas red-seq id no:6-bhq2,上游引物包含seq id no:4,下游引物包含seq id no:5;荚膜组织胞浆菌的探针为cy5-seq id no:9-bhq2,上游引物包含seq id no:7,下游引物包含seq id no:8。
19.优选的,所述检测试剂盒或芯片还包括pcr反应的试剂和/或dna提取所需试剂。其中,pcr反应的试剂包括但不限于taq dna聚合酶、dntps、酶稳定剂、taq dna聚合酶反应缓冲液、溴酚蓝染料或水中的一种或两种以上的组合。
20.优选的,所述的检测试剂盒或芯片检测的样本可以为受试者的外周血、骨髓、痰液、肺泡灌洗液或组织。
21.本发明还提供了一种探针,所述的探针包含耶氏肺孢子菌、弓形虫和/或荚膜组织胞浆菌的探针。
22.优选的,所述的耶氏肺孢子菌的探针靶向mtssu基因。进一步优选的,所述的耶氏肺孢子菌的探针包含seq id no:3所示核苷酸序列或者包含seq id no:3经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:3具有相同或相似功能的核苷酸序列。更进一步优选的,所述的耶氏肺孢子菌的探针如seq id no:3所示。
23.优选的,所述的弓形虫的探针靶向rep-529片段的保守区域。进一步优选的,所述的弓形虫的探针包含seq id no:6所示核苷酸序列或者包含seq id no:6经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:6具有相同或相似功能的核苷酸序列。更进一步优选的,所述的弓形虫的探针如seq id no:6所示。
24.优选的,所述的荚膜组织胞浆菌的探针靶向its片段(优选seq id no:14所示)。进一步优选的,所述的荚膜组织胞浆菌的探针包含seq id no:9所示核苷酸序列或者包含seq id no:9经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:9具有相同或相似功能的核苷酸序列。更进一步优选的,所述的荚膜组织胞浆菌如seq id no:9所示。
25.优选的,所述探针中seq id no:3、6或9的5’端包含荧光报告基团的修饰,3’端包含荧光淬灭基团的修饰。所述的荧光报告基团可以为常规使用的荧光报告基团,优选包括但不限于vic(绿色荧光蛋白)、fam(carboxy-fluorescein,羧基荧光素)、texas red(德克萨斯红)、hex(hexachlorofluorescein,六氯-6-甲基荧光素)、tamra(tetramethyl-6-carboxyrhodamine,6-羟基四甲基罗丹明)、tet(tetrachlorofluorescein,四氯-6-羧基荧光素)、joe(2,7-二甲基-4,5-二氯-6-羧基荧光素)、cy3(三氢-吲哚菁型染料)、cy5(三氢-吲哚菁型染料)、rox(6-羧基-x-罗丹明)、lc red640(红色染料640)或lc red705(红色染料
705)中的任意一种。所述的荧光淬灭基团可以为常规使用的,优选包括但不限于tamra(tetramethyl-6-carboxyrhodamine,6-羟基四甲基罗丹明)、dabcyl(4-(4-恶烷氨基苯偶氮)苯甲酸)、bhq1(black hole quencher 1)、bhq2(black hole quencher 2)或bhq3(black hole quencher 3)中的任意一种。
26.在本发明的一个具体实施方式中,所述的耶氏肺孢子菌的探针为vic-seq id no:3-bhq1。
27.在本发明的一个具体实施方式中,所述的弓形虫的探针为texas red-seq id no:6-bhq2。
28.在本发明的一个具体实施方式中,荚膜组织胞浆菌的探针为cy5-seq id no:9-bhq2。
29.本发明还提供了一种引物,所述的引物包含耶氏肺孢子菌、弓形虫和/或荚膜组织胞浆菌的引物。
30.优选的,所述的耶氏肺孢子菌的引物扩增mtssu基因。进一步优选的,上游引物包含seq id no:1所示核苷酸序列或者包含seq id no:1经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:1具有相同或相似功能的核苷酸序列,下游引物包含seq id no:2所示核苷酸序列或者包含seq id no:2经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:2具有相同或相似功能的核苷酸序列。更进一步优选的,所述的耶氏肺孢子菌的上游引物如seq id no:1所示,下游引物如seq id no:2所示。
31.优选的,所述的弓形虫的引物扩增rep-529片段的保守区域。进一步优选的,弓形虫的上游引物包含seq id no:4所示核苷酸序列或者包含seq id no:4经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:4具有相同或相似功能的核苷酸序列,下游引物包含seq id no:5所示核苷酸序列或者包含seq id no:5经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:5具有相同或相似功能的核苷酸序列。更进一步优选的,弓形虫的上游引物如seq id no:4所示,下游引物如seq id no:5所示。
32.优选的,荚膜组织胞浆菌的引物扩增its片段(优选seq id no:14所示)。进一步优选的,荚膜组织胞浆菌的上游引物包含seq id no:7所示核苷酸序列或者包含seq id no:7经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:7具有相同或相似功能的核苷酸序列,下游引物包含seq id no:8所示核苷酸序列或者包含seq id no:8经过一个或几个核苷酸的取代、缺失和/或插入且与seq id no:8具有相同或相似功能的核苷酸序列。更进一步优选的,荚膜组织胞浆菌的上游引物如seq id no:7所示,下游引物如seq id no:8所示。
33.本发明进一步公开了上述的探针或上述的引物在制备检测耶氏肺孢子菌、弓形虫和/或荚膜组织胞浆菌的检测试剂盒或芯片中的应用。
34.本发明还公开了一种检测耶氏肺孢子菌、弓形虫和/或荚膜组织胞浆菌的方法,所述的方法包括使用上述的探针和/或上述的引物进行检测。
35.优选的,包括以下步骤:提取耶氏肺孢子菌、弓形虫和荚膜组织胞浆菌的dna样品,进行pcr,其中pcr的反应条件为:94~96℃ 2~3 min;94~96℃ 15~30 s,55-60℃15~30s,35~40个循环。
36.优选的,检测的样本可以为受试者的外周血、骨髓、痰液、肺泡灌洗液或组织。
37.优选的,所述的检测方法不是疾病的诊断和治疗方法。
38.目前,临床上使用的三种病原体的检测方法如下:对于弓形虫临床常用抗弓形虫igm/igg抗体检测的方法结合临床症状和流行病学进行诊断;对于荚膜组织胞浆菌,临床使用镜检、培养以及血清学检测的方法进行病原体诊断;耶氏肺孢子菌肺炎,临床通常使用镜检和普通pcr的方法进行病原学诊断。镜检和培养方法具有敏感度低和检测周期长的缺点;免疫学方法容易发生交叉反应,特异性不高,容易误诊;普通pcr方法容易发生产物气溶胶污染,导致假阳性。
39.本发明应用弓形虫,荚膜组织胞浆菌和耶氏肺孢子菌的保守基因的序列设计了引物探针组合构建了弓形虫,荚膜组织胞浆菌和耶氏肺孢子菌同步检测的三重荧光定量pcr检测方法,本技术设计的引物探针组合共9条短序列,在同一体系中没有出现交叉反应,也没有形成二级结构,是从若干组合中特异性筛选获得的。因此,本技术设计的引物探针组合进行检测的方法具有敏感度高,特异性好,无需开盖有效避免了产物气溶胶污染,检测结果更准确的优势。三种病原体同步检测与单独检测每一种病原体比较更高效,大大缩短了检测时间,同时三种病原体同步检测具有鉴别诊断的优势。
40.本发明所述的“包含”或“包括”为开放式写法,当用于描述蛋白质或核酸的序列时,所述蛋白质或核酸可以是由所述序列组成,或者在所述蛋白质或核酸的一端或两端可以具有额外的氨基酸或核苷酸,但仍然具有与原序列相同或相似的活性。
41.本发明所述的“受试者”可以为人或非人哺乳动物,所述的非人哺乳动物可以为野生动物、动物园动物、经济动物、宠物、实验动物等等。优选的,所述的非人哺乳动物包括但不限于猪、牛、羊、马、驴、狐、貉、貂、骆驼、狗、猫、兔、鼠(例如大鼠、小鼠、豚鼠、仓鼠、沙鼠、龙猫、松鼠)或猴等等。
42.本发明所述的“和/或”包含该术语所连接的项目的所有组合,应视为各个组合已经单独地在本问列出。例如,“a和/或b”包含了“a”、“a和b”以及“b”。又例如,“a、b和/或c”包含了“a”、“b”、“c”、“a和b”、“a和c”、“b和c”以及“a和b和c。
附图说明
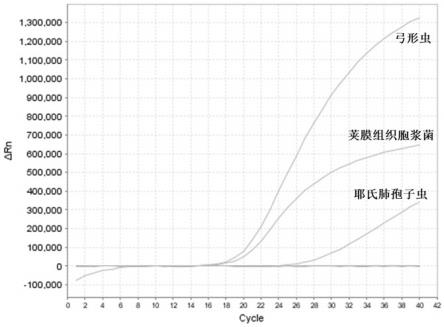
43.图1为实施例1中耶氏肺孢子菌样品的荧光定量pcr检测的扩增曲线;图2为实施例1中弓形虫样品的荧光定量pcr检测的扩增曲线;图3为实施例1中荚膜组织胞浆菌样品的荧光定量pcr检测的扩增曲线;图4为实施例1中耶氏肺孢子菌、弓形虫样品以及荚膜组织胞浆菌混合样品(1:1:1,加入量为各1μl)的荧光定量pcr检测的扩增曲线。
具体实施方式
44.下面结合说明书附图和具体实施例进一步阐述本发明。这些实施例仅用于说明本发明而不用于限定本发明的范围。下例实施例中未注明具体条件的实验方法,通常按照本领域常规条件或按照制造厂商建议的条件。如无特殊说明,均为常规方法。除非另行定义,文中所用的专业与科学用语与本领域技术人员熟悉的意义相同。
45.实施例1 耶氏肺孢子菌、弓形虫和荚膜组织胞浆菌检测体系的建立1、引物和探针的设计
为了满足在同一个体系中同时检测三种病原体,本实施例依据耶氏肺孢子菌mtssu基因以及弓形虫的rep-529片段的保守区域和荚膜组织胞浆菌its,设计引物和探针,结果见表1。
46.表1:设计的引物探针序列
2、构建标准质粒2.1目的片段的制备及纯化:(1)弓形虫以及耶氏肺孢子菌的dna样品从实验室保存的弓形虫以及耶氏肺孢子菌感染的临床样本中提取,使用的扩增引物如下:耶氏肺孢子菌mtssu的扩增引物序列如下:p-pj-f(seq id no:10):aaacgacggccagtgaattcgagtcgaatagaagaataaagap-pj-r(seq id no:11):accatgattacgccaagcttttcgctacttatgcctac弓形虫的rep-529的扩增引物序列如下:p-tg-f(seq id no:12)aaacgacggccagtgaattcatgcgatctagacgagacp-tg-r(seq id no:13)accatgattacgccaagcttcacagtgcatctggattc建立pcr扩增反应体系:2
×
gotaq green master mix 10μl,上游引物200nm,下游
引物200nm,dna样品20ng,无菌双蒸水补充至20μl。pcr扩增反应条件:95℃,5 min;95℃ 15 s,63℃ 15 s,72℃ 30 s,共35个循环;72℃ 5 min,4℃保存。扩增产物回收:采用2%琼脂糖凝胶电泳检测扩增产物,使用天根生物的通用性dna纯化回收试剂盒切胶回收目的片段。
47.(2)荚膜组织胞浆菌的its片段序列由上海生工生物有限公司合成并构建标准质粒,经测序确认合成基因正确。
48.荚膜组织胞浆菌its片段序列:cacgccgtggggggctgggagcctctgaccgggacccccccgcccccctacccggccacccttgtctaccggacctgttgcctcggcgggcctgcagcgatgctgccgggggagcttctcctccccgggcccgtgtccgccggggacaccgcaagaaccgtcggtgaacgattggcgtctgagcatgagagcgataataatccagtcaaaactttcaacaacggatctcttggttccgacatcgatgaagaacgcagcgaaatgcgataagtaatgtgaattgcagaattccgtgaatcatcgaatctttgaacgcacattgcgccccctggtattccggggggcatgcctgtccgagcgtcattgcaaccctcaagcgcggcttgtgtgttgggccatcgtcccccctcgaccggcgggacgtgcccgaaatgcagtggcggtgtcgagttccggtgcccgagcgtatggggctttgccacccgctctggaggcccggccggctccggcccaccatctcaacccccctctcacaccagg(seq id no:14)2.2质粒载体的酶切及纯化:(1)ecorⅰ和hindⅲ酶切质粒载体puc19线性化的酶切反应体系:hind
ⅲꢀ
1μl,ecor
ⅰꢀ
1μl,10
×
m buffer 2μl,puc19 1μg,dh2o 14μl。
49.(2)酶切的反应条件:37℃ 1h。
50.(3)线性化puc19质粒的回收:采用1%琼脂糖凝胶电泳检测步骤(2)酶切后的产物,使用天根生物的通用性dna纯化回收试剂盒切胶回收线性化的puc19质粒。
51.2.3目的片段与线性化质粒载体puc19的重组及转化:(1)重组反应体系:线性化载体puc19 50ng,目的片段8ng,2
×
easygeno assembly mix 5μl,无菌双蒸水补充反应体系至10μl;(2)反应条件:50℃水浴,15min;(3)取100μl感受态细胞dh5α置于冰浴中解冻;(4)在步骤(3)的感受态细胞dh5α悬液中加入步骤(2)的10μl重组产物,轻弹混匀,在冰浴中静置30min;(5)将步骤(4)的样品置于42℃水浴中放置90s,然后快速转移到冰浴中,使细胞冷却3min,该过程不要摇动离心管;(6)在步骤(5)的样品中加入350μl无菌的不含抗生素的37℃预热的soc培养基,混匀后置于37℃摇床震荡培养45min;(7)吸取步骤(6)的已转化的感受态细胞100μl,加到含100μg/ml氨苄青霉素的lb固体琼脂培养基上,用无菌的平板涂布棒轻轻的将细胞均匀涂开,将平板置于室温直至液体被吸收,倒置平板,37℃培养12-16h。
52.2.4单克隆菌株的鉴定:(1)随机挑取步骤2.3(7)中的单克隆菌株放入含有氨苄青霉素的lb培养基中培养,并送测序;(2)目的序列测序结果均含有插入的目的序列,质粒构建成功。
53.2.5质粒dna的提取(天根快速质粒小提试剂盒,货号dp105-02):(1)将测序鉴定含有目的序列的菌株在含有氨苄青霉素的lb培养基中扩大培养;
(2)将步骤(1)的培养菌株12000rpm离心1min,收集菌体;(3)在步骤(2)的样品中加入150μl溶液p1,涡旋振荡混匀;(4)在步骤(3)的样品中加入150μl溶液p2,温和的上下翻转6-8次,使菌体充分裂解;(5)在步骤(4)的样品中加入350μl溶液p5,立即快速上下颠倒数次,充分混匀;(6)将步骤(5)的样品12000 rpm离心2min,将上清液转移到吸附柱cp3中,12000 rpm离心30s,倒掉废液;(7)将步骤(6)的吸附柱cp3放入收集管中,并加入300μl漂洗液pwt,12000rpm离心30s,倒掉废液;(8)将步骤(7)的吸附柱cp3放回收集管,12000rpm离心1min;(9)将步骤(8)的吸附柱cp3置于一个新的离心管中,向膜的中间位置加50μl洗脱缓冲液tb,12000rpm离心30s,收集溶液,即为质粒dna,并用nanodrop定量。
54.3、使用构建的标准质粒测试耶氏肺孢子菌、弓形虫和荚膜组织胞浆菌检测系统(1)制备检测样品。将构建好的质粒dna稀释为浓度105copies/μl。
55.(2)荧光定量pcr扩增的反应体系:第一引物探针组合:hc-n-f 300nm、hc-n-r 300nm、探针hc-n-probe 250nm;pj-n-f 300nm、pj-n-r 300nm、探针pj-n-probe 250nm;tg-n-f 300nm、tg-n-r 300nm、探针tg-n-probe 250nm,上述引物和探针浓度是在反应体系中的终浓度,三种质粒dna各1μl,10μl的gotaq
®ꢀ
probe qpcr master mix,无菌双蒸水补齐至20μl;第二引物探针组合:hc-n-f 300nm、hc-n-r 300nm、探针hc-n-probe 250nm;pj-n-1-f 300nm、pj-n-r 300nm、探针pj-n-probe 250nm;tg-n-f 300nm、tg-n-r 300nm、探针tg-n-probe 250nm,上述引物和探针浓度是在反应体系中的终浓度,三种质粒dna各1μl,10μl的gotaq
®ꢀ
probe qpcr master mix,无菌双蒸水补齐至20μl;第三引物探针组合:hc-n-f 300nm、hc-n-r 300nm、探针hc-n-probe 250nm;pj-n-f 300nm、pj-n-r 300nm、探针pj-probe 250nm;tg-n-f 300nm、tg-n-r 300nm、探针tg-n-probe 250nm,上述引物和探针浓度是在反应体系中的终浓度,三种质粒dna各1μl,10μl的gotaq
®ꢀ
probe qpcr master mix,无菌双蒸水补齐至20μl;第四引物探针组合:hc-its2-f1 300nm、hc-its2-r1 300nm、探针hc-its2-probe1 250nm;pj-n-f 300nm、pj-n-r 300nm、探针pj-n-probe 250nm;tg-n-f 300nm、tg-n-r 300nm、探针tg-n-probe 250nm,上述引物和探针浓度是在反应体系中的终浓度,三种质粒dna各1μl,10μl的gotaq
®ꢀ
probe qpcr master mix,无菌双蒸水补齐至20μl;第五引物探针组合:hc-n-1-f 300nm、hc-n-1-r 300nm、探针hc-n-probe 250nm;pj-n-f 300nm、pj-n-r 300nm、探针pj-n-probe 250nm;tg-n-f 300nm、tg-n-r 300nm、探针tg-n-probe 250nm,上述引物和探针浓度是在反应体系中的终浓度,三种质粒dna各1μl,10μl的gotaq
®ꢀ
probe qpcr master mix,无菌双蒸水补齐至20μl。
56.(3)荧光定量pcr扩增的反应条件:95℃ 2min;95℃ 15s,59℃ 30s,40个循环。
57.(4)结果将表1设计的引物探针进行组合得到五组引物探针组合,进行试验验证,在相同加入量及扩增条件时,结果显示只有优选出的引物探针组合(表2)在同一个检测体系中能同
时检测三种病原体。
58.表2:扩增目标基因的引物序列:扩增目标基因的引物序列表2设计的引物探针组合结果见图1-4,获得的扩增曲线如图1-4所示,结果表明,使用弓形虫,荚膜组织胞浆菌和耶氏肺孢子菌三种病原体三重检测体系进行检测,在弓形虫标记的texas red荧光通道中,只看到弓形虫的一条扩增曲线,荚膜组织胞浆菌标记的
cy5荧光通道中,只看到荚膜组织胞浆菌的一条扩增曲线,耶氏肺孢子菌标记的vic荧光通道中,只看到耶氏肺孢子菌的一条扩增曲线,表明三个病原体的引物探针之间未发生交叉反应,因此,本技术设计的引物及探针可以对弓形虫、荚膜组织胞浆菌和耶氏肺孢子菌进行准确鉴定。
59.实施例2:单独检测和混合检测比较采用实施例1表2引物探针组合制备的检测体系对弓形虫,荚膜组织胞浆菌和耶氏肺孢子菌分别进行单独检测和混合检测。
60.(1)三种病原体的质粒dna稀释浓度为105copies/μl。
61.(2)荧光定量pcr扩增的反应体系和条件见表3。
62.表3:反应体系和条件检测结果见表4。
63.表4:单独检测与混合检测结果对比该实施例中,三种病原体混合检测和单独检测对比有如下优势:
(1)每种病原体检测用时2.5h,三种单独检测总计需要7.5h,使用本实施例发明的三种病原体混合检测,总计用时2.5h,有效的缩短了检测结果的报告时间。
64.(2)三种病原体单独检测,检验人员需要操作三次,上机三次,混合检测仅需一次便可完成,简化了操作流程,易于临床推广。
65.(3)三种病原体混合检测可对三种病原体进行鉴别诊断,可有效区分显微镜下形态相似的三种病原体,使得检测结果更准确,更好的指导后续的临床治疗。
66.实施例3:临床样本的检测1、选择临床样本:从确诊的患者中选取6例耶氏肺孢子菌感染的患者痰液样本、2例弓形虫感染的患者血样本和2例荚膜组织胞浆菌感染患者的痰液样本。
67.2、提取患者临床样本总dna:使用qiagen dneasy blood&tissue kit(货号:69506)提取弓形虫感染的血液临床样本的总dna;使用天根的植物基因组dna提取试剂盒提取(货号dp305)提取耶氏肺孢子菌和荚膜组织胞浆菌感染的痰液临床样本的总dna。
68.3、荧光定量pcr扩增提取的总dna(1)pcr反应体系(20μl):master mix(promega,a6001)
ꢀꢀꢀ
10μlhc-n-f(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μlhc-n-r(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μlhc-n-probe(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.5μlpj-n-f(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μlpj-n-r(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μlpj-n-probe(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.5μltg-n-f(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μltg-n-r(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.6μltg-n-probe(10μm)
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
0.5μltemplate
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
1 μldh2o
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
3.9μl(2)荧光定量pcr反应条件:95℃ 2min;95℃ 15s,60℃ 30s,40 cycles。
69.(3)荧光定量pcr的反应结果:临床样本检测结果见表5。
70.表5:临床样本检测
表5结果表明,表2引物探针组合进行各个临床样本的检测符合率为100%,特异性好。说明本发明制备的检测体系能够同时准确鉴定三种病原体,对三种疾病进行准确诊断。
71.本发明所述的检测方法与现有临床使用的检测方法(镜检和培养)相比较具有如下优势:(1)本发明(荧光定量pcr方法)的敏感度要优于镜检及培养方法,可提高检测敏感度,防治漏诊。
72.(2)本发明可以定量病原体,监测患者治疗过程中的病原体含量,进而判断药物的有效性及确定治疗终点,较传统的镜检及培养方法能更好的指导临床治疗。
73.以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1