一种细胞瞬时转染的方法与流程
1.本发明属于生物技术领域,涉及基因转染技术,具体涉及一种细胞瞬时转染的方法。
背景技术:
2.细胞膜是防止细胞外物质自由进入细胞的屏障,它保证了细胞内环境的相对稳定,使各种生化反应能够有序运行。正是因为细胞膜的生物屏障阻止了许多生物大分子物质进入细胞内,从而很大程度限制了这些物质在治疗领域的应用。因此,如何引导这些物质穿透细胞膜进入细胞内部是一个需要解决的问题。
3.基因转染是一种“将具生物功能的核酸转移或运送到细胞内并使核酸在细胞内维持其生物功能”的技术,基因转染技术不仅是研究转基因和基因表达的重要工具,而且是目前基因治疗的关键步骤。基因转染方法包括生物转染法、化学转染法、物理转染法。生物方法主要以病毒作为载体,通过病毒感染的方式将外源dna导入到细胞中,其中以逆转录病毒及腺病毒转染系统最为常用。物理化学方法中常用的有磷酸钙法、脂质体介导的转染、显微注射、电穿孔,以及最近出现的以高分子聚合物为载体的基因传递技术。基因转染需要一定的转染试剂将带有目的基因的载体运送到细胞内,目前最常用的转染试剂是阳离子脂质体和阳离子聚合物,它们容易透过细胞膜,其中,阳离子脂质体在体外基因转染中由于操作简单、转染效率较高、试剂商品化等优点,被众多实验室使用。
4.近年来,thermo fisher公司新开发的expi293f瞬时转染系统的转染效率和表达量有了较大的提升,但是进口商品化的转染试剂盒及培养基价格较贵,订购周期长,不太适用于产业化放大。因此,进口试剂国产化日益受到重视,摆脱进口依赖,研发进口产品的替代产品,进一步提高转染效率,降低科研和医疗成本、实现中国制造已经迫在眉睫。
技术实现要素:
5.本发明的目的是提供一种expi293f细胞瞬时转染进口试剂国产化替代方法。所要解决的技术问题不限于所描述的技术主题,本领域技术人员通过以下描述可以清楚地理解本文未提及的其它技术主题。
6.为实现上述目的,本发明首先提供了一种细胞瞬时转染的方法,所述方法包括如下步骤:
7.a1)细胞培养:采用表达培养基培养细胞,得到细胞培养物;
8.a2)转染:将表达载体与转染试剂、转染培养基混合,得到表达载体与转染试剂复合物,将所述表达载体与转染试剂复合物加入所述细胞培养物中进行培养18-22小时后向培养体系中加入转染增强剂继续培养,完成细胞瞬时转染;其中:
9.所述转染试剂为trlip高效dna转染试剂,所述转染培养基为转染专用减血清培养基,所述转染增强剂为opm-293profeed。
10.上述方法中,所述表达培养基可为下述任一种:
11.b1)进口表达培养基:expi293
tm expression medium;
12.b2)国产表达培养基:opm-293cd03 medium+6mm gln;
13.b3)国产表达培养基:opm-293cd05 medium。
14.所述表达载体可为质粒。
15.所述opm-293cd03 medium+6mm gln是在opm-293cd03 medium基础上添加 gln(谷氨酰胺)得到的液体培养基,所述opm-293cd03 medium+6mm gln中gln 的含量为6mm。
16.进一步地,所述trlip高效dna转染试剂(trlip高效dna transfection reagent) 可为北京密码子生物科技有限公司(www.codonx.com)产品,货号:kd0201-01。
17.进一步地,所述转染专用减血清培养基可为北京密码子生物科技有限公司产品,货号:km-0130。
18.进一步地,所述opm-293profeed可为上海奥浦迈生物科技有限公司 (www.opmbiosciences.com)产品,货号:f081918-001。
19.进一步地,所述expi293
tm expression medium(expi293
tm
表达培养基)可为thermo公司产品,货号:a1435102(https://www.thermofisher.cn/order/catalog/product/ a1435102?sid=srch-hj-a1435102)。
20.进一步地,所述opm-293cd03 medium可为上海奥浦迈生物科技有限公司产品,货号:81070-001。
21.进一步地,所述opm-293cd05 medium可为上海奥浦迈生物科技有限公司产品,货号:81075-001。
22.本发明实施例中所使用的opm-293cd03 medium+6mm gln是在opm-293cd03 medium基础上添加gln(谷氨酰胺)得到的液体培养基,使用效果等同于所述opm-293 cd05 medium。
23.上述方法中,所述细胞为经过驯化的细胞,所述驯化包括:在传代培养过程中,通过逐步降低所述进口表达培养基与所述国产表达培养基的体积比进行驯化。
24.上述方法中,所述驯化为将所述细胞复苏于所述进口表达培养基中,然后换为由所述进口表达培养基与所述国产表达培养基按照75:25的体积比组成的混合培养基进行培养,再更换为由所述进口表达培养基与所述国产表达培养基按照50:50的体积比组成的混合培养基进行培养、再更换为由所述进口表达培养基与所述国产表达培养基按照25:75的体积比组成的混合培养基进行培养、再更换为由所述进口表达培养基与所述国产表达培养基按照10:90的体积比组成的混合培养基进行培养,再更换为所述国产表达培养基进行培养,得到经过驯化的细胞。
25.所述经过驯化的细胞的制备方法包括:将所述细胞复苏于所述进口表达培养基中,接种传代至混合培养基中,所述混合培养基中所述进口表达培养基与所述国产表达培养基的体积比逐代依次为75:25、50:50、25:75、10:90和0:100,获得所述经过驯化的细胞。
26.具体地,所述经过驯化的细胞的制备方法包括:将所述细胞复苏于所述进口表达培养基中培养,以0.3
×
106个/ml-0.5
×
106个/ml的接种密度传代至混合培养基中,所述混合培养基中所述进口表达培养基与所述国产表达培养基的体积比逐代依次为 75:25、50:50、25:75、10:90和0:100,细胞密度达到3
×
106个-5
×
106个/ml,且细胞活率在95%以上时,获得所述经过驯化的细胞。
27.进一步地,上述方法中,所述培养的条件为37℃,8%co2摇床培养。
28.上述方法中,所述表达载体与转染试剂复合物中,所述表达载体与所述转染试剂的配比为0.8-1.0μg所述表达载体:2-3.2μl所述转染试剂。
29.进一步地,所述表达载体与所述细胞的配比为0.8-1.0μg所述表达载体:3
×
106个所述细胞;所述转染试剂与所述细胞的配比为2-3.2μl所述转染试剂:3
×
106所述细胞。
30.上述方法中,所述转染增强剂的添加量是所述培养体系的5%,所述5%为体积含量。
31.进一步地,上述方法中,所述表达载体(质粒)的添加量可为0.8-1.0μg/3
×
106个细胞,所述转染试剂的添加量可为2-3.2μl/3
×
106个细胞。
32.上述方法中,所述转染前一天将细胞培养液中的细胞密度可调整为2.5
×
10
6-3.0
×
106个/ml,转染当天细胞密度可为4.5
×
10
6-5.5
×
106个/ml,转染时细胞密度可调整为3.0
×
106个/ml。
33.上述方法中,所述细胞可为293细胞。
34.进一步地,所述293细胞可为expi293f细胞、293f细胞、293ft细胞、293f
tm
细胞、293t细胞、293t/17细胞、293t/17sf细胞或hke293细胞但不限于此。
35.上述方法中,所述表达载体可为质粒。
36.上述方法中,所述质粒可为蛋白表达质粒。
37.进一步地,所述蛋白可为cho密码子优化的带状疱疹ge糖蛋白、293密码子优化的带状疱疹ge糖蛋白、兔igg抗体(thermo公司,货号:a14662;)或新冠病毒s-rbd蛋白(刺突蛋白受体结合区)但不限于此。
38.本发明还提供了一种提高瞬时转染蛋白表达量的方法,所述方法包括利用本文中任一所述方法进行转染,培养经转染的细胞,所述经转染的细胞活率降至65%-75%时终止培养。
39.本文中“转染增强剂”和“补料”具有相同含义,可以互换使用。
40.本技术提供一种细胞瞬时转染的方法,具体地提供了expi293f细胞瞬时转染进口试剂国产化替代方法,包括原进口表达培养基的国产替换,原进口转染试剂的国产替换,原进口转染用减血清培养基的国产替换和原进口补料的国产替换。
41.为了优化上述进口试剂国产化替代方法,原进口表达培养基为expi293
tm
expressionmedium替换为国产表达培养基为opm-293cd03medium+6mmgln。
42.在本发明的一个实施方案中,所述方法包含如下步骤:
43.(1)expi293f细胞复苏于原进口表达培养基(expi293
tm
expressionmedium)中,培养3~4天后以0.3
×
106~0.5
×
106个/ml的接种密度传代至20~30ml的混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为75:25;将细胞置于37℃,8%co2,转速为125rpm的恒温摇床中进行培养;
44.(2)培养3~4天后细胞计数,活细胞密度达2
×
106~5
×
106个/ml,活率》90%,以0.3
×
106~0.5
×
106个/ml的接种密度传代至30ml的混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为50:50;
45.(3)培养3~4天后细胞计数,活细胞密度达2
×
106~5
×
106个/ml,活率》90%,以0.3
×
106~0.5
×
106个/ml的接种密度传代至30ml的混合培养基中,此时混合培养基中原进
口培养基与国产培养基的比例为25:75;
46.(4)培养3~4天后细胞计数,活细胞密度达2
×
106~5
×
106个/ml,活率》90%,以0.3
×
106~0.5
×
106个/ml的接种密度传代至30ml的混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为10:90;
47.(5)培养3~4天后细胞计数,活细胞密度达2
×
106~5
×
106个/ml,活率》90%,以0.3
×
106~0.5
×
106个/ml的接种密度传代至30ml的混合培养基中,此时混合培养基中国产培养基的比例为100%;
48.(6)在100%的国产培养基中继续传代培养2~3代,传代后3~4天时细胞的密度达到2
×
106~5
×
106个/ml,且细胞活率在95%以上,细胞已经完全适应了国产培养基,可以进行正常的细胞传代、转染和冻存。
49.更进一步地,为了优化上述进口试剂国产化替代方法,上述原进口转染试 expifectamine
tm 293替换为国产转染试剂为trlip高效dna transfection reagent (trlip高效dna转染试剂,北京密码子生物科技有限公司,货号:kd0201-01)。
50.更进一步地,为了优化上述进口试剂国产化替代方法,上述原进口转染用减血清培养基opti-mem
tm i reduced serum medium替换为国产转染专用减血清培养基(北京密码子生物科技有限公司,货号:km-0130)。
51.更进一步地,为了优化上述进口试剂国产化替代方法,所述原进口补料expifectamine
tm 293转染增强剂1和expifectamine
tm 293转染增强剂2替换为国产补料为opm-293profeed(上海奥浦迈生物科技有限公司,货号:f081918-001)。
52.第二方面,为了优化上述进口试剂国产化替代方法,优化的技术关键点包括所述任一细胞培养液,所述转染前一天将细胞培养液中的细胞密度调整为2.5
×
106~3.0
×
106个/ml,转染当天细胞密度应为4.5
×
106~5.5
×
106个/ml,转染时调整细胞密度为 3.0
×
106个/ml,所述细胞培养液中细胞存活率大于95%。
53.第三方面,根据第一方面所述进口试剂国产化替代方法和第二方面所述技术关键点,本技术提供一种提高expi293f细胞瞬时转染蛋白表达量的方法,包括以下步骤:
54.(1)分别准备转染质粒、含有待转染宿主细胞的细胞培养液;
55.(2)trlip高效dna转染试剂和转染专用减血清培养基混合后得到转染试剂混合液,将质粒dna和转染专用减血清培养基混合后得到质粒dna混合液;
56.(3)将所述转染试剂混合液逐滴加入至质粒dna混合液中,混匀后室温孵育,得到dna-转染试剂复合物混合液;
57.(4)将所述dna-转染试剂复合物混合液逐滴加入至所述细胞培养液中培养;
58.(5)转染后18~22h添加补料,活率降至65%-75%时终止培养。
59.其中所述细胞培养液中培养基为expi293
tm expression medium,所述补料为 opm-293profeed,添加量为培养体积的5%。
60.通过采用上述技术方案,能够有效提高瞬时转染效率,使得四种重组蛋白的表达水平为进口转染试剂的1~3倍。
61.综上所述,本技术具有以下有益效果:
62.1.由于本技术采用进口表达培养基及国产转染试剂及补料的优选组合,使得蛋白表达更高,同时可节约43%的成本。
63.2.由于本技术采用国产表达培养基及国产转染试剂及补料的优选组合,在成本上远远低于进口试剂套盒,可节约61%的成本,较低的试剂成本将带来较大的经济效益。
64.本发明经过反复实验,研制出了一种expi293f细胞瞬时转染进口试剂国产化替代方法,采用国产转染试剂、国产转染培养基和国产转染增强剂替代进口转染试剂、进口转染培养基和进口转染增强剂,经过与进口试剂进行对比实验表明,采用本发明所用转染试剂及培养基成本低,可降低43%-61%的成本,且转染效率和进口thermofisher公司开发的expi293f转染套盒相当甚至略高,具有成本低、转染效率高、订购周期短的优点。实现了进口试剂国产化,可降低科研和医疗成本,具有重要经济效益。
附图说明
65.图1为本技术方案
①②③
条件下获得的蛋白1纯化还原和非还原电泳图;其中,条带1为:方案
①
;条带2为:方案
②
;条带3为:方案
③
。
66.图2为本技术方案
④⑤⑥
条件下获得的蛋白1纯化还原和非还原电泳图;其中,条带16为:方案
④
;条带17为:方案
⑤
;条带18为:方案
⑥
。
67.图3为本技术方案
①②③
条件下获得的蛋白2纯化还原和非还原电泳图;其中,条带4为:方案
①
;条带5为:方案
②
;条带6为:方案
③
。
68.图4为本技术方案
④⑤⑥
条件下获得的蛋白2纯化还原和非还原电泳图;其中,条带19为:方案
④
;条带20为:方案
⑤
;条带21为:方案
⑥
。
69.图5为本技术方案
①②③
条件下获得的蛋白3纯化还原和非还原电泳图;其中,条带7为:方案
①
;条带8为:方案
②
;条带9为:方案
③
。
70.图6为本技术方案
④⑤⑥
条件下获得的蛋白3纯化还原和非还原电泳图;其中,条带22为:方案
④
;条带23为:方案
⑤
;条带24为:方案
⑥
。
71.图7为本技术方案
①②③
条件下获得的蛋白4纯化还原和非还原电泳图;其中,条带10为:方案
①
;条带11为:方案
②
;条带12为:方案
③
。
72.图8为本技术方案
④⑤⑥
条件下获得的蛋白4纯化还原和非还原电泳图;其中,条带25为:方案
④
;条带26为:方案
⑤
;条带27为:方案
⑥
。
73.图9为本技术方案
②
与对照组(方案
①
)4种蛋白表达水平的对比图;其中,方案
②
为进口表达培养基与国产转染试剂及补料的优选组合;对照组(方案
①
)为thermofisher公司开发的expi293f进口转染套盒方案。1、2、3、4分别表示蛋白1、蛋白2、蛋白3、蛋白4。
74.图10为本技术方案
⑤
与对照组(方案
①
)4种蛋白表达水平的对比图;其中,方案
⑤
为国产表达培养基与国产转染试剂及补料的优选组合;对照组(方案
①
)为thermofisher公司开发的expi293f进口转染套盒方案。1、2、3、4分别表示蛋白1、蛋白2、蛋白3、蛋白4。
75.附图中,蛋白1表示cho密码子优化的带状疱疹ge糖蛋白;蛋白2表示293密码子优化的带状疱疹ge糖蛋白;蛋白3表示兔igg抗体;蛋白4表示新冠病毒s-rbd 蛋白(刺突蛋白受体结合区)
具体实施方式
76.下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术
人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
77.下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
78.下述实施例中的主要试剂及其厂家信息如下:
79.expi293f
tm cells(expi293f细胞):thermo公司,货号:a14527;
80.expi293
tm expression medium:thermo公司,货号:a1435102;
81.pcgs3:merck公司;
82.antibody-expressing positive control vector(兔igg抗体表达质粒):thermo公司,货号:a14662;
83.sars-cov-2(2019-ncov)spike rbd gene orf cdna clone expression plasmid, c-his tag(codon optimized):北京义翘神州科技股份有限公司,货号:vg40592-ch;
84.expifectamine
tm 293transfection kit:thermo公司,货号:a14524;
85.包含(expifectamine
tm 293转染试剂、expifectamine
tm 293转染增强剂1、 expifectamine
tm 293转染增强剂2);
86.opti-mem
tm i reduced serum medium:thermo公司,货号:31985062;
87.l-谷氨酰胺溶液:merck公司,货号:g7513;
88.opm-293cd03 medium:上海奥浦迈生物科技有限公司,货号:81070-001;
89.opm-293cd05 medium:上海奥浦迈生物科技有限公司,货号:81075-001;
90.opm-293profeed:上海奥浦迈生物科技有限公司,货号:f081918-001;
91.trlip高效dna转染试剂:北京密码子生物科技有限公司,货号:kd0201-01;
92.转染专用减血清培养基:北京密码子生物科技有限公司,货号:km-0130;
93.protein a预装色谱柱:生工生物工程(上海)股份有限公司;
94.ni-nta 6ff his标签蛋白纯化试剂盒:生工生物工程(上海)股份有限公司;
95.centrifugal filters10k:millipore公司;
96.centrifugal filters 0.5ml 10k-10k:millipore公司;
97.pbs ph7.4(1
×
):thermo公司;
98.sure page
tm
,bis-tris,10x8,4-12%,12wells:南京金斯瑞生物科技有限公司。
99.下述实施例中的关键仪器及其厂家信息如下:
100.细胞计数仪:上海睿珏生物科技有限公司;
101.超净工作台:苏州安泰空气技术有限公司;
102.电热恒温水浴锅:上海一恒科学仪器有限公司;
103.二氧化碳摇床:crystal公司;
104.nanodrop 2000微量分光光度计:thermo scientific公司。
105.实施例1、质粒dna的获得
106.4种重组蛋白表达质粒的获得:
107.质粒1(cho密码子优化的带状疱疹ge糖蛋白表达质粒):带状疱疹ge糖蛋白 (ncbi登录号aag32558.1)的第1至546位的碳端依次融合ggggs连接肽和 hhhhhh标签,共计557个
氨基酸的目的序列委托生工生物进行cho密码子优化 dna序列。该dna序列替换pcgs3(merck)载体的hind iii和paci酶切位点之间序列,载体其他序列不变,得到的重组表达载体(即质粒1)。
108.质粒2(293密码子优化的带状疱疹ge糖蛋白表达质粒):带状疱疹ge糖蛋白 (ncbi登录号aag32558.1)的第1至546位的碳端依次融合ggggs连接肽和 hhhhhh标签,共计557个氨基酸的目的序列委托生工生物进行hek293密码子优化dna序列。该dna序列替换pcgs3(merck)载体的hind iii和paci酶切位点之间序列,载体其他序列不变,得到的重组表达载体(即质粒2)。
109.质粒3(兔igg抗体表达质粒):thermo公司产品,货号:a14662。
110.质粒4(新冠病毒s-rbd蛋白(刺突蛋白受体结合区)表达质粒):以sars-cov-2 (2019-ncov)spike rbd gene orf cdna clone expression plasmid,c-his tag(codonoptimized)(义翘神州,货号:vg40592-ch)为模板,引物1和引物3进行第一轮扩增;扩增片段作为第二轮扩增的模板,使用引物2和引物3进行第二轮扩增获得s-rbd 目标片段。该s-rbd目标片段无缝连接至pcgs3(merck)载体的hind iii和paci酶切位点之间,载体其他序列不变,得到的重组表达载体(即质粒4)。
111.引物1、引物2和引物3的序列如下所示:
112.引物1:5
’‑
tgctgctgcccctggtgagcagccagtgcagggtccaaccaacagagag-3’,
113.引物2:5
’‑
caccgtccttgacacgaagcttgccaccatgttcgtgttcctggtgctgctgcccctggtgagc-3’,
114.引物3:5
’‑
cagttagcctcccccttaattaattaatgatggtggtgatggtgag-3’。
115.扩大培养含有上述四种重组质粒的宿主菌dh5α,按照去内毒素试剂盒的使用方法,用去内毒素试剂盒提取上述4种重组蛋白表达质粒(质粒1、质粒2、质粒3和质粒4),随后经乙醇沉淀后晾干,并于重组质粒中加入灭菌去离子水使其完全溶解,用nanodrop 2000微量分光光度计测量浓度后于-20℃冻存备用,其浓度分别为2.0 mg/ml(质粒1)、1.5mg/ml(质粒2)、3.0mg/ml(质粒3)、2.5mg/ml(质粒4)。
116.实施例2、宿主细胞制备
117.expi293f细胞复苏:将装有expi293f细胞的冻存管置于37℃电热恒温水浴锅中 130s,使细胞快速解冻;使用0.055%的84消毒液擦拭冻存管外表面,于超净工作台中将细胞转入含有19ml expi293
tm expression medium(expi293细胞表达培养基)的摇瓶中,吸取1ml培养基加入冻存管,吹打两次,洗净冻存管中残留细胞,全部加入到摇瓶中,盖上瓶盖,摇匀。将细胞置于37℃,8%co2,转速为125rpm的恒温摇床(二氧化碳摇床)中进行培养。培养3~4天后以0.3
×
106个/ml的接种密度传代,传两代以上且细胞活率》95%可用于转染。
118.宿主细胞国产培养基适应性驯化:expi293f细胞复苏于原进口表达培养基 (expi293
tm expression medium)中,培养4天后以0.5
×
106个/ml的接种密度传代至 30ml的新鲜混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为 75:25;将细胞置于37℃,8%co2,转速为125rpm的恒温摇床中进行培养;
119.培养4天后细胞计数,活细胞密度达4.07
×
106个/ml,活率》90%,以0.5
×
106个 /ml的接种密度传代至30ml的新鲜混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为50:50;
120.培养3天后细胞计数,活细胞密度达3.19
×
106个/ml,活率》90%,以0.3
×
106个 /ml的接种密度传代至30ml的新鲜混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为25:75;
121.培养3天后细胞计数,活细胞密度达4.11
×
106个/ml,活率》90%,以0.3
×
106个 /ml的接种密度传代至30ml的新鲜混合培养基中,此时混合培养基中原进口培养基与国产培养基的比例为10:90;
122.培养3天后细胞计数,活细胞密度达4.42
×
106个/ml,活率》90%,以0.3
×
106个 /ml的接种密度传代至30ml的新鲜混合培养基中,此时混合培养基中国产培养基的比例为100%;
123.在100%的国产培养基中继续传代培养2代,传代后3天时细胞的密度达到 4.39
×
106个/ml,且细胞活率在95%以上,细胞已经完全适应了国产培养基,可以进行正常的细胞传代、转染和冻存。
124.实施例3、细胞转染
125.1)转染前24h以2.5
×
106个/ml的密度传代实施例2中的expi293f悬浮细胞至 293表达培养基中(进口:expi293
tm expression medium;国产:opm-293cd03 medium+6mm gln);次日采用细胞计数仪进行细胞计数后,分别以相应的新鲜的表达培养基调整细胞密度至3.0
×
106个/ml,分别得到进口expi293f
tm
细胞培养物和国产 expi293f
tm
细胞培养物。上述进口expi293f
tm
细胞培养物和国产expi293f
tm
细胞培养物的制备方法中,区别仅在于所用的293表达培养基不同,前者采用的293表达培养基是expi293
tm expression medium,后者采用的293表达培养基是opm-293cd03 medium+6mm gln。
126.opm-293cd03 medium+6mm gln是在opm-293cd03 medium基础上添加gln (谷氨酰胺)得到的液体培养基,opm-293cd03 medium+6mm gln中gln的含量为6mm,具体配制方法为1l的opm-293cd03 medium中加入30ml l-谷氨酰胺溶液 (200mm),混合均匀后即可使用,上述所使用的opm-293cd03 medium+6mm gln 也可直接使用opm-293cd05 medium代替,效果等同。
127.2)转染当天将进口与国产的293表达培养基、转染试剂及补料交叉组合共6种组合方案(
①
、
②
、
③
、
④
、
⑤
、
⑥
)进行上述4种重组表达质粒,共24瓶转染。6种方案均按照每ml细胞培养物转染1μg质粒的量及质粒原始浓度,计算转染25ml细胞所需原始质粒的体积。将4种重组表达质粒分别与转染试剂(进口:expifectamine
tm 293转染试剂,国产:trlip高效dna转染试剂),按1(ug):3.2(ul)比例即25 ug质粒与80ul转染试剂混合于3ml转染培养基中(进口:opti-mem
tm i reducedserum medium,国产:转染专用减血清培养基),上下颠倒混匀后室温反应10分钟,分别得到质粒与国产转染试剂复合物与质粒与进口转染试剂复合物这两种质粒与转染试剂复合物。其中,质粒为实施例1中的质粒1、质粒2、质粒3或质粒4。含有同一种质粒的两种质粒与转染试剂复合物的制备方法中,区别仅在于所用的转染试剂和转染培养基不同,质粒与国产转染试剂复合物采用的转染试剂是trlip高效dna转染试剂、转染培养基是转染专用减血清培养基,质粒与进口转染试剂复合物采用的转染试剂是expifectamine
tm 293转染试剂、转染培养基是opti-mem
tm i reduced serummedium。
128.3)将质粒与转染试剂复合物(方案
①④
中均是质粒与进口转染试剂复合物,其余 4个方案均是质粒与国产转染试剂复合物)缓慢滴入expi293f
tm
细胞培养物(方案
①②③
中
均是expi293f
tm
细胞使用进口表达培养基的培养物,方案
④⑤⑥
中均是 expi293f
tm
细胞使用国产表达培养基的培养物)中培养,边加边摇晃细胞培养物,使 dna与转染试剂复合物分散均匀。在37℃,8%co2,120rpm摇床中培养,其中方案
①②④⑤
在转染后18~22h添加补料(进口:expifectamine
tm 293转染增强剂1 和expifectamine
tm 293转染增强剂2,国产:opm-293profeed)。方案
①④
用 expifectamine
tm 293转染增强剂1和expifectamine
tm 293转染增强剂2进行补料,按培养体积0.6%和6%的比例分别添加expifectamine
tm 293转染增强剂1和 expifectamine
tm 293转染增强剂2,方案
②⑤
均用opm-293profeed进行补料,按培养体积5%的量添加opm-293profeed。当活率降至65%-75%时终止培养,以得到6 种方案表达4种目的蛋白的培养物,具体转染方案见表1,其中方案
①
为对照组。实施例1中的质粒1、质粒2、质粒3和质粒4均分别采用方案
①②③④⑤⑥
进行转染,得到s1-s12和s16-s27这24种实验,质粒1、质粒2、质粒3和质粒4均分别采用方案
①
进行转染的实验编号为s1、s4、s7和s10,质粒1、质粒2、质粒3和质粒4均分别采用方案
②
进行转染的实验编号为s2、s5、s8和s11,质粒1、质粒2、质粒3 和质粒4均分别采用方案
③
进行转染的实验编号为s3、s6、s9和s12,质粒1、质粒 2、质粒3和质粒4均分别采用方案
④
进行转染的实验编号为s16、s19、s22和s25,质粒1、质粒2、质粒3和质粒4均分别采用方案
⑤
进行转染的实验编号为s17、s20、 s23和s26,质粒1、质粒2、质粒3和质粒4均分别采用方案
⑥
进行转染的实验编号为s18、s21、s24和s27。
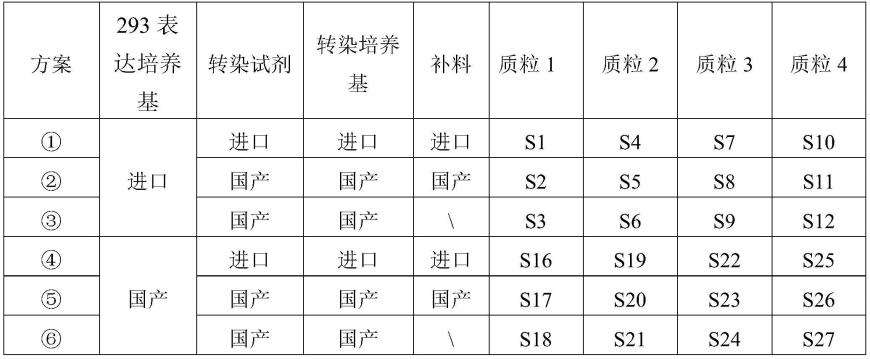
129.表1 expi 293f细胞转染方案
[0130][0131]
其中s1-s12、s16-s27为各组实验的编号。“\”表示未进行补料。
[0132]
实施例4、蛋白纯化
[0133]
his标签蛋白纯化(质粒1,质粒2和质粒4表达的重组蛋白):将上述各组实验 (s1-s6、s10-s12、s16-s21、s25-s27)的培养物于6000g离心30min,收集上清并采用超滤管centrifugal filters-10k(millipore公司)进行超滤浓缩,上清和结合/洗涤缓冲液(ni-nta 6ff his标签蛋白纯化试剂盒成分)按照体积比1:1混匀,静置20min充分孵育,得到超滤浓缩上清和结合/洗涤缓冲液混匀液。五倍柱体积的结合/洗涤缓冲液平衡柱子(生工生物ni-nta 6ff his标签蛋白纯化试剂盒成分),将超滤浓缩上清和结合/洗涤缓冲液混匀液加入柱子依靠重力流穿预装柱。用10-15倍柱体积的结合/洗涤缓冲液清洗柱子并收集流穿液。使用一个新的收集管重复该步骤,直到流穿液的吸光度280nm接近基线;用5-10倍柱体积的洗脱缓冲液洗脱柱上的目的蛋白,centrifugal filters 0.5ml 10k-10k(millipore公司)超滤浓缩置换成 pbs(ph 7.4)缓冲液。使用sds-page鉴定纯化目的蛋白,检测结果显示目的蛋白条带符合预期,灰度分析纯度大于90%(图1至图4,图7、图8)。
[0134]
抗体蛋白纯化(质粒3表达的兔igg抗体蛋白):将上述各组实验(s7-s9、s22-s24) 的培养物于6000g离心30min,收集上清并采用超滤管centrifugal filters-10k (millipore公司)进行超滤浓缩,上清和结合/洗涤缓冲液(生工生物protein a预装色谱柱的试剂盒成分)按照体积比1:1混匀,静置20min充分孵育,得到超滤浓缩上清和结合/洗涤缓冲液混匀液。五倍柱体积的结合/洗涤缓冲液平衡柱子(生工生物 protein a预装色谱柱的试剂盒成分),将超滤浓缩上清和结合/洗涤缓冲液混匀液加入柱子依靠重力流穿预装柱。用10-15倍柱体积的结合/洗涤缓冲液清洗柱子并收集流穿液。使用一个新的收集管重复该步骤,直到流穿液的吸光度280nm接近基线;用5-10 倍柱体积的洗脱缓冲液洗脱柱上的目的蛋白,centrifugal filters 0.5ml 10k
ꢀ‑
10k(millipore公司)超滤浓缩置换成pbs(ph7.4)缓冲液。使用sds-page鉴定纯化目的蛋白,检测结果显示目的蛋白条带符合预期,灰度分析纯度大于90%(图5、图6)。
[0135]
实施例5、蛋白表达水平的测定
[0136]
使用nanodrop仪器,采用bca方法测定蛋白浓度。根据目的蛋白浓度计算目的蛋白的具体表达量(单位:mg/l)。4种质粒在6种转染方案中的蛋白表达水平见表 2。方案
①
为thermo fisher公司开发的expi293f转染套盒,为对标方案。以下方案均为转染涉及的不同进口试剂的国产替换,方案
⑤
(全国产组合)与方案
①
表达水平相当(图10)。其中方案
②
(使用国产转染试剂和国产转染专用培养基及国产补料组合)4种质粒表达水平均比方案
①
要高,最大可达3倍(图9)。
[0137]
表2 expi 293f细胞转染蛋白表达量
[0138][0139]
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本技术欲包括任何变更、用途或对本发明的改进,包括脱离了本技术中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1