一种具有抗癌作用的菌株的分离及应用的制作方法
1.本发明属于微生物领域,具体涉及一种具有抗癌作用的乳酸片球菌分离及应用。
背景技术:
2.肿瘤作为当今医学界亟待克服的一大难题,已经发展出了多种治疗方案,譬如手术治疗、化疗、放疗、免疫治疗、靶向药物治疗等。近几年,微生物药物在肿瘤治疗领域不断兴起。
3.微生物治疗是肿瘤联合治疗的重要组成部分。微生物群可以调节人体免疫、抑制局部炎症、靶向肿瘤代谢和传导信号分子,肿瘤微生物治疗有单独和联合治疗2种模式。合理的微生物治疗不仅能治疗肿瘤相关炎症和肿瘤本身,更可能实现肿瘤的个体化治疗和改善肿瘤患者的预后。
4.乳酸菌在肿瘤治疗中可以发挥巨大作用。
5.中国专利202110786852.8中公开了一种赋予食物成分抗癌效能的肠道乳杆菌菌株,该肠道乳杆菌与i3c纯品或含i3c的蔬菜同服,可对肺癌、黑色素瘤、白血病等肿瘤发挥预防和治疗作用。该发明的肠道乳杆菌可以定植于哺乳动物消化道,维持其较低的ph微环境,可以促进食物中的i3c转化成为抗肿瘤活性更好的dim和ltr1,从而赋予或显著提高口服i3c的抗癌效果。
6.中国专利202110434508.2中公开了一种增强免疫检查点抑制剂治疗效应的干酪乳杆菌株,保藏编号为cctcc no:m 2020474。该干酪乳杆菌能够改善肿瘤模型小鼠的肠道微生态,促进肿瘤细胞表达cxcl10趋化因子,募集和增加肿瘤细胞组织内杀伤性cd8t淋巴细胞的浸润和活化,高效促进pd-1抗体的治疗效应,显著抑制肿瘤的生长。
7.乳腺癌是全球女性中最为常见的一种恶性肿瘤,大多数早期非转移性的乳腺癌(约70-80%)是可以治愈的,而三阴性乳腺癌(tnbc)约占所有乳腺癌的15-20%,其特征是缺乏雌激素受体(er)、孕激素受体(pr)和人表皮生长因子2(her2)分子标志物,在确诊后的3到5年内预后最差,远处复发的风险最高,严重威胁到女性健康。直到2019年,tnbc治疗仍仅限于化疗,近两年来,免疫疗法结合化疗也被应用于治疗tnbc,显示出良好的应用前景,但仍有大量tnbc患者对免疫治疗无免疫应答,且tnbc对放疗有耐药性,放疗后局部复发率较高。因此,tnbc的治疗在临床上依然是一个待解决的难题,急需寻找有效的治疗药物。
8.中国专利201080045207.0中公开了乳酸菌的摄取和乳腺癌的发病风险的关系,发现摄取含有干酪乳杆菌(lactobacillus casei)的活菌的女性的乳腺癌的发病率与不摄取这些的女性的乳腺癌的发病率相比,在统计上明显减少。此外,发现摄取干酪乳杆菌和来自大豆成分的女性的乳腺癌的发病率进一步减少,由此提供一种包括含有干酪乳杆菌的活菌的组合物的乳腺癌发病风险降低剂。但该发明中提供的制剂成分较为复杂,临床应用多有弊端,有进一步优化的空间。
9.现有技术中对于癌症的治疗,扩展相应微生物的种质资源库是十分必要的,可以为癌症的治疗提供更多的保障。
技术实现要素:
10.基于以上问题,本发明分离筛选出一株乳酸片球菌,该乳酸片球菌可以抑制肿瘤的生长速度,可以用于肿瘤的预防和治疗。此外,该乳酸片球菌还可以与其他的肿瘤抑制剂联合使用。
11.具体来说,本发明人已经研发用于治疗和预防癌症的新疗法。具体来说,本发明人已经确定乳酸片球菌(pediococcus acidilactici)物种的细菌菌株可以有效治疗和预防癌症。如实施例中所描述,经口服用包含乳酸片球菌的组合物可以减小癌症的小鼠模型中的肿瘤大小。
12.在优选实施方案中,本发明提供了一种包含乳酸片球菌物种的细菌菌株的组合物,其用于治疗或预防例如乳癌、肺癌或肝癌等癌症的方法中。本发明人已经确定用包含乳酸片球菌物种的细菌菌株的组合物治疗可以减少乳癌、肺癌和肝癌的小鼠模型中的肿瘤生长。在某些实施方案中,组合物用于在癌症治疗中减小肿瘤尺寸或预防肿瘤生长的方法中。使用乳酸片球菌的组合物可以特别有效用于在癌症治疗中减小肿瘤尺寸或预防肿瘤生长。
13.在本发明的优选实施方案中,组合物中的细菌菌株属于乳酸片球菌。也可使用密切相关的菌株,例如具有与乳酸片球菌的细菌菌株的16s rdna序列至少95%、96%、97%、98%、99%、99.5%或99.9%一致的16s rdna序列的细菌菌株。优选地,细菌菌株具有与seq id no.1至少95%、96%、97%、98%、99%、99.5%或99.9%一致的16s rdna序列。优选地,用于本发明的细菌菌株具有由seq id no.1表示的16s rdna序列。
14.因此,本发明还提供了一种包含具有与乳酸片球菌的细菌菌株的16s rdna序列至少95%一致的16s rdna序列的细菌菌株的组合物,其用于治疗或预防癌症的方法中。具体地说,本发明提供了一种包含具有与seq id no.1至少95%一致的16s rdna序列的细菌菌株的组合物,其用于治疗或预防癌症的方法中。在一些实施方案中,组合物中的细菌菌株不属于乳酸片球菌。在一些实施方案中,组合物中的细菌菌株不属于乳酸片球菌,而是密切相关的菌株。
15.在某些实施方案中,本发明的组合物用于经口服用。经口服用本发明的菌株可以有效地治疗癌症。
16.在某些实施方案中,本发明的组合物包含一种或多种药学上可接受的赋形剂或载剂。
17.在某些实施方案中,本发明的组合物包含已冻干的细菌菌株。冻干是一项制备允许传递细菌的稳定组合物的有效和便利的技术。
18.在某些实施方案中,本发明提供了一种包含如上所述的组合物的食品。
19.在某些实施方案中,本发明提供了一种包含如上所述的组合物的疫苗组合物。
20.另外,本发明提供了一种治疗或预防癌症的方法,其包括施用包含乳酸片球菌物种的细菌菌株的组合物。
21.在研发以上发明时,本发明人已经鉴别和表征特别适用于疗法的细菌菌株。本发明的乳酸片球菌菌株展示有效治疗癌症。因此,在另一个方面中,本发明提供了一种以保藏号cctcc no:m 2022095保藏的乳酸片球菌菌株或其衍生物的细胞。本发明还提供了包含此类细胞的组合物或此类细胞的生物纯培养物。本发明还提供了一种以保藏号cctcc no:m 2022095保藏的乳酸片球菌菌株或其衍生物的细胞,其用于治疗中,尤其用于癌症。类似地,
本发明提供了一种具有与seq id no.1至少95%一致的16s rdna序列的细菌菌株或其衍生物的细胞。本发明还提供了包含此类细胞的组合物或此类细胞的生物纯培养物。本发明还提供了一种具有与seq id no.1至少95%一致的16s rdna序列的细菌菌株或其衍生物的细胞,其用于治疗中,尤其治疗或预防癌症。
22.本发明还提供了包含具有与乳酸片球菌的细菌菌株的16s rdna序列至少95%一致的16s rdna序列的细菌菌株的组合物,其用于治疗中,例如用于治疗或预防癌症的方法中。具体地说,本发明还提供了包含具有与seq id no.1至少95%一致的16s rdna序列的细菌菌株的组合物,其用于治疗中,例如用于治疗或预防癌症的方法中。在一些实施方案中,组合物中的细菌菌株不属于乳酸片球菌,而是密切相关的菌株。
23.本发明提供了一种乳酸片球菌,其用于治疗中,例如用于治疗或预防癌症。类似地,本发明提供了一种包含乳酸片球菌物种的细菌菌株的组合物,其用于治疗中,例如用于治疗或预防癌症。在某些实施方案中,本发明的组合物包含具有与seq id no.1至少95%一致的16s rdna序列,例如是乳酸片球菌的细菌菌株,并且不含有任何其它细菌种属。在某些实施方案中,本发明的组合物包含具有与seq id no.1至少95%一致的16s rdna序列,例如是乳酸片球菌细菌菌株的单一菌株,并且不含有任何其它细菌菌株或物种。
24.本发明分离筛选出一株乳酸片球菌,该乳酸片球菌可以抑制肿瘤的生长速度,可以用于肿瘤的预防和治疗。该乳酸片球菌在本文中称为菌株pb-10。测试的pb-10菌株的16s rdna序列在seq id no.1中提供。菌株pb-10由苏州普瑞森基因科技有限公司以“乳酸片球菌”在中国典型培养物保藏中心保藏,分配保藏号cctcc no:m 2022095。
25.本发明提供的乳酸片球菌还可以与其他的肿瘤抑制剂联合使用,肿瘤抑制剂包括pd-1抑制剂、pd-l1抑制剂、ctla-4抑制剂、细胞毒性抗肿瘤药物、分子靶向药等。
26.菌株pb-10的基因组包含染色体,其染色体序列可以使用illumina,pacbio rs ii等平台产生这些。
27.本发明还预期与所述实施例中测试的菌株密切相关的细菌菌株有效治疗或预防癌症。在某些实施方案中,用于本发明的细菌菌株具有与乳酸片球菌的细菌菌株的16s rdna序列至少95%、96%、97%、98%、99%、99.5%或99.9%一致的16s rdna序列。优选地,用于本发明的细菌菌株具有与seq id no.1至少95%、96%、97%、98%、99%、99.5%或99.9%一致的16s rdna序列。优选地,序列一致性是针对seq id no.1。优选地,用于本发明的细菌菌株具有由seq id no.1表示的16s rdna序列。
28.作为以保藏号cctcc no:m 2022095保藏的细菌的生物型且适合用于本发明中的菌株可以通过对以保藏号cctcc no:m 2022095保藏的细菌的核苷酸序列进行测序来比对鉴别。举例来说,基本上全基因组可以测序,且用于本发明的菌株可以在其全基因组的至少80%上(例如在至少85%、90%、95%或99%上或在其全基因组上)与cctcc no:m 2022095保藏的细菌具有至少95%、96%、97%、98%、98%、99.5%或99.9%序列一致性。用于鉴别生物型的适合序列可以是其它基因序列,包括hsp60或重复序列。菌株生物型鉴别序列可以具有与以保藏号cctcc no:m 2022095保藏的细菌的对应序列有至少95%、96%、97%、98%、98%、99.5%或99.9%的一致性。在一些实施方案中,本发明的菌株具有与以cctcc no:m 2022095保藏的菌株pb-10的对应序列至少95%、96%、97%、98%、98%、99.5%或99.9%序列一致的序列并且包含与cctcc no:m 2022095保藏细菌染色体序列至少99%一
致(例如至少99.5%或至少99.9%一致)的16s rdna序列。在一些实施方案中,生物型菌株具有与以cctcc no:m 2022095保藏的菌株pb-10的对应序列至少95%、96%、97%、98%、98%、99.5%或99.9%序列一致的序列并且具有seq id no.1的16s rdna序列。
29.在某些实施方案中,用于本发明的细菌菌株具有与保藏号cctcc no:m2022095保藏的细菌具有序列一致性的染色体。在优选实施方案中,用于本发明的细菌菌株具有在cctcc no:m 2022095保藏细菌染色体序列的至少60%(例如至少50%、65%、70%、75%、80%、85%、90%、95%、96%、97%、98%、99%或100%)上与cctcc no:m 2022095保藏细菌至少90%序列一致(例如至少92%、94%、95%、96%、97%、98%、99%或100%序列一致)的染色体。举例来说,用于本发明的细菌菌株可以具有在cctcc no:m 2022095保藏细菌染色体序列的70%上与cctcc no:m 2022095保藏细菌染色体序列至少90%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的80%上与cctcc no:m 2022095保藏细菌染色体序列至少90%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的90%上与cctcc no:m 2022095保藏细菌染色体序列至少90%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的100%上与cctcc no:m 2022095保藏细菌染色体序列至少90%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的70%上与cctcc no:m 2022095保藏细菌染色体序列至少95%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的80%上与cctcc no:m 2022095保藏细菌染色体序列至少95%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的90%上与cctcc no:m 2022095保藏细菌染色体序列至少95%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的100%上与cctcc no:m 2022095保藏细菌染色体序列至少95%序列一致,或在cctcc no:m2022095保藏细菌染色体序列的70%上与cctcc no:m 2022095保藏细菌染色体序列至少98%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的80%上与cctcc no:m 2022095保藏细菌染色体序列至少98%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的90%上与cctcc no:m2022095保藏细菌染色体序列至少98%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的95%上与cctcc no:m 2022095保藏细菌染色体序列至少98%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的100%上与cctcc no:m 2022095保藏细菌染色体序列至少98%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的90%上与cctcc no:m 2022095保藏细菌染色体序列至少99.5%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的95%上与cctcc no:m 2022095保藏细菌染色体序列至少99.5%序列一致,或在cctcc no:m 2022095保藏细菌染色体序列的98%上与cctcc no:m 2022095保藏细菌染色体序列至少99.5%序列一致,或在cctcc no:m2022095保藏细菌染色体序列的100%上与cctcc no:m 2022095保藏细菌染色体序列至少99.5%序列一致的染色体。
30.本发明中,“pd-1”为程序性死亡受体1,是一种重要的免疫抑制分子。通过向下调节免疫系统对人体细胞的反应,以及通过抑制t细胞炎症活动来调节免疫系统并促进自身耐受。
31.本发明中,“mrs培养基”可以用于乳酸菌的分离培养或计数,主要成分可以包括:蛋白胨、牛肉浸粉、酵母浸粉、葡萄糖、磷酸氢二钾、柠檬酸三铵、醋酸钠、硫酸镁、硫酸锰、琼脂、吐温80等。
32.本发明中,“葡萄糖-酵母膏培养基、lbs培养基、mc培养基或sl培养基”均可理解为
本领域一般认知的培养基类型。
33.本发明中,“优化培养基”是指在本领域一般认知的培养基类型基础上,根据不同的目的和菌株类型对培养基的成分进行调整以使其更适用于特定条件的培养基类型。
34.本发明中,“对数生长期”是指细胞在一定的环境下经过了短暂的适应期,进而快速生长的时期,细胞以对数生长,即以2的n次方的速度生长(n为细胞的分裂次数),对数期最显著地特征是细胞的数目大量增加。
35.本发明中,“稳定期”也称“平台期”,是指细胞生长速率和死亡速率平衡,细胞的总个数基本保持不变的时期,细胞的对数生长期结束后进入稳定期。
36.一方面,本发明提供了一种乳酸片球菌。
37.所述的乳酸片球菌保藏号为:cctcc no:m 2022095,于2022年01月19日时间保藏于中国典型培养物保藏中心。
38.所述的乳酸片球菌的16s rdna序列为seq id no.1。
39.所述的乳酸片球菌菌落培养特征为:在mrs琼脂培养基上,培养24h后菌落呈白色凸起,表面湿润,不透明,边缘整齐,菌落直径在0.8-1.2mm;在显微镜下,菌体呈圆球,无芽孢,革兰氏阳性。在37℃恒温的条件下,在mrs肉汤培养基上生长较快,2h即进入对数生长期,6-8h到达稳定期。
40.另一方面,本发明提供了一种乳酸片球菌制备物。
41.所述的制备物通过前述的乳酸片球菌进行制备。
42.所述的制备物为培养物、发酵液、发酵液上清、发酵液沉淀、活菌、死菌、冻干粉中的一种或多种。
43.所述的培养物为前述的乳酸片球菌接种于培养基培养后得到,所述的培养基可以是本领域一般培养基。优选地,所述的培养基为mrs培养基、葡萄糖-酵母膏培养基、lbs培养基、mc培养基、sl培养基或前述培养基的优化培养基。
44.再一方面,本发明提供了一种乳酸片球菌的培养方法。
45.所述的培养方法中包括对前述的乳酸片球菌进行培养。
46.所述的培养方法中包括以下步骤:
47.s1、将权利要求1所述的乳酸片球菌接种于培养基;
48.s2、条件培养。
49.所述的培养基可以是本领域一般培养基。
50.优选地,所述的培养基为mrs培养基、葡萄糖-酵母膏培养基、lbs培养基、mc培养基或sl培养基。
51.所述的条件培养可以时好氧培养、厌氧培养或者兼性厌氧培养。
52.又一方面,本发明提供了一种生物菌剂。
53.所述的生物菌剂包括前述的乳酸片球菌。
54.又一方面,本发明提供了前述的乳酸片球菌和/或乳酸片球菌制备物和/或培养方法和/或生物菌剂在制备用于肿瘤预防或治疗或预后的药物中的应用。
55.所述的肿瘤可以是乳腺癌、肝癌、结肠癌、直肠癌、结肠直肠癌、胰腺癌、肾癌、纤维肉瘤、肺癌和胆管癌中的一种或多种。
56.所述的药物中包括前述的乳酸片球菌和/或乳酸片球菌制备物和/或生物菌剂。
57.或者所述的药物的制备方法中包括前述的培养方法。
58.又一方面,本发明提供了一种用于肿瘤预防或治疗或预后的药物。
59.所述的药物中包括前述的乳酸片球菌和/或乳酸片球菌制备物和/或生物菌剂。
60.或者所述的药物的制备方法中包括前述的培养方法。
61.所述的肿瘤可以是乳腺癌、肝癌、结肠癌、直肠癌、结肠直肠癌、胰腺癌、肾癌、纤维肉瘤、肺癌和胆管癌中的一种或多种。
62.优选地,所述的药物中还包括药学上可接受的添加剂或辅料。
63.所述的药学上可接受的添加剂或辅料包括但不限于:赋形剂、增稠剂、崩解剂、稳定剂、混悬剂、粘合剂、乳化剂、香精、色素等。
64.优选地,所述的药物剂型包括但不限于:片剂、丸剂、粉剂、混悬剂、凝胶、乳液、乳膏、颗粒剂、纳米颗粒、胶囊、栓剂、注射剂、喷雾和针剂。
65.在本发明应用较佳的实施方式中,上述预防或治疗肿瘤药品的有效成分包括并不限于乳酸片球菌,还可以包括其他的预防或治疗肿瘤的药物或抗体。
66.优选地,所述的抗体为pd-1。
67.本发明的有益效果:
68.本发明分离筛选出一株乳酸片球菌,该乳酸片球菌对癌症病人肿瘤免疫治疗的效果具有重要的影响,尤其是对于三阴性乳腺癌和肝癌。肠道微生物与免疫细胞之间能相互作用,共同调控人的免疫系统。本发明提供的乳酸片球菌可以用于制备肿瘤抑制剂及相应的药物,从而实现肿瘤预防或治疗。
69.保藏说明:
70.菌种名称:乳酸片球菌pb-10;
71.拉丁学名:pediccoccus acidilactici pb-10;
72.保藏号:cctcc no:m 2022095;
73.保藏时间:2022年01月19日;
74.保藏机构:中国典型培养物保藏中心;
75.保藏地址:中国武汉,武汉大学。
附图说明
76.图1为pb-10的菌落形态图。
77.图2为pb-10的革兰氏染色图。
78.图3为pb-10的体外酸耐受性结果图。
79.图4为pb-10的体外胆盐耐受性结果图。
80.图5为pb-10溶血性结果图。
81.图6为pb-10氨基脱羧酶活性结果。
82.图7为4t-1模型中各组小鼠存活率图。
83.图8为pb-10对乳腺癌(4t-1)的抑制作用结果图。
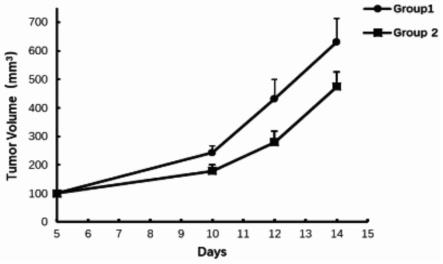
84.图9为pb-10对肝癌(h22)的预防和抑制作用结果图。
具体实施方式
85.下面结合具体实施例,对本发明作进一步详细的阐述,下述实施例不用于限制本发明,仅用于说明本发明。以下实施例中所使用的实验方法如无特殊说明,实施例中未注明具体条件的实验方法,通常按照常规条件,下述实施例中所使用的材料、试剂等,如无特殊说明,均可从商业途径得到。
86.基础实验例菌株分离、纯化及鉴定
87.以母乳为样品,在无菌条件下,将母乳用无菌pbs进行10倍梯度稀释,选取三个浓度梯度,涂布于mrs琼脂培养基上(购自青岛海博生物科技有限公司,货号:hb0384),同时用pbs做空白对照,置37℃恒温培养箱中厌氧培养24-72h,随后挑取不同形态的菌落进行革兰氏染色镜检,并于mrs琼脂培养基中进行2次划线纯化,再染色镜检,观察细菌形态及是否纯化。对纯菌株进行16s rdna基因分析,初步确定其种属,筛选得到一株菌。
88.对筛选得到的菌的16s rdna进行测序,序列见seq id no.1。将测序结果在ncbi库中进行比对,结果显示该菌株序列与乳酸片球菌有99%的同源性,表明分离出的菌株为乳酸片球菌,将分离到的菌株命名为pb-10。
89.分离到的菌株pb-10在mrs琼脂培养基上菌落形态如图1所示,该菌株在mrs琼脂培养基上,培养24h后菌落呈白色凸起,表面湿润,不透明,边缘整齐,菌落直径在0.8-1.2mm。经过染色后在光学显微镜下的形态如图2所示,在显微镜下,菌体呈圆形,无芽孢,为革兰氏阳性球菌。通过对该菌株全基因组序列分析得到相关种的全基因组序列系统发育树,与本菌株最接近的几株菌均来源于发酵食品。
90.将菌株pb-10于2022年01月19日保藏于中国典型培养物保藏中心,保藏编号为cctcc no:m 2022095。
91.实施例1菌株耐药性检测
92.采用药敏纸片扩散法进行,将mrs肉汤培养基(购自青岛海博生物科技有限公司,货号:hb0384-1)培养好的菌液,进行4000rpm离心15min,去掉上清液,用pbs进行悬浮,吹打均匀,将od值调整为0.6左右,均匀涂布于含有mrs固体培养基的培养皿中,待菌液完全吸收后,放置药敏纸片(含有抗菌药物或抗生素),一块平板放置一种药敏纸片(3片)和空白对照(1片),倒置培养于37℃培养箱,24h用直尺测量抑菌环直径,记录数据,根据纸片法抗菌药物试验标准(ws/t125—1999)判读结果。具体抗菌药物或抗生素的实验结果如下:
93.[0094][0095]
备注:s=敏感,i=中介,r=耐药。
[0096]
本菌株对青霉素和氨苄西林、红霉素、氯霉素和克林霉素表现为敏感;对四环素耐药程度为中介;对头孢拉定、呋喃唑酮、万古霉素、庆大霉素、复方新诺明和多粘菌素b表现为耐药性。
[0097]
实施例2菌株体外酸和胆盐耐受性试验
[0098]
(1)模拟胃液(simulated gastric fluid,sgf)实验
[0099]
1、取2.0g nacl和3.2g胃蛋白酶(索莱宝胃蛋白酶,1:3000,标识为每mg中含800-2500个活度单位),加7.0ml 37%稀盐酸和水使溶解至1000ml,溶液ph值为1.2。调ph至3.0(模拟人饭后肠液ph及小鼠空腹肠液ph),过滤除菌;
[0100]
2、集菌:菌株于37℃静止培养6h,达到对数生长期,将菌液分装于50ml无菌ep管,4000rpm室温离心15min后,弃上清,用pbs重悬菌体,并调取菌液od
600
值,得到细菌数约为2
×
109cfu/ml,随后取15ml无菌ep管,分别加入调好od值的6ml菌液,进行离心(条件同上)弃上清液,收集菌沉淀待用,1管pbs为对照组;
[0101]
3、人工胃液培养:将上述不同ph为3的人工胃液加入6ml至洗涤后收集的菌沉淀15ml离心管中,并吹打混匀,孵育培养1h、2h,并且每隔一小时进行涂布计数。实验结果见图3,孵育2h后活菌数仍保持在一个数量级,说明该菌株具有较强的耐酸能力。
[0102]
(2)模拟人体内胆盐环境实验
[0103]
1、胆汁配制:在目标菌培养基(mrs肉汤)溶液中加入牛胆粉(购自合肥巴斯夫生物科技有限公司,货号:n0101-100g),设置三个终浓度,分别为10g/l(1%牛胆粉)、20g/l(2%牛胆粉)和40g/l(4%牛胆粉),高压灭菌后备用,同时,以不加胆粉的培养基溶液0h作为对照。本实施例中选用mrs培养基。
[0104]
2、菌株收集同模拟胃液实验。
[0105]
3、牛胆粉培养:将配置含有0%、1%、2%和4%牛胆粉的mrs培养基分别加入10ml至洗涤后收集的菌沉淀20个15ml离心管中进行孵育培养0h、1h、2h、3h和4h,以0%牛胆粉培养基溶液0h作为对照组,并且每隔一小时进行涂布计数同时做出生长曲线。实验结果见图4,结果表明该菌株在1%-4%牛胆粉培养基中可正常生长,且随着孵育培养的时间增加,其
活菌数也在增加,说明该菌株对牛胆盐具备一定的耐受程度,且可正常生长繁殖。
[0106]
实施例3菌株体外安全性评价
[0107]
(1)溶血性检测
[0108]
将实验菌株在mrs液体培养基过夜培养,取合适梯度涂布于哥伦比亚血平板上(购买于上海科玛嘉微生物技术有限公司),37℃培养18-24h,观察菌落周围的溶血圈产生情况。菌株在哥伦比亚血平板上的溶血情况见图5,该菌未表现出溶血性。
[0109]
(2)氨基脱羧酶活性检测
[0110]
将用mrs肉汤过夜培养的新鲜菌液,分别接种于溴甲酚紫葡萄糖肉汤培养基(购买于青岛海博生物科技有限公司,货号:hb4174)和mrs肉汤培养基中,同时设立空白对照,18-24h后观察溴甲酚紫葡萄糖肉汤培养基颜色变化情况。菌株若能产生氨基脱羧酶,则能分解氨基酸产生胺和二氧化碳,使培养基变碱性,遇到溴甲酚紫呈紫色。氨基脱羧酶可将氨基酸脱羧还原成生物胺类物质,若胺类物质在体内积累过多,会引起中毒。实验结果见图6,结果表明实验菌株氨基脱羧酶活性为阴性。
[0111]
(3)硝基还原酶活性检测
[0112]
将mrs肉汤培养18h的实验菌液3000
×
g离心10min后取上清,稀释5倍后采用酶联免疫吸附试验测定其硝基还原酶活性,具体操作步骤参考试剂盒说明书(试剂盒购买于上海酶联生物科技有限公司)。硝基还原酶可将硝酸盐类物质还原成亚硝酸类物质,在体内积累过多后会引起中毒,大肠杆菌的硝基还原酶活性一般可达30u/l,结果表明本实验菌株的硝基还原酶活性远低于大肠杆菌。实验结果见下表:
[0113][0114]
(4)生物膜形成能力检测
[0115]
取mrs肉汤过夜培养的新鲜培养菌株200μl(接种了10%过夜培养的菌液的新鲜培养基)加样到96孔聚苯乙烯板上,37℃孵育72h,将培养液吸出,加200μl pbs清洗3次,然后每孔加入100μl甲醇固定15min,吸出培养孔中的甲醇,自然风干,加入0.5%结晶紫染色10min后吸出染液,蒸馏水清冲洗多余染液;把培养板倒置在滤纸上除去残余的水,并在37℃烘箱中烘干;完全干燥后,每孔加入100μl 33%冰乙酸溶液,在37℃培养箱中作用30min以溶解结晶紫,590nm条件下,用酶标仪测定培养孔中溶液的od值。以未接种菌的培养液作为阴性对照。生物膜形成能力越强,菌株的耐药性增强,增加临床上治疗细菌感染类疾病的
难度,生物膜形成能力一般认为a》2为强阳性,1-2之间为中等,a《1为阴性,本实验菌株生物膜形成能力较弱,增加菌株耐药性的能力较弱。实验结果见下表:
[0116]
样品a1值a2值a3值均值生物膜a值pb-100.5930.5440.5690.5690.502空白0.0660.0670.0680.0670.067
[0117]
实施例4代谢产物分析
[0118]
参考《中国药典》2020版,用气相色谱法对菌株发酵上清液中的乙酸、丙酸、丁酸、异丁酸、戊酸和异戊酸的含量进行检测。具体操作:取培养至对数生长晚期的菌液以1%接种量加入到40ml mrs肉汤培养基中,分别培养三管,培养24h,将菌液按6000rpm/min离心10min,各收集30ml上清液。委托苏州百拓生物技术服务有限公司进行上清液中代谢产物分析检测结果见下表,结果表明,实验菌株主要产乙酸,其次为丙酸。
[0119][0120]
实施例5菌株体内药效评价一
[0121]
利用鼠源乳腺癌细胞4t-1(上海一研生物科技有限公司)构建动物模型,细胞培养条件为1640培养基,含10%胎牛血清以及100u/ml青霉素和100μg/ml链霉素。在37℃、5%co2恒温环境中培养。动物模型选用的小鼠为7-8周龄的雌性balb/c小鼠,体重为18-20g,购自北京灵畅实验动物有限公司。饲养级别为spf级,光照/黑暗周期为12h。自由饮水饮食。
[0122]
实验菌株的制备:
[0123]
从-80℃取出甘油菌,在mrs琼脂平板上划线活化,37℃过夜培养,挑取单菌落接种于50ml mrs肉汤培养基中,37℃、150rpm过夜培养,以5%接种量转接于含有1.5l mrs肉汤的2l大瓶中,37℃、150rpm摇瓶发酵10h。将发酵好的发酵液于4℃、4000g的离心率下离心10min收集菌体,再用pbs洗涤一次,然后用含有20%无菌甘油溶液将菌体进行重悬、分装(每支装量为每组小鼠的灌胃所需活菌数,浓度调整到大约1
×
10
10
cfu/ml),-80℃冻存,给药时取出冻存菌液于37℃水浴锅中复溶,每只小鼠1
×
109cfu的剂量喂食。
[0124]
药效评价:
[0125]
小鼠到达实验室后适应一周左右,接种4t1细胞,具体操作:将从培养瓶中消化下来的4t1细胞收集到离心管中,1000rpm转速离心5min,弃上清液,加入pbs重悬并计数,在小鼠右下第二乳垫接种肿瘤细胞,接种量为3
×
105cells/只,每只小鼠接100μl,肿瘤接种日记为第0天。
[0126]
接种第9天根据小鼠肿瘤体积将小鼠分为4组,每组10只,每组平均瘤体积为97mm3,具体情况如下:group1 4t1乳腺癌模型对照组;group2 pd-1单抗+模型组;group 3:实验菌液+模型组、group4 pd-1单抗+实验菌液+模型组。其中实验菌液以灌胃方式给药,每天给药,一只小鼠给药量为200μl,活菌数为109cfu/只,连续给药3周;pd-1抗体(sigma)稀释至0.5g/l的浓度,按10μl/g的体重腹腔注射给药,一周两次,连续给药3周。每3-4天称量小鼠体重(g)和测量肿瘤的大小(mm3),肿瘤大小计算公式:
[0127]
肿瘤体积(mm3)=0.5
×
(肿瘤长径
×
肿瘤短径2)。
[0128]
实验结果见图7和图8,图7为小鼠存活率情况结果图,图8为肿瘤生长情况图。从图7中可以看出实验结束时实验菌液组(group3)小鼠存活率为100%,其次为pd-1与实验菌液联合给药组(group4),存活率为90%,均高于对照组(group1)和pd-1给药组(group2)的小鼠存活率;从图8中可以看出,与对照组(group1)相比,实验菌液组(group3)能显著降低肿瘤体积(p<0.01),肿瘤抑制率为23%,而pd-1单抗给药组(group3)和对照组无统计学差异,pd-1与实验菌液联合给药组(group4)对肿瘤体积有显著抑制效果(p<0.01)且对肿瘤抑制率大于单用菌液组(group3),肿瘤抑制率为33%。实验结果表明,该动物模型是对pd-1不敏感模型,单用pd-1并不能抑制肿瘤,但单用菌液能显著降低肿瘤大小,且在pd-1存在的情况下药效更显著。
[0129]
实施例6菌株体内药效评价二
[0130]
利用肝癌细胞h22(上海一研生物科技有限公司)构建动物模型,细胞培养条件为1640培养基,含10%胎牛血清以及100u/ml青霉素和100μg/ml链霉素。在37℃、5%co2恒温环境中培养。动物模型选用的小鼠为7-8周龄的雌性balb/c小鼠,购自南京君科生物科技有限公司。饲养级别为spf级,光照/黑暗周期为12h。自由饮水饮食。
[0131]
实验菌株的制备同实施例5。
[0132]
药效评价:
[0133]
小鼠到达实验室后适应一周左右,接种h22细胞。接种当天收集细胞,细胞,经pbs洗涤细胞一次后,用pbs重悬,并对细胞悬液进行计数,接种量为1
×
106cells/只,每只小鼠接100μl,肿瘤接种日记为第0天。
[0134]
接种第5天根据小鼠肿瘤体积将小鼠分为2组,每组8只,每组平均瘤体积为100mm3,具体情况如下:group1为h22模型对照组;group2为实验菌液给药组。其中实验菌液以灌胃方式给药,每天给药,一只小鼠给药量为200μl,活菌数为108cfu/只,连续给药2周,每3-5d测量肿瘤的大小(mm3),肿瘤大小计算公式:
[0135]
肿瘤体积(mm3)=0.5
×
(肿瘤长径
×
肿瘤短径2)。
[0136]
实验结果见图9,与group1模型组相比,group2(实验菌液组)对肿瘤的抑制率为25%。说明本发明中所用菌株对肝癌可起到一定的抑制作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1