一种倍半萜色酮类化合物及其分离和在制备抗胰腺癌药物中的应用
fh-1 至 fh-5;对组分 fh-1进行硅胶柱色谱,并用石油醚-乙酸乙酯(10:1)洗脱,得到 12 个组分 fh-1-1 至 fh-1-12。
7.对组分fh-1-7用二氯甲烷-乙酸乙酯(60:1)洗脱,得到八个组分fh-1-7-1至fh-1-7-8;对组分fh-1-7-5用二氯甲烷-乙酸乙酯(40:1)得到四个组分fh-1-7-5-1到 fh-1-7-5-4;(4)对组分fh-1-7-5-1使用hplc(c
18
,meoh/h2o= 76/24,流速=4 ml/min)纯化,得到化合物1;(5)对化合物1使用手性hplc(chiral cd-ph,石油醚:乙酸乙酯=84/16,流速= 3 ml/min)纯化,依次得到化合物 (+)-1、化合物 (
‑ꢀ
)-1。
8.通过旋光值、紫外光谱uv、圆二色光谱c、光谱ir、红外(kbr)、氢谱1h 和碳谱
13
c、nmr高分辨质谱hresims对上述分离得到的化合物(+)-1、化合物 (
‑ꢀ
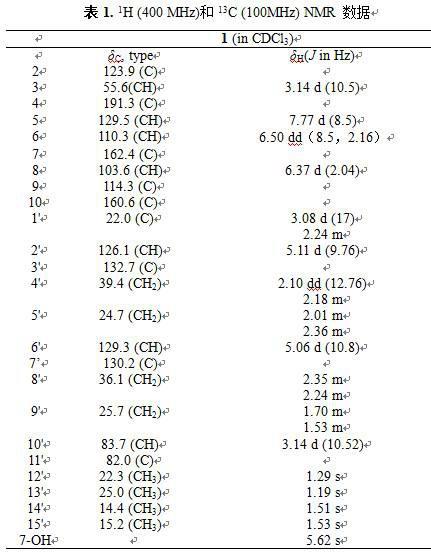
)-1进行分析,其1h (400 mhz)和13c (100mhz) nmr 数据见表1,并确定其结构式如下:
化合物(+)-1和化合物 (
‑ꢀ
)-1是无色油状,分子式是c
24h30
o5,质谱数据(m/z 399.2158, [m + h]
+ 399.2158) 可以推算出有5个不饱和度。3424-1
和1723.9 cm-1
处的强红外吸收表明存在羟基和羰基。1d nmr数据表明5,6,8-三取代苯环[δh7.77(d,j=8.5hz,h-5),6.50(dd,j=8.5,2.16hz,h-6),6.37(d,j=2.04hz,h-8)和δc129.5(c-5),110.3(c-6),162.4(c-7),103.6(c-8),114.39c-9),160.69c-10)],以及两个三取代烯烃键[5.11(d,j=9.76hz,h-2,h-6')和 δc126.1(c-2'), 129.3(c-6')]。两个h质子[δh3.14(d,j=10.5hz,h-3),3.14(d,j=10.52hz,h-10') 和 δc55.0(c-3),83.7(c-10')]。1d nmr数据也显示了24个碳信号,包括一个羰基δc 191.34(c-4)、四个甲基[δh 1.19(s,h3-13')、1.29(s,h3-12')、1.51(s,h3-14')和1.53(s,h3-15')]。
[0009]
通过对2d nmr谱的综合解释,进一步阐明了化合物(+)-1和化合物 (
‑ꢀ
)-1的平面结构。对1h-1
h cosy谱的分析表明存在四个相关体系,即ch(10’)-ch(8’)、ch(5)-ch(6)、ch(9’)-ch(1’)、ch(6’)-ch(5’)。hmbc数据在h-5/c-4/ c-7/c-9和 h-6/c-8/c-10, 和 h-8/c-6/c-10 的相关性表明a环的存在(如图1所示),在h-3/c-/c-2'/c-2/c-1' 、h-2'/ c-4'/c-15'、h
3-15'/c-3'/c-2'/c-4'、h
3-14'/c-7'/c-8'、h-6'/c-14'/c-8'、h-4'/c-6'、h-10'/c-11'/c-8'、h
3-13'/c-10'/c-11'/c-12'和h-12'/c-13'/c-11'的相关性表明,b、c、d环的存在(如图1所示)。绝对构型的测定通过ecd计算(图2-图7)。
[0010]
二、倍半萜色酮类化合物的抗胰腺癌活性本实验用人源胰腺癌细胞sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞,取对数生长期的sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞,接种于96孔板(每孔1
×
104个细胞),待细胞贴壁后,分别加入浓度范围为0.1-100
ꢀµ
m梯度的待测化合物,培
养72 h,然后每孔加入10
ꢀµ
l cck-8溶液继续培养4小时,振荡10 min,酶标仪450 nm测定吸光度值,采用mtt法检测新疆阿魏倍半萜色酮类化合物 (+)-1和 (-)-1对sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞的增殖抑制作用(图6),根据吸光值计算细胞存活率,并计算测试化合物ic
50
值。其中,紫杉醇(taxol)作为阳性对照药物。
[0011]
表2为化合物 (+)-1和(-)-1对胰腺癌sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞的抑制作用。其中,化合物 (+)-1抑制sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞的ic
50
值为11.77
±
1.83
ꢀµ
m、6.12
±
0.52
ꢀµ
m、8.57
±
0.59
ꢀµ
m、2.24
±
0.83
ꢀµ
m,化合物(-)-1抑制sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞的ic
50
值为15.67
±
1.53
ꢀµ
m、19.13
±
2.99
ꢀµ
m、14.57
±
0.65
ꢀµ
m、0.70
±
0.47
ꢀµ
m;结果显示,化合物 (+)-1和(-)-1对胰腺癌sw1990细胞、cfpac-1细胞、capan-2细胞和panc-1细胞都有显著的增殖抑制作用,表明化合物 (+)-1和(-)-1能够明显抑制胰腺癌细胞的增殖,具有抗胰腺癌潜在作用,具有开发胰腺癌治疗药物的潜能,可作为活性成分用于制备抗胰腺癌药物。即以新疆阿魏倍半萜色酮类化合物为活性组分,以药学或生理学可接受的辅料及常规药物制剂的制备工艺制成内服制剂或注射剂。内服制剂为散剂、颗粒剂、胶囊剂、软胶囊、粉剂、丸剂、片剂、口服液。
附图说明
[0012]
图1为化合物(+)-1、化合物(-)-1的1h-1
h cosy(黑色加粗) 和hmbc (黑色箭头)。
[0013]
图2为化合物(+)-1的绝对构型。
[0014]
图 3为化合物(-)-1的ecd谱。
[0015]
图 4为化合物(-)-1的cd谱。
[0016]
图 5为化合物(+)-1的绝对构型。
[0017]
图 6为化合物(+)-1的ecd谱。
[0018]
图 7为化合物(+)-1的cd谱。
[0019]
图 8为化合物 (+)-1和 (-)-1抑制胰腺癌细胞存活率。
具体实施方式
[0020]
(1)将干燥的新疆阿魏根用甲醇室温提取3次,每次7天,提取液合并,蒸发浓缩至无醇味,得到总提取物;(2)将总提取物分别用水分散溶解后分别用石油醚、二甲烷氯、乙酸乙酯和正丁醇进行萃取,得到石油醚相、二氯甲烷相、乙酸乙酯相、正丁醇相和水相;(3)乙酸乙酯相(260 g)在硅胶柱上进行色谱分离,用石油醚:乙酸乙酯(石油醚:乙酸乙酯体积比依次为40:1、30:1、20:1、10:1、8:1、6:1、5:1、4:1、3:1、2:1、1:1)进行洗脱,依次得到12个组分fa-fl;
对组分fh(61.3g) 进行硅胶柱色谱,用二氯甲烷:乙酸乙酯(50:1)洗脱,依次得到五个组分 fh-1至fh-5;对组分 fh-1(14.05 g)进行硅胶柱色谱,用石油醚:乙酸乙酯(10:1)洗脱,依次得到 12 个组分 fh-1-1 至 fh-1-12;对组分fh-1-7(393.6 mg)用二氯甲烷:乙酸乙酯(60:1)洗脱,得到八个组分fh-1-7-1至fh-1-7-8;对组分fh-1-7-5(67mg)用二氯甲烷:乙酸乙酯(40:1)得到四个组分fh-1-7-5-1到 fh-1-7-5-4;(4)对组分fh-1-7-5-1(24 mg)使用hplc(c
18
,meoh/h2o= 76/24,流速=4 ml/min)纯化,得到化合物1(4 mg,t
r = 65.052 min);(5)对化合物1使用手性hplc(chiral cd-ph,石油醚:乙酸乙酯= 84/16,流速=3 ml/min)纯化,依次得到化合物 (+)-1(1mg,tr=26.180min)和化合物(-)-1(0.9mg,tr=31.917 min)。
[0021]
化合物[(
±
)-1]:白色油状;mp 218-221
ꢀ°
c; uv (ch3cn) λmax (log ε) 204(3.131)nm, 274(2.356) nm; ir (kbr) ν
max = 3424, 2926.9, 1723.9, 1612.2, 1463.6, 1272.3, 1272.3, 1111.5, 1022.5, 1000.8, 972.0, 973.7 cm
−1; 1
h nmr 和
13
c nmr 数据如表1; 化合物 [(
±
)-1]的质谱 m/z 399.2158 [m + h]
+ (c
24h30
o5, 399.2158)。
[0022]
(+)-1:白色油状;+52.381
°ꢀ
(c 0.1, ch3oh); ecd (ch3oh) λmax (δε): 207(δε
ꢀ‑
38.385), 257 (δε
ꢀ‑
2.98), 268 (δε
ꢀ‑
4.96), 301 (δε 6.35), 328 (δε
ꢀ‑
1.44) nm。
[0023]
(-)-1:白色油状;-48.531
°ꢀ
(c 0.1, ch3oh); ecd (ch3oh)λmax (δε): 208 (δε 33.67), 249 (δε 0.77), 271 (δε 3.67), 300 (δε
ꢀ‑
5.54), 327(δε 0.96) nm。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1