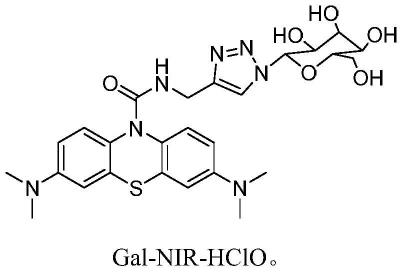
一种肝细胞靶向的次氯酸近红外荧光探针及其制备方法和应用
1.本发明属于次氯酸近红外荧光探针技术领域,具体涉及一种肝细胞靶向的次氯酸近红外荧光探针及其制备方法和应用。
背景技术:
2.肝脏作为调控新陈代谢的重要器官,具有去氧化、储存肝糖、合成分泌蛋白等功能。肝细胞癌作为一种常见的、侵袭性极强的肝脏恶性癌症,发病率和死亡率都很高,是导致人类死亡的三大恶性癌症之一。有研究表明,肝细胞内活性氧的异常累计是导致肝细胞癌的主要原因。次氯酸(hclo)作为一种常见的活性氧,参与调节了细胞内很多的生理和病理进程。生命体内的hclo主要由髓过氧化物酶催化h2o2与cl-的反应产生的。当体内的 hclo含量脱离正常水平范围时,通常伴随着各种病症,如炎症、动脉粥样硬化、肝损伤和癌症等。其中,肝损伤是一种常见疾病,其慢性积累会逐渐引发肝细胞癌。而肝损伤进程中通常伴随着肝细胞中hclo含量的异常,因此可以将hclo看做肝损伤的标志物。因此开发一种能够监测肝细胞内hclo含量水平的方法对早期肝损伤和肝癌的诊断具有极其重要的作用。
3.荧光成像技术因其独特的优势,如极高的灵敏度、良好的时空分辨率、可实现生物样品的无损检测等,在分析化学、生物医学中得到了越来越多的应用。而相较于传统的可见光区荧光探针,近红外荧光探针(λ
ex
》650nm,λ
em
》650nm)具有更低的光毒性、更深的穿透深度、更小的背景荧光,因此具有更大的成像优势,能够在活体层面为化学家、生物学家和临床医学诊断提供更全面与更准确的成像信息。而亚甲基蓝染料则是其中一种优良的近红外荧光染料,具有优良的光物理性质,其发射波长位于近红外区(约685nm),近年来常被用于构建目标物检测的近红外荧光探针。而目前肝细胞靶向的次氯酸近红外荧光探针仍报道较少,且性能有待进一步提高。
技术实现要素:
4.本发明针对目前次氯酸近红外荧光探针所面临的问题和现状,提供了一种肝细胞靶向的次氯酸近红外荧光探针,该荧光探针以半乳糖单元作为肝细胞靶向基团,用于肝细胞内 hclo的成像,该探针具有近红外发射、选择性好、肝细胞靶向能力优异等特点。
5.本发明还提供了上述肝细胞靶向的近红外荧光探针的制备方法及其在水环境、生物细胞体系、小鼠组织中选择性检测次氯酸的应用。
6.本发明为解决上述技术问题采用如下技术方案,一种肝细胞靶向的次氯酸近红外荧光探针,其特征在于该近红外荧光探针的结构式如下:
[0007][0008]
本发明所述的肝细胞靶向的次氯酸近红外荧光探针的制备方法,其特征在于具体步骤为:
[0009]
步骤s1:向500ml三颈烧瓶中加入10.0g亚甲基蓝、100ml水、50ml二氯甲烷和13.26g na2co3,将三颈烧瓶进行氮气保护,随后将21.78g na2s2o4溶解于140ml水中,并通过注射器注射到三颈烧瓶中,于40℃将反应液搅拌至灰黄色,并冷却至室温,随后将溶于40ml 二氯甲烷的5.56g三光气溶液滴加至于反应液中,滴加完毕后室温反应1h,然后将反应液用二氯甲烷萃取三次,并将得到的二氯甲烷萃取液用mgso4干燥,将干燥后的二氯甲烷萃取液过滤,并璇干溶剂,得到粗产物,将粗产物用硅胶柱纯化得到白色固体化合物1 2.9g,产率为53.2%,所用洗脱剂体积配比为石油醚/乙酸乙酯=1:1,其合成路线如下:
[0010][0011]
步骤s2:将2.0g化合物1、1.82g na2co3和0.58g三乙胺溶于100ml二氯甲烷中,并加入至250ml单口瓶中,随后将其放置于冰浴下搅拌,将溶于20ml二氯甲烷的1.27g炔丙胺溶液滴加至反应液中,滴加完毕后撤下冰浴,将反应液于室温反应8h,反应完成后向反应液中加入200ml冰水,继续搅拌10min,然后用乙酸乙酯萃取反应液,将乙酸乙酯萃取液用饱和nacl溶液洗涤,再用无水硫酸钠干燥,将干燥后乙酸乙酯萃取液过滤,并璇干溶剂,得到粗产物,将粗产物用硅胶柱纯化得到灰绿色固体化合物2 0.85g,产率40.3%,所用洗脱剂体积配比为二氯甲烷/甲醇=25:1,其合成路线如下:
[0012][0013][0014]
步骤s3:取0.73g化合物2、1.49g 2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖溴化物、119mg 维生素c钠和75mg五水合硫酸铜(ii)放置于200ml的圆底烧瓶中,然后向圆底烧瓶中倒入50ml水和20ml二氯甲烷的混合溶液,将得到的反应液在氮气保护下室温反应24h,将反应液用二氯甲烷萃取三次,得到的二氯甲烷萃取液用mgso4干燥,将干燥后的二氯甲烷萃取液过滤,并璇干溶剂,得到粗产物,将粗产物用硅胶柱纯化得到灰白色固体化合物 3 0.86g,产率58.1%,所用洗脱剂体积配比为二氯甲烷/乙酸乙酯=2:1,其合成路线如下:
[0015][0016]
步骤s4:将0.74g化合物3溶于50ml甲醇中,随后向其中加入0.65g甲醇钠,将得到的反应液于室温下搅拌24h后,再加入盐酸溶液调ph至中性,然后减压除去溶剂,得到粗产物,将粗产物用硅胶柱纯化得到目标荧光探针化合物gal-nir-hclo 0.24g,产率42%,所用洗脱剂体积配比为二氯甲烷/甲醇=5:1,其合成路线如下:
[0017][0018]
本发明所述的肝细胞靶向的次氯酸近红外荧光探针在水环境、生物细胞体系选择性检测次氯酸中的应用,其中检测包括水溶液中荧光检测、细胞成像检测、组织成像检测。
[0019]
本发明与现有技术相比具有以下有益效果:(1)该近红外荧光探针的合成相对比较容易,且后处理过程相对简单;(2)该近红外荧光探针实现了次氯酸的高选择性、高灵敏度、快速检测,具有抵抗生命体内其它分子干扰的能力;(3)该近红外荧光探针荧光探针具有近优异的肝细胞靶向能力与近红外区的发射,能够应用于肝脏组织中次氯酸的成像检测。该近红外荧光探针通过靶向肝细胞、降低生命体内自发荧光背景干扰、降低对生物样品的光损伤等特点,以获得更加准确及稳定的光学信号及成像效果。因此,本发明中的近红外荧光探针在肝细胞hclo检测领域具有广阔的应用前景,对hclo生物体生理和病理过程的作用机制的研究具有重要意义。
附图说明
[0020]
图1是实施例1制得的荧光探针化合物gal-nir-hclo在加入不同浓度次氯酸的荧光光谱图。
[0021]
图2是实施例1制得的荧光探针化合物gal-nir-hclo在加入不同浓度次氯酸的紫外可见吸收光谱图。
[0022]
图3是实施例1制得的荧光探针化合物gal-nir-hclo在发射波长为685nm处的的荧光强度随次氯酸根浓度(0-16μm)变化的关系曲线图,插图为荧光探针化合物 gal-nir-hclo在发射波长为685nm处的的荧光强度随次氯酸根浓度(0-2μm)变化的关系曲线图。
[0023]
图4是实施例1制得的荧光探针化合物gal-nir-hclo对不同物种的荧光响应情况:(1) pbs;(2)50μm h2o2;(3)50μm o
2-;(4)50μm t-buooh;(5)50μm
·
oh;(6)50μmno;(7)50μm onoo-;(8)50μm roo
·
;(9)50μm t-buoo
·
;(10)16μm hclo。
[0024]
图5是实施例1制得的荧光探针化合物gal-nir-hclo在不同ph条件下对次氯酸的响应情况。
[0025]
图6是实施例1制得的荧光探针化合物gal-nir-hclo在不同癌细胞中对外源性次氯酸的响应情况。
[0026]
图7是实施例1制得的荧光探针化合物gal-nir-hclo检测hepg2中内源性次氯酸的荧光成像图。
[0027]
图8是实施例1制得的荧光探针化合物gal-nir-hclo在小鼠肝脏切片中检测次氯酸的z轴深度扫描荧光成像图。
具体实施方式
[0028]
以下通过实施例对本发明的上述内容做进一步详细说明,但不应该将此理解为本发明上述主题的范围仅限于以下的实施例,凡基于本发明上述内容实现的技术均属于本发明的范围。
[0029]
实施例1
[0030]
荧光探针化合物gal-nir-hclo的合成
[0031]
(1)化合物1的合成
[0032]
向500ml三颈烧瓶中加入10.0g亚甲基蓝、100ml水、50ml二氯甲烷和13.26g na2co3,将三颈烧瓶进行氮气保护。随后将21.78g na2s2o4溶解于140ml水中,并通过注射器注射到三颈烧瓶中。于40℃将反应液搅拌至灰黄色(大约30min),并冷却至室温。随后将溶于40ml二氯甲烷的5.56g三光气溶液缓慢滴加至于反应液中,滴加完毕后室温反应1h。然后将反应液用二氯甲烷萃取三次,并将得到的二氯甲烷萃取液用mgso4干燥。将干燥后二氯甲烷萃取液过滤,并璇干溶剂,得到粗产物。将粗产物用硅胶柱纯化(体积比石油醚:乙酸乙酯=1:1)得到白色固体化合物1(2.9g,产率53.2%)。其合成路线如下:
[0033][0034]
(2)化合物2的合成
[0035]
将2.0g化合物1、1.82g na2co3和0.58g三乙胺溶于100ml二氯甲烷中,并加入至250ml 单口瓶中,随后将其放置于冰浴下搅拌。将溶于20ml二氯甲烷的1.27g炔丙胺溶液缓慢滴加至上述的反应液中。滴加完毕后,撤下冰浴,将反应液在室温下反应8h。反应完成后,向反应液中加入200ml冰水,继续搅拌10min。然后用乙酸乙酯萃取反应液。将乙酸乙酯萃取液用饱和nacl溶液洗涤三次次,再用无水硫酸钠干燥。将干燥后乙酸乙酯萃取液过滤,并璇干溶剂,得到粗产物。将粗产物用硅胶柱纯化(体积比二氯甲烷:甲醇=25:1)得到灰绿色固体化合物2(0.85g,产率40.3%)。其合成路线如下:
[0036][0037]
(3)化合物3的合成
[0038]
取0.73g化合物2、1.49g 2,3,4,6-四-o-乙酰基-α-d-吡喃半乳糖溴化物、119mg维生素c 钠和75mg五水合硫酸铜(ii)放置于200ml的圆底烧瓶中,然后向圆底烧瓶中倒入水和二氯甲烷的混合溶液(50ml/20ml)。将得到的反应液在氮气保护下室温反应24h。将反应液用二氯甲烷萃取三次,得到的二氯甲烷萃取液用mgso4干燥。将干燥后的二氯甲烷萃取液过滤,并璇干溶剂,得到粗产物。将粗产物用硅胶柱纯化(体积比二氯甲烷:乙酸乙酯=2:1) 得到灰白色固体化合物3(0.86g,产率58.1%)。其合成路线如下:
[0039][0040]
(4)荧光探针化合物gal-nir-hclo的合成
[0041]
将0.74g化合物3溶于50ml甲醇中,随后向其中加入0.65g甲醇钠,将得到的反应液于室温下搅拌24h后,加1m盐酸溶液调ph至中性,然后减压除去溶剂,得到粗产物。将粗产物用硅胶柱纯化(体积比二氯甲烷:甲醇=5:1)得到目标荧光探针化合物 gal-nir-hclo(0.24g,产率42%)。其合成路线如下:
[0042][0043]
实施例2
[0044]
荧光探针化合物gal-nir-hclo与不同浓度次氯酸作用的荧光光谱图的测定
[0045]
取实施例1制备的荧光探针化合物gal-nir-hclo溶于甲醇(meoh)中制成500μm 的储备液,从储备液中取出0.04ml加入到5ml的离心管当中,加入不同当量(0-16μm) 的次氯酸标准溶液,用pbs缓冲溶液(20mm,ph=7.4)的溶液稀释至4ml(meoh/pbs 体积比为1:99),以620nm为激发光,狭缝宽度设置为5nm/5nm,测量其荧光光谱。荧光光谱如图1所示,随着次氯酸加入,在685nm处的荧光逐渐增强,其荧光强度与次氯酸浓度的关系如图3所示,在4.0
×
10-8
至2.0
×
10-6
mol/l的范围内呈线性关系,所用的荧光测定仪器为fluoromax-4荧光分
光光度计。
[0046]
实施例3
[0047]
荧光探针化合物gal-nir-hclo与不同浓度次氯酸作用的紫外可见吸收光谱图的测定
[0048]
图2为实施例1制得的荧光探针化合物gal-nir-hclo与不同浓度的次氯酸作用后的紫外可见吸收光谱图,次氯酸的加入量为0-16μm。从图2中可以看出,在665nm可以观察到一个吸收峰,随次氯酸浓度的增加,其吸光度逐渐增加。紫外可见吸收光谱测定用的仪器为cary 100紫外-可见分光光度计。
[0049]
实施例4
[0050]
荧光探针化合物gal-nir-hclo对各种活性氧的选择性
[0051]
从实施例3中的荧光探针储备液中取出0.04ml加入到5ml的离心管当中,加入待考察竞争物质的标准溶液,用pbs缓冲溶液(20mm,ph=7.4)的溶液稀释至4ml(meoh/pbs 体积比为1:99),共考察了9种竞争物质,共配置10个样品,最后一个为次氯酸钠。以620nm 为激发光,狭缝宽度设置为5nm/5nm,测量其荧光光谱,结果如图4所示。由图4可以发现,细胞内其他活性氧对荧光探针化合物gal-nir-hclo在685nm处的荧光几乎没有影响,而次氯酸钠溶液的加入使探针gal-nir-hclo在685nm处的荧光显著增强。
[0052]
实施例5
[0053]
溶液ph值对荧光探针化合物gal-nir-hclo测定次氯酸的荧光响应的影响
[0054]
分别考察了ph值对空白荧光探针化合物gal-nir-hclo以及gal-nir-hclo+次氯酸 (15μm)的两种情况下荧光强度的影响,结果如图5。在ph=5.5-8范围内,ph对空白荧光探针化合物gal-nir-hclo的荧光强度基本无影响。而在次氯酸钠(15μm)存在的情况下,当ph=5.5时,检测体系的荧光强度最大,表明此时荧光探针对次氯酸的响应最好。从图5中可知,在ph处于5.5-8范围内,荧光探针化合物gal-nir-hclo对次氯酸根都显示出较好的响应。
[0055]
实施例6
[0056]
荧光探针化合物gal-nir-hclo对肝细胞靶向能力的考察
[0057]
将荧光探针化合物gal-nir-hclo(5μm)与hct116细胞、hela细胞、mcf-7细胞和hepg2细胞分别培养半个小时后,用杜氏磷酸盐缓冲液(dpbs缓冲液)清洗3次。随后加入naclo溶液(终浓度为20μm),培育30min后,再用dpbs缓冲液清洗3次。然后将hct116细胞、hela细胞、mcf-7细胞、hepg2细胞在激光共聚焦显微镜下成像。荧光成像的条件设定为:λ
ex
=635nm,发射波段设定为640-750nm。荧光成像结果如图6所示,从图中可知,只有人肝癌细胞(hepg2细胞)在经过探针gal-nir-hclo和次氯酸孵育后显示出明显的荧光增强。以上结果表明,荧光探针化合物gal-nir-hclo具有良好的细胞选择性,对肝细胞具有较好的靶向能力。
[0058]
实施例7
[0059]
荧光探针化合物gal-nir-hclo对肝癌细胞内源性次氯酸的成像
[0060]
首先,将探针gal-nir-hclo与正常的人体肝细胞(lo2细胞)和人体肝癌细胞(hepg2 细胞)进行培育,然后进行细胞成像。由荧光成像图7可知,正常的肝细胞没有明显荧光,而肝癌细胞由于其含有一定浓度的内源性hclo,则显示出明显的荧光信号。而当采用次氯酸消耗剂乙酰半胱氨酸(nac)对肝癌细胞进行培养后,肝癌细胞的荧光强度则明显降
低。由以上结果可知,荧光探针化合物gal-nir-hclo能够很好地检测肝癌细胞中内源性的次氯酸。
[0061]
实施例8
[0062]
荧光探针化合物gal-nir-hclo对肝脏组织切片中次氯酸的荧光成像
[0063]
在本实验中,采用小鼠肝脏组织作为成像目标。将小鼠肝脏组织制成切片后,用20μm 探针溶液孵育半小时,随后向其中加入naclo(100μm),继续培养30min。用杜氏磷酸盐缓冲液将制好的组织切片清洗三次,然后将其放到共聚焦显微镜下进行深度扫描成像。测试条件设定为激发波长为635nm,发射波长波段设定为680-750nm。结果如图8所示,肝脏组织发出了明显的荧光信号,其穿透深度可达108μm。由此可知,荧光探针化合物 gal-nir-hclo能够实现小鼠肝脏组织中外源性次氯酸的成像,且具有较好的成像深度。
[0064]
以上实施例描述了本发明的基本原理、主要特征及优点,本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明原理的范围下,本发明还会有各种变化和改进,这些变化和改进均落入本发明保护的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1