含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物及其制备方法和应用
1.本发明属于化学合成和药物应用领域,具体涉及一种含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物及其制备方法和应用。
背景技术:
2.化学农药是现代农业生产过程中不可缺少的元素,其具有适用范围广、防治对象多、生产成本低、防治效果高、经济效益高的特点,在病、虫、草害的防治上效果显著。高效、低毒、低残留是农药产业的发展方向,杂环类有机农药为近年来发展最为迅速的一类农药。1,2,4-噁二唑类杂环化合物不仅具有广泛的生物活性,如杀菌、杀虫、抗植物病毒、除草等活性,还具有选择性好、活性高、毒性低等特点,现正逐渐成为农药的一个重要类别。因此1,2,4-噁二唑类化合物的分子设计、合成与生物活性研究仍然是当今绿色农药创制的一个热点。
技术实现要素:
3.本发明的目的在于提供一种含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物及其制备方法和应用。
4.为达到上述目的,提出以下技术方案:
5.含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物,结构式如式(11)所示:
[0006][0007]
式(11)中,苯环上的h被取代基r单取代、多取代或不取代,单取代或多取代的取代基r各自独立地选自烷基、氟取代烷基或卤素。
[0008]
优选地,取代基r各自独立为甲基、三氟甲基、f、cl、br或i。
[0009]
进一步地,式(11)中的r为2-甲基、3-甲基、4-甲基、4-叔丁基、3-三氟甲基、2-氟、3-氟、4-氟、4-氯、4-溴、4-碘、2,4-二甲基、2,6-二甲基、3-氯-2-甲基、3,4-二氯或2,4-二氟。
[0010]
一种含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物的制备方法,包括如下步骤:
[0011]
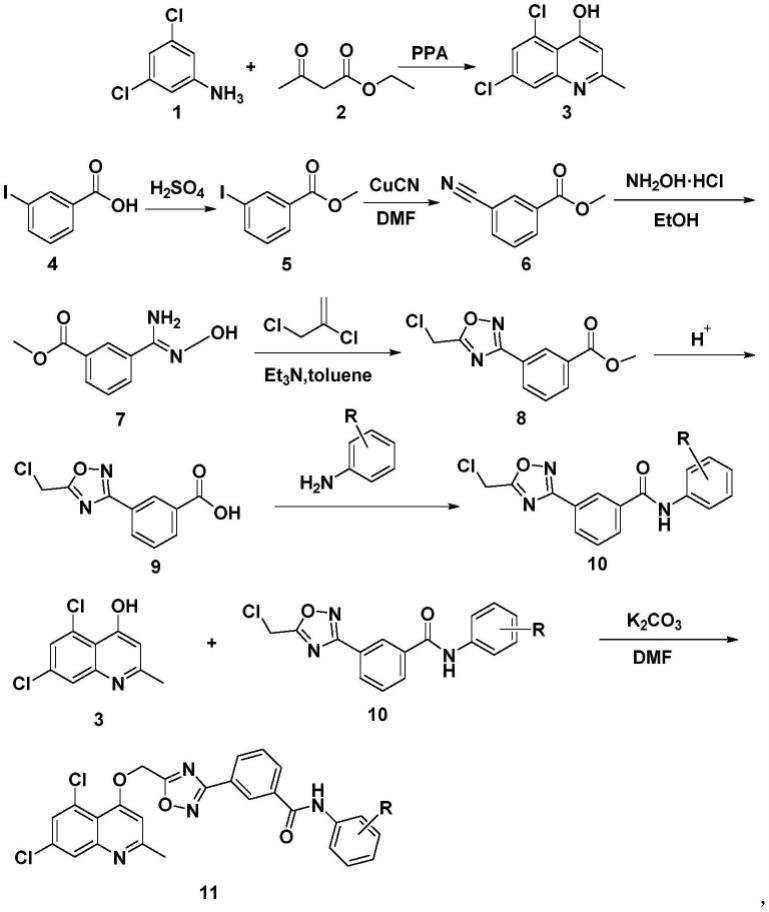
1)将式(1)所示的3,5-二氯苯胺和式(2)所示的乙酰乙酸乙酯溶解于多聚磷酸中,在其催化作用下,加热,一步关环成式(3)所示的中间体3;
[0012]
2)将式(4)所示的3-碘苯甲酸溶解于甲醇中,加入浓硫酸作为催化剂进行酯化反应,生成式(5)所示的3-碘苯甲酸甲酯;
[0013]
3)以dmf为溶剂,将式(5)所示的3-碘苯甲酸甲酯和氰化亚铜在l-脯氨酸的催化下
进行反应,生成式(6)所示的3-氰基苯甲酸甲酯;
[0014]
4)将步骤3)所得的3-氰基苯甲酸甲酯溶解于无水乙醇,在缚酸剂三乙胺的存在下与盐酸羟胺反应,得式(7)所示的3-(n'-羟基氨基甲酰氨基)苯甲酸甲酯;
[0015]
5)将步骤4)所得的化合物7溶解于无水甲苯和三乙胺,加入氯乙酰氯反应,生成式(8)所示的3-(5-(氯甲基)-1,2,4-噁二唑-3-基)苯甲酸甲酯;
[0016]
6)将步骤5)所得的化合物8在酸性条件下水解,生成式(9)所示的化合物9,化合物9再与取代苯胺进行缩合反应,得如(10)所示的中间体10;
[0017]
7)将步骤1)所得的中间体3和步骤6)所得的中间体10在k2co3催化下进行醚化反应,得如(11)所示的含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物;
[0018]
其反应过程如下:
[0019][0020]
苯环上的h被取代基r单取代、多取代或不取代,单取代或多取代的取代基r各自独立地选自烷基、氟取代烷基或卤素。
[0021]
进一步地,步骤3)中,3-碘苯甲酸甲酯和氰化亚铜的摩尔比为1:1.4~1.6,优选为1:1.5。
[0022]
进一步地,步骤3)中,反应分两个阶段进行,先在70~80℃下搅拌1~3h,再升温至100℃反应6~8h。
[0023]
进一步地,步骤4)中,3-氰基苯甲酸甲酯与盐酸羟胺的摩尔比为1:1.4~1.6,优选为1:1.5。
[0024]
进一步地,步骤5)中,3-(n'-羟基氨基甲酰氨基)苯甲酸甲酯、三乙胺和无水甲苯在0℃条件下搅拌2~3h后,滴加氯乙酰氯,-2~2℃下继续搅拌反应3~4h,然后升温至回流
反应。
[0025]
进一步地,步骤6)中,化合物9和二氯亚砜加热搅拌回流反应3~4h,旋蒸脱除二氯亚砜,然后加入thf,冰浴条件下滴加取代苯胺、三乙胺和thf的混合溶液,搅拌过夜。
[0026]
一种含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物在制备杀菌剂中的应用。
[0027]
本发明的有益效果在于:
[0028]
本发明的制备方法简单、操作方便,对所得的17个目标产物进行了杀菌活性测试,结果表明:在50ppm浓度下,所得产物对油菜菌核病菌具有不错的防治效果。
具体实施方式
[0029]
下面结合具体实施例对本发明作进一步说明,但本发明的保护范围并不限于此。
[0030]
反应过程如下:
[0031][0032]
苯环上的h不被取代或被取代基r独立取代为2-甲基、3-甲基、4-甲基、4-叔丁基、3-三氟甲基、2-氟、3-氟、4-氟、4-氯、4-溴、4-碘、2,4-二甲基、2,6-二甲基、3-氯-2-甲基、3,4-二氯或2,4-二氟。
[0033]
实施例1式(3)所示的5,7-二氯-2-甲基-4-羟基喹啉的制备:
[0034]
在250ml三口烧瓶中加入14.31g(0.11mol)乙酰乙酸乙酯和50.69g多聚磷酸(ppa),升温至90℃保持0.5h,搅拌下缓慢加入16.20g(0.10mol)3,5-二氯苯胺,继续升温至150℃反应5h,tlc监测反应结束。待反应液冷却至室温,加入100ml水搅拌析出灰色固体,抽滤,依次用石油醚和饱和碳酸氢钠水溶液洗涤,烘干得产物20.39g,收率89.4%。
[0035]
实施例2式(5)所示的3-碘苯甲酸甲酯的制备:
[0036]
在100ml三口烧瓶中加入3-碘苯甲酸2.53g(0.01mol)、50ml甲醇,滴加0.50ml浓硫酸,升温至回流反应,tlc跟踪监测反应进程,约8h结束。待反应液冷却至室温,旋蒸脱溶,加入50ml乙酸乙酯,用饱和碳酸钠水溶液调节体系ph值至7~8,分液取有机相,用无水硫酸钠干燥脱溶得2.39g米白色固体,收率90.4%。
[0037]
实施例3式(6)所示的3-氰基苯甲酸甲酯的制备:
[0038]
在100ml的三口烧瓶中加入通过实施例2制备得到的3-碘苯甲酸甲酯0.34g(1.30mmol)、氰化亚铜0.18g(2.00mmol)、l-脯氨酸0.15g(1.30mmol)和15ml dmf,待溶解后,升温至75℃,反应2h,继续升温至100℃反应,tlc跟踪监测反应,约6h结束。待反应液冷却至室温,用硅藻土抽滤除去滤渣,滤液加入100ml水和100ml乙酸乙酯萃取,有机相水洗(50ml
×
3),然后用无水硫酸镁干燥,旋蒸脱除乙酸乙酯,得0.17g黄色固体,收率81.9%。
[0039]
实施例4式(7)所示的化合物7的制备:
[0040]
在100ml三口烧瓶中加入通过实施例3制备得到的3-氰基苯甲酸甲酯1.16g(7.20mmol),45ml无水乙醇,在室温下,开启机械搅拌,随后缓慢加入盐酸羟胺0.75g(10.79mmol)、三乙胺1.10g(10.87mmol)开始反应,tlc跟踪监测反应进程,约3h结束,旋蒸脱溶,并将残余物溶于50ml乙酸乙酯和50ml饱和氯化钠水溶液中,分液取有机层,加入无水硫酸钠干燥,旋蒸脱溶得到淡黄色固体1.26g,收率90.2%。
[0041]
实施例5式(8)所示的化合物8的制备:
[0042]
在250ml三口烧瓶中加入通过实施例4制备得到的化合物70.97g(5.00mmol),三乙胺1.20g(12.00mmol),100ml无水甲苯,控温0℃,搅拌2h后,逐滴加入0.58g(5.20mmol)氯乙酰氯,0℃下继续搅拌反应3h,然后升温至115℃进行回流反应,tlc监测反应进程,约2h结束。待反应液冷却至室温,用150ml蒸馏水进行水洗,然后用饱和氯化钠水溶液洗涤,有机相加入无水硫酸钠干燥,旋蒸脱溶,烘干得到产物0.93g,收率73.8%。
[0043]
实施例6式(9)所示的化合物9的制备:
[0044]
在250ml的三口烧瓶中依次加入通过实施例5制备得到的5.00g(0.02mol)化合物8,30ml乙酸,30ml盐酸,升温至70℃反应3h,tlc监测反应结束。待反应液冷却至室温,析出大量白色固体,抽滤,水洗烘干得产物4.45g,收率93.6%,m.p.179~182℃;
[0045]1h nmr(400mhz,dmso-d6)δ:13.34(s,1h),8.53(s,1h),8.23(d,j=8.8hz,1h),8.14(d,j=7.8hz,1h),7.71(t,j=7.8hz,1h),5.19(s,2h).
[0046]
实施例7式(10)所示的中间体10a~10q的制备:
[0047]
在17个50ml的三口烧瓶中分别依次加入通过实施例6制备得到的0.24g(1.00mmol)3-(5-(氯甲基)-1,2,4-噁二唑-3-基)苯甲酸(化合物9),5ml二氯亚砜,加热搅拌回流反应3h,旋蒸脱除二氯亚砜,加入30ml thf,冰浴条件下逐滴加入混合溶液,对应的
混合溶液的成分为1.20mmol取代苯胺(苯环上的h不被取代或被取代基r独立取代为2-甲基、3-甲基、4-甲基、4-叔丁基、3-三氟甲基、2-氟、3-氟、4-氟、4-氯、4-溴、4-碘、2,4-二甲基、2,6-二甲基、3-氯-2-甲基、3,4-二氯或2,4-二氟),2.50mmol三乙胺,1ml thf,搅拌过夜经柱层析分离纯化分别得中间体10a~10q。具体数据见表1和表2。
[0048]
表1中间体化合物10a~10q理化数据
[0049]
目标化合物取代基团r外观收率%10ah黄色固体79.410b2-甲基黄色固体77.510c3-甲基白色固体69.710d4-甲基白色固体73.810e4-叔丁基白色固体75.710f3-三氟甲基黄色固体66.410g2-氟黄色固体75.910h3-氟黄色固体78.610i4-氟黄色固体67.110j4-氯黄色固体79.310k4-溴黄色固体73.410l4-碘黄色固体68.810m2,4-二甲基白色固体69.510n2,6-二甲基白色固体74.410o3-氯-2-甲基白色固体63.710p3,4-二氯黄色固体64.910q2,4-二氟黄色固体63.7
[0050]
表2中间体化合物10a~10q 1
h nmr、
13
c nmr和hrms数据
[0051]
[0052]
[0053]
[0054][0055]
实施例8目标产物11a~11q的制备:
[0056]
在17个100ml的单口烧瓶中对应各自加入(1.00mmol)通过实施例7制备得到的不同的中间体10(苯环上的h不被取代或被取代基r独立取代为2-甲基、3-甲基、4-甲基、4-叔丁基、3-三氟甲基、2-氟、3-氟、4-氟、4-氯、4-溴、4-碘、2,4-二甲基、2,6-二甲基、3-氯-2-甲基、3,4-二氯或2,4-二氟),然后加入(1.00mmol)中通过实施例1制备得到的5,7-二氯-2-甲基-4-羟基喹啉,0.35gk2co310 ml dmf,升温至60℃反应5h,tlc监测反应结束。待反应液冷却至室温,将其倒入100ml水中,并用乙酸乙酯萃取,无水硫酸镁干燥脱溶得粗产物,经快速柱层析分离纯化得目标化合物11a~11q。具体数据见表3和表4。
[0057]
表3含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物理化数据
[0058][0059]
[0060]
表4含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物1h nmr、
13
c nmr和hrms数据
[0061]
[0062]
[0063]
[0064][0065]
实施例9杀菌活性测试
[0066]
1测试样品:
[0067]
试验对象:番茄早疫病菌(alternaria solani)、小麦赤霉病菌(gibberella zeae)、水稻稻瘟病菌(pyricularia oryae)、辣椒疫霉病菌(phytophthora capsici)、油菜菌核病菌(sclerotinia sclerotiorum)、黄瓜灰霉病菌(botrytis cinerea)、水稻纹枯病菌(riziocotinia solani)、黄瓜枯萎病菌(fusarium oxysporum)、花生褐斑病菌(cercospora arachidicola)以及苹果轮纹病菌(physalospora piricola)。
[0068]
2试验处理:式11a~11q化合物分别用dmso溶解制成1%ec母液备用。试验采用采用抑菌圈法,评价供试化合物在50ppm的剂量下对10种试验靶标的室内杀菌活性,活性测试结果如表5所示;
[0069]
表5含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物杀菌活性
[0070]
[0071][0072]
含喹啉环1,2,4-噁二唑取代苯甲酰胺类化合物(17个)杀菌活性结果表明(表3),在50ppm测试浓度下,目标化合物11a~11q对10种供试菌种均显示出一定的抑制活性。对油菜菌核病,大部分化合物具有不错的抑制活性,如化合物11f、11i和11k抑制率达58.3%、63.9%和61.1%,化合物11a、11j、11n、11o及11q也有中等的抑制活性(50.0%~55.6%),但皆低于苯氧喹啉(77.8%)。对于花生褐斑病,化合物11a、11i及11j的抑制率为46.7%、53.3%和60.0%,优于苯氧喹啉(33.3%)。对于小麦赤霉病,化合物11i的抑制率为54.8%,优于苯氧喹啉(45.2%)。对番茄早疫病和辣椒疫霉病,部分化合物药效优于苯氧喹啉,但抑制率均低于50%,效果一般。
[0073]
本说明书所述的内容仅仅是对发明构思实现形式的列举,本发明的保护范围不应当被视为仅限于实施例所陈述的具体形式,本发明的保护范围也仅仅于本领域技术人员根据本发明构思所能够想到的等同技术手段。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1