猴痘病毒特异性检测靶标及其寡核苷酸和试剂盒的制作方法
1.本发明属于生命科学和生物技术领域,特别涉及一种猴痘病毒的特异性检测靶标、一种用于检测猴痘病毒的寡核苷酸、方法和试剂盒,采用荧光pcr技术,用于检测临床样本中的猴痘病毒核酸。
背景技术:
2.猴痘病毒(monkeypox virus)与人类历史上曾肆虐数千年的天花病毒是“近亲”。猴痘病毒于1958年被首次发现,当时一组用于研究的猴子中出现“痘状”传染病,因此得名。自世界卫生组织1980年宣布人类彻底消灭天花以来,猴痘病毒已成为对公共卫生影响最大的正痘病毒。自2022年5月13日以来,全球之前未流行猴痘病毒的国家报告了92例确诊病例和28例疑似病例,未来有可能在这些国家及其他国家发现更多病例。目前,猴痘的确诊和疑似病例主要来自英国、西班牙和葡萄牙,其余分布在澳大利亚、比利时、加拿大、法国、德国、意大利、荷兰、瑞典和美国。
3.猴痘病毒属于痘病毒科、正痘病毒属。痘病毒是所有动物病毒中构造最大且最复杂的一群病毒,种类较多,都是结构较为复杂的dna病毒。痘病毒依血清反应及形成方式分为六个亚属,正痘病毒属是痘病毒的第一亚属。在正痘病毒属家族中只有天花病毒、牛痘病毒、痘苗病毒和猴痘病毒四种可以引起人类感染,它们都含有可溶性的抗原、核蛋白抗原和红细胞凝集素,抗原性质基本相同,彼此之间有交叉免疫性。
4.猴痘病毒的形态与正痘病毒一致,外形为圆角砖形或卵圆形,大小200
‑‑
300nnl。外周是30nm的外膜,环绕匀质的核心体。猴痘病毒的基因组是双链dna,长约197kb,基因组末端包含一个相同但方向相反的6379bp末端反向重复序列。该病毒含190个开放阅读框(≥60个氨基酸),其中4个位于末端反向重复序列中。基因组的gc含量很低,约含33%,基因组可编码病毒复制时所需的多种酶类,故病毒可独立进行复制。
5.由猴痘病毒引起的猴痘是一种罕见的人畜共患病。人类猴痘流行有一些特征,主要发生于非洲,多见于热带雨林、居民稀少的地区。全年散发,6-8月份为发病高峰期,与降雨量大与人群户外活动增加有关。此外,猴痘流行的最重要的一个特征是人与入之间的传播十分罕见。
6.该病主要通过动物传播,人类可以因为被感染动物的咬伤或者直接接触感染动物的血液、体液和皮疹而感染猴痘。此外该病毒也可通过人与人传播,主要是通过长期的、直接的面对面接触时的呼吸道飞沫传播;另外,猴痘还可以通过直接接触猴痘病人的体液或者被污染的物品而传播。所有年龄组都可能感染此病,但没有预防接种的儿童死亡的危险性很高,大概有10%的病死率。
7.目前实验室诊断猴痘病毒的方法分为三类,第一类是培养分离的方法,通过细胞培养,然后分离出猴痘病毒;第二类是电镜检查,检测待检样本中是否有与正痘病毒形态一致的病毒存在;第三类是分子诊断的方法,采用荧光pcr方法特异性检测待检样本中的猴痘病毒核酸。然而,培养分离法虽然结果准确,但检测周期太长,容易出现假阴性结果,而且由
于进行活病毒操作,对实验室生物安全要求极高;电镜检查方法灵敏度不高,样本准备复杂周期长,而且电镜昂贵且操作及其复杂,不适合大范围推广;分子诊断法灵敏度高,特异性强,采用分子检测手段确定病毒是否存在具有很大优势。然而,目前市面上检测猴痘病毒的核酸产品仍然比较少,而且鉴于当前在一些国家传播的猴痘病毒毒株与之前主要在非洲传播的猴痘病毒毒株存在一些分子上的差别,仅根据早前在非洲传播的猴痘病毒毒株开发分子检测产品有可能出现漏检。此外,鉴于正痘病毒属的不同病毒成员存在较高的亲缘关系,现有的一些分子产品有可能出现交叉反应的现象。
技术实现要素:
8.本发明提供一种用于检测猴痘病毒的方法、寡核苷酸和试剂盒,选择了猴痘病毒基因组中的保守性dna片段(比如f3l基因中的保守性区域)设计第一引物对和第一探针,同时引入针对人体内参基因(比如人rnasep)的第二引物对和第二探针,可以有效地避免检测临床样本时遇到的假阴性。这种针对猴痘病毒的检测体系可以有效避免猴痘病毒漏检的问题。
9.在本发明中,位于每条探针5’端的x1、x2为荧光报告基团,位于每条探针3’端的y1、y2为发出荧光或不发出荧光的淬灭基团。优选地,第一探针的3’端还含有mgb分子。在本发明中,荧光报告基因可选自fam、vic、hex、rox、cy5、cy5.5等其中的一种,淬灭基团可以选择tamra、bhq(bhq1、bhq2或bhq3)、qsy、nfq等其中的一种。
10.本发明中的第一探针和第二探针的荧光报告基因和淬灭基团以诸如“fam-tarma/bhq”或“vic/hex/joe-tamra/bhq”之类的形式给出,
“‑”
左边的表示荧光报告基团,
“‑”
右边的表示淬灭基团。fam-tarma/bhq表示同一条探针的荧光报告基因为fam,淬灭基团可选自tarma或bhq。vic/hex/joe-tamra/bhq表示同一条探针的荧光报告基因可选自vic、hex或joe,淬灭基团可选自tamra或bhq。fam-mgbnfq表示同一条探针的荧光报告基因选自fam,淬灭基团选自nfq,与此同时该探针的3’端还含有mgb分子。vic/hex/joe-mgbnfq表示同一条探针的荧光报告基因选自vic、hex和joe中的一种,淬灭基团选自nfq,与此同时该探针的3’端还含有mgb分子。
11.本发明提供猴痘病毒基因组中的保守性dna片段,所述保守性dna片段的序列为seq id no:7或其互补序列。
12.本发明还提供用于检测猴痘病毒的寡核苷酸,所述寡核苷酸包括用于检测猴痘病毒基因组中保守性dna片段的第一引物对和第一探针。优选地,所述保守性dna片段是猴痘病毒特异性的,也就是该dna片段是猴痘病毒特有的。
13.进一步地,所述寡核苷酸还包括用于检测内参基因的第二引物对和第二探针。
14.进一步地,所述保守性dna片段来自猴痘病毒基因j1l,j2l,j3l,d1l,d2l,d3r,d4l,d5r,d6l,d7l,d8l,d9l,d10l,d11l,d12l,d13l,d14l,d15l,d16l,d17l,d18l,d19l,p1l,p2l,o1l,o2l,c1l,c2l,c3l,c4l,c5l,c6r,c7l,c8l,c9l,c10l,c11l,c12l,c13l,c14l,c15l,c16l,c17l,c18l,c19l,c20l,c21l,c22l,c23r,f1l,f2l,f3l,f4l,f5r,f6r,f7r,f8l,f9r,f10l,q1l,q2l,i1l,i2l,i3l,i4l,i5l,i6l,i7l,i8r,g1l,g2l,g3r,g4l,g5r,g6r,g7r,g8l,g9r,g10r,m1r,m2r,m3l,m4r,m5r,l1r,l2r,l3r,l4r,l5l,l6r,h1l,h2r,h3l,h4l,h5r,h6r,h7r,e1r,e2l,e3r,e4r,e5r,e6r,e7r,e8l,e9r,e10r,e11l,e12l,e13l,a1l,a2l,a3l,
a4l,a5l,a6r,a7l,a8l,a9r,a10l,a11l,a12r,a13l,a14l,a15l,a16l,a17l,a18l,a19r,a20l,a21l,a22r,a23r,a24r,a25r,a26l,a27l,a28l,a29l,a30l,a31l,a32l,a33r,a34l,a35r,a36r,a37r,a38r,a39r,a40l,a41l,a42r,a43r,a44r,a45l,a46r,a47r,a48r,a49r,a50r,a51r,b1r,b2r,b3r,b4r,b5r,b6r,b7r,b8r,b9r,b10r,b11r,b12r,b13r,b14r,b15l,b16r,b17r,b18r,b19r,b20r,b21r,k1r,r1r,n1r,n2r,n3r,n4r,j1r,j2r和j3r中特异性的保守性dna片段。根据这些特异性的保守性dna片段,可以设计出针对每个基因的引物和探针。
15.进一步地,所述保守性dna片段来自f3l基因。
16.进一步地,所述保守性dna片段的序列为seq id no:7或其互补序列。
17.进一步地,所述第一引物对和第一探针的碱基序列分别为seq id no:1~3。
18.进一步地,所述第二引物对和第二探针的碱基序列分别为seq id no:4~6。
19.进一步地,第一探针的荧光报告基团和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq、fam-mgbnfq和vic/hex/joe-mgbnfq中的任何一种,第二探针的荧光报告基因和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq中的任何一种。
20.本发明还提供一种检测猴痘病毒的方法,所述方法包括:(1)提取样品中的核酸;(2)利用一组引物和探针确定样本中是否存在猴痘病毒,其中,所述一组引物和探针包括第一引物对和第一探针,其碱基序列为seq id no:1~3。
21.进一步地,所述一组引物和探针还包括第二引物对和第二探针,其碱基序列为seq id no:4~6。
22.本发明还提供一种用于检测猴痘病毒的试剂盒,所述试剂盒包括荧光pcr反应液,所述荧光pcr反应液包括寡核苷酸,所述寡核苷酸至少包括用于检测猴痘病毒基因组中保守性dna片段的第一引物对和第一探针。
23.进一步地,所述寡核苷酸还包括用于检测内参基因的第二引物对和第二探针。
24.进一步地,所述保守性dna片段来自f3l基因。
25.进一步地,所述保守性dna片段的序列为seq id no:7或其互补序列。
26.进一步地,所述第一引物对和第一探针的碱基序列分别为seq id no:1~3。
27.进一步地,所述第二引物对和第二探针的碱基序列分别为seq id no:4~6。
28.进一步地,第一探针的荧光报告基团和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq、fam-mgbnfq和vic/hex/joe-mgbnfq中的任何一种,第二探针的荧光报告基因和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq中的任何一种。
29.进一步地,每条引物和探针的浓度范围为75~300nm。
30.进一步地,所述荧光pcr反应液还包括10~50mm tris(ph 8.0~9.2)、10~50mm kcl、10~20mm硫酸铵、0.01%~0.1%tween 20、0.2~2mg/ml bsa、0.1~0.3mm datp、0.1~0.3mm dttp、0.1~0.3mm dctp、0.1~0.3mm dgtp、0.1~0.3mm dutp和3~6mm氯化镁。
31.所述试剂盒还包括酶混合液,所述酶混合液包括1.5~3u taq dna聚合酶,0.5~3u taq抗体,0.1~2u ts-ung酶。
32.进一步地,所述试剂盒还包括核酸提取试剂,所述核酸提取试剂包括核酸提取液1、核酸提取液2和核酸提取液3,其中,所述核酸提取液1包括10~1000mm tris-edta,5~8m盐酸胍、1%~10%tritonx-100,ph 4~7,直径在80~800nm之间的具有超顺磁性核心和氧
化硅外壳的顺磁性氧化硅纳米磁珠,所述核酸提取液2包括10~1000mm tris-edta,40%~60%无水乙醇,核酸提取液3包括10mm tris-edta ph 8~9。
33.进一步地,所述试剂盒还包括阳性质控和阴性质控,所述阳性质控为猴痘病毒假病毒,所述阴性质控为0.9%nacl溶液。
34.进一步地,所述试剂盒操作流程为:(1)三步法提取样本核酸:第一步取0.5ml样本和0.5ml核酸提取液1,静止10min,磁力架吸附磁珠后弃上清;第二步加400μl核酸提取液2,涡旋混匀后静止5min,磁力架吸附磁珠后吸弃上清;第三步加入100μl核酸提取液3,涡旋混匀后静止5min,磁力架吸附磁珠后,取上清核酸溶液备用;(2)荧光pcr试剂配制:将荧光pcr反应液和酶混合液混匀,分别加入(1)中提取的样本核酸和阴性质控、阳性质控;(3)荧光pcr检测:进行荧光pcr扩增,扩增结束后确定样本中是否存在猴痘病毒。
35.有益效果:(1)本发明选择了猴痘病毒基因组中保守性dna片段(f3l基因)设计引物和探针,同时引入人类基因组管家基因rnasep作为内参基因,从而可以有效地避免临床样本采样失误、核酸提取失误等一系列因素导致的结果异常;(2)本发明可以从复杂样本检测出猴痘病毒,具有灵敏度高、特异性好、检测结果快速客观等优点,为诊断猴痘病毒感染提供可靠的结果。
附图说明
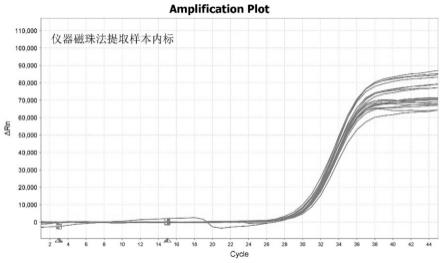
36.图1:作为对照的仪器磁珠法提取的核酸的检测结果。
37.图2:本发明的手工磁珠法提取的核酸的检测结果。
38.图3:本发明对阳性参考品p1的检测结果。
39.图4:本发明对阳性参考品p2的检测结果。
40.图5:本发明对阳性参考品p3的检测结果。
41.图6:本发明对阳性参考品p4的检测结果。
42.图7:本发明对阴性参考品n1-n10的检测结果。
43.图8:500copies/ml时,本发明针对f3l基因检测灵敏度验证结果图。
44.图9:250copies/ml时,本发明针对f3l基因检测灵敏度验证结果图。
45.图10:125copies/ml时,本发明针对f3l基因检测灵敏度验证结果图。
具体实施方式
46.在检测猴痘病毒的方法中,本发明选择采用猴痘病毒中的保守序列来设计引物和探针,同时引入人基因组管家基因rnasep作为内参基因(也称为内标基因),从而可以有效地避免临床样本采样失误、核酸提取失误等一系列因素导致的结果异常,更重要地,这还可以解决猴痘病毒漏检的问题。
47.通过针对之前出现的猴痘病毒毒株和2022年在全球很多国家出现的猴痘病毒毒株以及痘病毒科的其他病毒成员进行大规模的基因组序列比对,本发明发现猴痘病毒基因组中的一个特别保守的dna片段,可作为猴痘病毒的一个特异性的检测靶标,其序列为seq id no:7或其互补序列。根据这个特别保守的dna片段设计引物和探针,可有效提高检测猴痘病毒的特异性,降低交叉反应。与此同时,这也可以避免选择不太保守的基因组dna片段设计引物和探针时可能出现的漏检错检现象。
48.基于此,f3l基因的保守性dna片段(作为检测猴痘病毒的特异性检测靶标),以及设计出的引物、探针的序列如表1所示。
49.表1.引物、探针和保守性dna片段的具体序列
[0050][0051][0052]
表1第一探针和第二探针均为taqman探针,均含有一个荧光报告基团和一个淬灭基团,荧光报告基因可选自fam、vic、hex、rox、cy5、cy5.5等其中的一种,淬灭基团可以选择tamra、bhq、qsy、nfq等其中的一种。优选的荧光报告基团为fam和vic,这是因为这两种荧光报告基团在荧光pcr检测中具有本底荧光低和荧光检测信号高的优点。淬灭基团的选择原则在于淬灭基团的荧光吸收光谱与荧光报告基团的发射光谱存在重叠。表1中的这两条探针的荧光报告基团和淬灭基团优选组合方式为fam-mgbnfq、vic/hex/joe-bhq。优选地,每条探针的荧光报告基团各不相同,这样就可在单管中同时进行两通道检测。优选地,第一探针的3’端还含有mgb分子。
[0053]
优选地,第一探针的荧光报告基团和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq、fam-mgbnfq和vic/hex/joe-mgbnfq中的任何一种,第二探针的荧光报告基因和淬灭基团选自fam-tarma/bhq、vic/hex/joe-tamra/bhq中的任何一种。
[0054]
在进行荧光pcr之前,需要提取临床样本中的核酸(rna),提取核酸的方法有很多种,比如碱裂解法、磁珠法和柱提法。为了便于说明,本发明采用磁珠法提取临床样本中的核酸,所使用的核酸提取试剂包括核酸提取液1、核酸提取液2和核酸提取液3,所述核酸提取液1包括10~1000mm tris-edta,5~8m盐酸胍和1%~10%tritonx-100,ph 4~7,超顺
磁性氧化硅纳米磁珠(磁珠直径在80~800nm之间,具有核壳结构,即超顺磁性核心和氧化硅外壳),所述核酸提取液2包括10~1000mm tris-edta,40%~60%无水乙醇,核酸提取液3包括10mm tris-edta ph 8~9。
[0055]
不过注意的是,虽然这里采用手工磁珠法提取临床样本中的核酸,但是本发明并不局限于这种核酸提取方法,仪器磁珠法和柱提法等方法均可用于本发明的临床样本核酸提取。
[0056]
为了便于说明,在以下实施例中,以用于检测猴痘病毒f3l基因的探针的荧光报告基团和淬灭基团为fam-mgbnfq、用于人基因组管家基因rnasep的探针的荧光报告基团和淬灭基团为vic-bhq1为例进行说明。在本发明的实施例中使用的阳性质控为猴痘病毒假病毒。
[0057]
以下实施例进一步说明本发明。这些实施例不是用来限制本发明范围,而是提供对本发明的进一步理解。
[0058]
实施例1:临床样本核酸的提取
[0059]
为方便说明,本实施例中以正常人口咽拭子及血清作为临床样本,通过对本发明中描述的手工磁珠法进行临床样本核酸提取,并采用仪器磁珠法的提取试剂盒作为对照进行对比说明。
[0060]
取10例正常人口咽拭子及血清,按照本发明的三步法提取样本dna:第一步取0.5ml样本和0.5ml核酸提取液1,静止10min,磁力架吸附磁珠后弃上清;第二步加400μl核酸提取液2,涡旋混匀后静止5min,磁力架吸附磁珠后吸弃上清;第三步加入100μl核酸提取液3,涡旋混匀后静止5min,磁力架吸附磁珠后,取上清核酸溶液备用。
[0061]
本发明中核酸提取方法为手工磁珠法,采用三步法对临床样本分别进行裂解、洗涤及洗脱。采用艾康生物技术(杭州)有限公司生产的核酸提取试剂盒(磁珠法)作为对照在艾康生物技术(杭州)有限公司制造的核酸提纯仪上对同样的临床样本进行核酸提取(即仪器磁珠法),采用本发明的试剂盒检测人基因组管家基因rnasep,对检测到的ct值进行比较,对比结果如表2所示,扩增结果如图1和图2所示。由图1和图2可知,本发明的核酸提取方法(手工磁珠法)与利用仪器磁珠法提取核酸的检测结果基本一致。
[0062]
表2核酸提取方法检测结果对比
[0063][0064]
实施例2:利用荧光pcr方法检测猴痘病毒
[0065]
本实施例中采用试剂盒对猴痘病毒进行荧光pcr检测,试剂盒包括荧光pcr反应液、酶混合液、阳性质控、阴性质控。优选地,这种试剂盒还可包括实施例1中的核酸提取液1、核酸提取液2和核酸提取液3。荧光pcr反应液配制体系见表3。酶混合液配制体系见表4。阳性质控为猴痘病毒假病毒,阴性质控为0.9%nacl溶液。
[0066]
表3.荧光pcr反应液配制体系表(1人份)
[0067][0068]
表4.酶混合液配制体系(1人份)
[0069][0070]
检测临床样本中病原体猴痘病毒时,需将荧光pcr反应液和酶混合液混匀,以及计算所需的样本数n份[n=临床样本数+1管阳性对照+1管阴性对照]。将18μl荧光pcr反应液和2μl酶混合液加入到不同的反应管中,然后分别往不同的反应管中加入5μl实施例1中提取的核酸溶液、5μl阴性对照和5μl阳性对照。
[0071]
将各个反应管按一定顺序放入荧光pcr仪(abi q5)上,按以下程序进行荧光pcr扩
增,扩增程序如表5所示:
[0072]
表5.荧光pcr扩增程序
[0073][0074]
荧光pcr扩增结束后,根据fam通道、vic通道的ct值检测猴痘病毒是否存在,其检测结果判断如表6所示。
[0075]
表6.检测结果cutoff值及结果判读
[0076][0077]
a.猴痘病毒基因检测判读标准:
[0078]
1)阴性:ct值未检出;
[0079]
2)阳性:扩增曲线呈s型,且ct值≤40;
[0080]
3)可疑:扩增曲线呈s型,且40<ct值≤45,需复检;复检结果若一致,判定结果为该基因检测阳性。
[0081]
b.猴痘病毒核酸检测阳性判读标准:
[0082]
靶标基因检测结果为阳性,则判断为猴痘病毒核酸阳性。
[0083]
c.rnasep内参基因vic通道为阴性,说明样本中含有pcr反应抑制物、提取失败或实验过程中漏加样本,建议重新采样、提取及测试。极少数样本可能因采样问题出现猴痘病毒核酸检测结果为阳性,而内参无扩增信号或ct值>40,这种情况阳性结果仍然可信,必要时重新采样复测确认。
[0084]
临床样本常见检测结果如表7所示,其他异常结果需结合临床进行结果解释。
[0085]
表7.临床样本常见结果解释
[0086][0087]
实施例3:临床样本验证
[0088]
猴痘病毒实时pcr检测试剂盒的临床研究使用模拟临床样本进行,这些样本包括病变渗出液拭子、病变结壳、血清或口咽拭子,每种样本类型包括10个阴性样本,10个模拟标本(猴痘病毒假病毒),40个阳性标本和40个阴性标本。用对照试剂盒(monkeypox virus real time pcr kit(shanghai zj bio-tech co.,ltd.))对上述样品进行验证,并对结果进行比较。
[0089]
本发明针对猴痘病毒f3l基因的检测结果分析如表8所示。
[0090]
表8.猴痘病毒核酸检测临床验证结果
[0091][0092]
阳性符合率=[40/(0+40)]
×
100%=100%
[0093]
阴性符合率=[40/(0+40)]
×
100%=100%
[0094]
总符合率=[(40+40)/(40+40)]
×
100%=100%
[0095]
相对灵敏度=100%(95%置信区间:91.19%-100.00%)
[0096]
相对特异性=100%(95%可信区间:91.19%-100%)
[0097]
准确度=100%(95%置信区间:91.19%-100.00%)
[0098]
kappa=1
[0099]
kappa分析判断标准如下:
[0100]
kappa标准=1表示完全一致>0.75表示有很好的一致性
<0.4表示一致性不好=0表示两组结果是机遇造成的
[0101]
临床试验表明,本发明试剂的检测结果与对照结果在一致性分析中的kappa值为1,表明本发明试剂的检测结果与对照结果相关性好。
[0102]
实施例4参考品体系建立及评价
[0103]
本实施例中,针对本发明所述的试剂盒设置如下参考品进行性能评价。
[0104]
阳性参考品设置:选择含有猴痘病毒dna片段的假病毒颗粒浓度在1
×
104copies/ml~1
×
106copies/ml范围内的阳性参考品4份,标记为p1~p4。
[0105]
阴性参考品设置:选择2份牛痘病毒核酸提取物,标记为n1-n2;1份疫苗病毒核酸提取物,标记为n3;1份猴痘病毒阴性样本核酸提取物,标记为n4;
[0106]
按照实施例2种所述的方法对试剂盒中设置的参考品进行阴阳符合率的评价。结果如下所示:
[0107]
阳性参考品p1~p4检测结果为fam、vic通道检测结果均为阳性。如图3~6所示。
[0108]
阴性参考品n1~n4检测结果为fam通道检测结果均为阴性,vic通道检测结果为阳性。如图7所示。
[0109]
实施例5检测灵敏度分析
[0110]
按照实施例2所述的方法分别对含有猴痘病毒dna片段的假病毒颗粒在不同浓度(浓度分别为s1:500copies/ml、s2:250copies/ml、s3:125copies/ml)下重复20次检验,以95%检出率来确认试剂盒的检测下限。检测结果详见表9~11,f3l基因扩增引物探针对500、250copies/ml假病毒颗粒的检出率均为100%,f3l基因扩增引物探针对125copies/ml假病毒颗粒的检出率为75%。综上所述,本发明的试剂盒检测下限为250copies/ml。如图8~10所示。
[0111]
表9.检测限样本s1检测结果统计
[0112]
检测限样本s1f3l基因137.04237.11336.93436.76536.33637.00736.23835.94936.051035.961138.341236.541336.231436.701535.98
1637.431736.281837.431935.872036.93检出率(%)100%
[0113]
表10.检测限样本s2检测结果统计
[0114][0115][0116]
表11.检测限样本s3检测结果统计
[0117][0118][0119]
实施例6反应特异性分析
[0120]
本实施例中,针对本发明所述的试剂盒对其他冠状病毒及呼吸道病原体等交叉样本进行验证。结果详见表13,从结果可以得出,本发明的试剂盒对其他冠状病毒及呼吸道病原体检测无交叉反应,由此可知本发明的试剂盒特异性良好。
[0121]
表12.交叉病原体验证结果
[0122]
[0123]
[0124]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1