一株H9N2亚型禽流感病毒MDCK细胞冷适应减毒活疫苗株及其培育方法和应用
一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株及其培育方法和应用
技术领域
1.本发明涉及兽用药物领域,特别是涉及一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株及其培育方法和应用。
背景技术:
2.禽流感是由禽流感病毒(avian influenza virus,aiv)引起的禽类高发性疾病,以精神沉郁、食欲减退、咳嗽和喷嚏等呼吸道症状为主要临床症状,是一种高发性、烈性和高度接触性的传染性疾病。h9n2禽流感病毒宿主要包括:水禽、野鸟和家禽(如:火鸡、鸡、鸭子等)。低致病性禽流感h9n2感染鸡群一般不会直接导致鸡的死亡,但会导致产蛋率下降以及生长迟缓,给养禽业造成巨大的经济损失。
3.中国h9n2禽流感病毒于1994年在广东省广州市首次被发现。家禽感染h9n2亚型禽流感的临床症状表现为产蛋量下降和一定的死亡率,并且可造成水平传播。因为禽流感病毒变异和重组非常快,及时发现新型毒株,研究其抗原性和免疫原性,筛选出疫苗候选毒株是保证禽流感疫苗效果的最重要方式之一。
4.目前我国h9n2亚型禽流感的防控主要依靠于全病毒灭活疫苗,全病毒灭活疫苗主要刺激机体产生体液免疫,现阶段临床结果表明全病毒灭活疫苗已经不能够很好地保护家禽免受当前h9n2亚型aiv流行毒株的侵扰,而且灭活疫苗存在以下缺点:接种量大、免疫接种次数多、免疫时间短以及接种部位应激大。另外,灭活疫苗的制备主要依赖于鸡胚生产,如果鸡胚供应量不足很容易出现无疫苗可用的情况。现有的数据表明大量的家禽养殖场免疫h9n2禽流感疫苗后仍然爆发h9n2禽流感疫情。禽流感病毒是一种从呼吸系统到全身败血症等多种症状的禽类传染病,全病毒灭活疫苗不能刺激机体产生呼吸道粘膜免疫和细胞免疫,虽然体液免疫具有很高的水平,但是仍然不能保护鸡群免受h9n2禽流感病毒的侵扰。
5.活疫苗在刺激机体产生高水平中和抗体的同时,可以引起细胞免疫,还可以刺激鼻腔黏膜产生分泌型抗体。目前,俄罗斯和美国在冷适应减毒活疫苗方面的研究处于世界领先水平,已培育出a/ann arbor/6/60(h2n2)、b/ann abor/1/66、a/leningard/134/17/57(h2n2)和b/ussr/60/69等减毒基因供体株。2003年6月17日美国食品和药监局批准一种冷适应、减毒、三价活疫苗flumist,这是全球第一支流感减毒活疫苗,随后该疫苗在欧盟和加拿大也被获得批准使用。该疫苗已被证实具有安全性和有效性,具有加强控制流行性流感的潜力,而且在3-16岁儿童也被证实是安全有效的。以上所述表明:活疫苗在预防和控制流感方面具有良好的前景,是一种可选择的候选疫苗株。冷适应减毒活疫苗依赖细胞来繁殖病毒,可以摆脱流感病毒生产依靠鸡胚的这一缺陷,而且冷适应减毒活疫苗免疫机体后产生体液免疫、细胞免疫和粘膜免疫,可以摆脱全病毒灭活疫苗不能刺激机体产生粘膜免疫的缺陷。能够很好地保护禽类免受h9n2禽流感的侵扰,极大地改善当前灭活疫苗免疫之后仍然发病的困境。
技术实现要素:
6.本发明的目的是提供一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株及其培育方法和应用,以解决上述现有技术存在的问题,可以摆脱对鸡胚的依赖,而且可以刺激机体产生体液免疫、细胞免疫和粘膜免疫,从而保护家禽不受h9n2禽流感病毒的侵扰。
7.为实现上述目的,本发明提供了如下方案:
8.本发明提供一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株,所述冷适应减毒疫苗株分类命名为h9n2亚型禽流感病毒a/chicken/qingyuan/141-25-ca/2021,保藏时间为2022年5月22日,保藏单位为中国典型培养物保藏中心,保藏地址为中国.武汉.武汉大学;保藏编号为cctcc no:v202240。
9.本发明还提供所述的一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株的培育方法,包括:以一株h9n2亚型禽流感流行毒株作为亲本毒株,在mdck细胞中梯度降温培育获取h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株。
10.优选的是,所述亲本毒株为h9n2亚型禽流感流行毒株ck141/20。
11.优选的是,所述在mdck细胞中梯度降温培育,包括以下步骤:
12.(1)将单层mdck细胞接种亲本毒株ck141/20,33
±
0.5℃,5%co2恒温培养,收获初始病毒液,将所收获的初始病毒液反复冻融,并选择ha效价高的病毒液进行连续传代10代,病毒能够在33
±
0.5℃进行稳定地传代,收获33
±
0.5℃温度下的病毒液;
13.(2)依次采用30
±
0.5℃、28
±
0.5℃、26
±
0.5℃的培养温度,重复上述(1)的步骤,收获26
±
0.5℃温度下的病毒液;
14.(3)将步骤(2)收获的26
±
0.5℃温度下的病毒液,置于25℃,5%co2恒温培养,再经有限稀释法纯化5-10代,收集好纯化的病毒液,即得所述的h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株。
15.优选的是,在培养病毒过程中,所用的病毒维持液为:以体积比为1:1混合的dmem和dmem/f12培养基为基础培养基,添加终浓度为1.0mg/ml牛血清白蛋白溶液、100units/ml青霉素、0.1mg/ml链霉素、0.5-1.5μg/ml谷氨酰胺溶液和0.5-1.5μg/ml tpck-胰酶。
16.本发明还提供所述的一株h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗株在预防和控制h9n2亚型禽流感的疫苗研究和制备中的应用。
17.优选的是,所述冷适应减毒活疫苗株应用于鸡h9n2亚型禽流感的预防和控制中。
18.本发明公开了以下技术效果:
19.(1)本发明采用mdck细胞培育h9n2亚型禽流感病毒冷适应减毒活疫苗,此方法和传统培育禽流感疫苗有很大的区别,适用于培育禽流感疫苗和流感大流行疫苗。此方法和传统方法培养禽流感疫苗相比有以下优点:
①
可以摆脱传统方法过度依赖鸡胚的情况,能够及时提供大规模的疫苗;
②
成本低廉,且生产的疫苗无外源因子的污染;
③
不会因为鸡胚带有的外源病毒,从而造成的外源病毒的传播;
④
避免鸡胚传代过程中的抗原变异,保障流行疫苗的时效性和保护效率;
⑤
有标准化疫苗的生产过程,适用于禽流感大流行时禽流感疫苗的生产;
⑥
此方法生产的疫苗能够刺激机体产生体液免疫、细胞免疫和粘膜免疫,抵御h9n2禽流感的侵扰。
20.(2)本发明培育的h9n2亚型禽流感病毒mdck细胞冷适应减毒活疫苗可以作为禽流感大流行时疫苗的骨架,利用反向遗传技术,以“6+2”模式,以当前大流行毒株的ha和na基
因作为冷适应减毒活疫苗的ha和na,和本发明培育的冷适应减毒活疫苗的六个内部基因,拯救得到大流行冷适应重组减毒活疫苗株。获得mdck细胞冷适应减毒禽流感病毒疫苗毒种,极大促进了以mdck细胞为介质的大流行禽流感减毒活疫苗的开发与应用。
附图说明
21.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
22.图1为ck141/20在33℃连续降温传代血凝效价图;
23.图2为ck141/20在30℃连续降温传代血凝效价图;
24.图3为ck141/20在28℃连续降温传代血凝效价图;
25.图4为ck141/20在26℃连续降温传代血凝效价图;
26.图5为ck141/20在25℃连续降温传代血凝效价图;
27.图6为冷适应减毒活疫苗ck141-25-ca/21冷适应性鉴定的结果;
28.图7为冷适应减毒活疫苗ck141-25-ca/21温度敏感性鉴定的结果;
29.图8为冷适应减毒活疫苗ck141-25-ca/21血清hi抗体检测结果;
30.图9为冷适应减毒活疫苗ck141-25-ca/21淋巴细胞增殖结果;
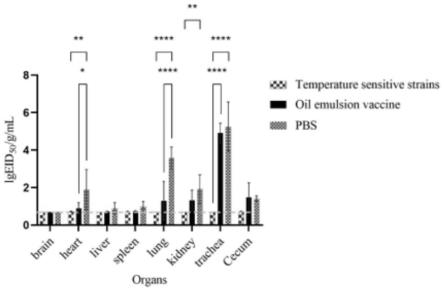
31.图10为攻毒后冷适应减毒活疫苗ck141-25-ca/21在不同脏器的病毒滴度。
具体实施方式
32.现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
33.应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
34.除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。
35.在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见的。本技术说明书和实施例仅是示例性的。
36.关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
37.实施例1
38.一种h9n2亚型禽流感冷适应减毒活疫苗的培育方法,包括如下步骤:
39.a、将h9n2亚型禽流感病毒在无菌磷酸盐缓冲液(pbs)与抗生素混合溶液中进行倍
比稀释,稀释至10-5
,将稀释的病毒液接种到9-11日龄的spf鸡胚中,此步骤用于扩增亲本毒株a/chicken/qingyuan/141/2021(简写为ck141/20,华南农业大学兽医学院禽病教研室提供)。
40.b、将培育18h后的致密单层的t-25培养瓶的mdck细胞,接种步骤a的亲本毒株ck141/20。病毒维持液成分为:dmem和dmem/f12(体积比1:1)为基础培养基,体积分数1%牛血清白蛋白溶液(终浓度为1.0mg/ml),体积分数1%双抗(青霉素终浓度为100units/ml,链霉素终浓度为0.1mg/ml),体积分数2%谷氨酰胺溶液(初始浓度为200mm),tpck-胰酶(终浓度0.5-1.5μg/ml),在33
±
0.5℃,5%co2恒温培养箱中培养72h,收获病毒液。
41.c、每隔6h观察细胞病变情况,待细胞病变达到70%-80%时或培养72h后,将细胞瓶置于-80℃反复冻融2-3次,收获病毒做好标记保存于-80℃备用。用0.5%的火鸡红细胞测定其ha效价,选择ha效价高的病毒液进行培育。
42.d、重复步骤b和c,连续传代10代,病毒能够在33
±
0.5℃进行稳定地传代,收获病毒液。
43.e、将培育18h后的致密单层的t-25培养瓶的mdck细胞,接种步骤d收获的病毒液。病毒维持液的成分与步骤b中一致,在30
±
0.5℃,5%co2恒温培养箱中培养72h,收获病毒液。
44.f、重复步骤e和c,连续传代10代,病毒能够在30
±
0.5℃进行稳定地传代,收获病毒液。
45.g、将培育18h后的致密单层的t-25培养瓶的mdck细胞,接种步骤f收获的病毒液。病毒维持液的成分与步骤b中一致,在28
±
0.5℃,5%co2恒温培养箱中培养72h,收获病毒液。
46.h、重复步骤g和c,连续传代10代,病毒能够在28
±
0.5℃进行稳定地传代,收获病毒液。
47.i、将培育18h后的致密单层的t-25培养瓶的mdck细胞,接种步骤h收获的病毒液。病毒维持液的成分与步骤b中一致,在26
±
0.5℃,5%co2恒温培养箱中培养72h,收获病毒液。
48.j、重复步骤i和c,连续传代10代,病毒能够在26
±
0.5℃进行稳定地传代,收获病毒液。
49.k、将培育18h后的致密单层的t-25培养瓶的mdck细胞,接种步骤j收获的26
±
0.5℃温度的病毒液。在25℃,5%co2恒温培养箱中培养72h,收获病毒液。对病毒进行有限稀释法纯化5-10代,收集好纯化的病毒,新毒株命名为a/chicken/qingyuan/141-25-ca/2021(简写ck141-25-ca/21),保存于-80℃备用。
50.l、本发明培育的ck141-25-ca/21在不同培育温度的相关实验数据见图1、图2、图3、图4和图5,表明本发明培育的冷适应减毒活疫苗能够在不同的温度条件下稳定传代,最终在25℃下适应环境能够进行稳定复制。
51.实施例2
52.本发明培育的冷适应减毒活疫苗ck141-25-ca/21符合人源商品化流感冷适应减毒活疫苗的特性,具有冷适应性、温度敏感特性和减毒特性,具体操作流程如下:
53.a、冷适应性的测定:将冷适应毒株和亲本毒株用病毒维持液进行10倍稀释,用于
冷适应性的测定。将冷适应毒株和亲本毒株分别按10-1
、10-2
…
10-11
、10-12
倍比稀释,100μl/孔接种到96孔板中,每个稀释度设8个平行,同时设置未接种病毒的对照组。
54.b、将接种病毒的细胞分别在33℃和25℃,5%co2的恒温培养箱培养,连续观察3天。病毒滴度以50%终点表示,并根据reed-muench方法计算半数组织培养感染剂量(median tissue culture infective dose,tcid
50
)。冷适应性是指培育的毒株在25℃低温下复制滴度与33℃下复制滴度相差在100倍以内。冷适应性测定的相关实验数据如图6所示,结果显示冷适应减毒活疫苗ck141-25-ca/21具有冷适应性。
55.c、温度敏感特性的测定:如果病毒在温度41℃下的复制滴度与在温度33℃下复制滴度相差100倍以上,那么就可以认为该病毒具有温度敏感特征。tcid
50
操作的具体流程见a,计算得到41℃和33℃的tcid
50
,得出新毒株是否符合温度敏感特性。温度敏感特性的相关实验数据如图7所示,结果显示冷适应减毒活疫苗ck141-25-ca/21具有温度敏感特性。
56.d、减毒特性的测定:对16只4周龄的spf鸡随机平均分成两组,分别为a1和a2组。经鼻孔接种1.0
×
106eid
50
(50%egg infectious dose,eid
50
)的病毒,a1组接种冷适应减毒活疫苗ck141-25-ca/21作为实验组,a2组接种亲本毒株ck141/20作为阴性对照组。每日观察并记录鸡的采食、饮水、精神状况、是否发病或死亡等,持续观察21d。每组在第3天宰杀3只鸡,检测其气管和肺脏组织的病毒滴度。表1是相关实验数据,结果显示冷适应减毒活疫苗ck141-25-ca/21具有减毒特性。
57.表1 ck141-25-ca/21的spf鸡实验结果
[0058][0059]
注:血凝实验的病毒检测下限为0.699log
10
eid
50
/g/ml,每个样品做三个重复,病毒滴度表示为平均滴度
±
标准差。
[0060]
综上所述:本发明培育的冷适应减毒活疫苗ck141-25-ca/21具有冷适应性、温度敏感特性和减毒特性。
[0061]
实施例3
[0062]
本发明培育的冷适应减毒活疫苗ck141-25-ca/21能够在鸡胚上稳定传代,且血凝效价高于mdck上传代的病毒血凝效价。具体实验步骤如下:
[0063]
a、将培育的冷适应减毒活疫苗ck141-25-ca/21,分别稀释至10-3-10-5
,分别接种9-11日龄的鸡胚,于25
±
0.5℃恒温培养箱培育72h后,在4℃放置4-8h后收获病毒液。
[0064]
b、将步骤a收获的病毒液稀释,重复步骤a的操作,进行连续传代,病毒液的血凝效价能够稳定在1:216-512。
[0065]
实施例4
[0066]
亲本毒株ck141/20和冷适应毒株ck141-25-ca/21的氨基酸变异情况
[0067]
a、按照飞捷试剂盒提取亲本毒株及冷适应毒株的病毒rna,再进行反转引物12bp(5’agcaaaagcagg3’)进行反转录。pcr体系(50μl)如表2所示,将体系混匀,再使用掌上离心机离心,在42℃水浴1-2h,获得cdna。将cdna保持于-20℃备用。
[0068]
表2
[0069][0070][0071]
b、获得cdna后,以cdna为模板,使用以下引物对(表3)及rtaq dna聚合酶扩增病毒的8个片段ha、na、ns、m、np、pa、pb1和pb2(冷适应毒株核苷酸序列分别如seq id no1-8所示),pcr体系如表4所示。反应条件为:95℃预变性5min,95℃变性30s,53℃退火30s,72℃延伸2min30s(1000bp/min),共35个循环,72℃延伸7min,12℃保存。
[0072]
表3
[0073][0074][0075]
表4
[0076][0077]
c、pcr扩增后,以1%琼脂糖凝胶电泳鉴定,阳性片段切胶,使用agarose gel dnapurification kit回收。
[0078]
d、将回收的目的基因dna与pmd19-t克隆载体相连,再转化至dh5α感受态细胞,在无抗lb液体培养基中孵育1h,然后均匀涂布在预热至37℃的amp
+
(氨苄青霉素)琼脂平板上培养18-20h。
[0079]
e、用10μl的枪头挑取阳性单个菌落,将带有阳性单个菌落枪头放入到500μl amp
+
抗性lb液体培养基的ep管中,于37℃,200rpm/min恒温摇床培育2-4h。然后菌液作为模板,用m13引物对检测菌落是否为阳性菌落。pcr程序如步骤b中一致。
[0080]
f、将pcr产物进行1%琼脂糖凝胶电泳,挑取鉴定为阳性的克隆菌,送至公司测序。最后使用dnastar7.1和mega software developmen软件对所得到的基因序列进行比对分析。
[0081]
g、相关实验数据见表5所示,一共发生了27处氨基酸的突变。
[0082]
表5亲本病毒(ck141/20)及其25℃低温培育毒株(ck141-25-ca/21)基因组比较分析
[0083][0084]
实施例5
[0085]
冷适应减毒活疫苗ck141-25-ca/21作为疫苗的安全性评价
[0086]
a、安全性评价:对15只4周龄的spf鸡随机平均分成三组,分别经鼻孔接种2倍剂量(2.0
×
106eid
50
)的测试疫苗ck141-25-ca/21、正常剂量(1.0
×
106eid
50
)毒株ck141/20以及pbs。每日观察并记录鸡的采食、饮水、精神状况、是否发病或死亡等,持续观察21d。
[0087]
b、ck141/20组、ck141-25-ca/21组和pbs鸡群在21d内精神正常,采食饮水正常,没有表现出典型h9n2亚型禽流感的症状。
[0088]
c、呼吸道组织的复制能力:对15只4周龄的spf鸡随机平均分成三组,分别经鼻孔
接种测试疫苗ck141-25-ca/21(1.0
×
106eid
50
)、毒株ck141/20(1.0
×
106eid
50
)和pbs。
[0089]
d、在接种后第3天每组分别处死3只鸡,取气管和肺脏组织,保存在青链霉素的磷酸盐缓冲溶液中,使用9-11日龄的鸡胚检测脏器的病毒滴度。结果见表6所示。
[0090]
表6在气管和肺脏中的复制滴度
[0091][0092]
注:血凝实验的病毒检测下限为0.699log
10
eid
50
/g/ml,每个样品做三个重复,病毒滴度表示为平均滴度
±
标准差。
[0093]
e、综上所述,本发明培育的冷适应减毒活疫苗ck141-25-ca/21具有良好的安全性,且不能在肺脏中复制,在气管中处于低水平复制。
[0094]
实施例6
[0095]
冷适应减毒活疫苗ck141-25-ca/21和全病毒ck141/20油乳剂灭活疫苗的免疫spf鸡的hi效价检测情况
[0096]
a、为检测冷适应减毒活疫苗和亲本病毒灭活疫苗的hi效价情况,将200μl含1.0
×
106eid
50
冷适应减毒活疫苗以滴鼻的方式免疫spf鸡(8只/组),油乳剂灭活疫苗组以相同病毒量的油乳剂灭活疫苗肌肉接种免疫,pbs皮下接种免疫阴性对照组。
[0097]
b、免疫后每隔7天采集血液分离血清并检测其hi效价,直至检测第21d。利用0.5%火鸡红细胞检测血清中hi抗体的滴度。
[0098]
c、相关实验数据见图8所示,结果表明:在免疫后第7d、第14d和第21d,冷适应减毒活疫苗组spf鸡的血清中血凝抑制抗体的滴度均高于油乳剂灭活疫苗组,能够刺激机体产生大量hi抗体,可以用于抵御外来病毒的侵扰,为h9n2禽流感病毒的防治奠定了基础。
[0099]
实施例7
[0100]
冷适应减毒活疫苗ck141-25-ca/21和亲本毒株ck141/20油乳剂灭活疫苗的免疫spf鸡的外周血淋巴细胞增殖情况
[0101]
a、为检测冷适应减毒活疫苗和亲本病毒灭活疫苗的外周血淋巴细胞增殖情况,将200μl含1.0
×
106eid
50
冷适应减毒活疫苗以滴鼻的方式免疫spf鸡(8只/组),油乳剂灭活疫苗组以相同病毒量的油乳剂灭活疫苗肌肉接种免疫,pbs皮下接种免疫阴性对照组。
[0102]
b、利用淋巴细胞分离液分离得到外周血淋巴细胞,应用xtt细胞增殖测定试剂盒进行淋巴细胞增殖测定(从每组中选择3只鸡)。在接种疫苗后第7d、第14d和第21d,使用含有抗凝管采集血液用于淋巴细胞增殖测定。
[0103]
c、使用定轨振荡器上轻轻混合1min,以确保颜色均匀分布。然后使用全波长酶标仪在450nm波长测量每个样品的吸光度,结果以3孔平均值表示。
[0104]
d、相关实验数据见图9所示,结果表明:在免疫后第7d、第14d和第21d,冷适应减毒活疫苗组spf鸡的外周血淋巴细胞的增殖能力高于油乳剂灭活疫苗组,能够刺激机体的淋
巴细胞快速增殖,可以用于抵御外来病毒的侵扰,为h9n2禽流感病毒的防治奠定了基础。
[0105]
实施例8
[0106]
冷适应减毒活疫苗ck141-25-ca/21和亲本毒株ck141/20油乳剂灭活疫苗的免疫保护效率
[0107]
a、在免疫后第21d后以流行毒株ck141/20攻毒,阴性对照组经鼻腔接种病毒液0.1ml(1.0
×
106eid
50
),实验组翅静脉接种病毒液0.1ml(1.0
×
106eid
50
)。
[0108]
b、攻毒后14d内每天连续观察,记录鸡的临床情况,统计死亡鸡和发病鸡的情况。在攻毒后第1d、2d、3d、4d、5d、6d、7d采集每只鸡咽喉和泄殖腔拭子,保存在含有青链霉素的pbs中,标记好保存在-80℃。
[0109]
c、鸡胚尿囊腔接种9-11日龄的鸡胚,每枚0.1ml,1个样品3个重复。37℃孵育72h测定所有鸡胚尿囊液的ha效价,记录ha阳性结果,以此确定疫苗免疫保护效率。
[0110]
d、相关实验数据见表7和8所示,结果表明:攻毒后第1d的咽喉拭子,pbs组和油乳剂组均100%检测出排毒,而冷适应减毒活疫苗组仅12.5%的病毒检出率。本发明培育的冷适应减毒活疫苗能够在病毒侵入机体的早期快速反应从而获得对该病毒的抵抗力,为h9n2禽流感病毒的防治奠定了基础。
[0111]
表7泄殖腔拭子病毒检测情况
[0112][0113]
表8咽喉拭子病毒检测情况
[0114][0115]
e、在攻毒后第3d时,每组随机选择3只鸡进行安乐死,然后进行剖检。剖检的脏器:脑、心、肝、脾、肺、肾、气管和盲肠,使用9-11日龄的鸡胚检测不同组织中病毒复制情况。
[0116]
f、相关实验数据见图10所示,结果表明:在病毒分布的主要器官气管和肺脏中,冷适应减毒活疫苗组检测不到病毒存在,油乳剂灭活疫苗组和pbs组均能检测到高水平的病毒滴度。本发明培育的冷适应减毒活疫苗能够保护鸡群免受病毒对肺脏和气管等组织的损害,帮助家禽不受h9n2禽流感的侵扰,为h9n2禽流感病毒的防治奠定了基础。
[0117]
上述实施例可见,本发明提供一株h9n2亚型禽流感病毒mdck细胞的冷适应减毒活疫苗,其基本特征:(a)冷适应减毒活疫苗ck141-25-ca/21属于当前流行的h9.4.2.5分支的
病毒;(b)透射电镜下病毒粒子多为球形,直径80-120nm,病毒外壳为囊膜结构;(c)冷适应减毒活疫苗在9-11日龄的鸡胚ha滴度为1:512,高于其在mdck的ha滴度;(d)冷适应减毒活疫苗经鼻腔途径感染4周龄的spf鸡后,在感染的14天内鸡群无发病和死亡。
[0118]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1