一种沙门氏菌马流产活疫苗的制备方法与流程
1.本发明属于兽用疫苗制备技术领域,尤其涉及一种沙门氏菌马流产活疫苗的制备方法。
背景技术:
2.马流产沙门氏菌病是由马流产沙门氏菌(salmonella abortus equi)引起的以马属动物流产为特征的传染病,只对马属动物具有致病性。早在18世纪末19世纪初,欧美地区发生过大批马流产的现象,该病全年都可发生,但主要发生于春秋两季,大多数表现为散发,有时呈地方流行性。马流产沙门氏菌易感染初孕马,主要在妊娠后期流产,多数马在发生流产前,一般无明显临床症状,突发流产,绝大多数为死胎,有少数存活的胎儿,在出生几天后,也会发生死亡。妊娠母马流产时,病原菌随流产胎儿、胎衣、羊水及阴道分泌物排出体外,患病公马可随精液排菌。感染马流产沙门氏菌的马常常成为该菌的病原携带者,也通常被认为是非疫区最初的传染源。
3.为了防治马流产沙门氏菌病,制备沙门氏菌马流产活疫苗,但是现有生产技术采用固体培养沙门氏菌马流产活疫苗,不控制ph、不添加补料、无do控制,接种后保持温度,在规定的时间收获。存在周期长、工作强度大、无中间控制,很难大规模生产。
技术实现要素:
4.有鉴于此,本发明的目的在于提供一种沙门氏菌马流产活疫苗的制备方法,采用本发明的制备方法周期短、工作强度小,适应于大规模生产。
5.为了实现上述发明目的,本发明提供了以下技术方案:
6.本发明提供了一种沙门氏菌马流产活疫苗的制备方法,包括以下步骤:
7.1)将马流产沙门氏菌c355弱毒菌接种于普通琼脂斜面上进行斜面培养,得到一级种子;
8.2)将所述步骤1)得到的一级种子接种于沙门氏菌液体培养基中进行二级种子培养,得到二级种子;
9.3)将所述步骤2)得到的二级种子接种于沙门氏菌液体培养基中进行发酵,得到发酵液,收集所述发酵液中的沙门氏菌;
10.4)将所述步骤3)得到的沙门氏菌与冻干保护剂混合,得到沙门氏菌马流产活疫苗。
11.优选的,所述步骤3)二级种子的接种量为1~2%。
12.优选的,所述步骤3)发酵的条件包括:温度为35~37℃,ph值为7.4~7.6,控制溶氧在40%~80%,溶氧下降时增加搅拌速度和通气量,搅拌速度不高于150rmp;从发酵第2h开始,每隔2h补充营养物质,所述营养物质为质量百分含量为50%的葡萄糖溶液,每次补加的量为发酵液总体积的0.5%,发酵的总时间为5~6h。
13.优选的,所述步骤2)二级种子培养的条件包括:温度为35~37℃,转速为150rpm,
培养时间为12h。
14.优选的,所述步骤3)收集发酵液中的沙门氏菌采用高速冷冻管式离心机或中空纤维浓缩系统进行收集。
15.优选的,当采用高速冷冻管式离心机收集沙门氏菌时,条件包括:48hz离心速度2l/min,温度为2~8℃。
16.优选的,当采用中空纤维浓缩系统收集沙门氏菌时,条件包括:对整个浓缩系统进行高压灭菌,灭菌完成后待系统冷却,开启动力泵,系统运行过程中控制中空纤维过膜压在0.1mpa以下,最后按浓缩比例收集浓缩菌液。
17.优选的,所述步骤4)冻干保护剂中含有明胶和蔗糖,所述明胶的质量百分含量为1~5%,所述蔗糖的质量百分含量为10~50%。
18.优选的,所述沙门氏菌马流产活疫苗中沙门氏菌的菌含量在1
×
10
10
cfu/头份以上。
19.优选的,所述步骤1)斜面培养的条件包括:温度为35~37℃,时间为18~20h。
20.本发明的有益效果为:
21.1、生产周期:原生产工艺生产一个批次按工艺流程到冻干结束至少需要7.5天,其中包括:一级菌种制备3天,二级菌种制备1天,制苗用菌液制备2.5天,菌液沉淀1天;本发明仅需4.5天,其中包括:一级菌种制备3天,二级菌种0.5天,细菌发酵、浓缩以及计数结果判定1天。
22.2、生产强度:原工艺因采取固体发酵,需要大量的人员同时操作,无菌操作,操作难度大,并且需要大量的扁瓶,本发明前期种子制备与原生产工艺基本一致,在制苗用菌生产阶段采用发酵罐生产浓缩设备进行浓缩,减少了人员工作强度,极大地降低了生产中污染发生的概率(原工艺二级种子为静置培养中途振荡1~2,需要1天,现在采用振荡培养只需要0.5天)。
23.3、产量:原生产工艺,每生产10000头份需要表面积25m2的普通琼脂扁瓶,按现生产所使用的扁瓶每个为0.025m2,合计需要1000个扁瓶,工作量极其庞大,本发明采用液体发酵再进行浓缩,仅需要40l发酵培养基。
24.4、本发明制备的疫苗在安全性和免疫效果上要优于原生产工艺。
附图说明
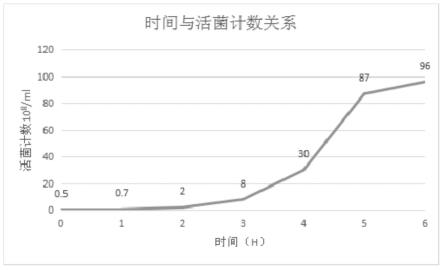
25.图1为实施例1中发酵过程中的时间与活菌计数关系。
具体实施方式
26.本发明提供了一种沙门氏菌马流产活疫苗的制备方法,包括以下步骤:
27.1)将马流产沙门氏菌c355弱毒菌接种于普通琼脂斜面上进行斜面培养,得到一级种子;
28.2)将所述步骤1)得到的一级种子接种于沙门氏菌液体培养基中进行二级种子培养,得到二级种子;
29.3)将所述步骤2)得到的二级种子接种于沙门氏菌液体培养基中进行发酵,得到发酵液,收集所述发酵液中的沙门氏菌;
30.4)将所述步骤3)得到的沙门氏菌与冻干保护剂混合,得到沙门氏菌马流产活疫苗。
31.本发明将沙门氏菌接种于普通琼脂斜面上进行斜面培养,得到一级种子。在本发明中,所述一级种子的制备时间为3d。本发明对普通斜面培养基没有特殊限定,采用培养沙门氏菌的培养基即可。在本发明中,所述沙门氏菌优选为马流产沙门氏菌c355弱毒菌,来源于中国兽医药品监察所。在本发明中,所述斜面培养的条件优选包括:温度为35~37℃,时间为18~20h。
32.本发明将得到的一级种子接种于沙门氏菌液体培养基中进行二级种子培养,得到二级种子。在本发明中,所述二级种子的制备时间为0.5d。本发明对所述沙门氏菌液体培养基没有特殊限定,本领域技术人员采用常规培养沙门氏菌的培养基即可。在本发明中,所述二级种子培养的条件优选包括:温度为35~37℃,转速为150rpm,培养时间为12h。
33.本发明将得到的二级种子接种于沙门氏菌液体培养基中进行发酵,得到发酵液,收集所述发酵液中的沙门氏菌。在本发明中,发酵、收集沙门氏菌以及活菌计数结果判定的总时间为1d。在本发明中,所述二级种子的接种量优选为1~2%。在本发明中,所述发酵的条件优选包括:温度为35~37℃,ph值为7.4~7.6,控制溶氧在40%~80%,溶氧下降时增加搅拌速度和通气量,搅拌速度不高于150rmp;从发酵第2h开始,每隔2h补充营养物质,所述营养物质为质量百分含量为50%的葡萄糖溶液,每次补加的量为发酵液总体积的0.5%,发酵的总时间为5~6h。本发明优选将所述发酵液进行浓缩,浓缩后再收集沙门氏菌。
34.在本发明中,收集发酵液中的沙门氏菌优选采用高速冷冻管式离心机或中空纤维浓缩系统进行收集。在本发明中,当采用高速冷冻管式离心机收集沙门氏菌时,条件优选包括:48hz离心速度2l/min,温度控制在2~8℃。在本发明中,当采用中空纤维浓缩系统收集沙门氏菌时,条件优选包括:对整个浓缩系统进行高压灭菌,灭菌完成后待系统冷却,开启动力泵,系统运行过程中控制中空纤维过膜压在0.1mpa以下。最后按浓缩比例收集浓缩菌液,离心按1/50(即使用冻干保护剂稀释至原发酵培养基体积的五十分之一),中空纤维为1/10(即中空纤维浓缩浓缩至原培养基体积的1/10,再加相应的冻干保护剂)。本发明对高压灭菌的条件没有特殊限定,采用常规即可,如121℃灭菌30min。
35.本发明将得到的沙门氏菌与冻干保护剂混合,得到沙门氏菌马流产活疫苗。在本发明中,所述冻干保护剂(溶剂为注射用水)中优选含有明胶和蔗糖,所述明胶的质量百分含量优选为1~5%,所述蔗糖的质量百分含量优选为10~50%。在本发明中,当采用高速冷冻管式离心机收集沙门氏菌时,选用的冻干保护剂中明胶的质量百分含量为1%,蔗糖的百分含量为10%。在本发明中,当采用中空纤维浓缩系统管道收集沙门氏菌时,选用的冻干保护剂中明胶的质量百分含量为5%,蔗糖的百分含量为50%。
36.在本发明中,所述沙门氏菌马流产活疫苗中沙门氏菌的菌含量优选在1
×
10
10
cfu/头份以上。
37.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
38.实施例1
39.沙门氏菌马流产活疫苗的制备方法,包括以下步骤:
40.(1)一级种子制备:马流产沙门氏菌c355弱毒菌(来源于中国兽医药品监察所)用
普通肉汤稀释,接种普通琼脂平板,37℃培养18~20小时(总共需要2天),选取中等大小的菌落数个,划线接种于普通琼脂斜面,35~37℃培养18~20小时(总共需要1天),经纯粹检验合格,作为一级种子;
41.(2)二级种子制备:取一级种子一支接种于沙门氏菌培养基中,35~37℃150rmp培养12小时(0.5天),取样做纯粹检验,合格后作为二级种子;
42.(3)菌液培养:接种前,调节沙门氏菌液体培养基温度至35~37℃,调节ph至7.4~7.6;将沙门氏菌的二级种子按培养基总量的1%~2%接种,进行发酵培养,发酵培养过程中,温度控制在35~37℃,ph控制在7.4~7.6,从第2小时开始,每两个小时补充营养物质。营养物质为质量百分含量为50%的葡萄糖溶液,每次补加量为发酵液总体积的0.5%,培养5小时,得沙门氏菌发酵菌液;
43.(4)菌液浓缩:发酵结束后,将发酵罐温度降至2~8℃,同时将搅拌速度降至50rmp,连接高速冷冻管式离心机管道或者中空纤维浓缩系统管道(发酵、浓缩、计数判定共1天);
44.①
使用高速冷冻离心:48hz离心速度为2l/min,离心完成后,在a级条件下收集沙门氏菌菌体,并用冻干保护剂稀释(1%明胶、10%蔗糖,均为质量百分含量),最终定容体积为发酵培养基体积的1/50。取样做纯粹检验和活菌计数;
45.②
使用中空纤维浓缩:浓缩至发酵培养基体积的1/10,在a级条件下收集浓缩后的菌体,再加入冻干保护剂(5%明胶、50%蔗糖,均为质量百分含量)。取样做纯粹检验和活菌计数;
46.(5)配苗:根据活菌计数结果,向浓缩后的菌液中加入冻干保护剂(中空纤维浓缩的菌液和冻干保护剂体积比例为1:5)(终浓度为1%明胶、10%蔗糖,均为质量百分含量),调节浓缩菌数中的细菌数量。不同规格的沙门氏菌马流产活疫苗(c355株)配苗如下表1所示;
47.表1沙门氏菌马流产活疫苗(c355株)配苗标准
[0048][0049]
(6)疫苗分装:将配苗好的疫苗液进行混合,组批,定量分装,分装时随时搅拌,使其混合均匀;
[0050]
(7)冻干结束后(冻干粉,具体菌含量根据活菌计数结果,按上述配苗标准应能达到设计头份数)做活菌计数、水分检验、真空度检验、安全检验、效力检验。
[0051]
对比文件1
[0052]
原工艺情况:(1)一级种子制备:马流产沙门氏菌c355弱毒菌(购买于中国兽医药品监察所)用普通肉汤稀释,接种普通琼脂斜面小管和普通肉汤小管繁殖后,用普通肉汤培
养物接种普通琼脂平板,37℃培养18~20小时,观察菌落形态,选取中等大小的菌落数个,接种普通琼脂斜面,37℃培养24小时,经纯粹检验合格,即为一级种子。在2~8℃保存,应不超过2个月,期间可移植1~2次(3天)。
[0053]
(2)二级种子繁殖:取一级种子接种于ph7.4~7.6的普通肉汤或马丁肉汤培养24小时,中间振荡1~2次。每瓶肉汤培养物用普通琼脂平板和斜面进行纯粹检验(1天)。在2~8℃保存,不超过2日。
[0054]
(3)制苗用菌液的制备:用种子液接种于ph7.4~7.6普通琼脂大扁瓶中,每瓶(扁瓶在接种前应置37℃放2~4日,肉眼检验应无菌生长),摇匀,使种子液布满琼脂,于37℃平放培养5~7小时后,抬高瓶口做倾斜培养36~48小时(2~2.5天)。经肉眼检查纯粹,加入稳定剂(含1%明胶、10%蔗糖,均为质量百分含量,ph7.4~7.6),将菌苔洗下,用三层纱布分组滤过于灭菌空瓶中,放2~8℃静置沉淀。
[0055]
(4)配苗与分装:经静置24小时(1天)并经检验纯粹的菌液,每瓶吸弃上清液的1/3后混匀,充分混匀。按规定头份定量分装,每头份菌含量为100亿/头份。分装后迅速进行真空干燥。
[0056]
由实施例1和对比例1可以得出:
①
生产周期:原生产工艺生产一个批次按工艺流程到冻干结束至少需要7.5天,本发明仅需4.5天。
②
生产强度:原工艺因采取固体发酵,需要大量的人员同时操作,无菌操作,操作难度大,并且需要大量的扁瓶,本发明制苗用菌生产阶段采用发酵罐生产浓缩设备进行浓缩,减少了人员工作强度,极大地降低了生产中污染发生的概率。
③
产量:原生产工艺,每生产10000头份需要表面积25m2的普通琼脂扁瓶,按现生产的所使用的扁瓶每个为0.025m2,合计需要1000个扁瓶,工作量极其庞大,本发明采用液体发酵再进行浓缩,仅需要40l发酵培养基发酵菌数在80~100cfu/ml,采用高速冷冻离心机,浓缩稀释后菌数为4000*108~4500*108cfu/ml,体积为800ml~1000ml,每头份配苗标准为200*108cfu按上述最低值计算,成品检验应为16头份/瓶。可以上报10头份规格。(s2022003~s2022006三批活菌计数结果分别为14.8头份/瓶、15.1头份/瓶、16.9头份/瓶)
[0057]
试验例
[0058]
成品安全性检验:按标签注明头份,将实施例1和对比例1的疫苗用马丁肉汤或者普通肉汤稀释,腹腔注射体重18~20g小鼠10只,每支0.2ml(含0.015头份),观察14日,应至少存活8只。
[0059]
效力检验:按瓶签注明头份,将疫苗用20%氢氧化铝胶生理盐水稀释,用体重18~20g小鼠15只,10只各腹腔注射0.2ml(含0.015头份),另5只作对照。接种21日后,每只小鼠各腹腔注射马流产沙门氏菌c77-1株(cvcc79001)普通肉汤24小时培养物0.2~0.3ml(4~5mld),观察14日。对照小鼠应全部死亡,免疫小鼠至少保护8只,结果见表2。
[0060]
表2安检、效检对比
[0061]
批号规格(头份/瓶)安检效检s202200110存活8只8/10保护s202200210存活6安检未合格,未做效检s202200310存活8只8/10保护s202200410存活10只9/10保护s202200510存活9只9/10保护
s202200610存活10只10/10保护
[0062]
注:上表s2022001~s2022003为对比例1制备的疫苗,s2022004~s2022006为本发明制备的疫苗从表2中可以得出,原生产工艺安全性和免疫效果均较本发明差。
[0063]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1