低毒性、高抗菌活性的β-多肽聚合物的制备方法及应用
本发明涉及多肽聚合物合成领域,尤其涉及一种低毒性、高抗菌活性的β-多肽聚合物的制备方法及应用。
背景技术:
1、自从1942年制药企业对青霉素进行大量生产并投入使用以来,人们已经合成了数百种抗生素,用以治疗人和动物的感染。然而,抗生素的滥用和误用导致了大量的污染,世界范围内的地表水、地下水、污水处理厂、土壤中都被多次检测到超标过量抗生素,这些药物的残留物以及耐药性微生物本身存在于水、土壤和空气中。由于旅行和贸易的全球化,抗微生物药物耐药性可以在数小时内传向世界各地;一方面抗生素的滥用导致了大量的耐药菌甚至超级病菌的出现,人们逐渐发现现有抗生素的治疗动物和人类感染疾病的潜力下降,最终导致大量的感染病例死亡,世界卫生组织预测抗微生物药物耐药性有可能比癌症更致命,每年可导致多达1000万人死于非命;另一方面,30年来没有新型抗生素进入市场,在目前条件下,很少有激励措施推动制药业研发此类抗生素。许多公司认为抗微生物药物没有足够的利润回报,不值得进行投资。
2、由于抗生素容易产生耐药性,因此研究人员将目光转向了一些新型抗菌剂的研究。其中天然来源的具有广谱抗菌特性且耐药性低的宿主防御肽引起了广泛的关注,其具正电荷和两亲性特征,能够破坏细菌的细胞膜,杀死细菌,但是宿主防御肽因其固有的缺点如容易被蛋白酶水解,制备成本高等限制了其应用。目前正在探索宿主防御肽的各种合成模拟物,包括各种α-多肽,β-多肽和类肽等。其中β-多肽聚合物是目前正在探索宿主防御肽的各种合成模拟物的一种,因其具有较高的抗菌活性,且不易被酶水解,因此被广泛应用于抗菌领域的研究。
3、早期研究人员发现,虽然β-多肽聚合物具有较高的抗菌活性,但是其具有较大的细胞毒性和溶血毒性,通过不同的方式注射到动物体内后,往往会引起动物的体内毒性如体内大出血,神经毒性,脏器衰竭甚至最终死亡,使其难以作为一种治疗体内感染的抗菌剂用于动物以及临床的治疗,因此早期的β-多肽聚合物一般作为体外抗菌的使用。
4、研究人员因此早期的研究通过不同的方法试图解决此类问题,如优化亲疏水比例,组装,包裹,通过调节聚合物中亲疏水性单体的比例以及不同亲疏水端基和侧链的密度,来改变聚合物的亲疏水性,从而改变聚合物的毒性;通过聚合物分子链之间的组装形成组装体降低聚合物的体内毒性;通过其他无毒纳米粒子包裹聚合物分子降低毒性。但是这些方法存在一些问题,如需要大量筛选聚合单体以调节疏水性变化和组装能力,需要复杂的程序来对包裹体进行设计,同时牺牲了β-多肽聚合物自身的抗菌活性。
5、因此,本领域仍需开发低毒性、高抗菌活性、能够应用到体内治疗感染,同时价格便宜能够大量制备的β-多肽聚合物。
技术实现思路
1、本发明的目的是通过一种简单的方法合成得到低毒性、高抗菌活性、能够应用到体内治疗感染,同时价格便宜能够大量制备的β-多肽聚合物。
2、本发明的第一方面,本发明提供一种β-多肽聚合物或其盐,其中,所述聚合物包含式i和式ii所示的重复单元
3、
4、其中,各rn相同或不同,各自独立地选自:h、卤素、羟基、氨基、苯基、c1-c6烷基、c1-c6卤代烷基、c1-c6烷氧基、c1-c6卤代烷氧基、c3-c8环烷基;p为1、2或3;
5、r1、r2、r’1、r’2各自独立地选自以下取代或未取代基团:氢、c1-c6烷基、c1-c6卤代烷基、c1-c6烷基羟基、c1-c6烷氧基、c1-c6烷基磺酰基、c1-c6烷基胍基、c1-c6烷基coo-、c1-c6烷基cso-、c1-c6烷基oco-、c1-c6烷基ocs-、c1-c6烷基conh-、c2-c6烯基、c2-c6炔基、c3-c12环烷基、c6-c12芳基、5-12元杂芳基、5-12元杂环基、c1-c6烷基-c6-c12芳基、氨基、c1-c6三氟烷基和其中,所述取代是指被一个或多个r取代;
6、p1为保护基,独立地选自以下基团:叔丁氧羰基(boc)、苄氧羰基(cbz)、芴甲氧羰基(fmoc)、邻苯二甲酰基(pht)、乙酰基(ac)、三氟乙酰基(tfa)、苄基(bn)、三苯基甲基(tr);p2选自以下基团:氢、取代或未取代的c1-c6烷基、取代或未取代的芳基、取代或未取代的5-12元杂芳基、取代或未取代的5-12元杂环基;其中,所述取代是指被一个或多个r取代;
7、或者r1和r2与它们连接的c原子共同形成取代或未取代的c5-c8环烷基或取代或未取代的5-8元杂环基;其中,所述取代是指被一个或多个r取代;
8、或者r1和r’1与它们连接的c原子共同形成取代或未取代的c5-c8环烷基或取代或未取代的5-8元杂环基;其中,所述取代是指被一个或多个r取代;
9、或者r2和r’2与它们连接的c原子共同形成取代或未取代的c5-c8环烷基或取代或未取代的5-8元杂环基;其中,所述取代是指被一个或多个r取代;
10、r3选自:h或-(l’)q’r’x;
11、rx和r’x各自独立地选自以下基团:nh2、r4nh、r4r’4n-、胍基(-nhc(=nh)nh2)、羟基、羧基、conh2、conhr4、conr4r’4、巯基、甲硫基、c2-c6烯基、c2-c6炔基、c1-c6烷基coo-、c1-c6烷基oco-、c6-c12芳基或5-12元杂环基;r4和r’4各自独立地为c1-c6烷基;
12、各l相同或不同,各l’相同或不同,l和l’各自独立地选自:-chr’-、-co-、-coo-、-s(=o)2-;q和q’各自独立地为0、1、2、3、4、5、6、7、8、9、10、11、12、13、14或15;r’选自:h、卤素、羟基、氨基、苯基、c1-c6烷基、c1-c6卤代烷基、c1-c6烷氧基、c1-c6卤代烷氧基、c3-c8环烷基;
13、r各自独立地选自:卤素、羟基、氨基、苯基、c1-c6烷基、c1-c6卤代烷基、c1-c6烷氧基、c1-c6卤代烷氧基、c3-c8环烷基、c1-c6烷基coo-、c1-c6烷基oco-、c1-c6烷基conh-、c1-c6卤代烷基conh-。
14、在另一优选例中,重复单元总数为5-5000的正整数,优选地为10-1000的正整数,优选地为20-100的正整数,更优选地为20-50(如30、40)的正整数。
15、在另一优选例中,r1、r2、r’1、r’2各自独立地选自:氢、c1-c4烷基、c1-c4卤代烷基、c1-c4烷基羟基、c1-c4烷氧基、c1-c4烷基磺酰基、c1-c4烷基胍基、c1-c4烷基coo-、c1-c4烷基oco-、c1-c4烷基cso-、c1-c4烷基ocs-、c2-c4烯基、c2-c4炔基、c3-c6环烷基、苯基、萘基、5-6元杂芳基、5-6元杂环基、c1-c4烷基-c6芳基、氨基、c1-c6三氟烷基或p1和p2的定义如上所述。
16、在另一优选例中,β-多肽聚合物的盐为药学上可接受的盐,优选地为盐酸盐、溴酸盐、三氟乙酸盐、磷酸盐、锂盐、钠盐、或钾盐。
17、在另一优选例中,β-多肽聚合物中的氨基酸为l构型、d构型、或者d构型l构型两者的混合。
18、在另一优选例中,所述聚合物为无规共聚物、交替共聚物或嵌段共聚物,较佳地,为无规共聚物。
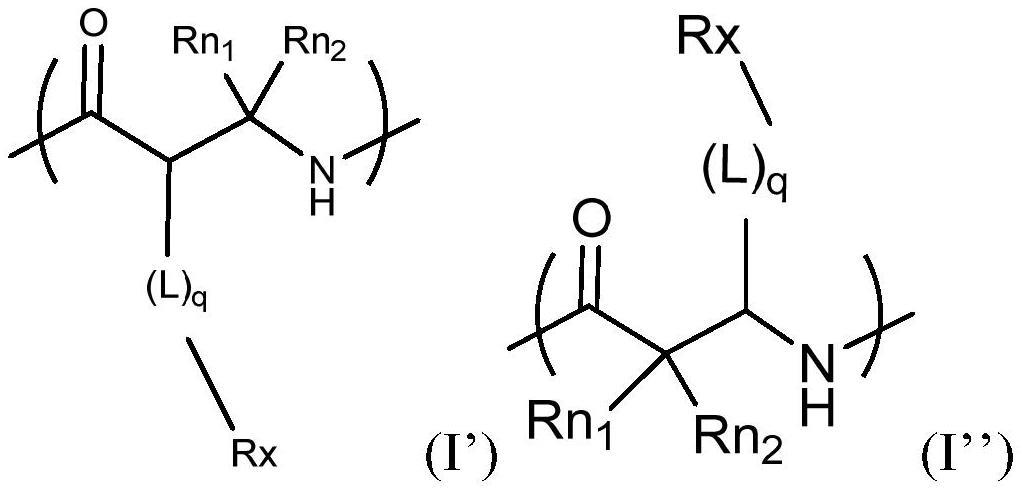
19、在另一优选例中,式i重复单元具有式i’或i”所示的结构
20、
21、其中,rn1和rn2各自独立地选自:h、c1-c6烷基、c1-c6卤代烷基、c1-c6烷氧基;
22、l、q和rx的定义如上所述。
23、在另一优选例中,l为ch2,q为1、2、3、4、5或6。
24、在另一优选例中,rn1和rn2各自独立地选自:h、甲基、乙基、丙基。
25、在另一优选例中,式ii重复单元具有式ii’、ii”、ii”’、ii””或ii””’所示的结构
26、
27、其中,r’各自独立地为1、2或3;
28、ra、r’a、rb、r’b各自独立地选自:h、取代或未取代的c1-c6烷基、取代或未取代的c1-c6烷氧基;其中,所述取代是指被选自下组的一个或多个基团取代:卤素、羟基、c1-c6烷基、c1-c6烷基coo-、c1-c6烷基oco-、c1-c6烷基conh-、c1-c6卤代烷基conh-;
29、r’1、r’2、l’、q’和r’x的定义如上所述。
30、在另一优选例中,r’1和r’2各自独立地为h、甲基、乙基、丙基、ch2nhcoch3、ch2nhcocf3。
31、在另一优选例中,式i重复单元选自:
32、
33、在另一优选例中,β-多肽聚合物重复单元中氨基酸为l构型、d构型、或者d构型l构型两者的混合。
34、在另一优选例中,式ii重复单元选自:
35、
36、在另一优选例中,β-多肽聚合物重复单元中氨基酸为l构型、d构型、或者d构型l构型两者的混合。
37、在另一优选例中,所述聚合物选自:
38、
39、
40、式中,n为5-5000的正整数;
41、a为0-100的正整数;
42、0%<x<100%,0%<y<100%,0%<y1<100%,0%<y2<100%,且x+y=100%,y=y1+y2;
43、rz选自:卤素、羧基、活性酯基团(-nhs活性酯或马来酰亚胺活性酯及其衍生物)、酰氯(-(co)cl)、环氧烷基(-ch(o)ch-)、巯基、c2-c15烯基、c2-c15炔基、叠氮、马来酰亚胺、邻二硫吡啶基(opss)、环糊精、金刚烷基;
44、rw为其中,波浪线表示连接处;
45、a’各自独立地为0-12的正整数;优选地,a’为0、1、2或3;
46、r11、r12、r13和r14各自独立地选自以下取代或未取代的基团:氢、c1-c6烷基、c1-c6卤代烷基、c1-c6烷基羟基、c1-c6烷基nh2、c1-c6烷氧基、c1-c6烷基磺酰基、c1-c6烷基胍基、c1-c6烷基coo-、硫代c1-c6烷基coo-、c1-c6烷基oco-、硫代c1-c6烷基oco-、c1-c6烷基conh-、c2-c6烯基、c2-c6炔基、c3-c12环烷基、c6-c12芳基、5-12元杂芳基、5-12元杂环基、c1-c6烷基-c6-c12芳基、氨基、c1-c6三氟烷基和其中,所述取代是指被一个或多个r取代;
47、p1为保护基,独立地选自以下基团:叔丁氧羰基(boc)、苄氧羰基(cbz)、芴甲氧羰基(fmoc)、邻苯二甲酰基(pht)、乙酰基(ac)、三氟乙酰基(tfa)、苄基(bn)、三苯基甲基(tr);p2选自以下基团:氢、取代或未取代的c1-c6烷基、取代或未取代的芳基、取代或未取代的5-12元杂芳基、取代或未取代的5-12元杂环基;其中,所述取代是指被一个或多个r取代;
48、r各自独立地选自:卤素、羟基、氨基、苯基、c1-c6烷基、c1-c6卤代烷基、c1-c6烷氧基、c1-c6卤代烷氧基、c3-c8环烷基、c1-c6烷基coo-、c1-c6烷基oco-、c1-c6烷基conh-、c1-c6卤代烷基conh-。
49、在另一优选例中,50%<x≤100%,0%≤y≤50%。
50、在另一优选例中,rz选自:-sh,和/或
51、rw为
52、在另一优选例中,n为10-1000的正整数,优选地n为20-100的正整数,更优选地n为20-50(如30、40)的正整数。
53、在另一优选例中,a为0、1、2、3、4、5、6、7、8、9或10。
54、在另一优选例中,所述聚合物选自:
55、
56、
57、
58、在另一优选例中,上述结构阴离子选自:cl-、br-、cf3coo-、h2po4-、hpo42-、po43-。
59、在另一优选例中,β-多肽聚合物为实施例中所示的β-多肽聚合物。
60、本发明第二方面,提供一种如第一方面所述的β-多肽聚合物或其盐的用途,用于
61、1)修饰到表面抗细菌、抗真菌、抗病毒、抗螨虫、抗肿瘤;
62、2)制备抗细菌、抗真菌、抗病毒、抗螨虫、抗肿瘤相关疾病的药物;
63、3)制备细胞粘附、组织工程、药物修饰、蛋白修饰、药物协同、药物递送、基因递送等领域的材料;
64、4)蛋白保护、细胞保护、组织和器官冷冻保护等领域的材料;或
65、5)水凝胶敷料和自组装等领域的材料。
66、在另一优选例中,所述细菌选自:金黄色葡萄球菌菌株、耐舒巴坦金黄色葡萄球菌s.a 2904、耐氨苄西林金黄色葡萄球菌s.a 2802、耐阿莫西林金黄色葡萄球菌s.a2902、耐头孢曲松金黄色葡萄球菌s.a 1306、耐环丙沙星金黄色葡萄球菌s.a 2202、耐青霉素金黄色葡萄球菌s.a xy201921、耐甲氧西林金黄色葡萄球菌s.a 0811、耐甲氧西林金黄色葡萄球菌s.a usa300 lac、耐甲氧西林金黄色葡萄球菌s.a usa300、耐氨曲南大肠杆菌e.c2410、耐头孢曲松大肠杆菌e.c 2709、耐头孢噻肟大肠杆菌e.c2714、大肠杆菌e.catcc25922,或其组合;
67、所述修饰到表面为修饰到医疗卫生器械表面、植入材料和器械表面、食品包装表面、衣物织物表面;
68、所述相关疾病为体内感染,优选地,所述体内感染为动物全皮层局部感染、动物的角膜炎局部感染、动物的骨植入物局部感染、动物肺炎感染、动物的腹膜炎系统感染,或其组合。
69、在另一优选例中,β-多肽聚合物或其盐具有较低的毒性同时兼具抗致病菌活性,优选地,所述毒性为体外哺乳细胞毒性、体外哺乳动物血液溶血毒性、哺乳动物体内急性体内毒性或长期体内毒性。
70、在另一优选例中,所述病菌为革兰氏阴性菌或革兰氏阳性菌。
71、在另一优选例中,所述动物为哺乳动物,优选地为人、小鼠或大鼠。
72、在另一优选例中,所述体内感染为小鼠全皮层局部感染、小鼠的角膜炎局部感染,大鼠的骨植入物局部感染、小鼠肺炎感染、小鼠的腹膜炎系统感染中的一种或两种以上的组合。
73、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!