一种检测猴痘病毒及其亚型的多重荧光定量PCR试剂盒
一种检测猴痘病毒及其亚型的多重荧光定量pcr试剂盒
技术领域
1.本发明属生物技术领域,涉及荧光定量pcr检测试剂盒,具体涉及检测感染性病毒的 多重荧光定量pcr试剂盒,是一种一步法多重实时荧光定量pcr在同一个反应管内检测血 液/分泌物标本中猴痘病毒及其亚型(猴痘-西非株和猴痘-刚果盆地株)的核酸检测技术,可 应用于猴病毒及其亚型的快速筛查和猴痘病毒流行病学研究。
背景技术:
2.猴痘是一种以皮肤出疹为特症的罕见的人畜共患病,由猴痘病毒引起的传染性疾病, 它属于痘病毒科,与天花病毒同属同属正痘病毒属。猴类及人类感染猴痘病毒的临床症状和 组织病理与天花感染难以区别,而且猴痘病毒与天花病毒有共同抗原,两者之间有很强的血 清交叉反应和交叉免疫。1958年,从实验室的猴子体内分离出猴痘病毒,其后在非洲的其他 动物(如松鼠、大鼠、小鼠、兔类、豪猪和穿山甲等)也检测出这种病毒。1970年,第一例 猴痘病毒感染在一名9个月大的非洲男婴中确诊。自那时以来,猴痘病毒逐渐蔓延到非洲其 他国家,主要是在中非和西非流行。几十年来,这种病毒一直在非洲传播并带来死亡。自2003 年以来,全球多个国家发现猴痘感染,且感染者多数接触过生病的动物。特别是自2021年6 月以来,猴痘病毒呈现全球蔓延的趋势,感染人数和死亡人数不端上升。随着猴痘病例的快 速蔓延,2022年5月20日,世界卫生组织(who)就猴痘召开紧急会议。自今年年初以来, 世卫组织非洲区域8个国家共报告了1536例疑似病例,其中59例得到确认,72例死亡。截 至6月8日,who报告显示全球有28个国家报告了1285例实验室确诊病例和1例疑似病例。 猴痘病毒常见的典型症状表现为发热、淋巴结肿大、随后出现集中在面部和四肢的皮疹等。 猴痘病毒主要通过人密切接触感染的动物传染,而当前猴痘病毒传播的主要方式为“人际间密 切接触”,但尚不清楚该病毒是否会通过气溶胶传播。病毒dna的基因组测序分析显示,猴 痘病毒主要包括两种亚型(猴痘病毒i型和猴痘病毒ii型),而当前流行的为猴痘病毒i型。 针对猴痘病毒的防控,who正在或部分制定临时指导方针,以支持成员国提高认识、监测、 实验室诊断和检测、病例调查和接触者追踪、临床管理和感染预防控制、疫苗和免疫以及风 险沟通和社区参与。实验室及时和准确的确认猴痘病毒是打破传播链,阻止疫情爆发的关键。 而当前针对猴痘病毒检测应用的主要是基于核酸扩增技术(naat)的实时/传统聚合酶链反 应(pcr)技术,也可以通过基因测序技术。实验室确认样本为皮疹表面渗出物,血液和分 泌物也是重要的补充。当前的检测猴痘的pcr技术主要是采用单重实时荧光pcr技术,因 此建立一步法多重实时荧光pcr技术来检测并鉴定猴痘病毒及其亚型对于疫情的防控至关重 要。
3.当前,国内外对猴痘病毒及其亚型(猴痘-西非株和猴痘-刚果盆地株)的检测主要是采 取单重核酸检测或基因测序技术。基因测序技术需要专业的人员,昂贵的检测费用及操作时 间长等因素严重影响该技术的广泛应用。单重实时荧光pcr技术虽然可快速检测猴病毒,但 对于鉴定其亚型(猴痘-西非株和猴痘-刚果盆地株)需要更多的费用。多重实时荧光定量pcr 技术以其全封闭检测、单管扩增实时定量、简便快捷、节约成本、重复性好等优
势,并具有 高特异性与敏感性,较于普通和单重pcr检测更加优化,可作为一种猴痘病毒及其亚型(猴 痘-西非株和猴痘-刚果盆地株)的快速、有效的检测手段。
技术实现要素:
4.本发明的目的是提供一种检测猴痘病毒及其亚型的多重荧光定量pcr试剂盒,是用于 猴痘病毒(hmpv)、猴痘-西非株亚型(hmpv/wa)、猴痘-刚果盆地株亚型(hmpv/cb) 和rnase p检测的一步法多重荧光定量pcr试剂盒。本试剂盒包含定量pcr反应液、酶混 合液、引物与探针混合液、标准品(合适浓度的hmpv、hmpv/wa、hmpv/cb和rnase p 的质粒)、阳性对照品(合适浓度的hmpv、hmpv/wa、hmpv/cb和rnase p的质粒)、 阴性对照品。盒体设有容器孔,分别放置定量pcr反应液管、酶混合液管、引物与探针混合 液管、标准品管(hmpv、hmpv/wa、hmpv/cb和rnase p质粒)、阳性对照品管(hmpv、 hmpv/wa、hmpv/cb和rnase p)、阴性对照品管。
5.其中定量pcr反应液管包含有pcr反应缓冲液管(含氯化镁和三磷酸脱氧核糖核苷酸混 合物等)、酶混合液管(含耐热taq dna聚合酶和耐热性rnaseh等)。引物与探针混合液管 包含四组引物和相应的四种不同荧光标记的探针,引物与探针混合液管为棕色管。阴性对照 为高温高压灭菌的depc(焦碳酸二乙酯)处理水,阳性对照为hmpv、hmpv/wa、hmpv/cb 和rnase p的阳性质粒样品。
6.一步法多重荧光定量pcr检测用上游引物和下游引物及相应的特异性探针序列如下:上游引物hmpv-f:5
’‑
gtcagcagtggcgattttct-3’下游引物hmpv-r:5
’‑
tgaaccagatggtcctctcaata-3’特异性探针hmpv-p:5
’‑
fam-taataaacacccacgtaaatacaaaacaga-bhq1-3’上游引物hmpv/wa-f:5
’‑
atatcactacggacataaaccattgt-3’下游引物hmpv/wa-r:5-acgtcgatgtcagaaataatcaac-3’特异性探针hmpv/wa-p:5
’‑
rox-taagttcctggatcggatgtcaccgc-bhq2-3’上游引物hmpv/cb-f:5
’‑
gatataggtgtcttcataacgcatt-3’下游引物hmpv/cb-r:5
’‑
gcgtgaatatctaaagattatggg-3’特异性探针hmpv/cb-p:5
’‑
cy5-tctcaaatacatgataggataatagaatgctaa-bhq3-3’上游引物rnase p-f:5
’‑
agatttggacctgcgagcg-3’下游引物rnase p-r:5
’‑
gagcggctgtctccacaagt-3’特异性探针rnase p-p:5
’‑
vic-ttctgacctgaaggctctgcgcg-bhq1-3’。
7.其中猴痘病毒、猴痘-西非株、猴痘-刚果盆地株及rnase p的特异性探针分别采用fam、 rox、cy5和vic四种不同荧光进行标记,且引物与探针由珠海辉睿生物科技有限公司合成。
8.上述标准品包括猴痘病毒、猴痘-西非株、猴痘-刚果盆地株及rnase p标准品,其保守 区基因序列如下:
9.猴痘病毒标准品序列为:atatttggtattaccacattaattatattgtcagcagtggcgattttctgtattacgtattat atatgtaataaacacccacgtaaatacaaaacagagaacaaagtctagattttgacttac ataaatatctgggataata
aaatctatcatattgagaggaccatctggttcaggaaagac agccataaccaaaaga。
10.猴痘-西非株标准品序列为:gattaaatattttaatagtatccattttatatcactacggacataaaccattgtatatttttt atgtttattagtgtacacattttggaagtaagttcctggatcggatgtcaccgcagtaata atgttgattatttctgacatcgacgtattatatagttttttaattccatatcttt。
11.猴痘-刚果盆地株标准品序列为:cttgatactttttctagaaaaaaaattgaattgatgatataggtgtcttcataacgcatta ttacgttagcattctattatcctatcatgtatttgagagtcttatatgtagcaaacatgata actgcaatacccataatctttagatattcacgcgtgctatggatggcattatcccgcggt。
12.rnase p标准品序列为:atgggacttcagcatggcggtgtttgcagatttggacctgcgagcgggttctgacctga aggctctgcgcggacttgtggagacagccgctcaccttggctattcagttgttgctatc。
13.本发明提供的试剂盒需保存于-20℃,并减少反复冻融次数;对引物与探针混合液进行 避光保存。
14.本发明的另一个目的是提供所述多重荧光定量pcr检测试剂盒在猴痘病毒、猴痘-西非 株和猴痘-刚果盆地株的核酸检测以及样本采集状态和核酸提取情况的判定中应用。
15.本发明试剂盒的使用方法:在每次荧光定量检测中均应设有阳性对照和阴性对照。标 准品用碧云天公司的te buffer(货号:st725)稀释为1
×
10
2-1
×
108copies/ml。
16.样本核酸的提取:取200ul血清样本进行提取。核酸提取采用geneaid公司的viralnucleic acid extraction kit ii,按照试剂盒内说明书进行提取操作,取10ul终产物样品核酸作 为后续模板。
17.核酸的检测:取10ul已抽提的待测样品核酸作为模板。反应总体积为20ul,其中荧 光定量pcr反应液和taq酶混液位10μl,引物与探针混合(20μmol/l,包含四组引物与荧 光探针)共3μl,模板5μl,剩余加水补足至终体积20μl。在abi 7500荧光定量pcr仪 上检测,反应程序为:预变性95℃,5min;然后变性95℃10s,退火和延伸58℃30s,在58℃ 进行多重荧光检测,共进行45个循环。
18.实验结果判断:
①
样本采集合格rnase p、猴痘病毒、猴痘-西非株和猴痘-刚果盆地株 检测的各自ct值对应相应的荧光标记的探针,样本采集合格及核酸提取成功,c
t
值《37则结 果均为阳性;其余检测样本c
t
值为≥40或undetermined时,报告为阴性。
②
检测样本猴痘病毒、 猴痘-西非株和猴痘-刚果盆地株的c
t
值≤40时,且扩增曲线良好,报告为阳性。
③
检测样本c
t
值37≤c
t
值《40的样本,建议复检,复检结果37≤c
t
值《40者,且扩增曲线良好,依据
②
的判断 标准报告为相应病毒阳性。根据所获得的标准曲线,计算待测标本中猴痘病毒、猴痘-西非株 和猴痘-刚果盆地株的病毒拷贝数(copies/ml)。
19.本研究针对猴痘病毒、猴痘-西非株和猴痘-刚果盆地株设计特异性引物与探针;同时以 核糖核酸酶rnase p作为内参。采用单管一步法多重实时荧光定量pcr,能够单管同时检测出 猴痘病毒、猴痘-西非株和猴痘-刚果盆地株病毒,不仅显著降低检测成本,更能获取丰富的 检测信息,内参的引入可判断样本核酸质量,协助检测结果的判断。另外,多重实时荧光定 量pcr同样具有极高的敏感性和特异性。
20.本发明的有益之处在于采用高特异性高灵敏度的一步法实时荧光定量pcr技术,
rnase p)、阳性对照品管(猴痘病毒、猴痘-西非株、猴痘-刚果盆地株、rnase p)、阴性对 照品管。
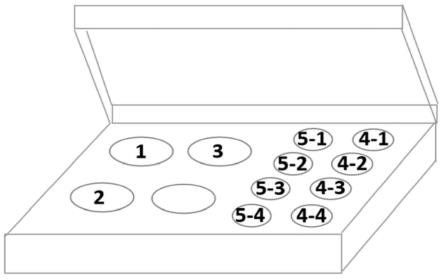
35.参见图1,本试剂盒包装内设有容器孔,用于放置对应试剂盒组分:定量pcr反应液 管与酶混合液管1(定量pcr反应液与酶混合液)、引物与探针混合液管2、阴性对照品管3、 标准品管(包括猴痘病毒标准品4-1、猴痘-西非株标准品4-2、猴痘-刚果盆地株标准品4-3、 rnase p标准品4-4,共4管)、阳性对照品管(包括猴痘病毒阳性对照品5-1、猴痘-西非株 阳性对照品5-2、猴痘-刚果盆地株阳性对照品5-3、rnase p阳性对照品5-4,共4管)。试 剂盒包含:定量pcr反应液与酶混合液、引物与探针混合液、标准品(猴痘病毒、猴痘-西 非株、猴痘-刚果盆地株、rnase p)、阳性对照品(猴痘病毒、猴痘-西非株、猴痘-刚果盆地 株、rnase p)、阴性对照品。
36.实施例2
37.1材料与方法
38.1.1质粒样本:猴痘病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)阳性质粒由珠海辉睿生物科技有限公 司无偿友情馈赠。
39.另外,其他疱疹病毒如肠道病毒71型(ev71)、单纯疱疹病毒(hsv)、eb病毒(ebv) 和巨细胞病毒(cmv)阳性标本由传染病诊治国家重点实验室和本实验室提供。
40.1.2引物与探针从ncbi基因库下载猴痘病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)涵盖国内外的 多条基因序列。利用dnaman软件对其进行了同源性比较,确定以上病毒基因组的保守区。 使用primer express 3.0软件在其保守区设计高度特异性的引物与taqman探针,引物和探针 序列均通过blast验证,具有较好特异性。
41.引物和探针序列如下:上游引物hmpv-f:5
’‑
gtcagcagtggcgattttct-3’下游引物hmpv-r:5
’‑
tgaaccagatggtcctctcaata-3’特异性探针hmpv-p:5
’‑
fam-taataaacacccacgtaaatacaaaacaga-bhq1-3’上游引物hmpv/wa-f:5
’‑
atatcactacggacataaaccattgt-3’下游引物hmpv/wa-r:5-acgtcgatgtcagaaataatcaac-3’特异性探针hmpv/wa-p:5
’‑
rox-taagttcctggatcggatgtcaccgc-bhq2-3’上游引物hmpv/cb-f:5
’‑
gatataggtgtcttcataacgcatt-3’下游引物hmpv/cb-r:5
’‑
gcgtgaatatctaaagattatggg-3’特异性探针hmpv/cb-p:5
’‑
cy5-tctcaaatacatgataggataatagaatgctaa-bhq3-3’上游引物rnase p-f:5
’‑
agatttggacctgcgagcg-3’下游引物rnase p-r:5
’‑
gagcggctgtctccacaagt-3’特异性探针rnase p-p:5
’‑
vic-ttctgacctgaaggctctgcgcg-bhq1-3’。
42.其中,rnase p的引物和探针序列引自j clin microbiol.2005apr;43(4):1851
–
1857。以 上引物和探针委托珠海辉睿生物科技有限公司合成。
43.1.3病毒核酸的提取与标准品定量标准:样本核酸的提取:吸取200ul血清标本于ep管中,进行核酸提取。核酸提取采用
geneaid 公司的viral nucleic acid extraction kit ii,按照试剂盒说明书进行提取,取10ul已抽提的待 测样品核酸作为模板。
44.合成各基因标准品片段,将其连接到质粒载体pmdtm19-t simple vector(takara公 司)上。转化后培养。鉴定后提取质粒dna,利用nanodrop nd-2000spectrophotometer 测定质粒dna浓度,确定dna的拷贝数,作为标准品定量母液。根据实验需要,将标准品 定量母液稀释至所需最高浓度,并做十倍稀释至最低浓度,-20℃保存备用。
45.1.4多重实时荧光定量pcr反应体系和条件的优化:核酸的检测:取5ul已抽提的待测样品核酸作为模板。反应总体积为20μl,其中荧光 定量pcr反应液和taq酶混液位10μl,引物与探针混合(20μmol/l,包含四组引物与荧光 探针)共3μl,模板5μl,剩余加水补足至终体积20μl。在abi 7500荧光定量pcr仪上 检测,反应程序为:预变性95℃,5min;然后变性95℃10s,退火和延伸58℃30s,在58℃ 进行多重荧光检测,共进行45个循环。
46.结果判断:选择荧光检测通道fam、rox、cy5、vic,荧光基线选取3-15个循环的 荧光信号的平均值,阈值设定以阈值线刚好超过阴性对照品的最高点。
①
样本采集合格猴痘 病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)检测的各自c
t
值对应相应的荧光标记的探 针。样本采集合格、核酸提取成功,则rnase p检测为阳性;当检测样本c
t
值为≥40、0和 无数值时,报告为阴性。
②
当检测猴痘病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)阳 性质粒/样本的c
t
值《37时,报告为阳性。
③
当检测样本c
t
值≥37且小于40的样本,建议 复检,复检结果c
t
值≥37且小于40者,依据
②
的判断标准报告为相应病毒阳性。体系的优 化试验,在以相同浓度阳性核酸为模板的反应体系中,采用矩阵法筛选引物和探针的最合适 浓度,引物浓度从1~20μm,探针浓度从1~20μm,根据最低ct值和最高荧光强度增加值 (δrn)选择最合适引物和探针浓度。
47.1.5多重实时荧光定量pcr特异性、敏感性和重复性试验选择猴痘病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)阳性标本(均来自猴痘病毒、 猴痘-西非株、猴痘-刚果盆地株阳性质粒)和其他疱疹病毒如ev71、hsv、ebv和cmv阳 性临床标本,遗憾的是国内暂时没有痘病毒及其亚型阳性的临床样本,用多重实时荧光定量 pcr方法验证方法的特异性;对已标定拷贝数(copies/ml)的猴痘病毒合成片段(10
8 copies/ml)、猴痘-西非株合成片段(108copies/ml)、猴痘-刚果盆地株合成片段(108copies/ml) 和rnase p合成片段(108copies/ml)分别稀释后,平行实验进行荧光定量pcr反应,验证 方法的灵敏度。此外,对每一个指定浓度的阳性标准品作3次重复检测,对实验所得的c
t
值计算其标准差与变异系数,验证方法的重复性。
48.2结果
49.2.1多重实时荧光定量pcr反应体系及条件核酸的检测:取5ul已抽提的待测样品核酸作为模板。反应总体积为20μl,其中定量 pcr反应液与酶混合液10μl,引物与探针混合液(20μmol/l,包含四组特异性引物和相应 的四种荧光探针)共3μl,模板5μl,加水补足至20μl。在abi 7500荧光定量pcr仪(或 者其他四色荧光及以上的pcr仪)上进行检测,反应参数为:反应程序为:预变性95℃,5min; 然后变性95℃10s,退火和延伸58℃30s,在58℃进行多重荧光检测,共进行45个循环。
50.2.2特异性试验
本发明建立的一步法多重荧光定量pcr方法对猴痘病毒及其亚型(猴痘-西非株、猴痘
‑ꢀ
刚果盆地株)具有良好的特异性,能完全检出阳性质粒标本,遗憾的是国内暂时没有阳性的 临床样本。本发明中的多重引物与探针与其他和其他疱疹病毒如ev71、hsv、ebv和cmv 阳性标本等均无交叉反应。该方法能特异性检测出质粒标本中的的猴痘病毒及其亚型(猴痘
‑ꢀ
西非株、猴痘-刚果盆地株),结果参见图2、图3、图4和图13。
51.2.3敏感性试验对猴痘病毒及其亚型(猴痘-西非株、猴痘-刚果盆地株)、rnase p敏感性进行检测,将 已标定拷贝数(copies/ml)的猴痘病毒合成片段(108copies/ml)、猴痘-西非株合成片段(10
8 copies/ml)、猴痘-刚果盆地株的合成片段(108copies/ml)和rnase p合成片段(108copies/ml) 分别作十倍梯度稀释后,用本试剂盒进行检测,检测结果显示该方法检测敏感性分别达到102、 102、102和102copies/ml。结果参见图5、图7、图9、图11。对猴痘病毒及其亚型(猴痘-西 非株、猴痘-刚果盆地株)阳性样本混合检测,病毒与内参检测结果显示可以实现单管同时检 测并区分上述病毒(参见图13)。
52.2.4重复性试验分别取猴痘病毒合成片段(终浓度为106copies/ml)、猴痘-西非株合成片段(10
6 copies/ml)猴痘-刚果盆地株合成片段(106copies/ml)和rnase p合成片段(106copies/ml), 按10倍梯度稀释为105与104,对106、105、104样本分别作3次重复检测,计算其变异系数 与标准差。结果显示,不同核酸浓度各自的检测c
t
值标准差在0.18~0.67之间,变异系数均 低于2.50%,具有较好的重复性(结果见表1)。
53.表1多重实时荧光定量pcr检测合成核酸的重复性试验
54.实施例3采用本试剂盒对临床样本的检测,临床样本主要来源于2022年4月至2021年6月间发 热门诊病原检测标本的废弃样本共50份。采用本方法中的多重实时荧光定量pcr对采集的 临床标本进行检测,结果如下:发热门诊检测标本共50份,猴痘病毒及其亚型(猴痘-西非 株、猴痘-刚果盆地株)的检测结果均为阴性。本试剂盒检测阳性结果与商用试剂盒(之江生 物)检测阳性结果符合度达100%。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1