检测流感病毒H5、H7、H9亚型的引物和探针及其应用、试剂和数字PCR试剂盒的制作方法
no.5和seq id no.6所示的核酸序列;
12.所述探针包括第一探针、第二探针和第三探针;
13.所述第一探针具有如seq id no.7所示的核酸序列;所述第二探针具有如seq id no.8所示的核酸序列;所述第三探针具有如seq id no.9所示的核酸序列。
14.作为进一步技术方案,所述探针的5’端连接有荧光报告基团,3’端连接有荧光淬灭基团。
15.作为进一步技术方案,所述荧光报告基团包括fam、cy5或hex;
16.优选地,所述荧光淬灭基团包括tamra、bhq1或bhq2。
17.第二方面,本发明提供了上述引物和探针在制备流感病毒h5、h7、h9亚型检测产品中的应用;
18.优选地,所述检测产品包括数字pcr试剂盒。
19.第三方面,本发明提供了一种试剂,包括所述的引物和探针。
20.第四方面,本发明提供了一种数字pcr试剂盒,包括所述的引物和探针以及数字pcr反应预混液。
21.作为进一步技术方案,所述数字pcr反应预混液,包括:buffer、mg
2+
、dntps、热启动taq酶和逆转录酶。
22.作为进一步技术方案,还包括阳性对照品;
23.所述阳性对照品包括h5亚型h基因片段、h7亚型h基因片段和h9亚型h基因片段。
24.作为进一步技术方案,所述阳性对照品为含有h5亚型h基因片段、h7亚型h基因片段和h9亚型h基因片段的重组质粒。
25.作为进一步技术方案,还包括阴性对照品;
26.所述阴性对照品为无核酸酶水。
27.与现有技术相比,本发明具有如下有益效果:
28.本发明提供的检测流感病毒h5、h7、h9亚型的引物和探针,其中引物具有如seq id no.1-6所示的核酸序列,探针具有如seq id no.7-9所示的核酸序列,该引物和探针特异性强,灵敏度高,能够用于制备检测流感病毒h5、h7、h9亚型的产品,实现对流感病毒h5、h7、h9亚型的检测。
29.本发明提供的数字pcr试剂盒,采用数字pcr的方法对目的核酸进行检测,其检测灵敏度明显优于荧光定量pcr或者胶体金,能够实现单拷贝模板量的检测。
附图说明
30.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
31.图1为h5亚型引物探针筛选;
32.图2为h7亚型引物探针筛选;
33.图3为h9亚型引物探针筛选;
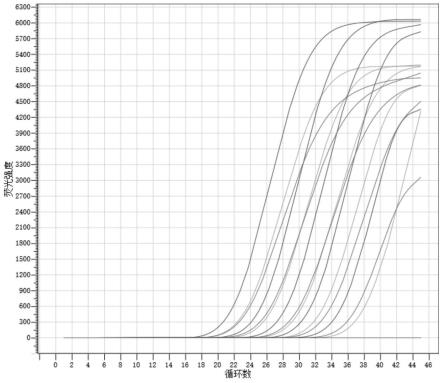
34.图4为流感病毒h5、h7、h9亚型三重实时荧光定量pcr扩增曲线图;
35.图5为流感病毒h5亚型引物探针特异性的实验结果示意图;
36.图6为流感病毒h7亚型引物探针特异性的实验结果示意图;
37.图7为流感病毒h9亚型引物探针特异性的实验结果示意图;
38.图8为流感病毒h5亚型引物探针灵敏度的实验结果示意图;
39.图9为流感病毒h7亚型引物探针灵敏度的实验结果示意图;
40.图10为流感病毒h9亚型引物探针灵敏度的实验结果示意图。
具体实施方式
41.下面将结合实施方式和实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施方式和实施例仅用于说明本发明,而不应视为限制本发明的范围。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
42.第一方面,本发明提供了一种检测流感病毒h5、h7、h9亚型的引物和探针,所述引物包括第一引物对、第二引物对和第三引物对;
43.所述第一引物对具有如seq id no.1和seq id no.2所示的核酸序列;所述第二引物对具有如seq id no.3和seq id no.4所示的核酸序列;所述第三引物对具有如seq id no.5和seq id no.6所示的核酸序列;
44.所述探针包括第一探针、第二探针和第三探针;
45.所述第一探针具有如seq id no.7所示的核酸序列;所述第二探针具有如seq id no.8所示的核酸序列;所述第三探针具有如seq id no.9所示的核酸序列。
46.在一些优选的实施方式中,所述探针的5’端连接有荧光报告基团,3’端连接有荧光淬灭基团。
47.在一些优选的实施方式中,所述荧光报告基团包括但不限于fam、cy5或hex;所述荧光淬灭基团包括但不限于tamra、bhq1或bhq2;或者采用本领域技术人员所熟知的其他荧光报告基团和荧光淬灭基团。
48.本发明提供的检测流感病毒h5、h7、h9亚型的引物和探针,特异性强,灵敏度高,能够用于制备检测流感病毒h5、h7、h9亚型的产品,实现对流感病毒h5、h7、h9亚型的检测。
49.第二方面,本发明提供了上述引物和探针在制备流感病毒h5、h7、h9亚型检测产品中的应用;
50.优选地,所述检测产品包括数字pcr试剂盒。
51.本发明提供的检引物和探针,特异性强,灵敏度高,因此,能够用于制备检测流感病毒h5、h7、h9亚型的产品,进而实现对流感病毒h5、h7、h9亚型的检测。
52.第三方面,本发明提供了一种试剂,包括所述的引物和探针。
53.本发明中对于试剂的具体种类不进行限定,包括上述引物和探针即可,可以用于流感病毒h5、h7、h9亚型。上述试剂由于含有上述引物和探针,因此具有特异性强,灵敏度高的优点。
54.第四方面,本发明提供了一种数字pcr试剂盒,包括所述的引物和探针以及数字
pcr反应预混液。
55.在一些优选的实施方式中,所述数字pcr反应预混液,包括:buffer、mg
2+
、dntps、热启动taq酶和逆转录酶。
56.将本发明提供的数字pcr试剂盒采用微滴数字pcr的方式,能够实现对h5/h7/h9亚型病毒样本的精准检测,以达到对流感病毒进行早期鉴别诊断以及疫情监测的目的,从而为流感病毒诊断提供一种新方法。
57.在一些优选的实施方式中,还包括阳性对照品,用于监控检测样本的均一性,保证检测结果的可比性。
58.本发明中,阳性对照品包括h5亚型h基因片段、h7亚型h基因片段和h9亚型h基因片段。
59.在一些优选的实施方式中,所述阳性对照品为含有h5亚型h基因片段、h7亚型h基因片段和h9亚型h基因片段的重组质粒。
60.在一些优选的实施方式中,还包括阴性对照品,用于监控检测试剂是否被污染。
61.本发明中,阴性对照品为无核酸酶水。
62.下面通过具体的实施例和对比例进一步说明本发明,但是,应当理解为,这些实施例仅仅是用于更详细地说明之用,而不应理解为用于以任何形式限制本发明。
63.实施例1
64.一种检测流感病毒h5、h7、h9亚型的引物和探针,包括第一引物对h5-f、h5-r;第二引物对h7-f、h7-r;第三引物对h9-f、h9-r;第一探针h5-p;第二探针h7-p;第三探针h9-p,引物和探针的序列如表1所示。
65.表1
66.h5-fgaatcaataggaacttaccaaatactg(seq id no.1)h5-rctgcattgtaacgacccattg(seq id no.2)h5-ptttattcaacagtggcgagttccc(seq id no.7)h7-fctaattgatggttggtatggtttc(seq id no.3)h7-raattgccgattgagtgctttt(seq id no.4)h7-pcagaatgcacagggagagggaactgct(seq id no.8)h9-fctggaatctgaagrracttacaaa(seq id no.5)h9-ragaacaaraaggcagcaaacc(seq id no.6)h9-pachatttattcgactgtygcctc(seq id no.9)
67.对比例1-1~对比例1-3
68.对比例1-1对比例1-3分别提供了一种检测流感病毒h5的引物和探针,引物和探针的序列如表2所示。
69.表2
[0070][0071]
对比例2-1~对比例2-3
[0072]
对比例2-1~对比例2-3分别提供了一种检测流感病毒h7的引物和探针,引物和探针的序列如表3所示。
[0073]
表3
[0074][0075][0076]
对比例3-1~对比例3-3
[0077]
对比例3-1~对比例3-3分别提供了一种检测流感病毒h9的引物和探针,引物和探针的序列如表4所示。
[0078]
表4
[0079][0080]
实施例2
[0081]
一种试剂盒,包括实施例1的引物和探针、反应预混液、阳性对照品和阴性对照品。其中反应预混液为:qscript xlt one-step rt-qpcr toughmix(quantabio)。
[0082]
阳性对照品:含有h5亚型h基因片段、h7亚型h基因片段、h9亚型h基因片段的重组质粒。
[0083]
阴性对照品:无核酸酶水。
[0084]
试验例1引物探针筛选
[0085]
1.扩增方法
[0086]
病毒核酸提取采用磁珠法,使用杭州博日科技股份有限公司生产的病毒核酸提取试剂盒对流感病毒样本进行核酸提取。按如表5配制数字pcr反应体系,总体积25ul。
[0087]
表5
[0088][0089][0090]
数字pcr反应
[0091]
微滴生成:
[0092]
将25μl反应体系加入到微滴反应芯片中,盖上盖子,转移至naica自动化微滴芯片数字pcr仪器中,同时打开压力泵调至数值1.28左右,压力增加到大气压+1000mbar生成微滴。
[0093]
pcr扩增:
[0094]
微滴生成后进入pcr扩增程序,如表6所示。
[0095]
表6
[0096][0097]
扩增结束后,取出芯片放入微滴读取仪,进行数据读取。
[0098]
2.引物探针筛选
[0099]
分别提取流感病毒h5、h7、h9亚型的核酸,对于流感病毒h5亚型核酸,分别以实施例1中第一引物对和第一探针、对比例1-1~对比例1-3的引物探针按照上述扩增方法进行扩增,结果如图1所示。(图1曲线从左至右依次为实施例1、对比例1-1、对比例1-2、对比例1-3的扩增曲线)。
[0100]
对于流感病毒h7亚型核酸,分别以实施例1中第二引物对和第二探针、对比例2-1~对比例2-3的引物探针按照上述扩增方法进行扩增,结果如图2所示。(图2曲线从左至右依次为实施例1、对比例2-1、对比例2-2、对比例2-3的扩增曲线)。
[0101]
对于流感病毒h9亚型核酸,分别以实施例1中第三引物对和第三探针、对比例3-1~对比例3-3的引物探针按照上述扩增方法进行扩增,结果如图3所示。(图3曲线从左至右依次为实施例1、对比例3-1、对比例3-2、对比例3-3的扩增曲线)。
[0102]
制备流感病毒h5、h7、h9亚型的混合核酸,对于流感病毒h5、h7、h9亚型的混合核酸,采用实施例1提供的引物和探针按照上述扩增方法进行扩增,混合核酸浓度依次稀释
10-1
,10-2
,10-3
,10-4
,10-5
,结果如图4所示。
[0103]
从图中可以看出,h5、h7、h9亚型引物和探针组合后的扩增曲线相互不影响,并且荧光强度高,曲线呈s型,说明筛选出来的引物对和探针非常好。
[0104]
试验例2数字pcr特异性实验
[0105]
选择与流感病毒核酸序列具有同源性,引起相同或相似临床症状的呼吸道病毒甲型h1n1流感病毒、甲型h3n2流感病毒、甲型h5n1流感病毒、甲型h7n9流感病毒、甲型h9n2流感病毒,乙型流感病毒,新型冠状病毒,同时设置阳性对照和阴性对照。分别采用实施例1提供的引物和探针进行检测,结果如图5、图6和图7所示(图5中,横坐标分别代表:1.h5n1,2.h1n1,3.h3n2,4.h7n9,5h9n2,6.乙型流感病毒,7新型冠状病毒,8阴性对照;图6中,横坐标分别代表:1.h7n9,2.h1n1,3.h3n2,4.h5n1,5h9n2,6.乙型流感病毒,7新型冠状病毒,8阴性对照;图7中,横坐标分别代表:1.h9n2,2.h1n1,3.h3n2,4.h5n1,5h7n9,6.乙型流感病毒,7新型冠状病毒,8阴性对照),从图中可以看出,仅能检测出h5、h7、h9,其它各种模板均为阴性,表明本发明的检测方法与其它病毒没有交叉反应,具有较强的特异性。
[0106]
试验例3数字pcr灵敏度实验
[0107]
采用流感病毒h5、h7、h9亚型病毒阳性样品依次进行4倍梯度稀释,稀释至4096倍,分别以实施例1提供的引物和探针,采用试验例1给出的检测方法进行检测,结果如图8、图9和图10所示(图8中,横坐标分别代表:1.h5n1核酸,2.h5n1核酸稀释4倍,3.h5n1核酸稀释16倍,4.h5n1核酸稀释64倍,5.h5n1核酸稀释256倍,6.h5n1核酸稀释1024倍,7.h5n1核酸稀释4096倍;图9中,横坐标分别代表:1.h7n9核酸,2.h7n9核酸稀释4倍,3.h7n9核酸稀释16倍,4.h7n9核酸稀释64倍,5.h7n9核酸稀释256倍,6.h7n9核酸稀释1024倍,7.h7n9核酸稀释4096倍;图10中,横坐标分别代表:1.h9n2核酸,2.h9n2核酸稀释4倍,3.h9n2核酸稀释16倍,4.h9n2核酸稀释64倍,5.h9n2核酸稀释256倍,6.h9n2核酸稀释1024倍,7.h9n2核酸稀释4096倍)。结果显示本体系h5亚型在1拷贝的模板量下,可以生产稳定的扩增(图8中的编号6)。h7亚型在2拷贝的模板量下,可以生产稳定的扩增(图9中的编号6)。h9亚型在1拷贝的模板量下,可以生产稳定的扩增(图10中的编号6)。
[0108]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1