非小细胞肺癌miRNA标志物及其应用的制作方法
非小细胞肺癌mirna标志物及其应用
技术领域
1.本发明涉及生物医学技术领域,尤其是涉及非小细胞肺癌mirna标志物及其应用。
背景技术:
2.在我国,肺癌发病率居恶性肿瘤的首位,大多数肺癌患者发现时已经为晚期,失去了手术治疗机会,其5年存活率仅为15-20%,而早期肺癌患者的5年生存率达40%左右。因此,早期发现和早期治疗对于提高肺癌患者的生存率至关重要。由于缺乏有效的早期诊断方法,在过去的几十年中,nsclc患者的存活率没有显著提高。
3.目前,肺癌检测和筛查的手段主要是通过x胸片、核磁共振成像和低剂量螺旋ct等影像学诊断筛查,然而,这2种筛查手段的特异性和准确性并不太理想。
4.微小rna(microrna,mirna)是一类内源性高度保守的长度为18-25个核苷酸的非编码单链小分子rna,主要通过转录后机制调控靶基因的翻译或表达,从而在肿瘤的发生、发展中有致癌和抑癌mirna的不同作用。mirna非常稳定地存在于人类血浆和血清中,并且能够抵抗rna内切酶的降解,可作为诊断肺癌的新的血清标志物指标。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的在于提供非小细胞肺癌mirna标志物及其应用,为非小细胞肺癌的特异性检测或辅助诊断提供新的途径和方法。
7.本发明提供的技术方案如下:
8.在一个方面,本发明提供了非小细胞肺癌mirna标志物,所述mirna标志物至少包括mir-3149;优选地,所述mirna标志物包括mir-3149和mir-6803-5p的组合。在一个实施方案中,所述mirna标志物由mir-3149和mir-6803-5p组成。
9.本发明所述mirna(mir-3149和/或mir-6803-5p)的序列为已知序列,在数据库mirbase中可获得其相应的序列。
10.本发明发现外周血mirna标志物(mir-3149和/或mir-6803-5p)在诊断为非小细胞肺癌患者的外周血中的表达与在对照样本中的表达相比显著上调;首次提出诊断标志物mir-3149可用于人群中非小细胞肺癌的检测或诊断的标志物,其不仅在非小细胞肺癌人群与健康人群中的表达量存在显著差异,而且在非小细胞肺癌中的敏感性可达到79.5%,可靠性高。
11.在一个优选的实施方案中,所述mirna标志物为血清mirna标志物。
12.在另一个方面,本发明提供了所述非小细胞肺癌mirna标志物在用于制备检测和/或诊断非小细胞肺癌的试剂盒中的应用。mir-3149可单独或与mir-6803-5p组合作为标志物用于临床非小细胞肺癌的检测或辅助诊断,因此,其可用于制备检测和/或诊断非小细胞肺癌的试剂盒。
13.在另一个方面,本发明提供了检测所述mirna标志物的产品在制备用于检测和/或
诊断非小细胞肺癌的试剂盒中的应用。具体地,检测所述mirna标志物的产品为能够检测所述mirna标志物的表达和/或转录的产品。
14.在一些具体的实施方案中,检测所述mirna标志物的产品为适用于如下方法的试剂:通过使用qrt-pcr、数字pcr、荧光染料法、印记杂交、原位杂交、阵列杂交、基因芯片或新一代测序来检测表达水平的试剂。在本发明中,使用适用于检测生物样品中的rna表达水平的任意技术可以测量样品中mirna的表达水平。用于测定生物样品(细胞、组织、体液)中rna表达水平的合适技术是本领域技术人员众所周知的。
15.在一个实施方案中,所述产品包含pcr扩增引物、探针、基因芯片中的一种或多种;优选地,所述产品为对所述mirna的表达量进行定量的试剂。更优选地,所述试剂适用于实时荧光定量pcr的试剂,包括扩增引物和/或探针。在本发明中,所述表达量为相对表达量,为相对于内参基因的表达量。
16.在一个实施方案中,所述试剂包含用于mir-3149/或mir-6803-5p扩增的引物和/或探针。
17.在另一个方面,本发明提供了一种非小细胞肺癌检测试剂盒,所述试剂盒含有用于mir-3149和/或mir-6803-5p扩增的引物和/或探针。
18.在一个具体的实施方案中,mir-3149的引物探针的序列如seq id no.1所示,mir-6803-5p的引物探针如seq id no.2所示。
19.本发明同时也提供了一种用于检测非小细胞肺癌标记物的mirna的探针组合,所述探针组合为seq id no.1和seq id no.2的组合。
20.在一个实施方案中,所述试剂盒还包含内参基因的扩增引物和/或探针;优选地,所述内参基因选自u6、gapdh及β-actin中的至少一种。
21.在一个实施方案中,所述试剂盒还包括rna提取缓冲液、rna反转录反应液和qpcr反应液中的至少一种。
22.针对受试者是否患有非小细胞肺癌或具有患非小细胞肺癌高风险的检测或诊断,可以通过测量来自所述受试者的测试样本中的mir-3149或mir-3149和mir-6803-5p的水平来诊断受试者是否患有非小细胞肺癌或具有患非小细胞肺癌高风险,其中与对照样本(健康人群样本)中的水平相比,受试样品中mir-3149或mir-3149和mir-6803-5p表达水平显著更高,指示着受试者患有非小细胞肺癌或具有患非小细胞肺癌高风险。
23.在本发明中,所述mirna的表达水平是浓度、log(浓度)、ct/cq数、2的ct/cq数次方中的任一种;所述样本为组织样本或体液样本,所述体液样本优选为血液样本,可选地,所述血液样本为血清样本或血浆样本。
24.在本发明中,所述非小细胞肺癌包括鳞状细胞肺癌、腺癌肺癌中的一种或多种。
25.在本发明中,可以通过包括以下步骤的方法获得所述mirna标志物的表达水平:
26.(a)采集空腹静脉血样本,分离血清;
27.(b)提取血清rna;
28.(c)以提取的rna为模板合成cdna;
29.(d)以合成的cdna为模板,采用所述mirna的特异性引物和探针,以实时荧光定量pcr法检测所述mirna分子标志物的表达量。
30.具体地,同时以u6 snrna作为内参进行rt-qpcr反应,根据荧光信号达到设定的阈
值时所经历的循环数,对待测样本中mirna的含量进行定量;血清mirna的相对表达量用2-δδct
表示。
31.有益效果:
32.本发明首次提供了对非小细胞肺癌具有较高诊断价值的生物标记物中mir-3149,非小细胞肺癌(nsclc)患者血清中mir-3149和mir-6803-5p的表达水平显著高于健康人组,差异有统计学意义(p<0.001)。血清mir-3149和mir-6803-5p在nsclc中的敏感性分别达到了79.5%和48.7%。因此,血清mir-3149和mir-6803-5p可以作为nsclc的肿瘤标志物指标;mir-3149单独或者与mir-6803-5p组合可以作为非小细胞肺癌检测或诊断用的新生物学标记。
33.此外,本发明还提供了用于检测mirna标志物的试剂盒,可以更加方便的检测mirna标志物的表达水平,为非小细胞肺癌的临床诊断和治疗提供基础。
附图说明
34.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
35.图1为本发明实施例提供的nsclc患者和健康人血清中mir-3149表达水平比较结果;
36.图2为本发明实施例提供的nsclc患者和健康人血清中mir-6803-5p表达水平比较结果;
37.图3为本发明实施例提供的nsclc患者和健康人血清中mir-3149表达水平的受试者工作曲线(roc)示意图;
38.图4为本发明实施例提供的nsclc患者和健康人血清中mir-6803-5p表达水平的受试者工作曲线(roc)示意图。
具体实施方式
39.下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
40.本发明中,若非特指,所采用的原料和设备等均可从市场购得或是本领域常用的。下述实施例中的方法,如无特别说明,均为本领域的常规方法。
41.实施例
42.1.研究对象
43.1.1病例组:首都医科大学附属北京胸科医院收治确诊的nsclc患者78例,其中男性58例、女性20例,平均年龄65.1岁;其中腺癌38例,鳞癌40例;早期(i+ii期)患者20例,晚期(iii+iv期)患者58例。所有nsclc患者为初次就诊,并经过病理学确诊为nsclc,以往未做过任何手术、化疗或放疗。
44.1.2健康对照组:北京胸科医院体检健康职工44名,其中男性21名、女性23名,平均年龄38.2岁,血压、血脂、血糖、肝肾功能、血常规等指标正常。
45.2.标本采集
46.采集nsclc患者和健康人空腹静脉血标本4ml,在2小时内离心分离血清,然后放置于-80℃超低温冰箱中保存,最后集中进行rna的提取。
47.3.血清rna的提取
48.使用mirneasy serum/plasma试剂盒(qiagen,德国)提取血清中的总rna。
49.4.实时荧光定量pcr(qrt-pcr)检测
50.应用qrt-pcr法对78例nsclc患者和44名健康人血清中mir-3149、mir-572、mir-638、mir-6803-5p、mir-7704的表达量进行检测。
51.qrt-pcr实验以合成的cdna为模板,同时以u6作为内参照,qrt-pcr反应体系为20μl。
52.pcr反应循环条件:95℃5分钟,95℃30秒,60℃1分钟,共进行40个循环;然后95℃15秒,60℃1分钟,95℃15秒,1个循环。qrt-pcr实验数据经过abi7500pcr仪软件进行分析,每个cdna样本的表达量检测均重复3次,血清mirna的相对表达量用2-δδct
表示。
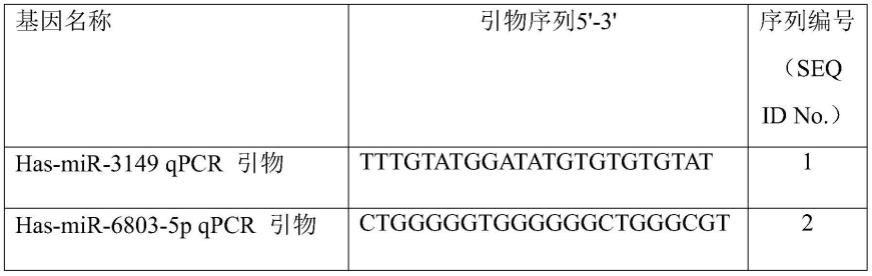
53.所使用的mirna荧光定量pcr的引物序列如下:
[0054][0055]
5.结果
[0056]
5.1nsclc患者血清中mir-572、mir-638和mir-7704的表达水平与健康人比较无统计学差异(p>0.05)。nsclc患者血清中mir-3149和mir-6803-5p的表达水平显著高于健康人对照,差异有统计学意义(p<0.001)(见表1、图1、图2)。
[0057]
表1.血清mir-3149和mir-6803-5p的检测结果m(qr)
[0058][0059]
注:nsclc与健康人对照比较,
a,b
p<0.001。
[0060]
5.2如表2所示,血清mir-3149对nsclc检测的敏感性为79.5%、特异性为75.0%;血清mir-6803-5p对nsclc检测的敏感性为48.7%、特异性为75.0%。
[0061]
表2.血清mir-3149和mir-6803-5p在nsclc中的敏感性、特异性
[0062][0063]
实施例3.mirna标志物mir-3149和mir-6803-5p的roc
[0064]
本发明以mir-3149和mir-6803-5p相对表达量为基础,通过roc曲线分析各自的诊断效果(图3、图4)。具体如下:
[0065]
绘制标志物的roc曲线,依据其曲线下面积来判断标志物非小细胞肺癌的诊断效果。
[0066]
结果显示单个mir-3149的auc是0.831;敏感度79.5%,特异度75%。
[0067]
结果显示单个mir-6803-5p的auc是0.765;敏感度48.7%,特异度75%。
[0068]
本发明发现血清mir-3149和mir-6803-5p可作为nsclc的肿瘤标记物,可用于nsclc的早期诊断指标。本发明所提供的2种标记物在人的血清中稳定存在,此2种标志物及其引物可用于制备nsclc早期诊断试剂盒,用于早期nsclc的辅助诊断参考指标。
[0069]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1