一种融合细胞外囊泡类似物的制备方法及其应用
1.本发明属于生物医药技术领域,具体涉及一种融合细胞外囊泡类似物的制备方法及其应用。
背景技术:
2.细胞源性微囊泡是细胞在激活、损伤或调信时经出芽方式释放的一类直径介于100~1000nm的膜性囊泡。细胞源性微囊泡携带母体细胞特征性生物信息分子(如脂质,蛋白质,dna,mrna,mirna),并可作为细胞间运输载体将这些生物分子传递给其他细胞。基于其生物信息分子传递功能,近来年越来越多的学者致力于将细胞源性微囊泡改造成药物释放纳米载体。与人工合成的纳米载体相比,细胞源性微囊泡具有多重优势:1)在药物到达肿瘤部位前,细胞源性微囊泡的双层磷脂结构可保护包裹于微囊泡内的药物,防止药物被降解或被代谢;2)细胞源性微囊泡到达肿瘤部位后,其双层磷脂结构可与肿瘤细胞膜直接融合,促进微囊泡内药物的释放;3)细胞源性微囊泡可透过生理屏障(如血脑屏障),并将药物有效释放于脑组织治疗脑部疾患;4)研究表明,未经修饰的细胞源性微囊泡即具有一定的肿瘤靶向性;5)细胞源性微囊泡具有更强的循环稳定性,可有效延长药物在体内的半衰期;6)最重要的是,多项临床试验结果表明,自身来源的微囊泡几乎没有免疫原性和毒性,而人工合成的纳米载体在免疫原性和毒性方面仍然存在不可回避的安全隐患。
3.当前,越来越多的证据证明usp14在肿瘤发生发展过程中具有重要调节作用,同时鉴于usp14活性位点内半胱氨酸巯基的活泼性,有很多研究已经将usp14的抑制剂作为抗肿瘤药物研究的新方向。但是静脉给药usp14抑制剂,药物会广泛的分布在体内,使得药物利用率不高,缺少靶向性,同时,也没有相关文献报道usp14抑制剂用于脑胶质瘤的防治。
4.中国专利文献cn 108619114 a中公开了一种负载地塞米松的巨噬细胞源微囊泡及其制备方法和应用,该方案中利用于鼠巨噬细胞系分泌的天然细胞微囊泡包载地塞米松,通过抑制促炎信号通路的活化和炎症细胞的浸润达到改善肾脏炎症的目的;但是存在着微囊泡产率较低,靶向性较差等问题。
5.有鉴于此,有必要提供一种融合细胞外囊泡类似物的制备方法来解决上述技术问题。
技术实现要素:
6.本发明的目的在于克服现有技术的不足,提供一种融合细胞外囊泡类似物的制备方法及其应用,解决现有的天然细胞微囊泡产率较低、载药后,靶向性较差等问题。
7.本发明的第一个目的在于提供一种融合细胞外囊泡类似物的制备方法。
8.一种融合细胞外囊泡类似物的制备方法,包括如下步骤:
9.s1、细胞融合:将单核细胞溶液与神经干细胞溶液混匀后,经挤压、通过滤膜后,得到融合细胞外囊泡类似物粗制液;
10.s2、融合细胞外囊泡类似物的纯化:将步骤s1中得到的融合细胞外囊泡类似物粗
制液进行高速离心,沉淀用缓冲液洗涤后,得到融合细胞外囊泡类似物。
11.进一步地,步骤s1中,所述单核细胞为来源于人单核细胞白血病细胞系thp-1细胞;所述神经干细胞为来源于人神经干细胞系rencell vm细胞。
12.进一步地,步骤s1中,所述单核细胞溶液与所述神经干细胞溶液混合的体积比为1:1;其中,所述单核细胞溶液中细胞个数为1
×
107个/ml,所述神经干细胞溶液中细胞个数为1
×
107个/ml。
13.进一步地,步骤s1中,经挤压后、依次通过10μm、5μm、1μm、200nm的滤膜。
14.进一步地,步骤s2中,所述高速离心的参数如下:100000~120000g,2~3h。
15.本发明的第二个目的在于提供一种融合细胞外囊泡类似物。
16.所述融合细胞外囊泡类似物由上述任一项所述的融合细胞外囊泡类似物的制备方法制得。
17.本发明的第三个目的在于提供一种负载usp14抑制剂的融合细胞外囊泡类似物。
18.所述负载usp14抑制剂的融合细胞外囊泡类似物由上述所述的融合细胞外囊泡类似物包载usp14抑制剂所制得。
19.本发明的第四个目的在于提供一种负载usp14抑制剂的融合细胞外囊泡类似物的制备方法。
20.所述制备方法具体如下:将融合细胞外囊泡类似物粗制液与usp14抑制剂溶液混合后,进行超声处理,超声完成后,在37℃孵育1h,即可得到负载usp14抑制剂的融合细胞外囊泡类似物粗制液,所述负载usp14抑制剂的融合细胞外囊泡类似物粗制液经上述骤s2中的纯化步骤,即可得到负载usp14抑制剂的融合细胞外囊泡类似物。
21.进一步地,所述usp14抑制剂溶液的终浓度为60μmol/l,所述usp14抑制剂为iu1-248。
22.本发明的第四个目的在于提供上述负载usp14抑制剂的融合细胞外囊泡类似物在制备治疗脑胶质瘤药物中的应用。
23.与现有技术相比,本发明具有如下优点:
24.本发明利用来源于人单核细胞白血病细胞系thp-1细胞和来源于人神经干细胞系rencell vm细胞,经挤压、通过不同孔径后得到融合细胞外囊泡类似物,然后包载usp14抑制剂,得到负载usp14抑制剂的融合细胞外囊泡类似物,所述融合细胞外囊泡类似物具有更强的胶质瘤趋化性,当经鼻内给药后,负载usp14抑制剂的融合细胞外囊泡类似物能绕过血脑屏障,通过三叉神经与嗅神经鼻内分支到达脑胶质瘤处,然后释放usp14抑制剂,解除usp14对于脑胶质瘤的恶性进展促进作用,从而缓解脑胶质瘤的生长与扩散。
附图说明
25.为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作简单的介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
26.图1为本发明实施例1制得的的融合细胞外囊泡类似物经共聚焦激光扫描显微镜检测结果,其中,图(a)为pkh67染料染色人神经干细胞系rencell vm细胞检测结果;图(b)
为dil染料染色人单核细胞白血病细胞系thp-1细胞检测结果;图(c)为融合细胞外囊泡类似物检测结果。
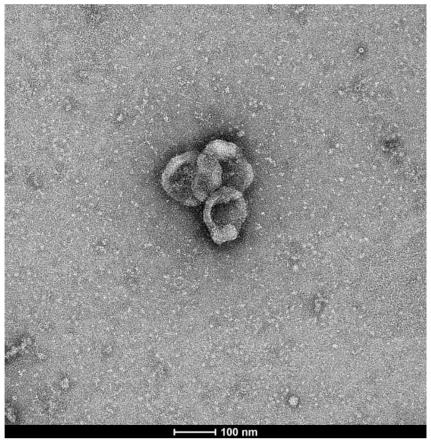
27.图2为本发明实施例2制得的负载usp14抑制剂的融合细胞外囊泡类似物的透射电镜结果图。
28.图3为本发明实施例2制得的负载usp14抑制剂的融合细胞外囊泡类似物的粒径结果图。
29.图4为本发明实施例3中小鼠经鼻给药负载usp14抑制剂的融合细胞外囊泡类似物后胶质瘤染色结果图。
具体实施方式
30.下面将结合本发明实施例中的附图对本发明实施例中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例,基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
31.本发明中的人神经干细胞系rencell vm细胞由南京医科大学神经生物研究所赠与。
32.本发明所使用的其他常规试剂和设备,如无特殊说明,均可市售获得。
33.实施例1融合细胞外囊泡类似物的制备
34.1.1细胞融合:将来源于人单核细胞白血病细胞系thp-1细胞溶液(1
×
107个/ml)与来源于人神经干细胞系rencell vm细胞溶液(1
×
107个/ml)等体积混匀后,经挤压、依次通过10μm、5μm、1μm、200nm孔径的滤膜,得到融合细胞外囊泡类似物粗制液;
35.1.2融合细胞外囊泡类似物的纯化:将步骤1.1中得到的融合细胞外囊泡类似物粗制液进行高速离心,所述高速离心的参数如下:100000~120000g,2~3h;沉淀用pbs缓冲液洗涤后,重复操作两次,即可得到融合细胞外囊泡类似物(coated ev mimics)。
36.用pkh67染料和dil染料分别染色人神经干细胞系rencell vm细胞、人单核细胞白血病细胞系thp-1细胞,用共聚焦激光扫描显微镜观察融合前和融合后细胞的情况,结果如图1所示。
37.从图中可以看出,人神经干细胞系rencell vm细胞和人单核细胞白血病细胞系thp-1细胞能融合得到融合细胞外囊泡类似物。
38.实施例2负载iu1-248的融合细胞外囊泡类似物的制备
39.将实施例1中制得的融合细胞外囊泡类似物粗制液与iu1-248溶液(终浓度为60μmol/l)混合后,进行超声处理,所述超声处理的参数如下:频率25khz,功率240w,进行6个循环,每个循环是4s的脉冲,2s的暂停,在冰上冷却2min;超声完成后,在37℃孵育1h,即可得到负载iu1-248的融合细胞外囊泡类似物粗制液,所述负载iu1-248的融合细胞外囊泡类似物粗制液进行高速离心,所述高速离心的参数如下:100000~120000g,2~3h;沉淀用pbs缓冲液洗涤后,重复操作两次,即可得到负载iu1-248的融合细胞外囊泡类似物(coated ev mimics/iu1-248)。
40.将制得的负载iu1-248的融合细胞外囊泡类似物(coated ev mimics/iu1-248)进行透射电镜观察和粒径测定,结果如图2和3所示。
41.从图2中可以看出,负载iu1-248的融合细胞外囊泡类似物有双膜层结构,从图3中可以看出,负载iu1-248的融合细胞外囊泡类似物的粒径大小在150nm左右;结果表明,融合后的细胞外囊泡类似物具有外囊泡的结构。
42.对比例1负载iu1-248的thp-1单核细胞的制备
43.将来源于人单核细胞白血病细胞系thp-1细胞溶液(1
×
107个/ml)经挤压、依次通过10μm、5μm、1μm、200nm孔径的滤膜,得到thp-1单核细胞溶液;然后与iu1-248溶液(终浓度为60μmol/l)混合后,进行超声处理,所述超声处理的参数如下:频率25khz,功率240w,进行6个循环,每个循环是4s的脉冲,2s的暂停,在冰上冷却2min;超声完成后,在37℃孵育1h,即可得到负载iu1-248的thp-1单核细胞,所述负载iu1-248的thp-1单核细胞进行高速离心,所述高速离心的参数如下:100000~120000g,2~3h;沉淀用pbs缓冲液洗涤后,重复操作两次,即可得到负载iu1-248的thp-1单核细胞。
44.对比例2负载iu1-248的rencell vm神经干细胞的制备
45.将来源于人神经干细胞系rencell vm细胞溶液(1
×
107个/ml)经挤压、依次通过10μm、5μm、1μm、200nm孔径的滤膜,得到rencell vm神经干细胞溶液;然后与iu1-248溶液(终浓度为60μmol/l)混合后,进行超声处理,所述超声处理的参数如下:频率25khz,功率240w,进行6个循环,每个循环是4s的脉冲,2s的暂停,在冰上冷却2min;超声完成后,在37℃孵育1h,即可得到负载iu1-248的rencell vm神经干细胞,所述负载iu1-248的rencell vm神经干细胞进行高速离心,所述高速离心的参数如下:100000~120000g,2~3h;沉淀用pbs缓冲液洗涤后,重复操作两次,即可得到负载iu1-248的rencell vm神经干细胞。
46.实施例3负载iu1-248的融合细胞外囊泡类似物经鼻给药小鼠疗效实验
47.选取荷瘤小鼠30只,分成3组,每组10只;实验组中负载iu1-248的融合细胞外囊泡类似物经dir染料染色,给药剂量为40mg/kg,空白对照组给药相同剂量pbs缓冲液,药物对照组给药相同剂量iu1-248溶液,实验组和空白对照组小鼠经鼻内滴鼻24h,药物对照组经尾脉注射给药24h后,经异氟烷气体麻醉后,注射荧光素钠以标记荧光素酶阳性的脑胶质瘤u87细胞在活体成像中显色,以此来检测载药融合细胞外囊泡类似物在荷瘤小鼠经鼻给药后对于胶质瘤的趋化性能,结果如图4所示。
48.从图中可以看出,实验组中负载iu1-248的融合细胞外囊泡类似物发光面积最小,这是由于其能直接靶向小鼠脑胶质瘤,释放iu1-248从而抑制脑胶质瘤的生长;相比于药物对照组经尾脉注射iu1-248,靶向性更好,治疗效果更加。
49.实施例4
50.选取荷瘤小鼠30只,分成3组,每组10只;每组分别经鼻内滴鼻实施例2制得的负载iu1-248的融合细胞外囊泡类似物、对比例1中制得的负载iu1-248的thp-1单核细胞和对比例2中制得的负载iu1-248的rencell vm神经干细胞24h,给药剂量为40mg/kg,经异氟烷气体麻醉后,注射荧光素钠以标记荧光素酶阳性的脑胶质瘤u87细胞在活体成像中显色,检测每组小鼠脑胶质瘤荧光染色后发光面积的大小,结果如下表1所示:
51.表1小鼠脑胶质瘤荧光染色后荧光发光面积的大小结果
[0052] 小鼠脑胶质瘤荧光染色后荧光发光面积(cm3)实施例10.003实施例20.008
实施例30.007
[0053]
从表中的结果可以看出,实施例1中制得的负载iu1-248的融合细胞外囊泡类似物靶向性更好,治疗效果更好。
[0054]
以上实施例,仅为本发明的具体实施方式,用以说明本发明的技术方案,而非对其限制,本发明的保护范围并不局限于此,尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,其依然可以对前述实施例所记载的技术方案进行修改或可轻易想到变化,或者对其中部分技术特征进行等同替换;而这些修改、变化或者替换,并不使相应技术方案的本质脱离本发明实施例技术方案的精神和范围,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1