一类氮铋辛环烷基铋类化合物及其合成方法
1.本发明属于有机合成领域,具体涉及一类氮铋辛环烷基铋类化合物及其合成方法。
背景技术:
2.过渡金属催化的还原偶联反应,是指在过渡金属催化剂与还原剂参与下,两个亲电试剂之间的偶联反应。过渡金属催化的还原偶联反应由于具有步骤经济性,化学选择性,底物官能团适用性广等优点已被广泛应用于精细化学品、药品、农用化学品以及多功能有机分子和复杂天然产品的合成。金属有机试剂作为一类构建碳-碳键以及碳-杂键中最为常用的偶联试剂目前已被广泛研究,目前已知的有机金属试剂中,有机锂试剂,格式试剂,有机锌试剂等绝大部分金属试剂对水,氧气较为敏感,以及官能团的耐受性差,这限制了其进一步的应用。氮-铋辛环有机铋卤化物由于具有独特的耐水抗氧的优势,因此结合还原偶联反应优势与氮
‑ꢀ
铋辛环有机铋卤化物优势,使得合成一类耐水抗氧型有机铋烷基偶联试剂并使之成为广泛应用的烷基化试剂成为可能。
技术实现要素:
3.本发明公开了一种氮铋辛环烷基铋类化合物的合成方法,该方法以氮-铋辛环有机铋氯和卤代烷烃为反应物,以n,n-二甲基甲酰胺为溶剂,在100℃条件下反应合成一系列新型氮
‑ꢀ
铋辛环铋烷基化合物。该反应可以在100℃下3小时内以中等至较高的产率进行。该合成方法具有条件温和,反应速度快,产率高,易操作,易于放大等优点,有利于实现其工业化生产。
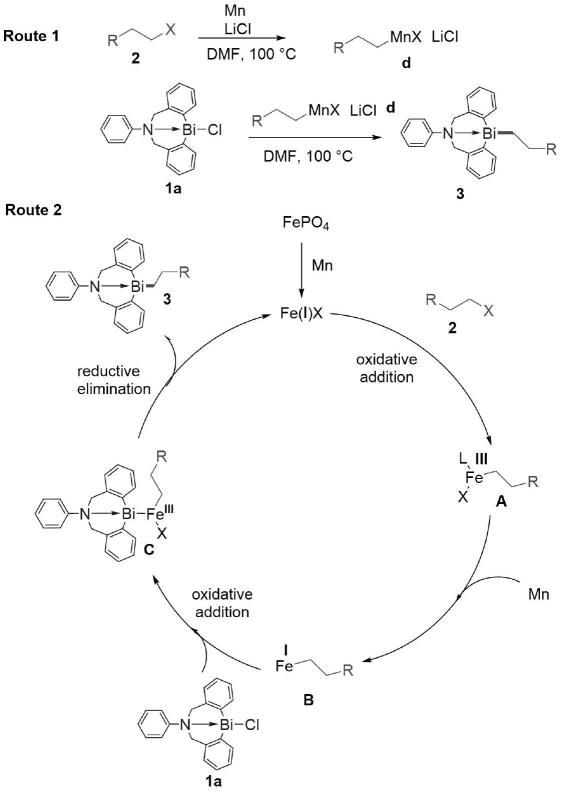
4.为了达到在温和条件下实现快速反应,并进而进行转化及应用试验,对反应机理的探讨必不可少。通过相关的控制实验,我们提出了两条可能的反应路径。路径一:(1)烷基卤化物在锰和氯化锂作用下形成烷基锰试剂;(2)烷基锰试剂直接与有机铋氯反应得到目标产物。路径二:(1)铁催化剂在锰的作用下被还原为+1价,与烷基卤化物氧化加成得到中间体a; (2)中间体a被锰还原为一价铁b,b与1a氧化加成得到三价铁配合物c;(3)c经过还原消除得到目标产物,同时铁被还原为+1价重新进入循环。
[0005][0006]
上述合成方法中,其中原料氮-铋辛环有机铋氯1a的合成方法如下:
[0007][0008]
上述合成方法中,以氮-铋辛环有机铋氯和卤代烷烃为原料,n,n-二甲基甲酰胺为溶剂, 100℃的温度,氮气氛围下反应12h。
[0009]
以该合成方法合成了一系列氮-铋辛环铋烷基化合物,其中产物结构式如下:
[0010][0011]
其中氮-铋辛环铋烷基合成方法,其特征在于,以氮-铋辛环有机铋氯1a(0.2mmol)和烷基卤代烃2(0.3mmol)为原料,磷酸铁(5mol%)为催化剂,2,2-联吡啶(5mol%)为配体,2.0当量的锰为还原剂,2.0当量的氯化锂为添加剂,在氮气氛围下,100℃反应3小时得到氮-铋辛环铋烷基化合物3a-3ab,产率10-87%。
附图说明
[0012]
图1为本发明的反应原理示意图。
具体实施方式
[0013]
为使本发明的上述特征、优点和目的能够更加明了易懂,下面结合具体实施方式对本发明内容做详细的说明。上面的描述中阐述了许多具体细节以便于充分理解本发明。但是本发明能够以很多不同于在此描述的其他方式来实施,本领域技术人员可以在不违背本发明内涵的情况下做类似改进,因此本发明不受下面公开的具体实施的限制。
[0014]
以下实施例中涉及的反应原料和催化剂,如果没有特殊说明,都为市面上常规的市售商品化试剂。
[0015]
氮-铋辛环铋烷基化合物制备实施例1-28
[0016]
实施例1
[0017]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2a 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 43%。
[0018]
内炔化合物3a的结构表征如下:
[0019]1h nmr(400mhz,cdcl3)δ7.86(d,j=6.9hz,1h),7.26(dd,j=12.3,4.2hz,1h),7.20 (dd,j=8.5,7.0hz,1h),6.97(d,j=8.2hz,1h),6.88
–
6.81(m,1h),4.64(d,j=15.0hz,1h), 4.31(d,j=14.9hz,1h),2.25
–
2.17(m,1h),2.03(ddd,j=16.4,11.5,6.9hz,1h),1.54
–
1.49 (m,1h),1.03
–
0.94(m,2h).
[0020]
13
c nmr(101mhz,cdcl3)δ149.2,145.2,144.6,136.6,129.3,128.9,127.9,127.5,119.9, 115.9,58.2,35.8,30.7,28.5,14.0.
[0021]
实施例2
[0022]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2b 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 73%。
[0023]
实施例3
[0024]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2c 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 47%。
[0025]
实施例4
[0026]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2d 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为87%。
[0027]
实施例5
[0028]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2e 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 36%。
[0029]
实施例6
[0030]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2f0.3 mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 38%。
[0031]
实施例7
[0032]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2g 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为68%。
51%。
[0049]
实施例16
[0050]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2p 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 87%。
[0051]
实施例17
[0052]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2q 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 65%。
[0053]
实施例18
[0054]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2r 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 74%。
[0055]
实施例19
[0056]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2s 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 59%。
[0057]
实施例20
[0058]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2t 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 41%。
[0059]
实施例21
[0060]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2u 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 80%。
[0061]
实施例22
[0062]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2v 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 52%。
[0063]
实施例23
[0064]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2w 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应
3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 10%。
[0065]
实施例24
[0066]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2x 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 54%。
[0067]
实施例25
[0068]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2y 0.3mmol,磷酸铁0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 34%。
[0069]
实施例26
[0070]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2z 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 80%。
[0071]
实施例27
[0072]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2aa 0.3mmol,磷酸铁 0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 19%。
[0073]
实施例28
[0074]
在10ml反应管内加入氮-铋辛环有机铋氯1a 0.2mmol,卤代烷烃2ab 0.3mmol,磷酸铁0.02mmol,2,2-联吡啶0.02mmol,锰粉0.4mmol,氯化锂0.4mmol,氮气氛围下,100℃反应3小时。反应结束后,经柱层析分离得到氮-铋辛环铋烷基化合物,为白色固体,产率为 69%。
[0075]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1