B族链球菌核酸检测试剂盒及其制造方法与流程
b族链球菌核酸检测试剂盒及其制造方法
技术领域:
1.本发明涉及链球菌核酸检测产品制造技术领域,具体的说是一种结构合理、操作简便,能够在保证检测准确性的前提下,显著降低成本及操作复杂度的b族链球菌核酸检测试剂盒及其制造方法。
背景技术:
2.无乳链球菌(streptococcus agalactiae)在兰氏抗原分类中属于b群,b群目前只发现这一种细菌,所以一般也称为b群链球菌(group b streptococcus,gbs)。gbs为一种β溶血的革兰阳性球菌,成对或呈短链状排列,根据细菌的荚膜多糖不同,gbs可分为ia、ib、ic、ii、iii、iv、v、vi、vii、viii和ix等。gbs是孕妇围产期和新生儿感染疾病的致病菌,引起孕产妇的绒毛膜羊膜炎,导致流产、胎膜早破及宫内感染,也可导致新生儿发生肺炎、脑膜炎、败血症等。2018年孕前和孕期保健指南中提到对高危因素的孕妇妊娠35~37周进行gbs筛查。
3.gbs常用的检测方法有抗原检测、显色培养基检测、核酸检测等,其中核酸检测有荧光pcr和常规pcr的方法。荧光pcr需要使用荧光pcr仪,仪器和试剂成本较高;常规pcr的扩增产物一般用琼脂糖凝胶电泳的方法检测,操作比较复杂,不方便医院使用。目前gbs核酸检测试剂一般需要进行核酸提取以提高检测试剂的灵敏度和特异性,操作比较繁琐而且增加了试剂成本。
技术实现要素:
4.本发明针对现有技术中存在的检测成本高、检测周期长、操作复杂等问题,提出了一种能够在保证检测准确性的前提下,显著降低成本及操作复杂度的b族链球菌核酸检测试剂盒及其制造方法。
5.本发明通过以下措施达到:
6.一种b族链球菌核酸检测试剂盒,包含样本处理液、pcr-mix、检测缓冲液、阴性和阳性对照品及金标检测卡,其特征在于,所述样本处理液为10mm pbs ph 7.2、0.05%tritonx-100、0.05%proclin-300,用于拭子样本的稀释处理;pcr-mix用于pcr扩增;检测缓冲液为50mm tris-hcl 8.0、0.1%tween-20、1%pvp-k30、0.9%nacl、0.05%proclin-300,用于pcr扩增产物稀释后的检测;金标检测卡主要有试纸条和卡壳组装而成,其中试纸条包括预固定有金标鼠源抗fam抗体的结合垫、预包被抗bio抗体、抗dig抗体和羊抗鼠的nc膜、吸水纸、样品垫、pvc底板。
7.本发明所述b族链球菌核酸检测试剂盒对应引物长度:20-25bp,序列需满足以下要求:(1)碱基排布随机性高,gc含量在40%-55%之间;(2)扩增片段避免形成二级结构而影响扩增;(3)扩增片段长度在180-300bp,不超过450bp,避免扩增序列太长引起层析检测灵敏度;(4)靶标基因和内参基因(外源加入,下同)的上游引物5’端均标记fam,靶标基因下游引物的5’端标记生物素(bio)、内参基因下游引物的5’端标记地高辛(dig);所述引物序
列如下:
8.引物序列(5
’‑3’
)cfb-ftggtagtcgtgtagaagccttacfb-rgatggtagctctatcagttggtgapdh-faccatgagaagtatgacaacgapdh-rcagctctcataccatgagtcctt
9.本发明还提出了一种b族链球菌核酸检测试剂盒的制造方法,其特征在于,包括pcr-mix配制和金标检测卡的制备,其中pcr-mix配制为:用无菌超纯水按照如下参数配制:50mm kcl、10mm tris-hcl、2mm mgcl2、0.2mm dntps、0.1u/μl taq dna聚合酶、靶标及内参上下游引物各10μmol/l、1%dmso、1.5%甲酰胺、10mm一水甜菜碱,充分混匀后,28μl/支分装至8联管,﹣20℃冷冻;
10.所述金标检测卡制备包括以下步骤:
11.步骤1:结合垫制备:
12.步骤1-1:取50ml胶体金溶液,快速搅拌加入300μl 0.1m k2co3,混匀后,快速搅拌中加入500μg fam标记抗体,室温旋转孵育10min;
13.步骤1-2:标记结束后,分别向其加入5.5ml 1%peg20000,混匀,室温条件下室温静置20min,封闭结束后,用高速冷冻离心机10000rpm/4℃/15min,弃上清;
14.步骤1-3:加入5ml胶体金标记物复溶液,得5ml fam抗体胶体金标记工作液;
15.步骤1-4:取出结合垫,在喷液的环境条件下放置至少平衡30min;将划膜喷金机的喷液参数设置为9μl/cm,对fam抗体胶体金标记工作液进行喷液包被,喷液完成后,将结合垫放置在电热鼓风干燥箱42℃干燥16-24小时;
16.步骤2:nc膜划线:将nc膜裁剪后,粘贴在pvc底板上,配制划线抗体并划线包被,如下:t1:靶标检测线,抗bio抗体划线浓度1μg/μl、buffer 10mm pb-7.4;t2:内参检测线,抗dig抗体划线浓度1μg/μl、buffer 10mm pb-7.2;c线:质控线,羊抗鼠多克隆抗体,划线浓度0.5μg/μl、buffer 10mm pb-7.8,划线参数为:1μl/cm,将划好的nc膜放置在电热鼓风干燥箱37-50℃干燥16-24小时;
17.步骤3:按以下步骤进行组装:
18.步骤3-1:干燥完成后,取出结合物垫,用裁纸刀或宽型切条机裁剪宽度为0.8cm的条带;步骤3-2:用裁纸刀或宽型切条机把样品垫裁切为宽3.2cm/条,吸水纸宽2.8cm/条;
19.步骤3-3:取出已包被好的pvc大板,按照先贴吸水纸、再贴结合垫、最后贴样品垫的顺序进行组装;
20.步骤4:将组装好的半成品大板,4mm/条裁切,然后装入卡壳,压壳后装入内包装袋封口,内包装袋含干燥剂,室温储存。
21.本发明中试剂盒利用菌落pcr(colony pcr)原理,免提取目的基因dna,直接以菌体热解后暴露的dna为模板进行pcr扩增;pcr扩增产物,采用胶体金层析法检测,达到定性检测孕妇生殖道分泌物样本中的b族链球菌dna的目的,方便操作并极大降低成本;pcr混合体系中含有内参基因和gbs-cfb基因片段的特异性引物;其中,内参基因(gapdh)的上游和下游引物的5’端分别被fam和dig修饰;靶标基因cfb的上游和下游引物的5’端分别被fam和bio修饰。pcr扩增产物的两端均含有标签,其中内参基因产物含有fam和dig标签,靶标cfb
基因扩增产物含有fam和bio标签,标签作为检测靶点,利用双抗体夹心法原理、胶体金层析技术进行定性检测。
附图说明:
22.附图1是本发明中检测流程示意图。
23.附图2是本发明中结果显示示意图。
具体实施方式:
24.下面结合附图和实施例,对本发明做进一步的说明。
25.实施例1:
26.本例提供了一种b族链球菌核酸检测试剂盒及其制造方法,其中b族链球菌核酸检测试剂盒,包含样本处理液、pcr-mix、检测缓冲液、阴性和阳性对照品及金标检测卡,所述样本处理液为10mm pbs ph 7.2、0.05%tritonx-100、0.05%proclin-300,用于拭子样本的稀释处理;pcr-mix用于pcr扩增;检测缓冲液为50mm tris-hcl 8.0、0.1%tween-20、1%pvp-k30、0.9%nacl、0.05%proclin-300,用于pcr扩增产物稀释后的检测;金标检测卡主要有试纸条和卡壳组装而成,其中试纸条包括预固定有金标鼠源抗fam抗体的结合垫、预包被抗bio抗体、抗dig抗体和羊抗鼠的nc膜、吸水纸、样品垫、pvc底板;
27.本例中所述b族链球菌核酸检测试剂盒对应引物长度:20-25bp,序列需满足以下要求:(1)碱基排布随机性高,gc含量在40%-55%之间;(2)扩增片段避免形成二级结构而影响扩增;(3)扩增片段长度在180-300bp,不超过450bp,避免扩增序列太长引起层析检测灵敏度;(4)靶标基因和内参基因的上游引物5’端均标记fam,靶标基因下游引物的5’端标记生物素(bio)、内参基因下游引物的5’端标记地高辛(dig);所述引物序列如下:
28.引物序列(5
’‑3’
)cfb-ftggtagtcgtgtagaagccttacfb-rgatggtagctctatcagttggtgapdh-faccatgagaagtatgacaacgapdh-rcagctctcataccatgagtcctt
29.本例中pcr mix是工作浓度的pcr扩增预混和溶液,包括50mm kcl、10mm tris-hcl、2mm mgcl2、0.2mm dntps、0.1u/μl taq dna聚合酶(高保真)、40μmol/l引物(靶标及内参上下游引物各10μmol/l)等pcr扩增必需组分(模板除外)。使用时,仅需在扩增体系中加入模板即可进行pcr,大大简化操作过程,缩短操作时间,降低污染(加样次数减少);
30.本试剂盒在pcr体系内含有添加剂(1%dmso、1.5%甲酰胺、10mm一水甜菜碱),降低dna二级结构,显著增强pcr扩增的灵敏度和特异性。
31.pcr扩增参数设定如下:
32.预变性:95℃5分钟;
33.扩增:94℃、20秒,55℃、20秒,72℃、25秒,共30个循环;
34.延伸:72℃、5分钟;
35.保温:4℃,不限时。
36.本例中金探针检测卡的结合垫上包被有胶体金标记的鼠源抗fam单克隆抗体,nc
膜检测区1(t1)预包被抗bio抗体(anti-bio抗体)、检测区2(t2)预包被抗dig抗体、质控区(c)预包被羊抗鼠二抗。在使用过程中,如附图2所示,阳性样本的pcr产物中含有gbs-cfb和内参基因片段,会分别在t1和t2形成“bio抗体-bio-cfb-fam-金标fam抗体”和“dig抗体-dig-内参基因-fam-金标fam抗体”复合物,形成肉眼可见的紫红色反应线;阴性样本的pcr产物中,只有内参基因片段,故只在t2形成肉眼可见的紫红色反应线;无论是阴性样本还是阳性样本,c线均应有条带。t2出现条带,预示pcr过程正常;c线出现条带,预示层析检测过程正常。
37.本例中检测试剂盒的制备包括pcr-mix配制和金标检测卡制备两部分,其中pcr-mix配制:用无菌超纯水按照如下参数配制:50mm kcl、10mm tris-hcl、2mm mgcl2、0.2mm dntps、0.1u/μl taq dna聚合酶(高保真)、靶标及内参上下游引物各10μmol/l、1%dmso、1.5%甲酰胺、10mm一水甜菜碱,充分混匀后,28μl/支分装至8联管,﹣20℃冷冻。
38.本例中金标检测卡制备具体包括结合垫的制备、nc膜的制备、产品组装等,具体为:1.结合垫制备:(1)取50ml胶体金溶液,快速搅拌加入300μl 0.1m k2co3,混匀后,快速搅拌中加入500μg fam标记抗体,室温旋转孵育10min。(2)标记结束后,分别向其加入5.5ml 1%peg20000,混匀,室温条件下室温静置20min,封闭结束后,用高速冷冻离心机10000rpm/4℃/15min,弃上清。(3)加入5ml胶体金标记物复溶液,得5mlfam抗体胶体金标记工作液。(4)取出结合垫,在喷液的环境条件下放置至少平衡30min;将划膜喷金机的喷液参数设置为9μl/cm,对fam胶体金标记工作液进行喷液包被。喷液完成后,将结合垫放置在电热鼓风干燥箱42℃干燥16-24小时。
39.2.nc膜的制备,具体为:将nc膜裁剪后,粘贴在pvc底板上,配制划线抗体并划线包被,如下:t1:靶标检测线,抗bio抗体划线浓度1μg/μl、buffer 10mm pb-7.4;t2:内参检测线,抗dig抗体,划线浓度1μg/μl、buffer 10mm pb-7.2;c线:质控线,羊抗鼠多克隆抗体,划线浓度0.5μg/μl、buffer 10mm pb-7.8.划线参数为:1μl/cm,将划好的nc膜放置在电热鼓风干燥箱37-50℃干燥16-24小时
40.3.半成品组装:干燥完成后,取出结合物垫,用裁纸刀或宽型切条机裁剪宽度为0.8cm的条带,用裁纸刀或宽型切条机把样品垫裁切为宽3.2cm/条,吸水纸宽2.8cm/条,取出已包被好的pvc大板,按照先贴吸水纸、再贴结合垫、最后贴样品垫的顺序进行组装;将组装好的半成品大板,4mm/条裁切,然后装入卡壳,压壳后装入内包袋(含干燥剂)并封口,室温储存。
41.下面对本例试剂盒的性能进行验证分析:
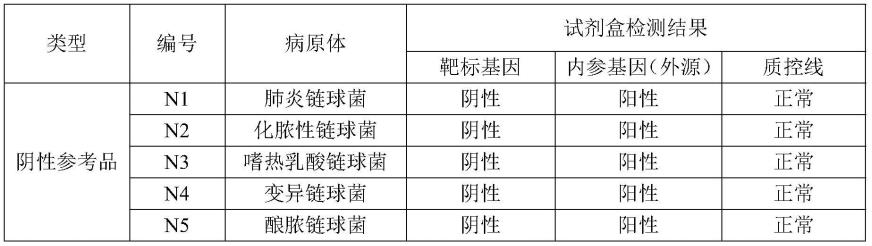
42.参考b族链球菌检测试剂技术指导原则,使用b群链球菌核酸检测试剂国家参考品(370030-201801),按照使用说明书操作,对该试剂盒进行验证,结果如下:
43.[0044][0045]
通过验证可知,本试剂盒阴性符合率和阳性符合率均为100%。
[0046]
本发明引入外源性内参基因(gapdh),实现同管扩增,最大限度降低pcr过程中的人为操作的误差;靶标及内参基因的上游引物用同一个fam标签修饰,实现用同一金标抗体检测,节约生产成本;靶标及内参基因的下游引物,用不同标签修饰,如靶标基因下游引物用bio修饰、内参基因下游引物用dig修饰,实现后续联检的特异性捕获;本发明中的nc膜包被,针对靶标和内参基因的下游引物修饰不同,特异性的选择捕获线。靶标基因捕获线包被抗bio抗体,与bio形成特异性配对;内参基因捕获线包被抗dig抗体,与dig形成特异性配对,通过两组特异性的配对,实现靶标和内参基因的联合检测,方便操作及节约成本。相对于同类检测试剂的检测方法为靶标基因和内参基因分开独立检测,现有同类产品存在增加操作误差及试剂成本的不足。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1