一种含活性醛基结构的高酯果胶及其制备方法与流程
1.本发明属于生物制药技术领域,具体涉及一种含活性醛基结构的高酯果胶及其制备方法。
背景技术:
2.果胶分子是一种阴离子杂多糖普遍的分布于高等植物的细胞壁中。根据果胶中的半乳糖醛酸酯化程度,可将果胶分为高酯化度果胶(dm>50%)以及低酯化度果胶(dm<50%)。果胶的酯化程度是影响果胶功能性,尤其是凝胶机制和凝胶性质的关键参数。此外,高酯果胶含有较高比例的疏水性甲酯化基团,增强了分子的乳化能力。传统的高酯果胶的制备基于热/酸提取,限制甲酯化半乳糖醛酸的皂化反应,但得到的果胶酯化度一般为70%左右。为进一步提高果胶的甲酯化度,通常利用甲醇与果胶的羧基发生酯化反应。
3.cn113731307a公开了一种含硫酸铵的高酯果胶凝胶及其制备方法与应用,具体公开了如下方法:1)将高酯果胶溶于水中,调节ph为4~7,获得高酯果胶溶液;将硫酸铵或硫酸铵水溶液与高酯果胶溶液混合,获得含硫酸铵的混合溶液;2)调节含硫酸铵的混合溶液的ph≤3.5,均质,静置,获得高酯果胶凝胶;步骤1)中含硫酸铵的混合溶液中硫酸铵的质量浓度为25%~30%,高酯果胶的质量浓度为0.2~1.5%。该技术方案中使用了硫酸铵,产品具有较大的局限性,还存在改进空间。
4.cn102643366a公开了一种间歇式酸提取乙醇沉淀的高酯果胶的生产方法,具体公开了将干桔皮浸泡于45℃温水中30min,使其充分吸水软化除掉可溶性杂质,把桔皮沥干放入沸水中灭酶,灭酶后的桔皮置于流水中漂洗至无色,然后用粉碎机粉碎,按粉碎后的桔皮颗粒与水按质量比即桔皮颗粒:水为1:5-20,控制ph值为1.0-3.0、温度为50-90℃,时间为30-90min条件下提取后过滤,将滤液进行真空旋转蒸发,所得到浓缩液中加入无水乙醇,沉淀、抽滤后所得滤饼控制温度为40℃进行干燥即得高酯果胶。该技术方案制备的方法比较简单,但是获得的果胶的酯化度并不高,存在改进的空间。
5.综述所述,现有技术仍缺乏一种制备方法简单酯化度高的氧化果胶。
技术实现要素:
6.针对现有技术的以上缺陷或改进需求,本发明提供了一种含活性醛基结构的高酯果胶及其制备方法,其目的在于通过特定的氧化剂选择性氧化非酯化半乳糖醛酸的邻二羟基,导致非酯化半乳糖醛酸降解并使得果胶分子链骨架断裂,形成甲酯化半乳糖醛酸含量更高的低分子量高酯化度果胶,最后获得制备方法简单酯化度高的氧化果胶。
7.为实现上述目的,按照本发明的一个方面,提供了一种含活性醛基结构的高酯果胶的制备方法,其特征在于,包括以下步骤:
8.(1)将果胶充分溶解得到果胶溶液,加入碱调节ph为5.0以下;
9.(2)加入特定氧化剂避光反应,特定氧化剂能够选择性氧化非酯化半乳糖醛酸的邻二羟基,促进非酯化半乳糖醛酸降解并使得果胶分子链骨架断裂,获得含活性醛基结构
的高酯果胶;
10.(3)加入终止剂终止反应,然后将反应溶液通过乙醇进行醇沉,分离醇沉产物冻干后即可获得氧化果胶。
11.作为优选,所述特定氧化剂为高碘酸钠、过氧化氢、次氯酸钠和氯酸钾中的至少一种。
12.作为优选,所述特定氧化剂为高碘酸钠。
13.作为优选,所述特定氧化剂与果胶的质量比为(0.01-0.1):1,优选为0.04:1。
14.作为优选,步骤(1)中所述果胶溶液的质量浓度为1.0%-2.5%。
15.作为优选,步骤(1)中所述果胶溶液的ph为4.0-5.0。
16.作为优选,所述果胶为柠檬皮果胶、橙皮果胶和苹果皮果胶中的至少一种。
17.作为优选,所述终止剂为乙二醇或聚乙二醇。
18.作为优选,反应时间优选为12h-24h。
19.按照本发明的另一方面,提供了一种所述的氧化果胶的制备方法制备本发明的有益效果有:
20.(1)本发明选用高碘酸盐作为氧化剂,具有高度专一的选择性氧化能力,没有明显的副反应,可以使半乳糖醛酸上的c
2-c3键断开,使原有的邻二羟基转变成具有高还原性的二醛基。非酯化的半乳糖醛酸更容易成为氧化位点,进而导致酯化度改变。因此该方法在制备活性更高的醛基果胶的同时降低分子量,同时提高果胶的酯化度。
21.(2)本发明中得到的氧化果胶的酯化度可以高于94%,且无需复杂的酯化反应,极大地丰富果胶的应用范围。
附图说明
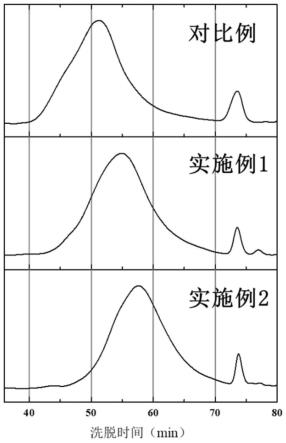
22.图1是实施例1-2及对比例的果胶分子量分布测试图;
23.图2实施例1-2及对比例的果胶分子形态测试图;
24.图3是实施例1-2和对比例的酯化度和醛基含量测试结果图。
具体实施方式
25.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
26.实施例
27.以下制造例中所使用的高酯化橙皮果胶购于广州市莱檬生物科技有限公司。实施例中所用仪器:扫描探针原子力显微镜multi-mode 8和高效液相色谱仪waters e2695。
28.1.果胶的醛基含量测定:参考文献“alkylated pectin:molecular characterization,conformational change and gel property”,将果胶水溶液(2.0%,ph 3.0)或者果胶乙醇溶液(25%,v/v)以相应溶剂稀释至5μg/ml。将3μl上述溶液涂布于清洁的云母片上,至于干燥器中充分干燥。
29.实验条件:扫描速度1.0hz,300khz驱动频率。在trapping模式下获得样本图像,并
用nano analysis软件处理。果胶凝胶的流变学测试
30.2.分子量测定:参考文献“structural characterization,antiproliferative and immunoregulatory activities of a polysaccharide from boletus leccinum rugosiceps”。将果胶样品溶解于20mm kh2po4缓冲液,充分溶解后用0.22μm微孔滤膜过滤得到浓度2-5mg/ml果胶溶液。将果胶样品与葡聚糖标准品(4.4,9.9,21.4,43.5,124,196,277,及401kda)在waters凝胶渗透色谱系统中检测,根据葡聚糖标准品的分子量与出峰时间绘制分子量标准曲线,据此鉴定果胶样品的分子量。
31.色谱方法:ultra hydrogel 1000(7.8
×
300mm)和ultra hydrogel500(7.8
×
300mm)串联,流动相为20mm kh2po4缓冲液,流速0.8ml/min,waters 2414示差检测器检测,柱温为35℃。
32.3.酯化度测定:参照文献“李鹏琳.果胶的酯化度和分子量对pb
2+
吸附性能的影响[d].”进行,称取果胶样品50mg放入250ml锥形瓶中,加入100ml不含co2的水,塞紧瓶塞,不断地振摇,使果胶样品全部溶解。随后加入酚酞指示剂,用0.02mol/l的naoh标准溶液滴定至微红色为止,记下所消耗naoh的体积(v1)。继续加入0.5mol/l的naoh标准溶液20.00ml,盖紧塞振摇15min后,接着再加入等摩尔的浓度为0.5mol/l的hcl标准溶液,再次充分振摇。最后加入酚酞指示剂,用0.02mol/l的naoh标准溶液滴定至微红色,记下消耗的naoh的体积(v2)。果胶酯化度计算式如下:
[0033]
酯化du(%)=v2/(v1+v2)*100
[0034]
4.醛基含量测定:参照文献“刘文迎.氧化纤维素/壳聚糖复合止血材料的制备及性能研究[d].”进行,称取一定量的氧化果胶,加入一定体积的0.25m的盐酸羟胺-甲基橙溶液,充分搅拌4h。最后用0.1m的标准naoh溶液滴定,至溶液颜色由粉红色变为黄色,其滴定总店为溶液ph=5.0。醛基含量[cho]计算公式如下:
[0035]
[cho]=(v_2-v_1)
×
c/m
[0036]
其中醛基含量[cho]单位为mmol/g;c:naoh溶度,mol/l;v_2:滴定终点需用naoh体积,ml;v_1:空白滴定消耗的naoh体积,ml;m:氧化果胶质量,g。
[0037]
实施例1
[0038]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至5.0;
[0039]
(2)将固体高碘酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的质量浓度达到50:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0040]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0041]
实施例2
[0042]
本实施例与实施例1不同之处在于,氧化剂与果胶的质量对比不同。
[0043]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0044]
(2)将固体高碘酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到10:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0045]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水
乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0046]
实施例3
[0047]
本实施例与实施例1不同之处在于,氧化剂与果胶的质量对比不同。
[0048]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0049]
(2)将固体高碘酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到100:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0050]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0051]
实施例4
[0052]
本实施例与实施例1不同之处在于,氧化剂与果胶的质量对比不同。
[0053]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0054]
(2)将固体高碘酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到25:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0055]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0056]
实施例5
[0057]
本实施例与实施例1不同之处在于,氧化剂不同。
[0058]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0059]
(2)将过氧化氢在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到10:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0060]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0061]
实施例6
[0062]
本实施例与实施例5不同之处在于,氧化剂与果胶的质量对比不同。
[0063]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0064]
(2)将过氧化氢在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到100:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0065]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0066]
实施例7
[0067]
本实施例与实施例1不同之处在于,氧化剂不同。
[0068]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0069]
(2)将次氯酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到10:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0070]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0071]
实施例8
[0072]
本实施例与实施例7不同之处在于,氧化剂与果胶的质量对比不同。
[0073]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0074]
(2)将次氯酸钠在避光条件下添加到果胶溶液中,使溶液中果胶与高碘酸的浓度达到100:1,加入高碘酸按的同时对果胶溶液持续搅拌,进行反应;
[0075]
(3)反应12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0076]
对比例
[0077]
本实施例与实施例1不同之处在于,未加入氧化剂。
[0078]
(1)将2.5g果胶加入100ml蒸馏水中,在磁力搅拌器中,30摄氏度条件下,搅拌至充分溶解得到果胶溶液,并调节ph至4.0;
[0079]
(2)不加入高碘酸钠,搅拌12h后加入10ml乙二醇终止氧化反应,将上述果胶溶液倒入3倍体积无水乙醇中沉淀,如此重复3次,最后冻干得到氧化果胶。
[0080]
表1实施例1-8的酯化度测试结果表
[0081]
实施例氧化剂质量比(果胶:氧化剂)酯化度实施例1高碘酸钠50:194.52%实施例2高碘酸钠10:186.03%实施例3高碘酸钠100:194.70%实施例4高碘酸钠25:194.13%实施例5过氧化氢10:163.98%实施例6过氧化氢100:156.53%实施例7次氯酸钠10:164.64%实施例8次氯酸钠100:157.85%对比例无\58.97%
[0082]
分析表1的数据可知:本发明氧化剂具有高度专一的选择性氧化能力,没有明显的副反应,可以使半乳糖醛酸上的c2-c3键断开,使原有的邻二羟基转变成具有高还原性的二醛基。非酯化的半乳糖醛酸更容易成为氧化位点,进而导致酯化度改变。因此该方法在制备活性更高的醛基果胶的同时降低分子量,同时提高果胶的酯化度。
[0083]
本发明中高碘酸盐是最佳的效果,得到的氧化果胶的酯化度可以高于94%,且无需复杂的酯化反应,极大地丰富果胶的应用范围。
[0084]
图1是实施例1-2及对比例的果胶分子量分布测试图;
[0085]
图2实施例1-2及对比例的果胶分子形态测试图;
[0086]
图3是实施例1-2和对比例的酯化度和醛基含量测试结果图。
[0087]
从图1和图2可以看出,本发明制备的氧化果胶(实施例1和2)的分子链较未氧化果胶(对比例)明显更短,分子量明显更小。而图3显示本发明的氧化改性显著增加了果胶的醛基含量和酯化度,且酯化度在更高的氧化程度时出现下降,因此本研究优选的氧化条件可
以制备含有活性醛基的低分子量高酯果胶。
[0088]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1