Z-构型的烯丙基氨基酸类衍生物、其制备方法及应用
z-构型的烯丙基氨基酸类衍生物、其制备方法及应用
技术领域
1.本发明涉及有机合成领域,尤其涉及一种z-构型的烯丙基氨基酸类衍生物及其制备方法和应用。
背景技术:
2.氨基酸是人体必需的营养物质,是人体蛋白质的基本单位。烯丙基氨基酸作为氨基酸家族中的一类,不仅是合成复杂分子的关键中间体,而且广泛存在于天然产物和药物分子中(j.med.chem.1986,29,1023;antibiot.1989,42,1556;bioorg.med.chem.2015,23,1011)。因此,有机化学家和药物学家发展了各种各样的方法来合成烯丙基氨基酸及其衍生物。然而,在现有的合成方法中,主要是合成e-构型的烯丙基氨基酸类衍生物。由于热力学的稳定性,合成z-构型的烯丙基氨基酸类衍生物面临非常巨大的挑战。因此,为了丰富氨基酸的种类,合成z-构型的烯丙基氨基酸类衍生物具有非常重要的价值。
3.过渡金属催化的脱酸转化反应已经成为了一类非常实用的方法来构建含有碳碳双键的分子。在该领域,钯催化的烯基碳酸酯的脱羧烯丙基化反应是研究的重点和热点;其中,烯基碳酸酯在钯的作用下形成高活性的π-烯丙基钯中间体是反应的关键。因此,发展新型的π-烯丙基钯中间体是该领域发展的一个重要方向。最近,兹伟伟课题组和郭武生课题组同时报道了烯基环状碳酸乙烯酯在钯的作用下,可以产生一种新型的烯丙基-π-烯丙基钯中间体,可以用于合成各种不同的环加成反应(j.am.chem.soc.,2021,143,1038;org.lett.,2021,23,351)。然而,到目前为止,仅仅郭武生课题组报道了一例烯丙基取代反应,用水作为亲核试剂,进攻烯丙基-π-烯丙基钯中间体,得到e-烯丙基醇产物(org.lett.,2021,23,3195)。因此,以新型的烯丙基-π-烯丙基钯中间体为烯丙基前体,与合适的亲核试剂反应,具有非常重要的研究价值和应用价值。
技术实现要素:
4.本发明的目的之一,就在于提供一类新的烯丙基氨基酸衍生物,且具有独特的z-构型,以解决上述问题。
5.为了实现上述目的,本发明采用的技术方案是这样的:z-构型的烯丙基氨基酸衍生物,具有如下结构式(ⅰ)所示的结构:
[0006][0007]
上述结构式中,r1基为芳基或烷基;r2基为烷基;ar基为苯环上各种取代的芳基、杂芳烃、萘基等。
[0008]
本发明运用氨基酸的前体吖内酯为亲核试剂,通过钯催化的烯丙基取代反应,高立体选择性构建了一系列z-构型的烯丙基氨基酸衍生物。
[0009]
通过文献调研,发明人发现,目前报道的合成方法主要是制备e-构型的烯丙基氨基酸类衍生物。由于z-构型的产物的热力学不稳定性,合成z-构型的烯丙基氨基酸类衍生物面临非常巨大的挑战。因此,制备z-构型的烯丙基氨基酸类衍生物不仅具有非常重要的科研价值,也可以丰富氨基酸的种类,为新药研究提供更多的氨基酸片段。
[0010]
本发明的目的之二,在于提供一种上述的烯丙基氨基酸衍生物的制备方法,采用的技术方案为:将烯基环状碳酸乙烯酯(ⅱ)、吖内酯(ⅲ)溶解在有机溶剂中,然后加钯源和配体,在-10℃~50℃温度下搅拌反应,待反应完毕后,分离纯化得到产物ⅰ,其中,
[0011]
所述烯基环状碳酸乙烯酯(ⅱ)具有如下结构:
[0012][0013]
所述吖内酯(ⅲ)具有如下结构:
[0014][0015]
其反应式为:
[0016][0017]
作为优选的技术方案:所述的反应溶剂选自甲苯、均三甲苯、二氯甲烷、氯仿、四氢呋喃、乙醚、乙腈、乙醇、甲醇、1,4-二氧六环、氯苯中的一种或者多种混合;进一步优选氯苯,反应收率更高。
[0018]
作为优选的技术方案:所述钯源为pd2(dba)3·
chcl3、pd(pph3)4、pd(tfa)2、pd(oac)2、pd(pph3)2cl2等;进一步优选pd(pph3)2cl2,反应收率更高。
[0019]
作为优选的技术方案:所述配体为各种磷配体;优选配体结构如下:
[0020][0021]
进一步优选l4,反应收率更高。
[0022]
作为优选的技术方案:所述反应温度0℃,反应收率更高,能耗相对更低。
[0023]
本发明的目的之三,在于展示该类化合物在有机合成中的有用性,本发明的化合物可以通过官能团转化,用于制备具有抗肿瘤尤其是抗肺瘤活性的药物。
[0024]
具体的,以式(ⅰ)的化合物中,r1基为ph基、r2基为bn基、ar基为ph基为例,具体转
化如下:
[0025][0026]
将产物溶解在四氢呋喃中,加入1.5当量的四氢吡咯,室温搅拌18小时,分离纯化就可以得到化合物a,收率为82%;结构鉴定:1h nmr(400mhz,cdcl3)δ8.12(bs,1h),7.78
–
7.70(m,2h),7.54
–
7.47(m,1h),7.46
–
7.33(m,5h),7.13
–
7.16(m,3h),7.12
–
7.04(m,2h),6.97
–
6.88(m,2h),6.78(dd,j=9.3,4.8hz,1h),4.05
–
3.88(m,2h),3.59
–
3.49(m,2h),3.44(d,j=11.4hz,1h),3.10(d,j=14.4hz,1h),2.89(dd,j=16.3,9.2hz,1h),2.84
–
2.72(m,1h),2.23(s,3h),1.88
–
1.70(m,4h);
13
c nmr(101mhz,cdcl3)δ198.4,168.8,166.4,144.5,138.0,135.9,135.4,135.3,131.6,129.8,129.4,128.7,128.4,128.3,128.0,127.1,127.0,65.3,38.0,33.7,27.2.hrms(esi)m/z:[m+h]
+
calcd for c
31h33
n2o3481.2486;found:481.2469.
[0027]
将产物溶解在甲醇中,加入2.5当量的碳酸钾,室温搅拌7小时,分离纯化就可以得到化合物b,收率为91%;结构鉴定:1h nmr(400mhz,cdcl3)δ7.68
–
7.59(m,2h),7.48
–
7.41(m,1h),7.40
–
7.27(m,5h),7.11
–
7.06(m,3h),6.98(d,j=7.3hz,2h),6.93(s,1h),6.87(dd,j=6.8,2.7hz,2h),6.71
–
6.62(m,1h),3.79(dd,j=13.5,2.0hz,1h),3.65(s,3h),3.64
–
3.55(m,1h),2.98(d,j=13.5hz,1h),2.82
–
2.71(m,1h),2.10(s,3h);
13
c nmr(101mhz,cdcl3)δ198.4,173.0,167.0,145.3,136.6,135.7,135.6,134.9,131.9,129.7,129.5,128.8,128.5,128.4,127.9,127.2,127.0,65.7,53.0,40.5,35.6,27.6.hrms(esi)m/z:[m+h]
+
calcd for c
28h28
no4442.2013;found:442.2018.
[0028]
上述化合物a、化合物b的细胞活性测试过程如下:将5000个人肺癌细胞a549分别接种到96孔细胞培养板中,并让其生长24小时。然后分别加入一定浓度的上述合成的化合物a(如前述结构所示的消旋体)和化合物b(如前述结构所示的消旋体),以抗肿瘤药物顺铂作为对照,作用48小时。然后测定化合物的平均50%的抑制浓度(ic
50
)。化合物a:ic
50
(a549)=18.9μm;化合物b:ic
50
(a549)=22.9μm,顺铂:ic
50
(a549)=23.96μm,可见,化合物a和化合物b具有与顺铂相当的抗a549活性。
[0029]
与现有技术相比,本发明的优点在于:本发明实现了钯催化的吖内酯和烯基环状碳酸乙烯酯的烯丙基取代反应。首次公开了一系列新的烯丙基氨基酸类衍生物及其合成方法。本发明所提供的烯丙基氨基酸类衍生物具有独特的z-构型,且含有一个季碳手性中心,不仅可以丰富氨基酸的种类,也可以为新药研究提供更多的氨基酸片段;同时,通过一定的官能团转化,所得产物初步证书具有抗肺癌活性。此外,本发明的制备方法具有新颖、简捷、操作简单、反应条件温和、收率高、立体选择性选择性高等优点。
附图说明
[0030]
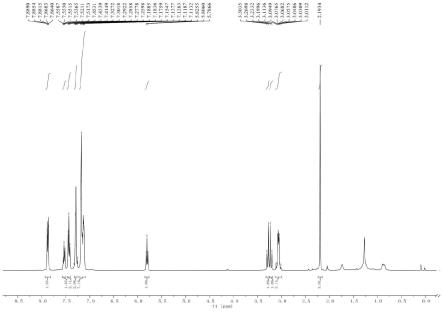
图1为实施例1制得的i-a的氢谱图;
[0031]
图2为实施例1制得的i-a的碳谱图;
具体实施方式
[0032]
下面将结合附图对本发明作进一步说明。
[0033]
本发明所用的原料、溶剂、催化剂、碱等,均为市购。
[0034]
实施例1:合成化合物
ⅰ‑a[0035][0036]
在一根干燥的反应试管中依次加烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,钯源和配体,以及溶剂搅拌反应。反应完全后,粗产品经柱色谱分离纯化得化合物i-a,不同的反应条件如表1所示,具体反应过程如下:
[0037][0038]
表1不同的反应条件
[0039]
entry[pd]配体溶剂温度(℃)时间(h)收率(%)z:e1pd2(dba)3·
chcl3l1甲苯rt2318》20:12pd2(dba)3·
chcl3l2甲苯rt2349》99:13pd2(dba)3·
chcl3l3甲苯rt2039》20:14pd2(dba)3·
chcl3l4甲苯rt2051》20:15pd2(dba)3·
chcl3l5甲苯rt4320》20:16pd2(dba)3·
chcl3l4ch2cl2rt2237》20:17pd2(dba)3·
chcl3l4二氧六环rt1559》20:18pd2(dba)3·
chcl3l4二甲苯rt2452》20:19pd2(dba)3·
chcl3l4氯苯rt1561》20:110pd2(dba)3·
chcl3l4氯苯04885》20:110pd2(dba)3·
chcl3l4氯苯502472》20:111pd(pph3)4l4氯苯04881》20:112pd(tfa)2l4氯苯04857》20:113pd(oac)2l4氯苯04881》20:114pd(pph3)2cl2l4氯苯04889》20:1
[0040]
从表1中可见,采用pd(pph3)2cl2为钯源(5mol%),l4(10mol%)为配体,氯苯作溶剂、反应温度为0℃,是较为优选的技术方案。
[0041]
所得化合物i-a为无色油状物,经hplc检测纯度为》99%;z:e》20:1。
[0042]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.93
–
7.82(m,2h),7.57
–
7.50(m,1h),7.47
–
7.40(m,2h),7.32
–
7.27(m,3h),7.22
–
7.09(m,7h),5.81(t,j=7.8hz,1h),3.29(d,j=13.5hz,1h),3.22(d,j=13.4hz,1h),3.13
–
3.00(m,2h),2.19(s,3h);
13
c nmr(101mhz,cdcl3)δ203.6,179.1,160.3,147.8,137.4,134.2,132.8,130.3,128.9,128.4,128.3,127.9,127.4,127.3,126.8,125.6,74.6,43.3,36.7,30.9;hrms(esi)m/z:[m+h]
+
calcd for c
27h24
no3410.1751;found:410.1753。氢谱、碳谱图如图1和图2所示。
[0043]
实施例2:合成化合物
ⅰ‑b[0044][0045]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
b 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-b,无色油状物;收率为72%;z:e》20:1。
[0046]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.83
–
7.75(m,2h),7.50
–
7.44(m,1h),7.40
–
7.33(m,2h),7.21
–
7.17(m,2h),7.13
–
7.03(m,5h),6.99
–
6.93(m,2h),5.71(t,j=7.7hz,1h),3.19(d,j=13.4hz,1h),3.12(d,j=13.4hz,1h),3.03
–
2.89(m,2h),2.10(s,3h);
13
c nmr(101mhz,cdcl3)δ203.1,179.0,160.3,146.6,135.8,134.5,134.1,132.9,130.3,129.1,128.9,128.6,128.3,127.9,127.5,127.4,125.5,74.5,43.3,36.7,30.9.hrms(esi)m/z:[m+h]
+
calcd for c
27h23
clno3444.1361;found:444.1366。
[0047]
实施例3:合成化合物
ⅰ‑c[0048][0049]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
c 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-c,无色油状物;收率为89%;z:e》20:1。
[0050]
结构鉴定:1h nmr(600mhz,dmso-d6)δ7.86
–
7.79(m,2h),7.63
–
7.56(m,1h),7.53
–
7.46(m,3h),7.33
–
7.25(m,2h),7.20
–
7.10(m,6h),5.92(t,j=7.7hz,1h),3.28(d,j=13.5hz,1h),3.19(d,j=13.5hz,1h),3.02
–
2.91(m,2h),2.17(s,3h);
13
c nmr(151mhz,dmso-d6)δ201.9,178.3,159.2,145.1,139.1,134.1,132.8,130.9,130.6,129.9,129.4,
128.9,127.8,127.3,127.0,125.8,124.9,122.0,73.6,41.9,35.9,30.6.hrms(esi)m/z:[m+h]
+
calcd for c
27h23
brno3488.0856;found:488.0861。
[0051]
实施例4:合成化合物
ⅰ‑d[0052][0053]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
d 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-d,白色固体;收率为80%;z:e》20:1。
[0054]
结构鉴定:1h nmr(400mhz,dmso-d6)δ7.85
–
7.77(m,2h),7.64
–
7.57(m,1h),7.55
–
7.47(m,3h),7.35
–
7.27(m,2h),7.23
–
7.07(m,6h),5.94(t,j=7.7hz,1h),3.29(d,j=13.4hz,1h),3.20(d,j=13.5hz,1h),3.03
–
2.92(m,2h),2.17(s,3h);
13
c nmr(101mhz,dmso-d6)δ202.4,178.5,159.3,145.1,139.2,134.4,133.1,131.1,130.9,130.1,129.4,129.1,128.0,127.9,127.5,127.2,126.0,125.0,122.1,73.7,41.9,35.9,30.8.hrms(esi)m/z:[m+h]
+
calcd for c
27h23
brno3488.0856;found:488.0856。
[0055]
实施例5:合成化合物
ⅰ‑e[0056][0057]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
e 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-e,无色油状物;收率为82%;z:e》20:1。
[0058]
结构鉴定:1h nmr(600mhz,cdcl3)δ7.87(dd,j=8.1,1.4hz,2h),7.57
–
7.50(m,1h),7.47
–
7.41(m,2h),7.19
–
7.13(m,5h),7.10(d,j=7.9hz,2h),7.04
–
6.98(m,2h),5.76(t,j=7.7hz,1h),3.28(d,j=13.5hz,1h),3.21(d,j=13.5hz,1h),3.09
–
3.00(m,2h),2.32(s,3h),2.19(s,3h);
13
c nmr(151mhz,cdcl3)δ204.0,179.1,160.3,147.7,138.3,134.5,134.2,132.8,130.3,129.5,128.9,128.3,127.9,127.4,127.2,125.8,125.6,74.7,43.3,36.7,30.9,21.2.hrms(esi)m/z:[m+h]
+
calcd for c
28h26
no3424.1907;found:424.1911。
[0059]
实施例6:合成化合物
ⅰ‑f[0060][0061]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
f0.1 mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-f,无色油状物;收率为77%;z:e》20:1。
[0062]
结构鉴定:1h nmr(600mhz,dmso-d6)δ7.88
–
7.80(m,2h),7.68
–
7.59(m,1h),7.56
–
7.49(m,2h),7.24
–
7.18(m,4h),7.17
–
7.12(m,3h),7.10
–
7.06(m,2h),5.80(t,j=7.8hz,1h),3.29(d,j=13.6hz,1h),3.21(d,j=13.5hz,1h),3.00
–
2.91(m,2h),2.85(p,j=6.9hz,1h),2.17(s,3h),1.17(s,3h),1.16(s,3h);
13
c nmr(151mhz,dmso-d6)δ203.5,178.6,159.2,148.6,146.8,134.4,134.1,133.1,130.1,129.2,128.0,127.5,127.2,126.9,126.6,125.0,124.5,73.9,42.0,35.8,33.1,30.8,23.7,23.6.hrms(esi)m/z:[m+h]
+
calcd for c
30h30
no3452.2220;found:452.2225。
[0063]
实施例7:合成化合物
ⅰ‑g[0064][0065]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
g 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-g,无色油状物;收率为87%;z:e》20:1。
[0066]
结构鉴定:1h nmr(600mhz,dmso-d6)δ7.86
–
7.80(m,2h),7.66
–
7.59(m,1h),7.54
–
7.50(m,2h),7.38
–
7.34(m,2h),7.21
–
7.17(m,2h),7.16
–
7.11(m,3h),7.11
–
7.07(m,2h),5.80(t,j=7.8hz,1h),3.28(d,j=13.6hz,1h),3.20(d,j=13.6hz,1h),2.99
–
2.90(m,2h),2.17(s,3h),1.24(s,9h);
13
c nmr(151mhz,dmso-d6)δ203.5,178.6,159.2,150.9,146.7,134.4,133.7,133.1,130.0,129.2,128.0,127.5,127.2,126.3,125.7,125.0,124.5,73.9,42.0,35.8,34.3,31.0,30.8.hrms(esi)m/z:[m+h]
+
calcd for c
31h32
no3466.2377;found:466.2383。
[0067]
实施例8:合成化合物
ⅰ‑h[0068][0069]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
h 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-h,白色固体;收率为75%;z:e》20:1。
[0070]
结构鉴定:1h nmr(400mhz,dmso-d6)δ7.83(d,j=7.7hz,2h),7.63
–
7.56(m,1h),7.52
–
7.45(m,2h),7.19
–
7.08(m,5h),7.04(d,j=7.7hz,1h),6.81(d,j=8.3hz,2h),5.70(t,j=7.9hz,1h),3.26(d,j=13.5hz,1h),3.17(d,j=13.5hz,1h),2.96
–
2.87(m,2h),2.17(s,3h),2.12(s,6h);
13
c nmr(101mhz,dmso-d6)δ203.4,178.8,159.7,147.5,137.0,136.9,134.7,133.3,130.4,130.2,129.3,128.3,128.2,127.8,127.5,125.5,124.8,124.4,74.4,42.5,36.4,30.9,19.7,19.5.hrms(esi)m/z:[m+h]
+
calcd for c
29h28
no3438.2064;found:438.2070。
[0071]
实施例9:合成化合物
ⅰ‑i[0072][0073]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
i 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-i,无色油状物;收率为88%;z:e》20:1。
[0074]
结构鉴定:1h nmr(600mhz,dmso-d6)δ7.91
–
7.81(m,5h),7.66
–
7.60(m,2h),7.55
–
7.47(m,4h),7.36(dd,j=8.6,1.9hz,1h),7.22
–
7.13(m,5h),6.02(t,j=7.8hz,1h),3.33(d,j=13.5hz,1h),3.24(d,j=13.6hz,1h),3.07
–
2.98(m,2h),2.23(s,3h);
13
c nmr(151mhz,dmso-d6)δ203.3,178.6,159.3,146.8,134.4,134.0,133.1,132.8,132.5,130.1,129.2,128.5,128.1,128.0,127.6,127.5,127.2,126.7,126.6,125.9,125.8,125.0,124.5,74.0,42.0,36.0,30.9.hrms(esi)m/z:[m+h]
+
calcd for c
31h26
no3460.1907;found:460.1912。
[0075]
实施例10:合成化合物
ⅰ‑j[0076]
[0077]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
j 0.1mmol,吖内酯
ⅲ‑
a 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-j,无色油状物;收率为87%;z:e》20:1。
[0078]
结构鉴定:1h nmr(400mhz,dmso-d6)δ7.85
–
7.73(m,2h),7.67
–
7.59(m,1h),7.52(t,j=7.7hz,2h),7.24
–
7.01(m,5h),5.22(t,j=7.8hz,1h),3.21(d,j=13.5hz,1h),3.13(d,j=13.4hz,1h),2.77(d,j=7.8hz,2h),2.21(s,3h),2.21-2.13(m,1h),1.67
–
1.45(m,5h),1.26
–
1.13(m,2h),1.08
–
0.90(m,3h);
13
c nmr(101mhz,dmso-d6)δ204.9,178.6,159.0,152.1,134.4,133.0,130.0,129.1,128.0,127.4,127.1,125.0,120.0,74.1,42.0,38.9,35.6,31.8,31.6,30.4,25.8,25.8,25.4.hrms(esi)m/z:[m+na]
+
calcd for c
27h29
nano3438.2040;found:438.2042。
[0079]
实施例11:合成化合物
ⅰ‑k[0080][0081]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
b 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-k,无色油状物;收率为82%;z:e》20:1。
[0082]
结构鉴定:1h nmr(600mhz,cdcl3)δ8.06
–
7.99(m,2h),7.61
–
7.57(m,1h),7.53
–
7.47(m,2h),7.29(dd,j=5.1,1.9hz,3h),7.15
–
7.10(m,2h),5.77(t,j=7.7hz,1h),2.97
–
2.86(m,2h),2.18(s,3h),1.58(s,3h);
13
c nmr(151mhz,cdcl3)δ203.6,180.2,160.3,147.7,137.4,133.0,129.0,128.9,128.4,128.1,127.3,126.9,125.8,69.5,37.5,30.9,23.4.hrms(esi)m/z:[m+h]
+
calcd for c
21h20
no3334.1438;found:334.1443。
[0083]
实施例12:合成化合物
ⅰ‑
l
[0084][0085]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
c 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-l,无色油状物;收率为71%;z:e》20:1。
[0086]
结构鉴定:1h nmr(400mhz,cdcl3)δ8.08
–
7.98(m,2h),7.62
–
7.56(m,1h),7.50(t,j=7.7hz,2h),7.33
–
7.26(m,3h),7.11(dd,j=6.7,2.9hz,2h),5.76(t,j=7.8hz,1h),3.03
–
2.85(m,2h),2.17(s,3h),2.06
–
1.97(m,2h),0.88(t,j=7.4hz,3h);
13
c nmr(101mhz,cdcl3)δ203.7,179.8,160.5,147.6,137.5,133.0,129.0,128.9,128.3,128.1,127.3,126.9,125.8,74.0,36.6,30.9,30.3,8.3.hrms(esi)m/z:[m+h]
+
calcd for c
22h22
no3348.1594;found:348.1598。
[0087]
实施例13:合成化合物
ⅰ‑m[0088][0089]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
d 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-m,无色油状物;收率为80%;z:e》20:1。
[0090]
结构鉴定:1h nmr(400mhz,chloroform-d)δ8.12
–
7.94(m,2h),7.63
–
7.54(m,1h),7.50(dd,j=8.5,6.9hz,2h),7.27(dd,j=5.6,2.4hz,3h),7.14
–
7.00(m,2h),5.69(t,j=7.8hz,1h),3.03(dd,j=14.8,7.3hz,1h),2.93(dd,j=14.8,8.1hz,1h),2.24(q,j=7.0hz,1h),2.16(d,j=1.4hz,3h),1.09(d,j=6.8hz,3h),0.96(d,j=6.8hz,3h);
13
c nmr(101mhz,cdcl3)δ203.8,179.8,160.4,147.7,137.5,132.9,129.0,128.8,128.3,128.1,127.3,127.2,125.8,76.7,34.8,34.5,30.8,17.2,16.9.hrms(esi)m/z:[m+h]
+
calcd for c
23h24
no3362.1751;found:362.1755。
[0091]
实施例14:合成化合物
ⅰ‑n[0092][0093]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
e 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-n,无色油状物;收率为89%;z:e》20:1。
[0094]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.93
–
7.82(m,2h),7.30(t,j=3.3hz,3h),7.19
–
7.08(m,9h),5.80(t,j=7.8hz,1h),3.27(d,j=13.5hz,1h),3.21(d,j=13.5hz,1h),3.12
–
2.98(m,2h),2.19(s,3h);
13
c nmr(101mhz,cdcl3)δ203.6,178.8,165.6(d,j=255.8hz),159.4,147.7,137.4,134.1,130.4,130.3,128.9,128.4,128.3,127.4,127.3,126.8,121.8(d,j=3.1hz),116.2(d,j=22.4hz),74.6,43.3,36.7,30.9.hrms(esi)m/z:[m+h]
+
calcd for c
27h23
no3428.1656;found:428.1667。
[0095]
实施例15:合成化合物
ⅰ‑o[0096][0097]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
f0.1 mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-o,无色油状物;收率为82%;z:e》20:1。
[0098]
结构鉴定:1h nmr(600mhz,cdcl3)δ7.90
–
7.85(m,1h),7.77
–
7.71(m,1h),7.52
–
7.48(m,1h),7.37(t,j=7.9hz,1h),7.31(dd,j=5.1,2.0hz,3h),7.22
–
7.11(m,7h),5.79(t,j=7.7hz,1h),3.28(d,j=13.5hz,1h),3.22(d,j=13.5hz,1h),3.10
–
3.01(m,2h),2.19(s,3h);
13
c nmr(151mhz,cdcl3)δ203.6,178.5,159.2,147.8,137.4,135.1,134.0,132.9,130.3,130.2,128.9,128.4,128.3,127.9,127.5,127.4,127.3,126.7,126.0,74.7,43.2,36.7,30.9.hrms(esi)m/z:[m+h]
+
calcd for c
27h23
clno3444.1361;found:444.1362。
[0099]
实施例16:合成化合物
ⅰ‑
p
[0100][0101]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
g 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-p,无色油状物;收率为82%;z:e》20:1。
[0102]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.75
–
7.62(m,2h),7.38
–
7.26(m,5h),7.24
–
7.05(m,7h),5.80(t,j=7.8hz,1h),3.28(d,j=13.5hz,1h),3.21(d,j=13.5hz,1h),3.10
–
3.01(m,2h),2.38(s,3h),2.19(s,3h);
13
c nmr(101mhz,cdcl3)δ203.7,179.1,160.5,147.7,138.8,137.4,134.2,133.7,130.3,128.9,128.8,128.4,128.3,128.3,127.4,127.3,126.9,125.5,125.2,74.6,43.3,36.7,30.9,21.4.hrms(esi)m/z:[m+h]
+
calcd for c
28h26
no3424.1907;found:424.1919。
[0103]
实施例17:合成化合物
ⅰ‑q[0104][0105]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
h 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-q,无色油状物;收率为84%;z:e》20:1。
[0106]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.51
–
7.47(m,2h),7.32
–
7.27(m,3h),7.21
–
7.14(m,6h),7.14
–
7.10(m,2h),5.79(t,j=7.7hz,1h),3.27(d,j=13.5hz,1h),3.20(d,j=13.4hz,1h),3.05(d,j=7.7hz,2h),2.34(s,3h),2.33(s,3h),2.19(s,3h);
13
c nmr
(101mhz,cdcl3)δ203.7,179.1,160.7,147.7,138.6,137.4,134.7,134.2,130.3,128.9,128.4,128.3,127.4,127.3,126.9,125.7,125.4,74.5,43.3,36.8,30.9,21.3.hrms(esi)m/z:[m+h]
+
calcd for c
29h28
no3438.2064;found:438.2072。
[0107]
实施例18:合成化合物
ⅰ‑r[0108][0109]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
i 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-r,无色油状物;收率为81%;z:e》20:1。
[0110]
结构鉴定:1h nmr(400mhz,cdcl3)δ7.43
–
7.34(m,1h),7.30
–
7.23(m,3h),7.18(d,j=7.0hz,3h),7.16
–
7.10(m,4h),6.95
–
6.85(m,2h),5.71(t,j=7.7hz,1h),3.23(d,j=13.5hz,1h),3.18(d,j=13.5hz,1h),3.11
–
2.96(m,2h),2.13(s,3h);
13
c nmr(101mhz,cdcl3)δ203.8,178.3,161.1(dd,j1=262.6hz,j2=5.4hz),153.7(d,j=2.2hz),148.1,137.3,133.9(d,j=10.4hz),133.7,130.4,128.9,128.4,127.6,127.4,126.1,112.4,112.3(d,j=1.8hz),112.2(d,j=1.6hz),112.1,74.8,43.2,36.5,30.8.hrms(esi)m/z:[m+h]
+
calcd for c
27h22
f2no3446.1562;found:446.1561。
[0111]
实施例19:合成化合物
ⅰ‑s[0112][0113]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
i 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-s,无色油状物;收率为74%;z:e》20:1。
[0114]
结构鉴定:1h nmr(600mhz,cdcl3)δ8.23(d,j=1.7hz,1h),7.95
–
7.89(m,1h),7.84
–
7.74(m,3h),7.52
–
7.47(m,1h),7.47
–
7.42(m,1h),7.19
–
7.15(m,3h),7.14
–
7.10(m,2h),7.09
–
7.00(m,5h),5.75(t,j=7.7hz,1h),3.23(d,j=13.5hz,1h),3.16(d,j=13.5hz,1h),3.07
–
2.96(m,2h),2.12(s,3h);
13
c nmr(151mhz,cdcl3)δ203.7,179.0,160.4,147.8,137.4,135.4,134.2,132.6,130.3,129.4,129.2,128.9,128.5,128.3,128.3,128.0,127.4,127.3,127.1,126.8,123.5,122.7,74.8,43.4,36.8,30.9.hrms(esi)m/z:[m+na]
+
calcd for c
31h25
nano3482.1727;found:482.1732。
[0115]
实施例20:合成化合物
ⅰ‑
t
[0116][0117]
在一根干燥的反应试管中依次加入烯基环状碳酸乙烯酯
ⅱ‑
a 0.1mmol,吖内酯
ⅲ‑
i 0.1mmol,pd(pph3)2cl2(5mol%)和配体l4(10mol%),以及溶剂氯苯(1ml),反应混合液在0℃下搅拌反应;反应完全后,粗产品经柱色谱分离纯化得化合物i-s,无色油状物;收率为79%;z:e》20:1。
[0118]
结构鉴定:1h nmr 600mhz,cdcl3)δ7.60
–
7.49(m,2h),7.33
–
7.27(m,3h),7.23
–
7.15(m,5h),7.15
–
7.10(m,2h),7.10
–
7.04(m,1h),5.86
–
5.72(m,1h),3.26(dd,j=13.6,3.8hz,1h),3.20(dd,j=13.5,3.8hz,1h),3.11
–
3.00(m,2h),2.20(d,j=3.8hz,3h);
13
c nmr(151mhz,cdcl3)δ203.7,178.4,156.1,147.8,137.4,134.1,132.0,131.9,130.3,128.9,128.4,128.3,128.2,128.0,127.4,127.3,126.7,74.6,43.3,36.7,30.9.hrms(esi)m/z:[m+h]
+
calcd for c
25h22
no3s416.1315;found:416.1324。
[0119]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1