LncRNAIFA吸附miR-26a在猪卵巢颗粒细胞中的应用
本发明属于细胞工程和基因工程,具体涉及lncrna ifa吸附mir-26a在猪卵巢颗粒细胞中的应用。
背景技术:
1、lncrna通常指长度超过200个核苷酸连接的内源性细胞rna分子,具有与mrna类似的结构,但不具备蛋白编码的能力,然而大量的研究早已表明,lncrna并非都是转录噪音,许多lncrna通过不同的机制,在包括机体发育、疾病等过程中均发挥着极其重要的生物学功能。lncrna作为竞争性内源rna(cerna)与mrna竞争吸附mirna从而促进mrna的表达,是lncrna经典的生物学作用模式。
2、lncrna ifa(inhibitor of follicular atresia,暂命名)为针对猪卵巢颗粒细胞进行rna-seq所获得的lncrna。lncrna ifa可以抑制卵巢颗粒细胞的凋亡、促进卵巢颗粒细胞的增殖与细胞周期进程,并增强卵巢颗粒细胞的细胞活性。
3、micrornas(mirnas)是一种内源性的非编码rna,长度通常为23个核苷酸连接,mirna最常见的生物学作用模式是通过与蛋白质编码基因的mrna配对从而对基因发挥转录后的抑制效果,从而调控基因的表达。
4、mir-26a作为一种mirna,在不同种类的细胞中均有着重要的生物学功能,目前已经有大量的研究表明mir-26a可以通过对基因的转录后调控进而影响细胞的凋亡、分化、增殖及迁移等。研究显示,mir-26a可以通过靶向hmga1基因,促进肺癌肿瘤的进展;在肉骨瘤和膀胱癌细胞中,mir-26a呈现低表达,并抑制细胞的增殖、迁移与侵袭;在猪卵巢颗粒细胞中,mir-26a可以促进细胞凋亡、抑制细胞增殖与细胞周期进程,并降低细胞活性。
技术实现思路
1、为解决相关问题,本发明的首要目的在于提供一种调控猪卵巢颗粒细胞lncrnaifa表达的方法。
2、本发明的另一目的在于提供lncrna ifa吸附mir-26a在猪卵巢颗粒细胞中的应用。
3、为了实现上述发明目的,本发明采用以下技术方案:
4、一种调控猪卵巢颗粒细胞lncrna ifa表达的方法,体外环境下,mir-26a通过靶向lncrna ifa的rna分子从而负调控猪卵巢颗粒细胞中lncrna ifa的表达;通过调节mir-26a的表达水平,可实现猪卵巢颗粒细胞中lncrna ifa表达的调控;所述的lncrna ifa的核苷酸序列如seq id no:1所示。
5、进一步地,mir-26a可以与lncrna ifa的rna分子结合并调控其表达水平,mir-26a的表达水平升高,lncrna ifa表达量上升,mir-26a的表达水平降低,lncrna ifa表达量下降。
6、进一步地,mir-26a的表达水平升高通过mir-26a模拟物实现,采用的mir-26amimic是针对mir-26a成熟mirna设计并合成的小片段单链rna,所述小片段单链rna的序列与相应的mirna序列相同。所述过表达mir-26a时采用的mir-26a mimic的序列为:5’-uucaaguaauccaggauaggcu-3’(seq id no.4)。
7、进一步地,mir-26a的表达水平降低通过mir-26a核酸抑制物实现,采用的mir-26ainhibitor是针对mir-26a成熟mirna设计并合成的小片段单链rna,所述小片段单链rna的序列与相应的mirna序列反向互补。所述干扰mir-26a时采用的mir-26a inhibitor的序列为:5’-agccuauccuggauuacuugaa -3’(seq id no.5)。
8、lncrna ifa竞争性吸附mir-26a在猪卵巢颗粒细胞中的应用,体外环境的猪卵巢颗粒细胞中,由增加外源性lncrna ifa引起的促进细胞增殖、抑制细胞凋亡、促进细胞活性、促进细胞周期进程中的任意一种或多种功能表型,能在增加外源性mir-26a后逆转。
9、进一步地,增加外源性lncrna ifa通过基因过表达技术实现,采用的基因过表达载体通过如下方式制备得到:
10、(1)提取猪卵巢颗粒细胞的rna,将其逆转录成cdna,以cdna为模板进行pcr扩增,得到目的片段;
11、(2)将目的片段连接到用限制性内切酶bamh i和xba i酶切后的pcdna3.1载体上,得到重组载体。
12、步骤(1)中进行pcr扩增所用引物如下所示:
13、lncrna ifa f:5’-ggcgatgcctgggtacatgg-3’;
14、lncrna ifa r:5’-gagaccgcgtccactccgcc-3’。
15、本发明所述lncrna ifa(inhibitor of follicular atresia,暂命名)为针对猪卵巢颗粒细胞进行rna-seq所获得的lncrna,其核苷酸序列如seq id no:1所示。
16、本发明前期通过基因工程和细胞工程技术,发现lncrna ifa可以促进卵巢颗粒细胞的增殖、抑制凋亡,同时增强卵巢颗粒细胞的细胞活性,加快卵巢颗粒细胞的细胞周期进程。具体为通过edu(5-ethynyl-2'-deoxyuridine)实验证明,在体外环境下,过表达lncrnaifa可以促进卵巢颗粒细胞的增殖(p<0.01),而干扰lncrna ifa则抑制卵巢颗粒细胞的增殖(p<0.05);通过cck8(cell counting kit-8)实验证明,在体外环境下,过表达lncrnaifa后卵巢颗粒细胞的细胞活性显著增强(p<0.01),而干扰lncrna ifa后卵巢颗粒细胞的细胞活性被显著抑制(p<0.01);通过流式细胞术(flow cytometry,fcm)实验证明,在体外环境下,过表达lncrna ifa可显著抑制卵巢颗粒细胞的凋亡(p<0.01),并加快卵巢颗粒细胞的细胞周期进程(p<0.05),干扰lncrna ifa后,卵巢颗粒细胞凋亡率显著下降(p<0.001),且细胞周期进程被显著抑制(p<0.01)。
17、本发明前期通过生物信息学手段,确定了lncrna ifa序列中存在的mir-26a结合位点。
18、本发明的验证结果如下:
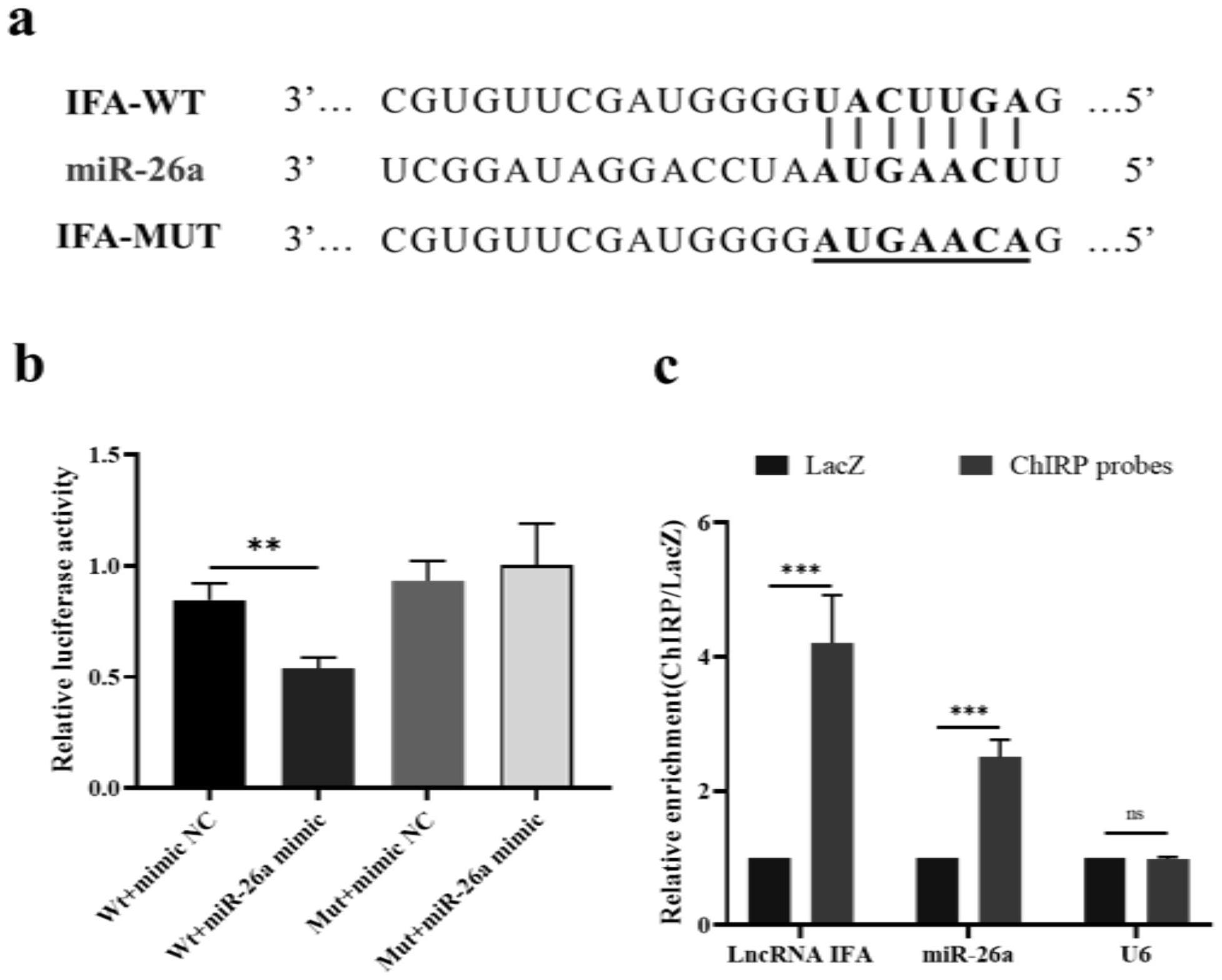
19、1、本发明通过生物信息学手段预测到lncrna ifa序列中存在的mir-26a结合序列,预测结果显示lncrna ifa序列中存在一个mir-26a的结合位点(图1中a)。
20、2、本发明通过pull down实验检测到,lncrna ifa与mir-26a存在直接结合(图1中b)。
21、3、本发明通过双荧光素酶实验检测到,与转染pglo-ifa-wt+mimic nc组的细胞相比,pglo-ifa-wt+mir-26a mimic组的细胞相对荧光活性显著下降;而pglo-ifa-mut+mimicnc组与pglo-ifa-mut+mir-26a mimic组细胞的相对荧光活性无显著差异(图1中c)。
22、4、本发明通过qpcr检测到,在过表达mir-26a后,lncrna ifa的表达量显著下降,而干扰mir-26a后,lncrna ifa的表达量显著上升(图2)。
23、5、本发明通过cck8(cell counting kit-8)实验证明,在体外环境下,过表达lncrna ifa后卵巢颗粒细胞的细胞活性显著增强;而同时过表达lncrna ifa与mir-26a后卵巢颗粒细胞的细胞活性又出现了显著下降(图4中c)。
24、6、本发明通过流式细胞术(flow cytometry,fcm)实验证明,在体外环境下,过表达lncrna ifa可显著抑制卵巢颗粒细胞的凋亡,并加快卵巢颗粒细胞的细胞周期进程;而同时过表达lncrna ifa与mir-26a后卵巢颗粒细胞的凋亡比例出现回升,细胞周期进程被再次阻滞(图3)。
25、7、本发明通过edu(5-ethynyl-2'-deoxyuridine)实验证明,在体外环境下,过表达lncrna ifa后卵巢颗粒细胞的增殖率显著升高;而同时过表达lncrna ifa与mir-26a后卵巢颗粒细胞的增殖率又出现了显著下降(图4中b)。
26、本发明以lncrna ifa与mir-26a为研究对象,采用分子细胞生物学的方法,首先验证了lncrna ifa与mir-26a的直接结合;随后检测了mir-26a对lncrna ifa表达量的调控,证明了mir-26a对lncrna ifa的表达量存在负调控;最后研究了lncrna ifa与mir-26a对卵巢颗粒细胞增殖、凋亡、活性及周期的影响,证实了mir-26a可以逆转lncrna ifa对卵巢颗粒细胞的凋亡与增殖、周期、活性的影响。
27、本发明相对于现有技术具有如下的优点及效果:
28、本发明通过生物信息学与分子生物学实验预测并验证了lncrna ifa序列中存在的mir-26a结合位点;在过表达或干扰mir-26a后检测了lncrna ifa的表达量;在过表达lncrna ifa及mir-26a后检测了卵巢颗粒细胞的细胞活性、增殖和凋亡水平、细胞周期进程的变化,为卵巢颗粒细胞的增殖凋亡调控机制研究积累了材料。本研究的发明结果显示,lncrna ifa可以通过竞争性吸附mir-26a,发挥其促进卵巢颗粒细胞增殖、抑制卵巢颗粒细胞凋亡、加快卵巢颗粒细胞的细胞周期进程,同时提高卵巢颗粒细胞活性的生物学功能。
- 还没有人留言评论。精彩留言会获得点赞!