基于生物酶定向剪切技术的人源胶原蛋白制备方法与流程
1.本发明涉及人源胶原蛋白生产具领域,特别是一种基于生物酶定向剪切技术的人源胶原蛋白制备方法。
背景技术:
2.人源胶原蛋白是利用基因工程技术,得到巴氏毕赤酵母基因工程菌;对基因工程菌进行发酵培养,实现重组人源胶原蛋白的诱导表达,得到含有重组人源胶原蛋白的发酵液;从发酵液中纯化重组人源胶原蛋白。
3.随着现代生物技术的发展,利用转基因技术和基因重组技术,可以在动物、植物和微生物表达体系获得重组人胶原蛋白,解决了传统提取方法存在的病毒隐患等缺点,同时也改善了胶原蛋白的亲水性、免疫排异性等。国内外一些研究机构及生物公司相继投入研究开发重组胶原蛋白,杨霞等在2012 年通过重复iii型胶原肽段并与ii型胶原肽段融合在大肠杆菌中获得高表达;我国西北大学的范代娣等利用大肠杆菌通过高密度发酵培养生产类人胶原蛋白,得到高表达的类人胶原,并以此为原材料开发组织工程材料和化妆品,但其设计的部分氨基酸序列并非人源胶原蛋白序列,同时,细菌表达产生的致热源使表达产物难以应用于临床,而且目的蛋白常以包涵体形式表达,致使产物纯化困难,另外原核表达系统的翻译后修饰加工体系不完善,表达产物的生物活性较低等缺点影响产品的品质。因此,在制备人源胶原蛋白的技术领域,亟需开发一种纯度高、安全性高、亲水性强、生物相容性好的人源胶原蛋白,并且可以实现不在细菌上进行表达的方法。
4.另外现有的人源胶原蛋白在生产时,还存在如下问题:发酵周期过长,发酵水平较低,而且制备得到的重组人源胶原蛋白溶液的稳定性差,容易析出,重组人源胶原蛋白生物学活性难以长期保持。
技术实现要素:
5.本发明的目的在于提供一种基于生物酶定向剪切技术的人源胶原蛋白制备方法,解决背景技术中提到的问题。
6.为解决上述的技术问题,本发明采用以下技术方案:一种基于生物酶定向剪切技术的人源胶原蛋白制备方法,包括如下步骤(1)优选人源蛋白中iii型胶原蛋白基因螺旋区的dna片段,利用crispr基因编辑技术和pcr技术将dna片段进行密码子优化和拼接重组,利用引物中加入的酶切位点,将基因片段切成粘性末端,并与相应酶切处理过的pet-22b 的表达载体共孵育,加入t4dna连接酶,4℃连接12小时,转化大肠杆菌dh5α;用氨苄青霉素钠-lb平板筛选挑出白斑克隆,利用分子克隆的碱裂解法或者煮沸法提取质粒,提取质粒后进行测序确定重组质粒含有正确的基因序列阅读框架,构建成功重组表达载体,将其命名为pet22b-ntod;(2)将得到的pet22b-ntod与毕赤酵母进行混合转化,挑取单克隆,并对其扩大培养后获得重组基因工程菌;(3)将步骤(2)获得的重组基因工程菌接种后进行发酵培养获得发酵液;(4)收集步骤(3)中的发酵液,离心获
得发酵液上清液,对发酵液上清液进行纯化后获得最终产物。
7.利用了crispr基因编辑技术和pcr技术,对基因进行优化和编辑,将dna片段进行密码子优化和拼接重组,使得制作出来的人源化胶原蛋白使用时的水溶性更好,并且可以适应使用者的体温标准,提高使用者使用重组人源胶原蛋白与人体的相容性,应用于人体上时减少人体的免疫排斥和过敏现象,方便对医药医疗的应用。
8.作为本发明的进一步优选,所述步骤(2)将pet22b-ntod与毕赤酵母进行混合转化,挑取单克隆具体是指将重组质粒pet22b-ntod转入毕赤酵母x33感受态细胞中,培养,得阳性转化子x33/pet22b-ntod感受态细胞;再利用阳性转化子x33/pet22b-ntod感受态细胞进行培养,对所得菌株进行筛选,得到产人源蛋白重组基因工程菌株,挑取单克隆。
9.该方法构建的产人源蛋白重组基因工程菌株活力高,稳定性好。
10.作为本发明的进一步优选,所述步骤(3)中加入的毕赤酵母重组基因工程菌种液与发酵培养基的质量份数分别为毕赤酵母重组基因工程菌种液45-48份、发酵培养基500-600份。
11.作为本发明的进一步优选,所述步骤(3)中的发酵过程包括四个阶段,所述四个阶段依次分别为起始发酵阶段、补充甘油发酵阶段、甲醇诱导发酵阶段和最终稳定发酵阶段,所述起始发酵阶段时搅拌转速为200rpm、罐压为0.05mpa,调节空气流量和转速使溶氧>30%,起始发酵阶段的ph值为控制在5.5;当碳源耗尽后,溶氧陡然上升时开始补充甘油发酵阶段,补充甘油发酵阶段开始流加50%甘油,补充碳源,至菌体湿重为214g/l,停止补加甘油,此时发酵培养时间为14小时;甘油耗尽后开始甲醇诱导发酵阶段,甲醇诱导发酵阶段需要将ph值控制在5,甲醇诱导发酵阶段开始流加10%(w/v)甘油含量的甘油-甲醇混合液,调节转速、空气流量和流加甲醇速度使溶氧>22%,甲醇诱导发酵阶段的时间为76h,76h后停止流加甘油-甲醇混合液进入最终稳定发酵阶段,最终稳定发酵阶段流加甲醇,最终稳定发酵阶段的时间为5h。
12.化了毕赤酵母的发酵工艺,解决了发酵周期过长,发酵水平较低的问题,其次本发明创造性的利用镍琼脂糖凝胶柱结合葡聚糖凝胶柱对重组人源胶原蛋白进行分离纯化,纯化工艺相对简单,得到的蛋白纯度较高;而且,本发明对纯化过程中使用的各种溶液的组分、浓度及ph进行优化,并且在得到的目的蛋白洗脱液中添加合适浓度的牛血清白蛋白和edta-2na,得到重组人源胶原蛋白保存液,显著提高了重组人源胶原蛋白的稳定性,有利于重组人源胶原蛋白活性的长期保持,另外可以看到由于本发明中的使用的制作提取质粒时使用了crispr基因编辑技术和pcr技术进行改造,因此发酵效果明显得到了提高。
13.作为本发明的进一步优选,所述起始发酵阶段和补充甘油发酵阶段的培养温度为30~32℃,甲醇诱导发酵阶段的培养温度为28~30℃,最终稳定发酵阶段的培养温度为27~28℃。
14.本发明在发酵过程中,在不同的培养阶段控制不同的温度,可以控制菌体生长,提高了重组人源胶原蛋白的生物合成速率,发酵时间缩短的同时重组人源胶原蛋白的表达量增加,表达量可达27g/l,发酵水平提高了30%以上,节约了生产成本,特别适用于重组人源胶原蛋白的工业化大规模生产,能够为产业化生产带来巨大的实际应用价值。
15.作为本发明的进一步优选,在甲醇诱导发酵阶段向发酵培养基中加入谷胱甘肽,其中谷胱甘肽的加入量为0.1~1g/l。
16.本发明在发酵过程中,选取在甲醇诱导发酵阶段加入谷胱甘肽,提高了重组人源胶原蛋白的生物合成速率,并且采用连续流加的方式,能够进一步提高重组人源胶原蛋白的生物合成速率,发酵时间缩短,同时重组人源胶原蛋白的表达量增加,结合温度以及基因编辑的效果发酵水平提高了55%以上,节约了生产成本,有利于重组人源胶原蛋白的工业化大规模生产。
17.作为本发明的进一步优选,所述甲醇诱导发酵阶段完成后向发酵罐中一次性添加0.2~0.5ml-赖氨酸或l-精氨酸。
18.发酵过程中,通过在最终稳定发酵阶段前,一次性向发酵罐添加0.2-0.5ml-lys或0.2-0.5ml-arg,使得大罐发酵产物重组人源胶原蛋白稳定保留90%以上。同时l-lys市场价格约240元/kg,l-arg约70元/kg,明显降低了生产用的氨基酸成本,减少企业人力、物力的损失,稳定供货,为企业产生巨大的经济价值。
19.作为本发明的进一步优选,所述发酵培养时培养基由如下原料制成85%h3po426.7ml/l;caso4
·
2h2o1.175g/l;k2so418.2g/l;mgso4
·
7h2o14.9g/l;koh4.13g/l;甘油40.0g/l;ptm14.35ml/l;丙酮酸钠0.5g/l。
20.作为本发明的进一步优选,所属步骤(4)中离心获得发酵液上清液时离心的转速为12000-16000rpm,离心的时间为30-50min。
21.与现有技术相比,本发明至少能达到以下有益效果中的一项:1、利用了crispr基因编辑技术和pcr技术,对基因进行优化和编辑,将dna片段进行密码子优化和拼接重组,使得制作出来的人源化胶原蛋白使用时的水溶性更好,并且可以适应使用者的体温标准,提高使用者使用重组人源胶原蛋白与人体的相容性,应用于人体上时减少人体的免疫排斥和过敏现象,方便对医药医疗的应用。
22.2、在发酵过程中精确控制各个阶段的温度,提高了重组人源胶原蛋白的生物合成速率,发酵时间缩短的同时重组人源胶原蛋白的表达量增加,表达量可达27g/l,发酵水平提高了30%以上,节约了生产成本,特别适用于重组人源胶原蛋白的工业化大规模生产,能够为产业化生产带来巨大的实际应用价值。
23.3、在甲醇诱导发酵阶段加入谷胱甘肽,进一步提高了重组人源胶原蛋白的生物合成速率,采用连续流加的方式,发酵时间缩短,同时重组人源胶原蛋白的表达量增加,结合温度以及基因编辑的效果发酵水平提高了55%以上,节约了生产成本,更有利于重组人源胶原蛋白的工业化大规模生产。
24.4、发酵过程中,通过在最终稳定发酵阶段前,一次性向发酵罐添加0.2-0.5ml-lys或0.2-0.5ml-arg,使得大罐发酵产物重组人源胶原蛋白稳定保留90%以上。同时l-lys市场价格约240元/kg,l-arg约70元/kg,明显降低了生产用的氨基酸成本,减少企业人力、物力的损失,稳定供货,为企业产生巨大的经济价值。
25.具体实施方式
26.为使本发明实施方式的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明实施方式中的技术方案进行清楚、完整地描述,显然,所描述的实施方式是本发明一部分实施方式,而不是全部的实施方式。
27.需要说明的是,在不冲突的情况下,本发明中的实施方式及实施方式中的特征可以相互组合。
28.在本发明的描述中,需要说明的是,术语“中心”、“上”、“下”、“左”、“右”、“竖直”、“水平”、“内”、“外”等指示的方位或位置关系为基于所示的方位或位置关系,或者是该发明产品使用时惯常摆放的方位或位置关系,或者是本领域技术人员惯常理解的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,术语“第一”、“第二”等仅用于区分描述,而不能理解为指示或暗示相对重要性。
29.在本发明的描述中,还需要说明的是,除非另有明确的规定和限定,术语“设置”、“安装”、“相连”、“连接”应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是直接相连,也可以通过中间媒介间接相连,可以是两个元件内部的连通。对于本领域的普通技术人员而言,可以具体情况理解上述术语在本发明中的具体含义。
30.具体实施例1:一种基于生物酶定向剪切技术的人源胶原蛋白制备方法,包括如下步骤(1)优选人源蛋白中iii型胶原蛋白基因螺旋区的dna片段,利用crispr基因编辑技术和pcr技术将dna片段进行密码子优化和拼接重组,利用引物中加入的酶切位点,将基因片段切成粘性末端,并与相应酶切处理过的pet-22b 的表达载体共孵育,加入t4dna连接酶,4℃连接12小时,转化大肠杆菌dh5α;用氨苄青霉素钠-lb平板筛选挑出白斑克隆,利用分子克隆的碱裂解法或者煮沸法提取质粒,提取质粒后进行测序确定重组质粒含有正确的基因序列阅读框架,构建成功重组表达载体,将其命名为pet22b-ntod;(2)将得到的pet22b-ntod与毕赤酵母进行混合转化,挑取单克隆,并对其扩大培养后获得重组基因工程菌;(3)将步骤(2)获得的重组基因工程菌接种后进行发酵培养获得发酵液;(4)收集步骤(3)中的发酵液,离心获得发酵液上清液,对发酵液上清液进行纯化后获得最终产物。
31.利用了crispr基因编辑技术和pcr技术,对基因进行优化和编辑,将dna片段进行密码子优化和拼接重组,使得制作出来的人源化胶原蛋白使用时的水溶性更好,并且可以适应使用者的体温标准,提高使用者使用重组人源胶原蛋白与人体的相容性,应用于人体上时减少人体的免疫排斥和过敏现象,方便对医药医疗的应用。
32.具体实施例2:本实施例是在具体实施例1的基础上对步骤(2)进行了进一步的说明,所述步骤(2)将pet22b-ntod与毕赤酵母进行混合转化,挑取单克隆具体是指将重组质粒pet22b-ntod转入毕赤酵母x33感受态细胞中,培养,得阳性转化子x33/pet22b-ntod感受态细胞;再利用阳性转化子x33/pet22b-ntod感受态细胞进行培养,对所得菌株进行筛选,得到产人源蛋白重组基因工程菌株,挑取单克隆。
33.该方法构建的产人源蛋白重组基因工程菌株活力高,稳定性好。
34.具体实施例3:本实施例是在具体实施例1的基础上对步骤(3)进行了进一步的说明,所述步骤(3)中加入的毕赤酵母重组基因工程菌种液与发酵培养基的质量份数分别为毕赤酵母重组基因工程菌种液45份、发酵培养基500份。
35.具体实施例4:本实施例是在具体实施例1的基础上对步骤(3)进行了进一步的说明,所述步骤(3)中加入的毕赤酵母重组基因工程菌种液与发酵培养基的质量份数分别为毕赤酵母重组基因工程菌种液46份、发酵培养基600份。
36.具体实施例5:本实施例是在具体实施例1的基础上对步骤(3)进行了进一步的说明,所述步骤(3)中加入的毕赤酵母重组基因工程菌种液与发酵培养基的质量份数分别为毕赤酵母重组基因工程菌种液48份、发酵培养基580份。
37.具体实施例6:本实施例是在具体实施例1的基础上对步骤(3)进行了进一步的说明,所述步骤(3)中的发酵过程包括四个阶段,所述四个阶段依次分别为起始发酵阶段、补充甘油发酵阶段、甲醇诱导发酵阶段和最终稳定发酵阶段,所述起始发酵阶段时搅拌转速为200rpm、罐压为0.05mpa,调节空气流量和转速使溶氧>30%,起始发酵阶段的ph值为控制在5.5;当碳源耗尽后,溶氧陡然上升时开始补充甘油发酵阶段,补充甘油发酵阶段开始流加50%甘油,补充碳源,至菌体湿重为214g/l,停止补加甘油,此时发酵培养时间为14小时;甘油耗尽后开始甲醇诱导发酵阶段,甲醇诱导发酵阶段需要将ph值控制在5,甲醇诱导发酵阶段开始流加10%(w/v)甘油含量的甘油-甲醇混合液,调节转速、空气流量和流加甲醇速度使溶氧>22%,甲醇诱导发酵阶段的时间为76h,76h后停止流加甘油-甲醇混合液进入最终稳定发酵阶段,最终稳定发酵阶段流加甲醇,最终稳定发酵阶段的时间为5h。
38.化了毕赤酵母的发酵工艺,解决了发酵周期过长,发酵水平较低的问题,其次本发明创造性的利用镍琼脂糖凝胶柱结合葡聚糖凝胶柱对重组人源胶原蛋白进行分离纯化,纯化工艺相对简单,得到的蛋白纯度较高;而且,本发明对纯化过程中使用的各种溶液的组分、浓度及ph进行优化,并且在得到的目的蛋白洗脱液中添加合适浓度的牛血清白蛋白和edta-2na,得到重组人源胶原蛋白保存液,显著提高了重组人源胶原蛋白的稳定性,有利于重组人源胶原蛋白活性的长期保持,另外可以看到由于本发明中的使用的制作提取质粒时使用了crispr基因编辑技术和pcr技术进行改造,因此发酵效果明显得到了提高。
39.具体实施例7:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,所述起始发酵阶段和补充甘油发酵阶段的培养温度为30~32℃,甲醇诱导发酵阶段的培养温度为28~30℃,最终稳定发酵阶段的培养温度为27~28℃。
40.本发明在发酵过程中,在不同的培养阶段控制不同的温度,可以控制菌体生长,提高了重组人源胶原蛋白的生物合成速率,发酵时间缩短的同时重组人源胶原蛋白的表达量增加,表达量可达27g/l,发酵水平提高了30%以上,节约了生产成本,特别适用于重组人源胶原蛋白的工业化大规模生产,能够为产业化生产带来巨大的实际应用价值。
41.具体实施例8:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,在甲醇诱导发酵阶段向发酵培养基中加入谷胱甘肽,其中谷胱甘肽的加入量为0.1g/l。
42.本发明在发酵过程中,选取在甲醇诱导发酵阶段加入谷胱甘肽,提高了重组人源胶原蛋白的生物合成速率,并且采用连续流加的方式,能够进一步提高重组人源胶原蛋白
的生物合成速率,发酵时间缩短,同时重组人源胶原蛋白的表达量增加,结合温度以及基因编辑的效果发酵水平提高了55%以上,节约了生产成本,有利于重组人源胶原蛋白的工业化大规模生产。
43.具体实施例9:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,在甲醇诱导发酵阶段向发酵培养基中加入谷胱甘肽,其中谷胱甘肽的加入量为0.6g/l。
44.具体实施例10:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,在甲醇诱导发酵阶段向发酵培养基中加入谷胱甘肽,其中谷胱甘肽的加入量为1g/l。
45.具体实施例11:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,所述甲醇诱导发酵阶段完成后向发酵罐中一次性添加0.2ml-赖氨酸或l-精氨酸。
46.发酵过程中,通过在最终稳定发酵阶段前,一次性向发酵罐添加0.2-0.5ml-lys或0.2-0.5ml-arg,使得大罐发酵产物重组人源胶原蛋白稳定保留90%以上。同时l-lys市场价格约240元/kg,l-arg约70元/kg,明显降低了生产用的氨基酸成本,减少企业人力、物力的损失,稳定供货,为企业产生巨大的经济价值。
47.具体实施例12:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,所述甲醇诱导发酵阶段完成后向发酵罐中一次性添加0.3ml-赖氨酸或l-精氨酸。
48.具体实施例13:本实施例是在具体实施例6的基础上对发酵过程进行了进一步的说明,所述甲醇诱导发酵阶段完成后向发酵罐中一次性添加0.5ml-赖氨酸或l-精氨酸。
49.具体实施例14:本实施例是在具体实施例1的基础上对发酵培养进行了进一步的说明,所述发酵培养时培养基由如下原料制成85%h3po426.7ml/l;caso4
·
2h2o1.175g/l;k2so418.2g/l;mgso4
·
7h2o14.9g/l;koh4.13g/l;甘油40.0g/l;ptm14.35ml/l;丙酮酸钠0.5g/l。
50.具体实施例15:本实施例是在具体实施例1的基础上对步骤(4)进行了进一步的说明,所属步骤(4)中离心获得发酵液上清液时离心的转速为12000rpm,离心的时间为50min。
51.具体实施例16:本实施例是在具体实施例1的基础上对步骤(4)进行了进一步的说明,所属步骤(4)中离心获得发酵液上清液时离心的转速为14000rpm,离心的时间为30min。
52.具体实施例17:本实施例是在具体实施例1的基础上对步骤(4)进行了进一步的说明,所属步骤(4)中离心获得发酵液上清液时离心的转速为16000rpm,离心的时间为35min。
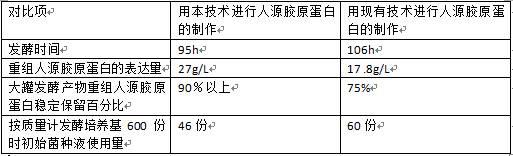
53.与国内现有技术相比本方案的优势如下表所示:
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1