循环肿瘤细胞在制备微血管侵犯分级评估试剂盒中的应用
1.本发明涉及医学检测技术领域,尤其涉及循环肿瘤细胞在制备微血管侵犯分级评估试剂盒中的应用。
背景技术:
2.微血管侵犯(mvi),主要指在显微镜下于内皮细胞衬覆的血管腔内见到癌细胞巢团。大量研究证实了微血管侵犯(mvi)与肝癌不良预后之间的相关性。提早发现(比如在术前进行预判)微血管侵犯 (mvi)对医生手术策略的制定和术后综合治疗均具有重要指导意义。
3.研究显示血管侵犯是肿瘤细胞脱离原发灶进入血液循环形成循环肿瘤细胞(circulating tumor cells,ctcs)最重要的途径,而mvi作为血管侵犯的主要环节,在ctcs形成的过程中也可能起到一定的促进作用。与单个肿瘤病灶进行活检相比,ctcs不仅创伤小,而且能够更好地反映整个肿瘤的特性,因此被称为“液体活检”。之前报道肝癌ctcs与大血管侵犯(门静脉癌栓)的发生紧密相关,针对大血管侵犯目前术前通过影像学已经可以准确地诊断,从而指导治疗,但是血管侵犯的另一特殊类型mvi是否可通过检测ctcs而辅助术前预测还没有相关的实验报道。
4.肝癌mvi可精细化分级为m0、m1、m2三个不同级别——
5.m0:即未发现,在肿瘤组织的切片内未发现微血管侵犯,预后通常尚可;
6.m1:即低危组,在全部组织切片内的微血管侵犯数≤5个,且微血管侵犯发生于近癌旁肝组织;
7.m2:即高危组,在肿瘤组织切片内的微血管侵犯数>5个,或者微血管侵犯发生于远癌旁肝组织。
8.目前术前预测mvi主要依靠影像学检查、宏观的肿瘤特点以及血清标志物,并不能准确判断患者mvi分级情况。
技术实现要素:
9.为了解决现有技术的不足,本发明提供了循环肿瘤细胞在制备微血管侵犯分级评估的试剂盒中的应用,研究显示循环肿瘤细胞的数量可作为精确化微血管侵犯分级评估的重要指标。本发明还提供了一种微血管侵犯分级评估的试剂盒,不但能够区分是否存在微血管侵犯还可实现m1、m2的精细化分级,有助于提高术前对肝癌患者预后不良程度地预测准确度,医护人员可依据预测结果制定更有针对性的治疗方案。
10.本发明的第一方面提供了循环肿瘤细胞在制备微血管侵犯分级评估试剂盒中的应用。
11.本发明优选的,所述微血管侵犯分级评估试剂盒为肝癌患者微血管分级评估试剂盒。
12.本发明的第二方面提供了一种微血管侵犯分级评估的试剂盒,包括外周血循环肿
瘤细胞含量检测试剂。根据外周血中循环肿瘤细胞的含量可实现对微血管侵犯的精细化分级,根据检测结果,当在肿瘤组织切片内未发现微血管侵犯时,判断微血管侵犯为m0级;当在肿瘤组织切片内的微血管侵犯数≤5个时,判断微血管侵犯为m1级;当在肿瘤组织切片内的微血管侵犯数>5个时,判断微血管侵犯为m2 级。
13.本发明优选的,所述外周血循环肿瘤细胞含量检测试剂包括磁性纳米探针。本发明进一步优选的,所述外周血循环肿瘤细胞含量检测试剂包括聚合物修饰的磁性纳米探针,所述聚合物修饰的磁性纳米探针的组成及其制备方法见中国专利cn202110738850.1记载,该专利通过全文引用的方式作为本技术说明书的一部分;在本发明的一些具体实施方式中,采用下述聚合物修饰的磁性纳米探针:所述的聚合物为阳离子型聚合物;所述的聚合物附着或包覆于磁性纳米材料表面,形成带正电荷的所述聚合物修饰的磁性纳米材料;所述的磁性纳米材料为核-壳结构,所述的核为磁性纳米粒子,所述的壳为改性层;所述的改性层附着或包覆于所述磁性纳米粒子的表面,形成改性层复合的磁性纳米粒子;其中,所述的聚合物修饰的磁性纳米材料中,所述的聚合物与所述的磁性纳米材料的质量比为1:10至20:1。
14.本发明优选的,所述外周血循环肿瘤细胞含量检测试剂还包括抗凝预处理试剂和pbs缓冲液。
15.优选的,所述试剂盒还包括总胆红素含量检测试剂、白蛋白含量检测试剂、丙氨酸氨基转移酶含量检测试剂、天冬氨酸氨基转移酶含量检测试剂、甲胎蛋白含量检测试剂、癌胚抗原含量检测试剂和碳水化合物抗原199含量检测试剂中的一种或多种;在本发明的一些具体实施方式中,试剂盒还可以包括与微血管侵犯分级评估具有强相关性的血液指标,总胆红素(tbil)含量检测试剂、白蛋白(alb)含量检测试剂和甲胎蛋白(afp)含量检测试剂中的一种或多种。
16.本发明的第三方面提供了上述技术方案所述微血管侵犯分级评估的试剂盒在制备预测肝癌患者术后预后状况的试剂盒中的应用。
17.与现有技术相比,本发明的有益效果:
18.1、本发明提供了循环肿瘤细胞在制备微血管侵犯分级评估的试剂盒中的应用以及一种微血管侵犯分级评估的试剂盒,可实现术前对微血管侵犯程度的精确化预测,以前的方法只能进行mvi存在性的判断(有或无),该方法不仅能实现mvi有无的判定,还能进一步预测mvi的精细化分级(1级或2级),有利于术前制定更有效的治疗方案,采取更具针对性,更积极的外科治疗策略。
19.2、本发明所述微血管侵犯分级评估的试剂盒仅需外周血取样,避免了传统术后病理确诊的局限性,特别是手术穿刺活检、影像学、血清标志物的不足。同时本预测方法具有快速、无创、成本低廉的特点,有利于临床推广使用。
20.3、本发明还提供了所述微血管侵犯分级评估的试剂盒在制备预测肝癌患者术后预后状况的试剂盒中的应用,本发明在临床样本的术后的随访与数据分析中发现ctc的数量水平在评估患者不良预后的准确性、便捷性等方面更为优异。
附图说明
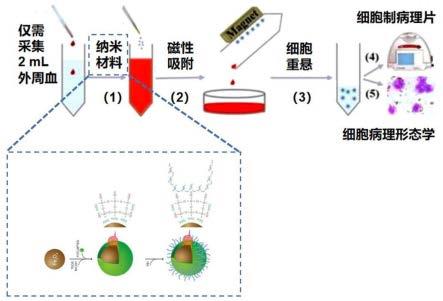
21.图1为实施例1对外周血样本检测ctcs细胞含量的方法流程图;
22.图2为实施例1中利用聚合物修饰的磁性纳米探针对临床不同 mvi等级的临床样本外周血中ctcs水平检测的结果;
23.图3为实施例1中应用迪夫-快速染色液对癌细胞进行染色的结果;
24.图4为实施例1中对肝癌患者外周血中捕获到的ctcs的典型图例,该结果已经病理学专家确认;
25.图5为实施例1中的对肝癌患者微血管侵犯(mvi)的病理判定参照图;
26.图6为实施例1中对各个指标进一步以受试者工作曲线(roc) 判断各独立因素术前预测肝癌mvi的性能,具体是通过roc曲线获得的曲线下面积(auc)对各指标的预测性能进行比较,体现ctcs 预测mvi的优异性;
27.图7是本发明实施例七中随访的研究结果,表明ctcs数量水平在肝癌患者预后评估中具有重要价值。
具体实施方式
28.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。下列实施例中未注明具体条件的实验方法,通常按照常规条件,或按照制造厂商所建议的条件。
29.实施例1
30.一、肝癌患者入组标准以及需要采集的基本临床信息内容
31.收集符合以下标准的病例:
①
术前经b超、ct和(或)mri 诊断为肝癌,无肝外转移灶,术后病理证实为肝癌;
②
首次行手术切除治疗,术前未接受任何化疗、放疗和其他治疗;
③
术中切缘距肿瘤边缘至少1cm以上,边缘阴性;
④
术前影像学检查未见大血管侵犯;
⑤
排除全身情况差,肝功能child-pugh c级。
32.收集每个病例患者的临床特征,包括性别、年龄、最大肿瘤直径、肿瘤结节数量、肿瘤边缘光滑度、肝硬化、乙型肝炎病毒感染情况。
33.以及收集常规血清学检测指标包括总胆红素(tbil)、白蛋白 (alb)、丙氨酸氨基转移酶(alt)、天冬氨酸氨基转移酶(ast)、甲胎蛋白(afp)、癌胚抗原(cea)、碳水化合物抗原199(ca199)。
34.收集并记录以上各项临床指标,尤其是对后续传统血液指标(总胆红素、白蛋白、丙氨酸氨基转移酶、天冬氨酸氨基转移酶、甲胎蛋白癌胚抗原、碳水化合物抗原199)与液体活检指标(ctc)对mvi 预测性能上的比较提供数据依据。
35.本专利纳入研究队列的肝癌患者群体共218例,患者的临床特征如表1所示。
36.表1纳入研究队列的患者临床特征
[0037][0038]
二、外周血收集ctcs细胞悬液
[0039]
如图1所示,术前采集肝癌患者外周血2ml,置于含edta的抗凝管中,分别从抗凝血标本中,取200μl十份等分试样,并加入2mlpbs。为尽可能地降低血清蛋白对电荷干扰作用。再加入60μg聚合物修饰的磁性纳米探针(nps),该聚合物修饰的磁性纳米探针的制备方法如中国专利cn202110738850.1所示。在冰上充分混合纳米探针和血液并孵育5分钟。随后将该管放置在磁性架上,保持一个管侧面向磁性侧。10分钟后,磁体将附着有nps的细胞拉到管侧,倒出该管中的上清液,用2ml pbs洗涤管子两次,同时磁体仍在原位。将管从磁性支架移除,轻轻地用200ul pbs重悬管中的内容物,获得细胞悬液。
[0040]
步骤一所述临床218例肝癌患者样本的外周血ctcs检测结果如图2所示,由图2可以看出,肝癌患者在不同的mvi分级(mvi=0/1/2) 的分组下,其ctcs数量具有显著性差异,这证明ctc是潜在的可以预测mvi等级的指标。
[0041]
三、对收集的ctcs细胞悬液进行制片并且染色
[0042]
将步骤二获得的细胞悬液利用甩片机(离心参数为1000r,5 min)制成细胞片。使用迪夫-快速染色液将该细胞片上的细胞进行细胞染色。具体步骤如下:
[0043]
(1)将片子自然干燥或酒精灯火焰处理或diff-quikfixative固定20s。
[0044]
(2)用diff-quik
ꢀⅰ
染色5~10s(上下提动玻片2-3次,使染液均匀分布),立即取
出。
[0045]
(3)放入diff-quik
ꢀⅱ
染色10~20s(上下提动玻片2-3次,使染液均匀分布),立即取出。
[0046]
(4)水洗片子后立即趁湿在显微镜下观察。
[0047]
细胞染色后的片子典型图例如图3所示,观察后将该细胞片用二甲苯透明,封固、保存。
[0048]
四、对循环肿瘤细胞进行细胞形态学鉴定
[0049]
在显微镜下,观察细胞片中细胞的核形态。如具有下列中的特征,则视为循环肿瘤细胞。
[0050]
1)核大:癌细胞核比正常大1-5倍。
[0051]
2)核大小不等:由于各个癌细胞核增大程度不一致,同一视野的癌细胞核,大小差异悬殊。
[0052]
3)核畸形核膜增厚:癌细胞核可出现明显的畸形,表现为细胞核形态不规则,呈结节状、分叶状等,核膜出现凹陷,褶皱,使核膜呈锯齿状。
[0053]
4)核深染:由于癌细胞核染色质增多,颗粒变粗,核深染,有的可呈墨水滴样,同时因核内染色质分布不均,核的染色深浅不一。
[0054]
5)核质比例失常:癌细胞核增大明显,超过细胞体积的增大,故核质比例失常。并且癌细胞分化愈差,核质比例失常愈明显。
[0055]
若患者检出循环肿瘤细胞,用可拍摄的显微镜拍照并保存,注意标记好比例尺,临床肝癌患者外周血中捕获到的ctcs典型图例如图 4所示。
[0056]
五、肝癌患者mvi情况的病理学诊断
[0057]
包括术中病理材料取材,其部位及数量按照《原发性肝癌标准化病理诊断指南(2015年版)》进行,获得病理标本。
[0058]
将上述病理标本切成2-3mm厚的连续切片,用10%甲醛固定,每个肝脏切片包埋在石蜡中并用苏木精和伊红染色进行组织病理学检查。肝癌患者mvi评估的判定准则及典型图像如图5所示。
[0059]
六、传统指标及ctcs在临床术前预测mvi的性能评价
[0060]
斯皮尔曼相关系数分析计算各因素与肝癌微血管侵犯的相关性,纳入肿瘤相关变量包括肿瘤大小,数目,包膜,边界,位置等所有基线资料,进行logistic单因素和多因素分析,找出独立预测因子。
[0061]
将独立预测因子以受试者工作曲线(roc)判断各独立因素术前预测肝癌mvi的价值,据此评价新型液体活检指标ctc的预测效果,结果如图6所示,由图6可以看出各指标在术前预测mvi的性能上 (性能可通过受试者曲线下与坐标轴围成的面积进行比较),ctc指标要优越于常规血清学指标(甲胎蛋白、白蛋白、总胆红素),具体数据为:循环肿瘤细胞的受试者工作特征曲线下面积=0.8976>甲胎蛋白的受试者工作特征曲线下面积=0.6303>白蛋白的受试者工作特征曲线下面积=0.5986>总胆红素的受试者工作特征曲线下面积=0.5442。
[0062]
七、肝癌患者随访
[0063]
术后起,每三个月给患者打电话进行随访,询问患者的生存状态。死亡记录为1,存
活记录为0。
[0064]
整合收集到的全部资料,包括患者的在不同时间点的生存状态,以及术前的ctcs水平。绘制不同ctcs数量水平的患者生存曲线,分析ctcs数量水平与患者预后的相关性。
[0065]
不同ctcs数量水平的患者生存曲线如图7所示,该曲线结果显示ctcs的数量水平对患者预后评估具有重要价值。
[0066]
综上所述,本实施例基于癌细胞表面电荷的非抗体依赖纳米技术的捕捉系统,利用聚合物修饰的磁性纳米探针稳定性好,重复性强,捕获效率高的特点,并且可以保证捕捉到的细胞活性良好,实现外周血ctcs的高效捕获,有利于进一步研究外周血ctcs的生物学功能,探讨其与肝癌发生发展的关系。通过对捕捉到的ctcs数量、形态学进行表征及分析,验证其对肝癌mvi不同等级的预测效果,同时纳入肝癌相关变量包括肿瘤大小,数目,包膜,边界,位置等所有基线资料,进行分析,比较ctcs在预判mvi等级是否具有优异性。通过患者随访,了解患者的生存状态,将该数据绘制生存曲线,可验证 ctcs在肝癌患者预后评价中是否具有价值。实验结果显示:
[0067]
(1)本实施例验证了ctcs作为检测指标可实现精细化肝癌mvi 预测,避免了传统术后病理确诊的局限性,特别是手术穿刺活检、影像学、血清标志物的不足。同时本预测方法具有快速、无创、成本低廉的特点,有利于临床推广使用。以前的方法只能进行mvi存在性的判断(有或无),该方法不仅能实现mvi有无的判定,还能进一步预测mvi的精细化分级(1级或2级),有利于术前制定更有效的治疗方案,采取更具针对性,更积极的外科治疗策略。
[0068]
(2)本实施例验证ctcs在肝癌患者预后评估的重要价值。通过聚合物修饰的磁性纳米探针实现外周血ctcs的高灵敏度检测将更有利于进一步探讨其与肝癌发生发展的关系。本发明在临床样本的术后的随访与数据分析中发现ctc的数量水平在评估患者预后具有重要意义。
[0069]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1