一种抗HIV的抗体及其制备方法和应用与流程
一种抗hiv的抗体及其制备方法和应用
技术领域
1.本发明属于细胞免疫学、基因工程领域,涉及一种抗hiv的抗体及其制备方法和应用。
背景技术:
2.人类免疫缺陷病毒(human immunodeficiency virus,hiv)是造成人类免疫系统缺陷综合征—艾滋病(acquried immunodeficiency syndrome,aids)的病毒。hiv感染后会攻击人体cd4
+
t淋巴细胞,人类免疫系统被破坏,易发生机会性感染和恶性肿瘤,病死率较高,且目前无彻底治愈的方法。
3.hiv属于逆转录病毒科慢病毒属,分为两个亚型:1型和2型。其中hiv-2主要流行在西欧,北美和非洲西部地区,该病毒株毒性较弱。而hiv-1则在世界各地广泛存在,是世界上艾滋病流行的主要病毒株,该病毒株毒性较强。hiv成为迄今为止在疫苗研发和药物开发过程中所经历的最为可怕的病原微生物,虽然在对抗hiv的过程中,本领域研究人员进行了大量生物学的基础研究,但相对于其他病原体,hiv的高突变性、免疫逃逸、窗口期短等特点,为对抗hiv的治疗和疫苗的研发工作带来重重困难。
4.hiv感染机体之后,可以诱导机体产生特异性的抗体反应。然而,其中一部分抗体仅具有与病毒结合的能力,病毒与之结合后仍具有感染宿主细胞的能力,我们称之为结合抗体。而另一部分抗体在与病毒结合后,可以使病毒失活,即具有中和病毒的能力,我们称之为中和抗体 (neutralizing anubody, nab)。广谱中和抗体及其识别表位的筛选鉴定为利用反向疫苗学技术进行艾滋病疫苗研发提供了重要基础,能够产生广谱中和抗体的感染者可作为潜在的通过疫苗诱导相似中和抗体的模型,通过模仿广谱中和抗体在机体内与病毒共进化及亲和力的成熟过程,使用不同的天然膜蛋白进行序贯接种,以结合并激活广谱中和抗体的未突变共同祖细胞,促使特异性前体b细胞分化成熟为分泌广谱中和抗体的浆细胞,实现通过疫苗接种诱导产生广谱中和抗体的目的。
5.自上世纪八十年代以来,艾滋病的流行已经夺去超过3400万人的生命。据世界卫生组织(who)统计,2017年,全世界有3690万人感染上hiv,其中仅59%的hiv感染者接受抗逆转录病毒疗法(art)治疗。目前为止hiv仍然是全球最大的公共卫生挑战之一,因此急需深入研究hiv的检测方法。目前,p24 抗原检测能够在病毒开始复制后检测到血液中的可溶性 p24 抗原,但易出现假阳性。因此,阳性结果必须经中和试验确认,该结果才可作为hiv感染的辅助诊断依据。hiv p24 抗原检测阴性,只表示在此试验中无反应,不能排除hiv感染。病毒核酸检测方法具有很高的灵敏度,但是,由于 hiv 基因的多样性,没有一套引物可以覆盖所有的hiv序列,检测的敏感性又受到限制。此外,现有的病毒核酸或是检测仪器、检测试剂昂贵,或是操作复杂,对操作人员要求高,既难以在一般实验室推广,又不适用于对大量患者的快速检测,同样不适合广泛的临床应用。
6.因此,既要提高检测的敏感性、特异性、缩短窗口期,又要简便、快速和降低成本已成为 hiv 检测技术发展的要求和方向,很多的研究正致力于寻找hiv病毒检测的替代技
术。
技术实现要素:
7.本发明的目的之一在于提供一种抗hiv的广谱中和抗体。
8.本发明的目的之二在于提供了一种筛选抗hiv广谱中和抗体的方法。
9.本发明的目的之三在于提供了检测或治疗hiv感染的药物和途径。
10.为了实现上述目的,本发明采用如下技术方案:本发明的第一方面提供了一种抗hiv广谱中和抗体,所述抗体包括重链互补决定区cdr1、cdr2和cdr3,所述重链互补决定区cdr1、cdr2和cdr3的序列分别如seq id no.1、seq id no.2、seq id no.3所示 ;以及轻链互补决定区cdr1、cdr2和cdr3,所述轻链互补决定区cdr1、cdr2和cdr3的序列如seq id no.5、seq id no.6、seq id no.7所示。
11.进一步,所述抗体包含:(a)与seq id no .4的氨基酸序列具有至少90%,优选95%序列同一性的重链可变区序列;(b)与seq id no .8的氨基酸序列具有至少90%,优选95%序列同一性的轻链可变区序列;或者(c)如(a)中的重链可变区序列和如(b)中的轻链可变区序列。
12.进一步,所述抗体的重链可变区的氨基酸序列如seq id no.4所示;所述抗体的轻链可变区的氨基酸序列如seq id no.8所示。
13.进一步,所述抗体包含抗体重链可变区和/或抗体轻链恒定区的全部或者部分。
14.进一步,所述抗体可包括具有全长重链和轻链的完全抗体分子或其结合片段并且可以是但不限于fab、经修饰的fab、fab'、经修饰的f(ab')2、fv、单结构域抗体(例如vh或vl或vhh)、scfv、二价、三价或四价抗体、双特异性-scfv、双抗体、三抗体、四抗体和以上任何抗体的表位结合片段。
15.本发明的第二方面提供了一种编码本发明的第一方面所述的抗体或其抗原结合片段的核酸分子。
16.进一步,所述的编码抗体的核酸分子可以可操作地连接至一种或多种调控元件,诸如启动子和增强子,其允许核苷酸序列在预期目标细胞(例如,经过遗传修饰以合成所编码抗体的细胞)中表达。
17.进一步,所述的核酸分子包括:脱氧核糖核酸(dna),其包括例如互补dna(cdna)和基因组dna;核糖核酸(rna),特别是信使rna(mrna);dna或rna的合成形式;以及包含两个或更多个这些分子的混合聚合物。
18.进一步,所述的核酸分子可以是线性或环状的。
19.进一步,所述的核酸分子包括有义链和反义链,以及单链和双链形式。
20.进一步,所述的核酸分子可包含天然存在或非天然存在的核苷酸。非天然存在的核苷酸的例子包括带有衍生糖、磷酸盐连接或化学修饰残基的核苷酸碱基。
21.进一步,核酸分子还包括适于在体外和/或体内例如在宿主或患者体内直接表达本发明所述抗体的载体的dna和rna分子。此类dna(例如,cdna)或rna(例如,mrna)分子的载体可以是未修饰的或经过修饰的。
22.本发明的第三方面提供了包含本发明第二方面所述的核酸分子的载体。
23.进一步,所述载体包括但不限于线性多核苷酸、质粒和病毒载体。
24.进一步,所述病毒载体包括但不限于慢病毒载体、逆转录病毒载体、腺病毒 载体、腺相关病毒载体。
25.本发明的第四方面提供了一种重组细胞,所述的重组细胞包含本发明第二方面所述的核酸分子或本发明第三方面所述的载体。
26.进一步,所述重组细胞包括原核细胞、真核细胞。进一步,所述原核细胞包括细菌、放线菌、蓝细菌、支原体、衣原体、立克次氏体。
27.进一步,所述细菌包括大肠杆菌、枯草杆菌、鼠伤寒沙门氏菌、假单胞菌属、链霉菌、葡萄球菌。
28.进一步,所述真核细胞包括哺乳动物细胞、昆虫细胞、植物细胞、酵母细胞。
29.进一步,所述哺乳动物细胞包括人类细胞,具体可包括取自于人体的细胞或市售的成品细胞系:例如rpe1细胞、sw480细胞、u87mg细胞、hos细胞、c8166 细胞、mt-4细胞、molt-4细胞、hela细胞、ht1080细胞、293细胞、te671细胞等。
30.本发明的第五方面提供了一种包含本发明第一方面所述的抗体、本发明第二方面所述的核酸分子、本发明第三方面所述的载体或本发明第四方面所述的重组细胞的药物组合物。
31.进一步,所述的抗体可通过与适当的药学上可接受的载体组合而配制成药物组合物,并且可配制成呈固体、半固体、液体或气体形式的制剂,诸如片剂、胶囊剂、散剂、颗粒剂、软膏、溶液、栓剂、注射剂、吸入剂和气雾剂。
32.进一步,可作为药学上可接受的载体或其组分的一些物质的具体例子是糖类,如乳糖、葡萄糖和蔗糖;淀粉,如玉米淀粉和土豆淀粉;纤维素及其衍生物,如羧甲基纤维素钠、乙基纤维素和甲基纤维素;西黄蓍胶粉末;麦芽;明胶;滑石;固体润滑剂,如硬脂酸和硬脂酸镁;硫酸钙;植物油,如花生油、棉籽油、芝麻油、橄榄油、玉米油和可可油;多元醇,如丙二醇、甘油、山梨糖醇、甘露糖醇和聚乙二醇;海藻酸;乳化剂,如tween;润湿剂,如月桂基硫酸钠;着色剂;调味剂;压片剂、稳定剂;抗氧化剂;防腐剂;无热原水;等渗盐溶液;磷酸盐缓冲液等。
33.进一步,本发明所述的药物组合物可口服给药、注射给药、非胃肠道给药、通过吸入喷雾给药、局部给药、直肠给药、鼻给药、颊给药、阴道给药或通过植入的贮药装置给药。
34.进一步,本发明所述的药物组合物可以以任何口服剂型的形式口服给药,包括但不限于胶囊、片剂、乳剂和水悬浮液、分散剂和溶液。对于口服片剂,常用载体包括乳糖和玉米淀粉。一般还加入润滑剂例如硬脂酸镁。以胶囊形式口服给药,适用的稀释剂包括乳糖和无水玉米淀粉。当口服施用水悬浮液和/或乳液时,可将活性组分悬浮或溶解在油相中,并与乳化剂和/或悬浮剂合并。如果需要的话,可加入一些甜味剂和/或矫味剂和/或着色剂。
35.进一步,本发明所述的药物组合物可使用能够产生所需治疗作用或诊断作用的任何方便的方式将所述的抗体施用至宿主。因此,可将药剂掺入多种制剂中以供治疗施用。
36.进一步,所述药物组合物还包括第二治疗剂。
37.进一步,所述的第二治疗剂是抗病毒剂。
38.进一步,所述的抗病毒剂包括:非核苷逆转录酶抑制剂,蛋白酶抑制剂,融合抑制
剂、整合酶抑制剂。
39.进一步,所述的非核苷逆转录酶抑制剂包括奈韦拉平、地拉韦啶、依非韦伦,依曲韦林和利匹韦林。
40.进一步,所述的蛋白酶抑制剂中的蛋白酶可以是从放线菌发酵液中分离到亮肽素、抗痛素、糜蛋白酶抑素、抑弹性蛋白酶醛、抑胃蛋白酶素、磷酰胺素等,能分别抑制胰蛋白酶、木瓜蛋白酶、糜蛋白酶、弹性蛋白酶、胃蛋白酶、金属蛋白酶等各种蛋白酶。
41.进一步,所述的蛋白酶抑制剂包括茚地那韦、沙奎那韦、利托那韦、奈非那韦、安普那韦。
42.进一步,所述的融合抑制剂包括多肽类hiv-1融合抑制剂。
43.进一步,所述的多肽类hiv-1融合抑制剂包括c肽类融合抑制剂、n肽类融合抑制剂、以gp41融合肽(fp)为靶标的融合抑制剂、非天然氨基酸修饰的hiv-1融合抑制多肽。
44.进一步,所述的c肽类融合抑制剂包括t-20.进一步,所述的n肽类融合抑制剂包括dp-107.进一步,所述的以gp41融合肽(fp)为靶标的融合抑制剂包括virip。
45.进一步,所述的非天然氨基酸修饰的hiv-1融合抑制多肽包括d型环18肽。
46.进一步,所述的整合酶抑制剂包括拉替拉韦(ral)、艾维雷韦(evg)、 多替拉韦(dtg)以及bictegravir(bic)。
47.本发明的第六方面提供了一种hiv的检测产品,所述的产品包括本发明的第一方面所述的抗体或其抗原结合片段。
48.凡是包含本发明所述抗体的能够检测出hiv表达水平的检测产品均包括在本发明的范围之内。
49.进一步,所述检测产品包括但不限于检测试剂盒、芯片或高通量测序平台。
50.进一步,所述试剂盒包括化学发光液。
51.进一步,所述化学发光液包括酶促反应发光剂、直接化学发光剂、电化学发 光剂。
52.进一步,酶促反应发光剂包括酶促反应酶和酶促反应酶的发光底物。
53.进一步,酶促反应酶包括辣根过氧化物酶、碱性磷酸酶、葡萄糖氧化酶、β-半乳糖苷酶、溶菌酶、苹果酸脱氢酶。
54.进一步,酶促反应酶的发光底物包括辣根过氧化物酶的发光底物、碱性磷酸酶的发光底物、葡萄糖氧化酶的发光底物、β-半乳糖苷酶的发光底物、溶菌酶的发光底物、苹果酸脱氢酶的发光底物。
55.进一步,所述辣根过氧化物酶的发光底物包括鲁米诺或其衍生物、对-羟基苯乙酸。
56.进一步,所述碱性磷酸酶的发光底物包括 amppd、4-甲基伞形酮磷酸盐。进一步,所述直接化学发光剂包括不需要酶的催化作用,只需要改变溶液ph 条件就能发光的试剂。
57.进一步,所述电化学发光剂包括在电极表面进行电化学反应而发出光的物质。
58.本发明的第七方面提供了一种用于生成本发明第一方面所述的抗体的方法,所述方法包括:培养本发明的第四方面所述的重组细胞。
59.进一步,在如下条件下在培养基中培养所述重组细胞,所述条件容许由所述载体
编码的多肽的表达并且装配抗体或其片段,并自所述重组细胞或所述重组细胞的培养基纯化所述抗体。
60.本发明的第八方面提供了一种疫苗,所述的疫苗包含特异性结合本发明第一方面所述的抗体的表位。
61.进一步,所述的疫苗可以是基于dna的疫苗、基于rna的疫苗或基于病毒转导的疫苗。
62.进一步,所述的疫苗可以是预防性的或治疗性的。
63.本发明的第九方面提供了如下任一项所述的应用:(a)本发明的第一方面所述的抗体、本发明的第二方面所述的核酸分子、本发明的第三方面所述的载体、本发明的第四方面所述的重组细胞、本发明的第五方面所述的药物组合物在制备治疗hiv 感染或hiv相关疾病的药物中的应用;(b)本发明的第一方面所述的抗体、本发明的第二方面所述的核酸分子、本发明的第三方面所述的载体、本发明的第四方面所述的重组细胞、本发明的第六方面所述的检测产品在制备检测hiv感染或hiv相关疾病诊断、预后或治疗监测的产品中的应用;(c)本发明的第一方面所述的抗体在hiv免疫组织化学测定中的应用。
64.进一步,所述的检测包括定量或定性检测。
65.进一步,诊断hiv相关疾病的方法通常涉及获得来自患者的生物样品(例如,血液、血清、唾液、尿、痰、细胞拭子样品或组织活检物)与hiv抗体接触,以及确定与对照样品或预定截止值相比,抗体是否优先与样品结合,从而表明hiv病毒的存在。
66.定义术语“fab”片段是指抗体的木瓜蛋白酶消化产生两个相同的抗原结合片段,各自具有单一抗原结合位点,和残余的“fc”片段。所述的f(ab')2片段是胃蛋白酶处理得到的,其具有两个抗原结合位点并且仍然能够交联抗原。
67.术语“fv”是含有完全的抗原识别位点和抗原结合位点的最小抗体片段。这个区域由紧密、非共价缔合的一条重链和一条轻链可变结构域的二聚体组成。在这种构型中,每个可变结构域的三个cdr相互作用以限定vh-vl二聚体表面上的抗原结合位点。总的来说,六个cdr赋予抗体以抗原结合特异性。然而,即使单个可变结构域(或只包含三个对抗原具特异性的cdr的一半fv)也具有识别和结合抗原的能力,但亲和力相比于整个结合位点较低。
68.术语“单链fv”或“sfv”或“scfv”抗体片段包含抗体的vh和vl结构域,其中这些结构域存在于单一多肽链中。在一些实施方案中,fv多肽进一步包含在vh与vl结构域之间的多肽连接子,其能够使sfv形成抗原结合所需的结构。
69.术语“特异性结合”是指两个分子形成在生理条件下相对稳定的复合体,特异性结合的特点在于高亲和力和低至中容量,非特异性结合通常具有低亲和力和中至高容量。通常,当亲和常数k高于106m-1
或优选高于108m-1
时,认为结合是特异性的。必要时,通过改变结合条件减少非特异性结合而基本上不影响特异性结合。上述条件为本领域所公知,且本领域技术人员使用常规技术就可选择合适的条件。所述条件通常用抗体浓度、溶液离子强度、温度、供结合时间、非相关分子(例如:血清白蛋白、乳酪蛋白)浓度等来限定。
70.术语“核酸分子”或“多核苷酸”包括任何包含核苷酸聚合物的化合物和/或物质。每个核苷酸由碱基特别是嘌呤或嘧啶碱基(即,胞嘧啶(c)、鸟嘌呤(g)、腺嘌呤(a)、胸腺嘧
啶(t)或尿嘧啶(u))、糖(即,脱氧核糖或核糖)及磷酸基团构成。通常,核酸分子通过碱基序列进行描述,其中所述碱基代表核酸分子的一级结构(线性结构)。碱基序列通常由5’至3’表示。
71.术语“载体”是指能够载运与其相连接的另一核酸的核酸分子,该术语包括作为自我复制核酸结构的载体以及掺入已引入宿主细胞的基因组中的载体。某些载体能够指导与其可操作地连接的核酸分子的表达。
72.术语“可变”表示抗体中可变区的某些部分在序列上有所不同,它形成了各种特定抗体对其特定抗原的结合和特异性。可变性集中于轻链和重链可变区中称为互补决定区(cdr)或超变区中的三个片段中。天然重链和轻链的可变区中各自包含四个fr区(可变区中较保守的部分),它们大致上呈β-折叠构型,由形成连接环的三个cdr相连,可形成部分β-折叠结构。每条链中的cdr通过fr区紧密地靠在一起并与另一条链的cdr一起形成了抗体的抗原结合部位。恒定区不直接参与抗体与抗原的结合,但是它们表现出不同的效应功能。
73.术语“非核苷逆转录酶抑制剂”指一类通过与hiv逆转录酶聚合位点附近的疏水结合口袋结合而发生作用的药物小分子。
74.术语“蛋白酶抑制剂”广义上指与蛋白酶分子活性中心上的一些基团结合,使蛋白酶活力下降,甚至消失,但不使酶蛋白变性的物质。
75.术语“整合酶抑制剂”是指抑制整合酶的药物,即抑制逆转录病毒复制过程,阻断催化病毒dna与宿主染色体dna的整合。
76.术语“治疗”或“处理”或“减轻”可互换使用,并且指治疗性处理和防范性或预防性措施两者;其中目的是预防或减缓(减轻)靶向的病理状况或病症。需要治疗的对象包括那些已经具有病症的对象以及那些易于具有病症的对象或那些要预防病症的对象。若在接受治疗量的依照本发明方法的抗体后,患者显示下列一项或多项的可观察到的和/或可测量的降低或缺乏,则受试者或哺乳动物是成功“治疗”感染的:受感染细胞的数目减少或受感染细胞的缺乏;被感染的总细胞的百分比降低;和/或以一定程度减轻一种或多种与特定感染有关的症状;降低的发病率和死亡率,和生活质量问题的改善。
附图说明
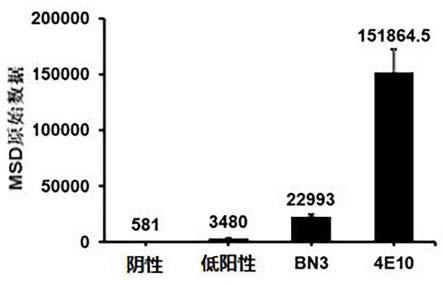
77.图1是pcdna3.1(+)-fc表达载体图;图2是人源化gtl小鼠外周血成熟b细胞分选图;图3是bn3抗体自身反应性检测(hep-2 elisa)图;图4是bn3抗体与hiv表面抗原gp140-trimer结合活性检测图。
具体实施方式
78.人源化gtl小鼠,是将人胎儿脐带血中cd34
+
的造血干细胞、胎儿肝和胸腺组织移植到nod/scid/il2rγ
null
小鼠体内,使人的造血细胞、淋巴细胞在gtl小鼠体内发育。由于人b细胞处在小鼠体内的发育环境中,对于人体来讲的这类自身反应/多反应性b细胞克隆可能被清除的比例降低,从而可以更多地保留下来。基于此,我们建立了人源化gtl小鼠模型,研究gtl小鼠体内人b细胞的发育情况,发现75%的成熟b细胞具有自身/多反应性,比例相当高。在对这些自身/多反应性抗体进行研究过程中,发现了具备hiv广谱中和抗体特征
的抗体。
79.下面结合附图和实施例对本发明作进一步详细的说明。
80.以下实施例仅用于说明本发明而不用于限制本发明的范围。
81.实施例1抗hiv抗体的制备1、成熟b细胞的分选buffer1: 500 ml 1
×
pbs + 2 ml 0.5 m edta + 25 ml 10% bsa (含2 mm edta, 0.5%bsa)(1)收集人源化gtl小鼠外周血200 μl,加入200μl buffer1;(2)加入10倍体积的ack lysing buffer (fisher/biowhittaker),室温孵育10 min,1500 rpm离心10 min;(3)弃上清,加入10 ml buffer 1洗细胞,1500 rpm离心10 min;(4)弃上清,加入10 μl buffer 1重悬细胞;加入流式抗体,标记成熟b细胞:anti-cd5/fitc (ucht2, ebioscience)anti-cd19/pe (sj25-c1, bd pharmingen)anti-cd10/apc (bc96, ebioscience)anti-cd27/pe-cy7 (o323, ebioscience)anti-igm/pe-cy5 (g20-127, bd pharmingen)(5)流式细胞仪(facs sorter)分选成熟b细胞(cd5-cd19+cd10-cd27
‑ꢀ
igm+),将单个细胞收集到96孔pcr板中,内置4μl细胞裂解液;(6)将分选到的细胞至于干冰上,并尽快保存于-70℃冰箱。
82.(7)结果:如图2所示,分选获得成熟b细胞。
83.2、抗体的鉴定(1)反转录合成cdna,用invitrogen公司的superscript
®ꢀ
iii first-strand synthesis system合成体系;(2)第一轮pcr,扩增抗体重链vh基因、轻链vl基因,用qiagen公司的hotstar 试剂盒;(3)第二轮巢式pcr,扩增抗体vh基因、vl基因,用qiagen公司的hotstar 试剂盒;(4)将第二轮pcr产物vh片段、vl片段分别连入t载体,转化jm109感受态细菌;(5)用pcr法鉴定含vh片段、vl片段的阳性克隆;(6)选择来自同一细胞的,经pcr鉴定为阳性的vh和vl产物,将其组装成单链抗体scfv。
84.(7)通过sfii、not i酶切位点,将scfv连入含igg1-fc的pcdna3.1(+)-fc表达载体(含igg1-fc标签,图1),转化jm109感受态细菌。
85.(8)用pcr法鉴定含scfv片段的阳性克隆并测序,获得序列正确的scfv /pcdna3.1(+)-fc克隆。
86.(9)抗体序列如表1所示表1抗体序列
3、抗体的真核表达和亲和纯化 将测序正确的scfv /pcdna3.1(+)-fc质粒,用lipofectamine 2000(invitrogen)瞬时转染hek 293t细胞。293t细胞接种于15 cm的培养板中,含20 ml培养基,细胞铺板至90%时,用40μg质粒dna,100 μl lipofectamine2000,按操作指南进行转染。转染8-10h后换液,换液后48h收集细胞上清,用protein a亲和层析法(protein a sepharose cl-4b,ge healthcare)纯化抗体(表达的抗体含fc标签),经超滤浓缩后获得scfv-fc抗体蛋白。
87.实施例2抗体特性的检测1、自身反应性检测抗体的自身反应性采用临床上标准的抗核抗体检测试剂盒(quanta lite
™ꢀ
ana elisa,inova diagnostics, inc.)进行检测,检测试剂盒中提供了阴性反应样品、低阳性反应样品、高阳性反应样品。4e10是一个hiv广谱中和抗体,也是一个自身/多反应性抗体,
实验中我们制备了4e10 scfv-fc,用作阳性对照抗体。检测步骤如下:(1)包被:ana 试剂盒中的elisa板已经进行了抗原包被;(2)一抗:加入 50 μg/ml scfv-fc蛋白50 μl,室温反应2h;(3)二抗:弃去孔中液体,pbst洗涤3次,加入hrp标记的羊抗人igg-fc抗体,室温反应1h;(4)显色:弃去孔中液体,pbst洗涤3次,加入tmb底物溶液,每孔100μl,室温避光显色3分钟;(5)检测:加入2n h2so4100μl终止反应,酶标仪450nm处进行检测。
88.(6)结果:如图3所示,scfv-fc抗体(命名为bn3)抗核反应显示出强阳性,几乎与4e10 scfv-fc相当。表明bn3与人类核抗原反应,是一种自身反应性抗体。
89.2、多反应性检测抗体的多反应性是检测抗体和自然界多种公认常见抗原的反应,包括人单链dna(ssdna)、人双链dna(dsdna)、重组人胰岛素(insulin)、人心磷脂(cardiolipin)、牛血清白蛋白(bsa)、细菌脂多糖(lps)等。源于人源化gtl小鼠的抗体多反应性通过基于电化学发光法的msd(gaithersburg, md, usa)平台进行评价。实验中,4e10 scfv-fc用作阳性对照抗体。
90.(1)包被:用ssdna、dsdna、insulin、cardiolipin、bsa、lps各10 μg/ml为多反应性抗原,包被384孔msd板,4℃孵育过夜;(2)封闭:弃去孔中液体,pbst洗涤3次,加入 10% fbs 100μl封闭elisa板,室温孵育1h;(3)一抗:弃去孔中液体,pbst洗涤3次,加入 5 μg/ml scfv-fc蛋白15μl,室温孵育反应2h;(4)二抗:弃去孔中液体,pbst洗涤3次,加入1 μg/ml带sulfo标签的羊抗人igg-fc抗体15μl,室温反应2h;(5)弃去孔中液体,pbst洗涤3次,根据操作指南,反应板在msd sector imager 2400进行读取。
91.(6)结果:bn3与ssdna、dsdna、insulin、cardiolipin、bsa、lps抗原反应均显示出强阳性,几乎与4e10 scfv-fc相当,表明bn3与这些抗原都反应,是一种多反应性抗体。
92.3、hiv抗原结合反应检测基于msd平台技术,设置了bn3与hiv表面抗原gp140-trimer结合实验,用5 μg/ml gp140-trimer(来自hiv-yu2病毒株)包被384孔msd板,方法同上。实验中,仍以4e10 scfv-fc为阳性对照抗体,在自身反应性检测结果中显示阴性和低阳性反应的抗体,这个实验中被用作阴性对照和低阳性反应对照。
93.结果如图4所示,bn3与gp140-trimer显示出较强的结合活性,大约为4e10 scfv-fc 结合活性的15%,是阴性对照的40倍,低阳性对照的6.6倍,这表明bn3具有hiv抗原结合活性,具备进一步开发的价值。
94.上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1