一种5-烷基吡啶-2,3-二羧酸酯的连续流合成工艺的制作方法
1.本发明属于有机合成技术领域,具体涉及一种5-烷基吡啶-2,3-二羧酸酯的连续流合成工艺。
背景技术:
2.5-烷基吡啶-2,3-二羧酸酯是合成咪唑啉酮类化合物的重要中间体。咪唑啉酮类化合物如咪草烟、甲基咪草烟等在农药方面应用广泛,其作为高效除草剂,通过植物茎叶与根吸收,在木质部与韧皮部进行传导,积累于分生组织,抑制生长,最终造成植物死亡。咪唑啉酮类除草剂开发成功后,由于其选择性强、杀草谱广、用量低及对环境安全等原因,迅速在农业生产中推广使用。
3.专利us5322948报道以马来酸二乙酯、1-戊烯-3-酮和硫酸氢铵为原料,于95℃反应20小时制备5-乙基吡啶-2,3-二羧酸二乙酯,收率仅为51%。成本高,反应时间久,且收率低。
4.专利us4948896报道以2-亚氨基-丁二酸二乙酯和2-乙基丙烯醛为原料,在对甲苯磺酸作用下回流15小时制备5-乙基吡啶-2,3-二羧酸二乙酯,收率仅为84.6%。但由于原料昂贵导致成本过高。
5.专利us4973695报道以2-氯-3-氧代丁二酸二乙酯酯、2-乙基丙烯醛为主原料,加入大量铵盐高温反应4h制备5-乙基吡啶-2,3-二羧酸二乙酯,收率76.5%。后处理产生大量废水废盐,对环境不友好。
6.现有技术存在成本高、反应时间久、三废污染大等技术问题。
技术实现要素:
7.针对现有技术存在的问题,本发明的目的在于涉及提供一种5-烷基吡啶-2,3-二羧酸酯的连续流合成工艺的技术方案,该方法具有收率高,杂质少,后处理方便,三废污染少等优点,且大大了降低安全隐患,适于工业化生产应用。
8.本发明具体通过以下技术方案实现:
9.一种5-烷基吡啶-2,3-二羧酸酯的连续流合成工艺,其包括以下步骤:
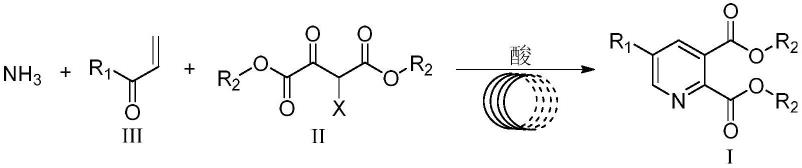
10.将式ii所示的2-卤代-3-氧代丁二酸酯溶于含有氨气的醇溶液,与式iii所示的1-烷烯-3-酮于负载有固体酸的管道反应器中进行反应;反应液蒸馏脱溶得5-烷基吡啶-2,3-二羧酸酯;
11.具体反应式如下:
12.13.其中,r1选自c1-c4的烷基或含有一个氧的c1-c4醚;r2选自c1-c4的烷基;x为卤素。
14.进一步,所述2-卤代-3-氧代丁二酸酯与1-烷烯-3-酮的摩尔比为1:1.01~1.5。
15.进一步,所述2-卤代-3-氧代丁二酸酯与氨的摩尔比为1:1.1~3.0。
16.进一步,所述含有氨气的醇溶液的醇为甲醇、乙醇、正丙醇或异丙醇,浓度为2-30%。
17.进一步,所述固体酸为al2o3、al2o
3-sio2或阳离子交换树脂。
18.进一步,所述管道反应器的反应温度60~90℃,停留时间30~600秒。
19.进一步,所述管道反应器的反应压力为0~1.5mpa。
20.本发明通过采用上述技术,与现有技术相比,具有如下有益效果:
21.1)本发明通过采用2-卤代-3-氧代丁二酸酯、1-烷烯-3-酮和氨气为原料,其价格相对低廉,可降低成本。
22.2)本发明使用管道反应器,具有反应时间段,杂质小,收率高的优点,且相比传统反应釜安全隐患大大降低。
23.3)本发明使用负载固体酸,其可重复利用,副产氯化氢经水吸收得高纯盐酸溶液可用于其它产品生产。三废污染少,适于工业化生产应用。
附图说明
24.图1为实施例1中的1h nmr图谱;
25.图2为实施例1中的
13
cnmr图谱;
26.图3为实施例2中的1h nmr图谱;
27.图4为实施例2中的
13
cnmr图谱。
具体实施方式
28.下述的实施案例为本发明的具体描述。本发明实施案例的制备方法仅用于说明本发明,而不是对本发明的限制,本发明的保护范围并不仅限于此,在本发明的构思前提下,对本发明制备方法的简单改进都属于本发明要求保护的范围。
29.实施例1:5-乙基吡啶-2,3-二羧酸二乙酯的制备
30.2-氯-3-氧代丁二酸二乙酯100g溶于229g 5%氨乙醇(1.5eq)溶液,与2-氯-3-氧代丁二酸二乙酯溶液与1-戊烯-3-酮41.6g(1.1eq)混合进入90℃的装有阳离子交换树脂的管式反应器,滞留时间为5分钟,管道反应压力为1.5mpa。所得反应液减压蒸馏至析出固体,降温,过滤,烘干得5-乙基吡啶-2,3-二羧酸二乙酯103.2g,hplc纯度>98%,收率91.02%。
31.5-乙基吡啶-2,3-二羧酸二乙酯的1h nmr图谱和
13
cnmr图谱如图1和2所示:
[0032]1h nmr(cdcl3,500mhz)δ:8.52(d,j=5.0hz,1h),7.88(d,j=5.0hz,1h),4.35-4.40(q,2h),4.29-4.34(q,2h),2.65-2.70(q,2h),1.34(t,j=5.0hz,3h),1.31(t,j=5.0hz,3h),1.22(t,j=5.0hz,3h);
13
cnmrδ:165.2,164.8,150.3,140.2,135.5,125.9,61.10,61.0,24.8,13.9,13.1,13.0。
[0033]
实施例2:5-甲基吡啶-2,3-二羧酸二乙酯的制备
[0034]
2-氯-3-氧代丁二酸二乙酯100g溶于280g 3%氨乙醇(1.1eq)溶液,与2-氯-3-氧代丁二酸二乙酯溶液与丁烯酮41g(1.3eq)混合进入80℃的装有al2o3的管式反应器,滞留
时间为8分钟,管道反应压力为1.0mpa。所得反应液减压蒸馏至析出固体,降温,过滤,烘干得5-甲基吡啶-2,3-二羧酸二乙酯97.8g,hplc纯度>97.0%,收率90.7%。
[0035]
5-甲基吡啶-2,3-二羧酸二乙酯的1h nmr图谱和
13
cnmr图谱如图3和4所示:
[0036]1h nmr(cdcl3,500mhz)δ:8.58(d,j=5.0hz,1h),7.941(m,j=5.0hz,1h),4.43-4.47(q,2h),4.37-4.41(q,2h),2.43(s,3h),1.42(t,j=5.0hz,3h),1.38(t,j=5.0hz,3h);
13
cnmrδ:166.1,165.8,151.9,147.9,137.6,135.2 126.8,62.1,61.9,18.2,14.1,14.0。
[0037]
实施例3:5-甲基吡啶-2,3-二羧酸二甲酯的制备
[0038]
2-氯-3-氧代丁二酸二甲酯100g溶于262.2g 10%氨甲醇(3eq)溶液,与2-氯-3-氧代丁二酸二甲酯溶液与丁烯酮43.2g(1.2eq)混合进入70℃的装有al2o3-sio2的管式反应器,滞留时间为10分钟,管道反应压力为0.1mpa。所得反应液减压蒸馏至析出固体,降温,过滤,烘干得5-甲基吡啶-2,3-二羧酸二甲酯92.2g,hplc纯度大于97.0%,收率84.16%。
13
cnmr(cdcl3,500mhz)δ:168.1,164.6,151.0,148.1,135.2,131.3,117.5,51.5,51.5,18.0。
[0039]
实施例4:5-甲氧基甲基吡啶-2,3-二羧酸二甲酯的制备
[0040]
2-氯-3-氧代丁二酸二甲酯100g溶于349.6g 5%氨甲醇(2eq)溶液,与2-氯-3-氧代丁二酸二甲酯溶液与4-甲氧基-戊烯-3-酮61.8g(1.2eq)混合进入75℃的装有阳离子交换树脂的管式反应器,滞留时间为5分钟,管道反应压力为0.5mpa。所得反应液减压蒸馏至析出固体,降温,过滤,烘干得5-甲氧基甲基吡啶-2,3-二羧酸二甲酯106.8g,hplc纯度>98.68%,收率85.71%。
13
cnmr(cdcl3,500mhz)δ:168.1,164.6,156.9,142.0,130.9,121.6,118.5,55.8,51.5,51.5。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1