一种干细胞外泌体的制备方法以及在治疗男性勃起功能障碍中的应用与流程
:
1.本发明属于药物研究领域,具体提供了一种干细胞外泌体的制备方法以及在治疗男性勃起功能障碍中的应用。
背景技术:
2.勃起功能障碍(erectile dysfunction,ed)是一种常见的男科疾病,指男性无能达到性生活所需要的充分勃起或维持勃起时间过短的病症,各个年龄段均可发生,以中老年为主,且年龄越大发病率越高。随着对于男性生理特征的研究不断深入,逐渐认识到阴茎勃起活动的关键是海绵体内平滑肌的有序松弛,在下丘脑室旁核和内侧视前核的控制下,血液流入海绵体,海绵体充满血液并压缩导静脉,减少静脉血液流出;在神经系统方面,神经信号通过副交感神经系统经海绵体神经到达阴茎,海绵状神经末梢释放的一氧化氮启动勃起过程,而来自内皮细胞的一氧化氮则起到维持勃起的作用。一氧化氮在进入平滑肌时会刺激环磷酸鸟苷(环gmp)产生,蛋白激酶g被环状gmp激活,其打开钾通道同时关闭钙通道,低细胞内钙导致海绵体内平滑肌组织松弛,导致动脉流量增加,同时静脉闭塞活动,从而启动和维持勃起;当环状gmp被阴茎磷酸二酯酶降解时,下层平滑肌再次收缩,过程逆转。上述任何过程引起的病理性病变都可能导致勃起功能障碍,包括但不限于心理因素(如自尊心丧失、焦虑和抑郁)、神经系统疾病(如多发性硬化)、激素原因(如性腺功能减退、甲状腺功能减退)、外伤(如骨盆骨折、脊髓损伤)、高脂血症、中风、睡眠呼吸暂停、慢性阻塞性肺病、多发性硬化、尿路感染和病变、医源性损伤(例如经尿道前列腺切除术)和各种药物影响(抗抑郁药、抗高血压药、抗精神病药、阿片类药物和消遣性药物)等等。
3.除保持良好的生活习惯(如戒烟、戒酒、加强体育锻炼)和适当进行心理辅导之外,研究人员开发出了多种治疗勃起功能障碍的药物和方法,包括:(1)l-精氨酸,一种氨基酸补充剂,可作为产生一氧化氮合酶的必需底物,补充l-精氨酸已被证明可以增加一氧化氮合酶水平,进而改善勃起功能;(2)磷酸二酯酶5抑制剂(pde-5抑制剂),如西地那非和他达拉非,是目前治疗勃起功能障碍的一线药物,它们通过抑制磷酸二酯酶来减少环状gmp的降解,从而增加海绵体平滑肌和海绵体动脉血流的松弛而开启勃起过程,但是使用pde-5抑制剂可能产生头痛、消化不良、鼻塞和轻微的视觉变化等不良反应;(3)外部真空装置,该装置的外筒放置在阴茎上以形成气密密封,患者使用小型手动(或电池供电)真空泵在阴茎周围产生负压,使阴茎体充满血液,并在阴茎根部周围放置弹性带来维持这种人工勃起;(4)前列腺素e1,是人体最有效的天然平滑肌松弛剂,它通过增加海绵体循环amp水平而启动勃起,具有较少的全身副作用和良好的疗效等特点,但是海绵体内注射会导致疼痛、阴茎异常勃起、注射部位出血或瘀伤等副作用;(5)手术治疗,包括阴茎血运重建手术、动脉球囊血管成形术、静脉结扎手等,虽然可以取得较好的治疗效果,但是临床实践中许多男性患者不希望进行该类手术,该疗法接受性较差。
4.干细胞是具有多向分化能力的可自我更新的细胞,除自我更新能力和多向分化能
in a diabetic rat model by delivering proangiogenic microrna,sexual medicine,2019,7(2):241-250)利用usc外泌体增强大鼠内皮细胞标志物的表达,减少胶原蛋白沉积,改善了神经源性勃起反应。然而,干细胞外泌体的治疗效果仍有待改善,以便进一步提高对勃起功能障碍的治疗效果。
7.神经生长因子(ngf)及酪氨酸激酶a(trka)受体和p75神经营养因子受体信号通路在人神经系统传导机制中起关键作用,与疼痛、过敏、炎症反应等多项生理过程相关。有报道称,该信号通路在勃起功能障碍中也发挥重要调节作用,在胚胎晚期和出生后阶段,交感神经元的发育和存活需要神经生长因子(ngf)及其受体trka,而交感神经具有拮抗阴茎勃起的作用,因此研究人员(lin g,li h,zhang x,et al.novel therapeutic approach for neurogenic erectile dysfunction:effect of neurotrophic tyrosine kinase receptor type 1monoclonal antibody.eur urol 2015,67:716-26)使用一种特异性trka单克隆抗体(trka-mab)可通过阻断外周交感神经元的再生来治疗海绵状神经损伤(cni)引起的ed,将trka-mab局部递送至cni大鼠的主要骨盆神经节或海绵体可显着抑制海绵体中酪氨酸羟化酶阳性交感神经纤维,并增强背神经中nnos阳性纤维,从而诱导勃起功能的恢复。
8.有鉴于现有技术中对于勃起功能障碍新型治疗手段的开发需要,本发明提供了一种药物组合物,包括来自干细胞的外泌体和靶向trka的单克隆抗体,既能够利用干细胞外泌体所携带的多种细胞因子和免疫调节因子,促进海绵体内细胞增殖和血管修复,还能够利用trka单克隆抗体的神经系统调节作用,从多个层面上促进勃起功能恢复,发挥协同作用。
技术实现要素:
9.为解决上述技术问题,本发明中提供了一种治疗男性勃起功能障碍的药物组合物,其特征在于,所述药物组合物包括干细胞外泌体和抗trka抗体,所述抗trka抗体的重链可变区包括如seq id no:1所示的hcdr1、seq id no:2所示的hcdr2、seq id no:3所示的hcdr3,以及轻链可变区包括如seq id no:4所示的lcdr1、seq id no:5所示的lcdr2、seq id no:6所示的lcdr3。
10.本发明中使用干细胞外泌体与抗trka抗体相配合治疗男性勃起功能障碍,既能够促进海绵体内细胞增殖,防止细胞凋亡,促进血管再生保证海绵体充血过程顺畅,还能够调节神经信号传导,维持一氧化碳合酶的正常水平,从多角度协作作为,促进勃起功能恢复。
11.进一步的,所述抗体的重链可变区氨基酸序列如seq id no:7所示。
12.进一步的,所述抗体的轻链可变区氨基酸序列如seq id no:8所示。
13.本发明中所述的单克隆抗体,为发明人自行开发研制,能够与目标抗原高特异性结合,有效调节ngf/trka/p75信号通路的生理信号传导过程。
14.进一步的,所述干细胞外泌体来自脂肪干细胞、间充质干细胞、胚胎干细胞、神经干细胞、内皮祖细胞中的一种或几种;优选的,所述干细胞外泌体来自脐带间充质干细胞。
15.现有技术中已经报道多种干细胞外泌体对勃起功能障碍具有治疗作用,可在不同程度上促进一氧化氮合酶分泌,诱导海绵体内皮细胞和平滑肌细胞增殖,促进勃起功能修复。本发明中选用脐带间充质干细胞来源的外泌体,不仅来源便利,而且排斥反应降低,其
多向诱导能力更强,有利于后期的临床应用。
16.进一步的,所述干细胞外泌体的制备方法包括:取洁净脐带组织,使用冰预冷的无菌磷酸盐缓冲液洗涤3次,剔除动静脉血管,用组织剪将脐带剪成长约0.5厘米的小段,置于培养基中,于37℃、5%co2条件下进行原代培养;原代培养至5-10天更换一次培养基,继续进行培养,当细胞达到亚融合状态时,进行传代培养,共培养3-5代;当传代培养细胞融合度达到85%以上时,采用超速离心法收集干细胞外泌体。
17.进一步的,所述培养基为为dmem/f12,并添加10%fbs、10μg/ml人胰岛素、5ng/ml egf、5ng/ml bfgf、10ng/ml hgf、10ng/ml ngf、8μg/ml硫酸锌和10ng/ml亚硒酸钠。
18.采用该培养基能够有效促进脐带间充质干细胞生长,提高生长速率,还能够有效诱导外泌体表达,提高外泌体内容物含量,改善其生理功能,提高组织修复能力。
19.进一步的,所述药物组合物还包括药学上可以接受的药物载体。
20.进一步的,所述药物载体包括稀释剂、赋形剂、填充剂、粘合剂、湿润剂、润滑剂、崩解剂、吸收促进剂、表面活性剂、吸附载体以及香味剂、甜味剂中的至少一种.
21.本发明还提供了一种所述的药物组合物在制备治疗男性勃起功能障碍的药物中的应用。
22.进一步的,所述男性勃起功能障碍包括糖尿病性勃起功能障碍和神经损伤性勃起功能障碍。
23.有益效果
24.本技术提供了一种药物组合物及其在制备治疗男性勃起功能障碍药物中的应用,具有以下优势:
25.(1)所述药物组合物中包括干细胞外泌体,优选为脐带间充质干细胞来源的外泌体,能够促进海绵体平滑肌细胞增殖,诱导和维持一氧化氮合酶高水平表达,改善阴茎勃起功能;
26.(2)所述药物组合物中包括抗trka抗体,具有全新的轻链和重链结构,可与目标抗原高特异性结合,调节神经信号传导;
27.(3)本发明所提供的干细胞外泌体和抗trka抗体可产生协同作用,升高模型动物的阴茎海绵体内压,维持vegf高水平表达,促进勃起功能恢复。
附图说明
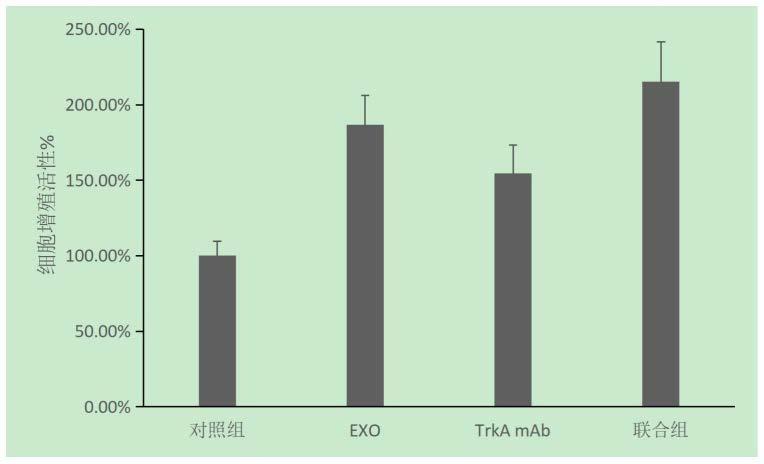
28.图1:ccsmcs细胞增殖能力;
29.图2:ccsmcs细胞nnos表达水平;
30.图3:大鼠icp/map比值;
31.图4:大鼠海绵体中vegf表达水平。
具体实施方式
32.以下非限制性实施例可以使本领域的普通技术人员更全面地理解本发明,但不以任何形式限制本发明。凡基于本发明上述内容所实现的技术均应当属于本技术要求保护的范围之中。
33.以下实施例中所述实验方法,如无特殊说明,均为常规方法;所述试剂生物材料、
检测试剂盒,如无特殊说明,均可从商业途径获得。
34.实施例1脐带来源间充质干细胞外泌体制备
35.据报道,多种干细胞外泌体具有勃起功能改善作用,包括但不限于胚胎干细胞、脂肪干细胞、尿路干细胞、内皮祖细胞、骨髓间充质干细胞等等,但是胚胎干细胞受到伦理学限制,且来源不稳定,故难以在临床上大规模应用;其他成体干细胞虽然一定的积极治疗作用,但是其多向分化能力随着机体的生长和细胞分化成熟程度加深而受到限制,故潜在治疗作用有限。因此,本发明中选择脐带间充质干细胞作为研究对象,既可以避免伦理学的困扰,又能够利用其较强的多向分化能力和免疫调节能力,在初步实验中,其所分泌的干细胞外泌体相对于其他成体干细胞具有更强大的生理活性。
36.取人洁净脐带,置于一次性无菌培养皿中,使用冰预冷的无菌pbs缓冲液洗涤3次,剔除动静脉血管,用组织剪将脐带剪成长约0.5厘米的小段,置于培养基中,于37℃、5%co2条件下进行原代培养。所述培养基为dmem/f12,并添加10%fbs、10μg/ml人胰岛素、5ng/ml egf、5ng/ml bfgf、10ng/ml hgf、10ng/ml ngf、8μg/ml硫酸锌和10ng/ml亚硒酸钠,其中hgf、ngf、亚硒酸钠的加入对于干细胞的培养和外泌体分泌至关重要,加入上述组分不仅使得脐带间充质干细胞生长速度提高,还有利于外泌体的分泌以及内容物种类和含量的调节。
37.原代培养至5-10天更换一次间充质干细胞培养基,继续进行培养,当细胞达到亚融合状态时,进行传代培养,共培养3-5代。
38.当传代培养细胞融合度达到85%以上时收集干细胞外泌体:将细胞上清液收集于离心管中,3000g、4℃条件下离心20min,以去除死细胞;12000g、4℃条件下离心30min,以去胞碎片;收集上清液,依次使用0.45μm、0.22μm滤膜进行过滤,进一步除去杂质;收集滤液,转移至离心管中,在超速离心机中100000g、4℃条件下超速离心2h,去除上清液,得到外泌体沉淀。经扫描电子显微镜检测,所述外泌体直径在70-150nm之间,符合后续实验要求。
39.实施例2抗trka抗体设计和获得
40.通过杂交瘤法制备抗trka单克隆抗体(trka-mab),具体步骤包括:
41.将人trka抗原蛋白(购自北京百普赛斯生物科技股份有限公司)采用弗氏完全佐剂按1:1比例进行乳化,皮下注射6周龄的balb/c小鼠,免疫剂量为500μg/只;从首次免疫开始,每4周加强免疫一次,加强免疫2次,用弗氏不完全佐剂代替弗氏完全佐剂,方法与剂量同首次免疫;第2次加强免疫一周后眼底静脉采血测效价和抑制率,有效抑制且效价达到1:10000以上时,进行1次冲击免疫,三天后取脾细胞与骨髓瘤细胞融合,筛选阳性孔。利用有限稀释法对阳性孔进行克隆,得到并建立稳定分泌红霉素单克隆抗体的杂交瘤细胞株。然后,将balb/c小鼠(8周龄)腹腔注入灭菌石蜡油0.8ml/只,一周后腹腔注射杂交瘤细胞5
×
105个/只,10天后采集腹水,采用rprotein g琼脂糖凝胶亲和层析法对腹水进行纯化,获得目标trka-mab抗体。利用分子互相作用分析平台biacore,检测所述抗体与trka蛋白的亲和力,其kd值为25.25nm,亲和力在纳摩尔水平,说明其具有较高的目标抗原结合活性。
42.经鉴定,所述trka-mab抗体的重链cdr区,包括如seq id no:1所示的lcdr1、seq id no:2所示的lcdr2、seq id no:3所示的lcdr3;轻链cdr区,包括如seq id no:4所示的hcdr1、seq id no:5所示的hcdr2、seq id no:6所示的hcdr3。进一步的,所述抗体的重链可变区氨基酸序列如seq id no:7所示,轻链可变区氨基酸序列如seq id no:8所示.
43.实施例3细胞体外实验
44.阴茎海绵体平滑肌细胞(ccsmcs)是构成ccsm的基本单位,其在保障阴茎海绵体平滑肌(ccsm)舒张和收缩生理功能中处于核心地位,因此本实施例中选用ccsmcs为研究对象,进行细胞水平研究。
45.3.1 ccsmcs原代培养
46.选择健康雄性sd大鼠,适应性饲养1周后,断颈处死大鼠,无菌条件下切开包皮,阴茎脚水平横行切取阴茎,使用无菌冰预冷的pbs缓冲液洗涤,去除阴茎软骨、尿道及背侧血管等组织。pbs漂洗去血细胞后,将海绵体组织剪成长宽约2-5mm小组织块,按0.5cm的间隔放置到含有10%fbs的dmem培养基中,37℃、5%co2培养箱中静置培养。3-5天后更换培养基,并除去未贴壁的组织块,继续培养细胞至80%融合时进行传代,细胞传代培养2-3代后,经鉴定为海绵体平滑肌细胞。
47.3.2 ccsmcs增殖实验
48.培养ccsmcs至对数生长期后,胰酶消化收集细胞,使用新鲜培养基调节细胞浓度,随后将细胞接种于96孔板中,每孔5
×
105个细胞,于37℃、5%co2、条件下培养12h后,分别设置:exo组(加入50μg/ml脐带间充质干细胞外泌体)、trka-mab组(加入50μg/mltrka-mab抗体)、联合组(加入50μg/ml脐带间充质干细胞外泌体和50μg/mltrka-mab抗体)、对照组(加入等量培养基);于37℃、5%co2条件下培养48h后,每孔加入20μl浓度为5mg/ml的mtt溶液,37℃孵育4h,去上清液,加入150μl dmso轻轻震荡,用酶标仪检测其在490nm处的吸光度(od值),按照如下公式计算细胞增殖活性,细胞增殖活性=实验组od值/对照组od值
×
100%。
49.如图1所示,脐带间充质干细胞外泌体可显著促进海绵体平滑肌细胞增殖,相比于空白对照组有显著提高,且其促增殖能力强于trka-mab,在联合组中这种促进增殖趋势得到了强化。
50.3.3一氧化氮合酶表达水平检测
51.生理上,阴茎勃起需要副交感神经末梢释放的一氧化氮(no)来实现,而一氧化氮合酶(neural nosynthase,nnos)是机体内释放和维持no水平的重要催化物质,它的多少在一定程度上决定了是否能够得到足够量的no,以启动和维持勃起功能。本实施例中采用western blot法检测ccsmcs中的nnos含量。
52.细胞培养和处理方式通3.2节。处理完成后收集细胞于ep管中,加入含有1%pmsf(蛋白酶抑制剂)的ripa裂解液,混匀后置于冰上孵育30min,4℃12000g离心10min,吸取上澄清液至新的ep管中,取少量上清进行蛋白定量,蛋白样品储存于-20℃冰箱备用。
53.各组蛋白样品进行蛋白质凝胶电泳,电泳条件为浓缩胶30min,电压为90v,分离胶约1h,电压110v;使用甲醇浸泡pvdf膜活化5min,在25v电压下转膜,把蛋白质从胶中转移到pvdf膜上;膜正面朝上在37℃封闭液中摇动孵育2h,然后使用tbst清洗3次;pvdf膜正面朝上浸泡于一抗稀释液中(抗体购自abcam公司),4℃孵育过夜,tbst洗涤3次;pvdf膜正面朝上浸泡于二抗稀释液中,37℃孵育2h,tbst洗涤3次;滴加显色剂,进行拍照检测。
54.如图2所示,使用exo或trka-mab处理后ccsmcs中的nnos水平均有所提高,且二者的促进水平近似,共同使用exo和trka-mab后,细胞内的nnos含量进一步提高,说明能够有效促进细胞内no表达,为启动和维持勃起功能提供了有利条件。
55.实施例4动物体内实验
56.4.1大鼠神经损伤勃起障碍模型构建
57.选择健康sd雄性大鼠,适应性饲养1周后,戊巴比妥钠腹腔注射进行麻醉,剃除下腹部的体毛并用碘伏消毒。在大鼠耻骨上方、腹部中线出作切口暴露膀胱、前列腺腹侧叶,钝性分离直至定位到盆神经节,找到海绵体神经,使用止血钳对海绵体神经进行夹损(持续时间约1min,间隔30s后再持续约1min),另一侧做相同处理,最后关闭腹腔缝合伤口。
58.4.2实验分组和给药处理
59.将造模成功的sd大鼠随机分为4组,每组10只,分别为:exo组(用微量注射器将25mg/kg脐带间充质干细胞外泌体注射到大鼠海绵体内)、trka-mab组(用微量注射器将25mg/kg trka-mab抗体注射到大鼠海绵体内)、联合组(用微量注射器将25mg/kg脐带间充质干细胞外泌体和25mg/kg trka-mab抗体注射到大鼠海绵体内)、对照组(用微量注射器将等体积生理盐水注射到大鼠海绵体内),上述各组每周给药一次,共给药4次,治疗4周后检测治疗效果。
60.4.3大鼠勃起功能检测
61.检测大鼠海绵体内压(intracavernous pressure,icp)和实时动脉压(mean arterial pressure,map),具体步骤包括:大鼠麻醉后,暴露完整的阴茎和前列腺,定位盆大神经节和海绵体神经,用无菌洁净导管插入海绵体,导管另一端连接到压力测量装置;暴露右侧颈动脉,并在动脉中放置一个装有肝素生理盐水溶液的套管,用以测量动脉压,套管的另一端通过压力传感器与信号发生器连接,在海绵体神经上放置刺激电极,在电极刺激下,测量大鼠的icp和map,并计算每只大鼠的最大icp/map比值。
62.如图3所示,经过治疗后icp/map比值有不同程度的恢复,其中exo恢复效果强于trka-mab,在联合使用中icp/map比值升高最多,说明联合方式可显著改善大鼠神经损伤后的勃起功能障碍。
63.4.4 vegf表达水平检测
64.血管内皮生长因子(vascular endothelial growth factor,vegf)是一种高度特异性的促血管内皮细胞生长因子,具有促进血管通透性增加、细胞外基质变性、血管内皮细胞迁移、增殖和血管形成等作用,在阴茎勃起过程中,vegf表达水平的高低可反映阴茎充血情况的好坏,对维持正常勃起功能具有重要作用。
65.本实施例中通过elisa法检测海绵体组织中的vegf含量,治疗4周后脱颈处死大鼠,取海绵体组织,在4℃下进行组织匀浆,用含1%蛋白酶抑制剂的ripa裂解液提取阴茎海绵体组织中的蛋白质,使用elisa试剂盒(购自酶联生物公司)检测组织中的vegf含量,具体步骤按照试剂盒说明书进行。结果如图4所示,经过治疗处理后大鼠海绵体中的vegf水平有所提高,exo组和trka-mab表达水平类似,联合组略高于其他两个治疗组,说明本发明所提供的治疗药物能够促进海绵体中的vegf表达,利于阴茎正常充血,进而启动和维持勃起功能。
66.虽然本发明参考其示例性的实施例已经进行了具体显示和描述,本领域的技术人员应当理解的是,在不偏离由所附权利要求书所涵盖的本发明的范围的情况下,可以在其中做出在形式和细节方面的多种改变。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1