一种特草定的制备方法与流程
1.本发明涉及一种特草定的制备方法,特别涉及一种原料稳定易得、原料毒性小、工艺简洁、耗时少的特草定的制备方法,属于农药制备技术领域。
背景技术:
2.特草定,化学名称5-氯3-(1 ,1-二甲基乙基)-6-甲基-2,4(1h ,3h)-二羟基嘧啶,分子式:c9h
13
cln2o2,结构式如下:特草定是由杜邦1967年研发上市,用于控制一年生杂草、阔叶杂草和一些多年生杂草,如鹅肠菜、马唐、宝盖草、野芥末等,多用于甘蔗、苜蓿、桃子、黑莓、覆盆子、山核桃、薄荷、芦荟等作物。
3.特草定产品上市时间较早,但是关于特草定的制备方法,国内外公布的制备方法却很少。专利cn109651266a以乙酰乙酸乙酯为原料,与氨源缩合生成3-氨基巴豆酸乙酯,再与叔丁基异氰酸酯关环反应生成中间体,最后氯代生成特草定,反应式如下:该工艺使用毒性极大的叔丁基异氰酸酯,价格较高,而且异氰酸酯基活泼,存储难度大,在生产过程中存在较大的安全隐患。
4.专利ca716060以及文献[synthesis and studies with 2-c
14-labeled bromacil and terbacil]公开了一种特草定的合成方法,由叔丁胺合成叔丁基脲,与乙酰乙酸乙酯反应,再自身缩合生产中间体,最后氯代生成特草定,反应式如下:
该合成工艺存在以下问题:1,原料叔丁基脲的制备需要叔丁胺与氰酸钠(钾)反应,反应收率低;2,叔丁基脲与乙酰乙酸乙酯的合成副产物多,收率低,反应时间长,造成产品生产成本高。
技术实现要素:
[0005]
针对现有技术中特草定的制备工艺存在的各种不足,本发明提供了一种特草定的制备方法,该方法为特草定的制备提供了一种新的工艺路线,所用原料毒性小、生产安全性高,对设备要求简单,适合工业化生产。
[0006]
本发明具体技术方案如下:一种特草定的制备方法,该方法包括以下步骤:(1)6-甲基尿嘧啶和烷基化试剂发生烷基化反应,生成3-叔丁基-6-甲基尿嘧啶;(2)将3-叔丁基-6-甲基尿嘧啶与氯化试剂进行氯化反应,得到特草定。
[0007]
进一步的,步骤(1)中,以6-甲基尿嘧啶为原料,通过烷基化反应得到3-叔丁基-6-甲基尿嘧啶。所述烷基化反应指的是有机化合物分子中连在碳、氧和氮上的氢原子被烷基所取代的反应。烷基化反应是现有技术中比较成熟的一类反应,本领域技术人员根据现有技术可以自行选择其反应条件,例如催化剂、碱、溶剂、反应温度、原料用量等。
[0008]
进一步的,在本发明中,烷基化反应所用的烷基化试剂可以为叔丁基卤代烃或叔丁醇,这些原料简单易得,且无毒性,成本低。
[0009]
进一步的,所述叔丁基卤代烃可以为氯代叔丁烷、溴代叔丁烷、碘代叔丁烷等。6-甲基尿嘧啶与叔丁基卤代烃的摩尔比为1:1~1.5,例如1:1、1:1.05、1:1.1、1:1.15、1:1.2、1:1.25、1:3、1:1.35、1:1.4、1:1.45、1:1.5,优选为1:1~1.2。
[0010]
进一步的,步骤(1)中,烷基化反应在无催化剂或有催化剂存在下进行,当有催化剂存在时,反应的收率更高。所述催化剂可以为相转移催化剂、酸催化剂、分子筛催化剂、贵金属催化剂。其中,相转移催化剂可以使处于两个互不相溶的液相系统中的反应物进行反应,反应无需在无水条件下操作,常用的相转移催化剂有季铵盐 (q+x-)、四级膦盐[(c2h5)3p
+
ch2c6h5]cl-或冠醚等。其中,季铵盐是最为常用的相转移催化剂,可以为四丁基氯化铵、
四丁基溴化铵、四丁基碘化铵、四丁基硫酸氢铵中的一种或多种。
[0011]
进一步的,所述酸催化剂可以为路易斯酸,例如al2cl6等,所述分子筛催化剂可以为nax型沸石分子筛等,所述贵金属催化剂可以为过渡金属催化剂,例如cui、fecl2等。
[0012]
优选的,烷基化反应的催化剂为相转移催化剂。
[0013]
进一步的,步骤(1)中,6-甲基尿嘧啶与催化剂的摩尔比为1:0.02~0.5,例如1:0.02、1:0.05、1:0.1、1:0.2、1:0.3、1:0.4、1:0.5,优选为1:0.02~0.1。
[0014]
进一步的,步骤(1)中,当催化剂为相转移催化剂、分子筛催化剂或贵金属催化剂时,烷基化反应在碱存在下进行,反应产物经过中和反应,得到3-叔丁基-6-甲基尿嘧啶;当催化剂为酸催化剂时,烷基化反应不加入碱。所述碱为氢氧化钠、碳酸钠、碳酸氢钠、氢氧化钾、碳酸钾、碳酸氢钾、二乙胺、三乙胺中的一种或多种,这碱可以为纯物质,也可以是它们的溶液状态。6-甲基尿嘧啶与碱的摩尔比为1:1~10,例如1:1、1:1.1、1:1.2、1:1.5、1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9、1:10,优选为1:1~5。
[0015]
进一步的,步骤(1)中,当烷基化试剂为叔丁基卤代烃时,烷基化反应需在溶剂存在下进行,以溶解叔丁基卤代烃。当烷基化试剂为叔丁醇时,烷基化反应可以在无溶剂条件下进行,也可以在有溶剂条件下进行,这是因为叔丁醇自身既可以作为原料,也可以作为溶剂,如果在无溶剂条件下进行时,可以加大叔丁醇的用量,使其同时既作为原料又作为溶剂使用。
[0016]
进一步的,步骤(1)中,烷基化反应的溶剂可以为二甲基亚砜(dmso)、n,n二甲基甲酰胺(dmf)、甲苯、二甲苯等。溶剂的质量一般为6-甲基尿嘧啶的5-10倍。
[0017]
进一步的,步骤(1)中,当烷基化试剂为叔丁基卤代烃时,6-甲基尿嘧啶与烷基化试剂的摩尔比为1:1~1:5,例如1:1.05、1:1.1、1:1.2、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5,优选1:1~1:2;当烷基化试剂为叔丁醇时,因为叔丁醇可以作为溶剂使用,因此其用量有一定变化,当反应在溶剂存在下进行时,叔丁醇无需作为溶剂,因此6-甲基尿嘧啶与叔丁醇的摩尔比为1:1~1:5,例如1:1.05、1:1.1、1:1.2、1:1.5、1:2、1:2.5、1:3、1:3.5、1:4、1:4.5、1:5,优选1:1~1:2;当叔丁醇作为溶剂使用时,6-甲基尿嘧啶与叔丁醇的摩尔比为1:10~30,例如1:10、1:15、1:20、1:25、1:30,优选1:15~20。
[0018]
进一步的,步骤(1)中,烷基化反应温度为20~200℃,例如20℃、50℃、80℃、100℃、120℃、150℃、180℃、200℃,优选为80~100℃。烷基化反应至原料完全消耗为止,烷基化反应时间一般为2~24h,例如2h、4h、6h、8h、10h、15h、20h、24h,优选为8~12h。
[0019]
进一步的,步骤(2)中,所述氯化试剂为氯气、磺酰氯、三氯氧磷、五氯化磷或二氯亚砜,优选为氯气。
[0020]
进一步的,步骤(2)中,氯化反应在水环境下进行。
[0021]
进一步的,步骤(2)中,3-叔丁基-6-甲基尿嘧啶与氯化试剂的摩尔比为1:1~1:1.5,优选1:1.1~1:1.2。
[0022]
进一步的,步骤(2)中,氯气为氯源时,氯化反应的温度为70℃-100℃,优选80-90℃。
[0023]
在本发明某一具体实施方式中,提供了一种以叔丁基卤代烃或叔丁醇为烷基化试剂、以氯气为氯化试剂制备特草定的方法,反应方程式如下:
具体制备步骤如下:(1)烷基卤代烃为烷基化试剂时:将6-甲基尿嘧啶、烷基卤代烃、季铵盐催化剂,二甲基亚砜(dmso)加入反应瓶,升高反应温度,滴加碱的(水)溶液,保温反应,反应结束后,加水淬灭,调节ph至中性析出,过滤分离,水洗,得到湿料3-叔丁基-6-甲基尿嘧啶。
[0024]
(2)叔丁醇为烷基化试剂时:将6-甲基尿嘧啶、叔丁醇、季铵盐催化剂和碱加入反应瓶,升温加热回流反应;反应结束后,过滤分离,得到3-叔丁基-6-甲基尿嘧啶盐。
[0025]
(3)将反应得到的3-叔丁基-6-甲基尿嘧啶(盐)加入到水中,升高反应温度,通入氯气,有固体逐渐析出,液相跟踪反应结束后,降温,过滤水洗,烘干得到特草定原药。
[0026]
本发明与现有技术相比具有以下优势:1、本发明以6-甲基尿嘧啶为原料,6-甲基尿嘧啶可以用乙酰乙酸甲酯和尿素合成,该原料是一种用途较广的医药和农药中间体,经过烷基化反应合成3-叔丁基-6-甲基尿嘧啶,烷基化反应利用胺基与烷基化试剂反应,该反应路线成熟,应用广泛。同样的,本发明所用的烷基化试剂原料稳定易得,毒性小,三废低,具有很大的工业生产优势。
[0027]
2、本发明避免了使用低沸点、易挥发的原料,反应副产物少,降低了生产成本。
[0028]
3、本发明利用烷基化反应合成原料药的中间体,制备过程不需要有毒原料,对设备要求简单,通过对反应条件的优化和筛选,原子利用率高,反应时间短,催化剂可选择范围广,收率高,成本低,适合于工业化生产。
附图说明
[0029]
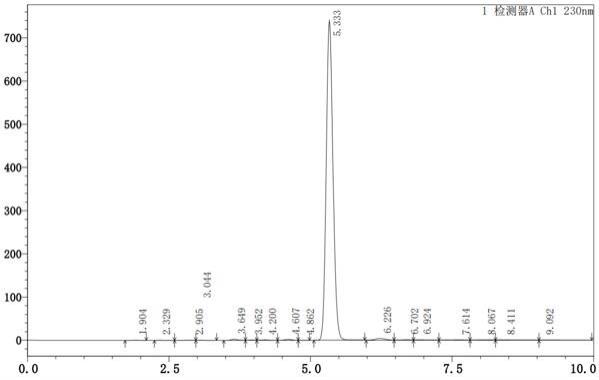
图1为实施例27所得产物特草定的hplc图谱。
具体实施方式
[0030]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明的一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0031]
本发明未详尽描述的方法和装置均为现有技术,不再赘述。
[0032]
实施例1称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、3.3g(0.01mol)
四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率91.5%(以6-甲基尿嘧啶计)。
[0033]
实施例2称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、1.7g(0.005mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率82.3%(以6-甲基尿嘧啶计)。
[0034]
实施例3称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g n,n-二甲基亚砜(dmso),开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率89%(以6-甲基尿嘧啶计)实施例4称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加26g(0.12mol)50%碳酸钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率85%(以6-甲基尿嘧啶计)实施例5称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、0.53g(0.002mol)al2cl6加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率80.5%(以6-甲基尿嘧啶计)实施例6称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、0.64g(0.002mol)nax分子筛加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率83.2%(以6-甲基尿嘧啶计)实施例7称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、0.4g(0.002mol)cui加入四口烧瓶中,加入 100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率84.7%(以6-甲基尿嘧啶计)
实施例8称取13.0g(0.1mol)6-甲基尿嘧啶、13.8g(0.1mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率85.5%(以6-甲基尿嘧啶计)。
[0035]
实施例9称取13.0g(0.1mol)6-甲基尿嘧啶、16.6g(0.12mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率92%(以6-甲基尿嘧啶计)。
[0036]
实施例10称取13.0g(0.1mol)6-甲基尿嘧啶、16.6g(0.12mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至50℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,50℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率64.4%(以6-甲基尿嘧啶计)。
[0037]
实施例11称取13.0g(0.1mol)6-甲基尿嘧啶、16.6g(0.12mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至100℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,100℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率88.6%(以6-甲基尿嘧啶计)。
[0038]
实施例12称取13.0g(0.1mol)6-甲基尿嘧啶、16.6g(0.12mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应3h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率56.8%(以6-甲基尿嘧啶计)。
[0039]
实施例13称取13.0g(0.1mol)6-甲基尿嘧啶、16.6g(0.12mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应10h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率90.8%(以6-甲基尿嘧啶计)。
[0040]
实施例14称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至
80℃,滴加25.7g(0.12mol)50%碳酸氢钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率73.3%(以6-甲基尿嘧啶计)。
[0041]
实施例15称取13.0g(0.1mol)6-甲基尿嘧啶、14.5g(0.105mol)溴代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,滴加24.2g(0.12mol)50%碳酸氢钾水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率68.8%(以6-甲基尿嘧啶计)。
[0042]
实施例16称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率77.5%(以6-甲基尿嘧啶计)。
[0043]
实施例17称取13.0g(0.1mol)6-甲基尿嘧啶、11.2g(0.12mol)氯代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率78.2%(以6-甲基尿嘧啶计)。
[0044]
实施例18称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、0.53g(0.002mol)al2cl6加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率71.7%(以6-甲基尿嘧啶计)。
[0045]
实施例19称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、0.64g(0.002mol)nax分子筛加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率63.2%(以6-甲基尿嘧啶计)实施例20称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、0.4g(0.002mol)cui加入四口烧瓶中,加入100g n,n-二甲基甲酰胺(dmf),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束加水淬灭,调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率75.2%(以6-甲基尿嘧啶计)。
[0046]
实施例21称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、3.3g(0.01mol)
四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至100℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,100℃保温反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率74.7%(以6-甲基尿嘧啶计)。
[0047]
实施例22称取13.0g(0.1mol)6-甲基尿嘧啶、9.8g(0.105mol)氯代叔丁烷、3.3g(0.01mol)四丁基溴化铵加入四口烧瓶中,加入100g 二甲苯,开启机械搅拌,升温至80℃,滴加16g(0.12mol)30%氢氧化钠水溶液,滴加过程中温度升高,滴加完毕,80℃保温反应12h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率76.3%(以6-甲基尿嘧啶计)。
[0048]
实施例23称取13.0g(0.1mol)6-甲基尿嘧啶、7.9(0.105mol)叔丁醇、0.4g(0.002mol)cui加入四口烧瓶中,加入4.9g(0.12mol)氢氧化钠加入,100g 二甲基亚砜(dmso),开启机械搅拌,升温至80℃,保温反应8h,液相取样检测,反应结束后,加水调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率75.2%(以6-甲基尿嘧啶计)。
[0049]
实施例24称取13.0g(0.1mol)6-甲基尿嘧啶、7.9(0.105mol)叔丁醇、0.4g(0.002mol)cui加入四口烧瓶中,加入4.9g(0.12mol)氢氧化钠加入,100g 二甲苯,开启机械搅拌,升温至92℃,回流带水反应8h,液相取样检测,反应结束加水淬灭,水相调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率81.4%(以6-甲基尿嘧啶计)。
[0050]
实施例25称取13.0g(0.1mol)6-甲基尿嘧啶、7.9(0.105mol)叔丁醇、0.26g(0.002mol)fecl2加入四口烧瓶中,加入13g(0.12mol)碳酸钠加入,100g 二甲苯,开启机械搅拌,升温至92℃,回流带水反应8h,液相取样检测,反应结束加水淬灭,加水调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率85.6%(以6-甲基尿嘧啶计)。
[0051]
实施例26称取13.0g(0.1mol)6-甲基尿嘧啶、130g(1.74mol)叔丁醇、、0.4g(0.002mol)cui加入四口烧瓶中加入4.9g(0.12mol)氢氧化钠加入,开启机械搅拌,升温至80℃,回流反应8h,液相取样检测,反应结束负压脱溶除去溶剂,加水调节ph至中性,有固体析出,过滤分离,水洗烘干后得到3-叔丁基六甲基尿嘧啶产品,收率84.8%(以6-甲基尿嘧啶计)。
[0052]
实施例27称取38g(0.2mol)实施例1的3-叔丁基-6-甲基尿嘧啶、300g水加入四口烧瓶中,升温加热至85℃,开始通氯,控制通氯速度,3.5h通入17g(0.24mol),液相中控未转变化,原料未转将至1%以下停止通氯,降至室温后,过滤分离,水洗,烘干得到特草定原药,产品收率95.2%。
[0053]
实施例28称取38g(0.2mol)实施例1的3-叔丁基-6-甲基尿嘧啶、300g水加入四口烧瓶中,升温加热至85℃,开始通氯,控制通氯速度,3.5h通入21.5g(0.3mol),液相中控未转变化,原
料未转将至1%以下停止通氯,降至室温后,过滤分离,水洗,烘干得到特草定原药,产品收率93.2%。
[0054]
上述实施例只为阐述本发明合成特草定原药的方法,不能限制本发明的保护范围。本领域技术人员应该明白,凡在本发明精神和原则之内,所做的任何修改、同等替换、改进等,都在本发明受保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1