嗜热链球菌FUA329及其发酵生产尿石素A的方法
嗜热链球菌fua329及其发酵生产尿石素a的方法
技术领域
1.本发明属于生物工程技术领域,提供了一种来自人母乳源的嗜热链球菌fua329,以及利用其发酵鞣花酸生产尿石素a的方法。
背景技术:
2.1980年,在喂食鞣花酸的大鼠代谢物内,尿石素a被首次发现,其分子式为c
13
h8o4,相对分子质量为228.2。随后,研究发现尿石素a具有多种生物活性。如调节线粒体的生物合成和自噬诱导的线粒体损伤清除以增强肌肉功能;调节雌激素受体抑制高脂饮食介导的子宫肿瘤发生的概率;通过调节雄激素受体防治前列腺癌;可显著抑制典型的炎症因子,例如对肠炎、骨关节炎、神经炎、肾脏炎、椎间盘病变等具有抑制作用;可有效降低心脏代谢风险;可预防d-半乳糖诱导的脑衰老,改善认知障碍;可预防并逆转由高脂饮食造成的肥胖,改善代谢功能,且无副作用。
3.大量的研究表明鞣花酸代谢为尿石素的过程中,有多种肠道微生物及酶的参与。根据肠道微生物代谢鞣花酸是否产生尿石素及其产生的尿石素的种类,可以将人分成三种类型:尿石素a型,终产物为尿石素a;尿石素b型,终产物为尿石素b和异尿石素a;尿石素0型,不产生尿石素。有研究发现,患有代谢综合症和大肠癌等慢性病的人群中,尿石素b型比例显著增加,在40岁以上人群中,仅有约50%的人为尿石素a型。由于尿石素a具有多种益生性功能,且尿石素a型人群在老年人及患有慢性疾病的人群中所占比例较低,因此,2018年,美国fda批准了尿石素a可应用于膳食补充剂。amazentis公司开发了高纯度尿石素a为主要成分的营养补充剂商品mitopure,用于抵抗细胞和肌肉衰退。
4.目前,尿石素的工业化生产主要是利用化学法,但该方法反应时间长、成本高、耗能大、产品价格昂贵。如果开发获得可转化鞣花酸生成尿石素a的新一代益生菌,则既可以利用微生物发酵法制备尿石素a,又可以发酵富含鞣花酸的茶叶和食品,制备富含尿石素a的益生菌发酵饮品。但是,目前仅报道有gordonibacter urolithinfaciens和gordonibacter pamelaece可体外转化鞣花酸生成异尿石素a,bifidobacterium pseudocatenulatum可转化鞣花酸生成尿石素a和尿石素b,且上述菌株均从人体肠道中分离得到。株式会社大赛璐利用eggerthella sp.、clostridium boltec、clostridium citroniae、clostridium asparagiforme等菌株混合发酵可转化鞣花酸制备尿石素a。因此,探索多渠道能转化鞣花酸生成尿石素a的菌株,筛选一株能在体内和体外产生的尿石素a的菌株,能弥补当前尿石素a制备技术的不足,对工业生产具有重要的意义。
技术实现要素:
5.本发明针对上述技术存在的不足,提供一株人母乳源的嗜热链球菌fua329(streptococcus thermophilus)。
6.一种嗜热链球菌fua329,该菌株已经于2022年5月23日保藏于中国普通微生物菌种保藏管理中心,保藏编号为cgmcc no.24963。
7.本发明提供的嗜热链球菌fua329用于产尿石素a。
8.本发明提供一种组合物用于制备改善肠道菌群药物的用途,所述组合物含有嗜热链球菌fua329。
9.一方面,本发明提供了所述嗜热链球菌fua329的筛选方法,包括以下步骤:
10.i)验证产尿石素a的母乳样本:在无菌条件下,将母乳样本接种到含有鞣花酸的abb液体培养基中,厌氧条件下培养4天,以含鞣花酸不含母乳的培养基和含母乳不含鞣花酸的培养基做对照,每天收集一次样本,用有机溶剂c2h3n:h2o:hcooh(80:19.9:0.1,v:v:v:)等体积萃取,进行hplc和hplc-ms/ms分析,筛选出产尿石素a的母乳样本;
11.ii)筛选产尿石素a的菌株:用已被验证产尿石素a的母乳样本发酵液,添加生理盐水稀释后,取0.1ml涂布在abb固体平板上,在厌氧条件下培养之后,获取多个微生物菌落,每个菌落分别接种于含有鞣花酸的abb液体培养基中,并在厌氧条件下进行发酵培养后,对发酵液进行hplc和hplc-ms/ms分析,筛选出产尿石素a的菌株,命名为fua329。
12.另一方面,本发明提供了所述嗜热链球菌fua329用于产尿石素a的方法,包括以下步骤:
13.1)菌种活化:取-80℃冰箱里保藏于甘油管中的fua329于abb固体培养基上进行三区划线,获得单菌落;
14.2)种子培养:将活化得到的菌株fua329的单菌落接种到种子培养基中培养获取种子液;
15.3)发酵培养:将种子液接种于添加了鞣花酸的发酵培养基中进行发酵培养;
16.4)分离提取:将发酵液离心,所得上清液即为尿石素a粗提取液。
17.所述步骤1)中的abb固体培养基配方为添加有2%琼脂的abb厌氧基础肉汤培养基。
18.所述步骤2)中的种子培养基为abb厌氧基础肉汤培养基,ph6.8
±
0.2,其配方包括:蛋白胨16.0g/l,酵母浸粉7.0g/l,氯化钠5.0g/l,淀粉1.0g/l,葡萄糖1.0g/l,丙酮酸钠1.0g/l,精氨酸1.0g/l,琥珀酸钠0.5g/l,半胱氨酸盐酸盐0.5g/l,碳酸氢钠0.4g/l,焦磷酸铁0.5g/l,氯化血红素0.005g/l,维生素k 0.0005g/l,巯基乙酸钠0.5g/l,二硫苏糖醇1.0g/l。
19.所述步骤2)中的培养条件为在37℃厌氧条件下培养24h。
20.所述步骤3)中的发酵培养基为含20μm鞣花酸的abb厌氧基础肉汤培养基。
21.所述步骤3)中的种子液的接种量为2%。
22.所述步骤3)中的发酵培养条件为在37℃厌氧条件下培养48h。
23.所述步骤4)中的离心条件为在12000
×
g、4℃离心10min。
24.本发明的有益效果:本发明提供了一株来自人母乳源的能转化鞣花酸生成尿石素a的嗜热链球菌fua329,为尿石素a的制备提供了一种新的途径。该技术操作方便,产量高(转化率82%),适合大批量生产尿石素a。并且,本发明提供的嗜热链球菌fua329安全性高,益生性好,具有潜力成为新型益生菌。
附图说明
25.图1为菌株fua329的革兰氏染色图(
×
1000);
26.图2为菌株fua329菌落形态图;
27.图3为菌株fua329系统进化树;
28.图4为尿石素标样液相图(a),a图中峰的数字1为尿石素d,2为鞣花酸,3为尿石素m6,4为尿石素c,5为异尿石素a,6为尿石素a,7为尿石素b;尿石素a标样质谱图(a)图5菌株fua329发酵液的液相图(b);菌株fua329转化鞣花酸产生尿石素a发酵液质谱图(b);
29.图6为菌株fua329溶血平板实验结果图;
30.图7为菌株fua329发酵转化鞣花酸生成尿石素a的转化过程;
31.图8为菌株fua329在体外不同ph和胆盐浓度处理后的酸耐受性和胆盐耐受性实验结果。
具体实施方式
32.下面结合具体实施例对本发明作进一步说明,以使本领域的技术人员可以更好的理解本发明并能予以实施,但所举实施例不作为对本发明的限定。
33.实施例1菌株的筛选
34.实施例1:菌株的分离与鉴定
35.本发明涉及的菌株fua329是在人母乳源中分离得到的嗜热链球菌fua329,该菌株已经于2022年5月23日保藏于中国普通微生物菌种保藏管理中心,保藏单位地址:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所菌种保藏中心。联系电话为010-64807355,保藏编号为cgmcc no.24963。该菌株16s rrna基因序列的genbank登录号为om892001。
36.1.菌株的筛选:
37.1)验证产尿石素a的母乳样本:在无菌条件下,将1ml母乳样本接种到含有20μm鞣花酸的abb液体培养基中,厌氧条件下培养4天,以含鞣花酸不含母乳的培养基和含母乳不含鞣花酸的培养基做对照,每天收集一次10ml样本,用有机溶剂c2h3n:h2o:ch2o2(80:19.9:0.1,v:v:v:)等体积萃取,进行hplc和hplc-ms/ms分析,筛选出产尿石素a的母乳样本;
38.2)筛选产尿石素a的菌株:用已被验证产尿石素a的母乳样本发酵液,添加生理盐水稀释至10-3-10-7
后,取0.1ml涂布在abb固体平板上,在厌氧37℃条件下培养24-48h之后,获取93个微生物菌落,每个菌落分别接种于含有20μm鞣花酸的abb液体培养基中,并在37℃厌氧条件下进行发酵培养48h,进行hplc和hplc-ms/ms分析,筛选出产尿石素a的菌株,命名为fua329。
39.2.形态学鉴定:
40.所述菌株fua329为革兰氏阳性球菌,在abb厌氧基础肉汤培养基中37℃生长48h,菌落呈圆形,乳白色半透明,表面湿润,边缘规则,无晕环,中央突起,直径0.5-1.0mm,易挑取,如图1和图2所示。
41.3.生理生化鉴定:
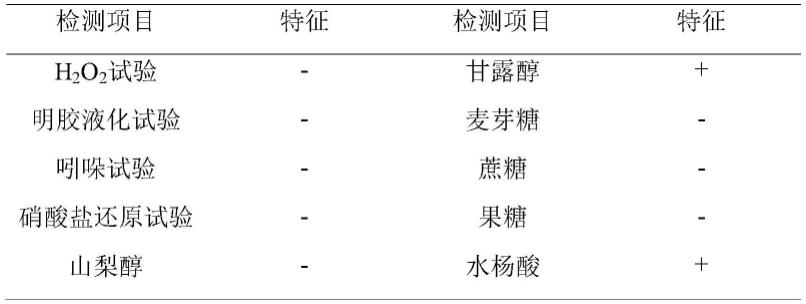
42.参照常见细菌系统鉴定手册(东秀珠,蔡妙英.常见细菌系统鉴定手册.北京,科学出版社,2001),对菌株进行水杨酸试验,h2o2试验,明胶液化试验,吲哚试验,硝酸盐还原试验,甘露醇、山梨醇、麦芽糖、蔗糖、果糖利用等试验,初步确定菌株种属。实验结果显示,该菌株在甘露醇试验和水杨酸试验中呈阳性,h2o2试验,明胶液化试验,吲哚试验,胆汁溶菌实
验,山梨醇、麦芽糖、蔗糖、果糖试验结果均为阴性。部分生理生化结果见表1。
43.表1菌株fua329的生理生化试验结果
[0044][0045]
注:+:阳性;-:阴性;
[0046]
4.菌株fua329 16s rrna序列的扩增和分析
[0047]
用axygen试剂盒提取得到fua329的基因组,选用扩增原核微生物16s rrna序列的通用引物于pcr mix体系中反应。
[0048]
所述用于pcr反应的通用引物:27f:5
’–
agagtttgatcctggctcag-3’;1492r:5
’‑
ggttaccttgttacgactt-3’。
[0049]
所述反应体系(25μl)为:2
×
max premix(12.5μl),上下游引物(各0.75μl),dna模板(0.5μl),ddh2o(10.5μl)。反应程序:98℃变性2min;98℃变性10s,55℃退火5s,72℃延伸10s,30-35个循环;72℃终延伸2min。序列测序后提交genbank(登录号:om892001),将该序列与genbank数据库中的序列进行同源性比对,发现与菌株streptococcus thermophilus dsm20617
t
(登录号:nr118998)16s rrna基因序列相似度达99.57%。系统发育树表明菌株fua329与streptococcus thermophilus亲缘关系最近,见图3。
[0050]
嗜热链球菌fua329 16s rrna基因序列的genbank登录号为om892001,具体序列如下:
[0051]
tgcggcagctataatgcagtagaacgctgaagagaggagcttgctcttcttggatgagttgcgaacgggtgagtaacgcgtaggtaacctgccttgtagcgggggataactattggaaacgatagctaataccgcataacaatggatgacccatgtcatttatttgaaaggggcaaatgctccactacaagatggacctgcgttgtattagctagtaggtgaggtaacggctcacctaggcgacgatacatagccgacctgagagggtgatcggccacactgggactgagacacggcccagactcctacgggaggcagcagtagggaatcttcggcaatgggggcaaccctgaccgagcaacgccgcgtgagtgaagaaggttttcggatcgtaaagctctgttgtaagtcaagaacgagtgtgagagtggaaagttcacactgtgacggtagcttaccagaaagggacggctaactacgtgccagcagccgcggtaatacgtaggtcccgagcgttgtccggatttattgggcgtaaagcgagcgcaggcggtttgataagtctgaagttaaaggctgtggctcaaccatagttcgctttggaaactgtcaaacttgagtgcagaaggggagagtggaattccatgtgtagcggtgaaatgcgtagatatatggaggaacaccggtggcgaaagcggctctctggtctgtaactgacgctgaggctcgaaagcgtggggagcgaacaggattagataccctggtagtccacgccgtaaacgatgagtgctaggtgttggatcctttccgggattcagtgtcgcagctaacgcattaagcactccgcctggggagtacgaccgcaaggttgaaactcaaaggaattgacgggggcccgcacaagcggtggagcatgtggtttaattcgaagcaacgcgaagaaccttaccaggtcttgacatcccgatgctatttctagagatagaaagttacttcggtacatcggtgacaggtggtgcatggttgtcgtcagctcgtgtcgtgagatgttgggttaagtcccgcaacgagcgcaacccctattgttagttgccatcattcagttgggcactctagcgagactgccggtaat
aaaccggaggaaggtggggatgacgtcaaatcatcatgccccttatgacctgggctacacacgtgctacaatggttggtacaacgagttgcgagtcggtgacggcaagctaatctcttaaagccaatctcagttcggattgtaggctgcaactcgcctacatgaagtcggaatcgctagtaatcgcggatcagcacgccgcggtgaatacgttcccgggccttgtacacaccgcccgtcacaccacgagagtttgtaacacccgaagtcggtgaggtaaccttttggagccagccgcctaaggtgaatgcag。
[0052]
实施例2菌株fua329发酵转化鞣花酸生产尿石素a的过程及其鉴定
[0053]
种子培养基为abb厌氧基础肉汤培养基,其配方包括蛋白胨16.0g/l,酵母浸粉7.0g/l,氯化钠5.0g/l,淀粉1.0g/l,葡萄糖1.0g/l,丙酮酸钠1.0g/l,精氨酸1.0g/l,琥珀酸钠0.5g/l,半胱氨酸盐酸盐0.5g/l,碳酸氢钠0.4g/l,焦磷酸铁0.5g/l,氯化血红素0.005g/l,维生素k0.0005g/l,巯基乙酸钠0.5g/l,二硫苏糖醇1.0g/l,ph6.8
±
0.2。
[0054]
发酵培养基为含20μm鞣花酸的abb厌氧基础肉汤培养基。
[0055]
1.菌株的活化:将保种于-80℃冰箱中的嗜热链球菌fua329在abb固体培养基上三区划线活化;
[0056]
2.种子液的制备:将菌株fua329的单菌落接种到种子培养基中,在37℃厌氧条件下培养24h获取种子液;
[0057]
3.发酵液的制备:将种子液以1%接种量接种至发酵培养基,在37℃厌氧条件下培养48h,12000
×
g、4℃离心10min,取上清液即为尿石素a发酵液;
[0058]
4.hplc和uplc-ms鉴定分析:取1.0ml发酵液与c2h3n:h2o:ch2o2(80:19.9:0.1,v:v:v)溶液等体积混合,充分混合后用注射器吸取1.0ml,过0.22μm有机滤膜后加入到hplc进样瓶中并做好标记,进行检测分析。
[0059]
1)hplc分析:在250
×
4.6mm,粒度为5μm的zorbax sb-c18柱(agilent,usa)上进行样品的色谱分离分析。以乙腈和1%甲醇为流动相,进样量5μl,流速为1ml/min。在305nm条件下进行记录。洗脱的梯度为:0~15min,0~20%乙腈;15~20min,20~70%乙腈;20~21min,70~95%乙腈;21~24min,95~100%乙腈;24~25min,100~20%乙腈;尿石素标样配置:分别称量0.005g尿石素a、尿石素c、尿石素d和异尿石素a,0.004g尿石素b和0.006g尿石素m6,加入1ml水和1ml c2h3n:h2o:ch2o2(80:19.9:0.1,v:v:v)溶液,混匀后,过0.22μm的有机滤膜到进样瓶,得到浓度为20μm的尿石素标样。
[0060]
2)hplc-ms/ms分析:采用c18色谱柱(acquity uplc beh c18,2.1
×
50mm,1.7μm),使用acquity qda esims对样品进行150~1000da分析,流动相为0.2%甲酸和乙腈,流速0.5ml/min,进样量50μl。洗脱的梯度为:0~6min,10~100%乙腈;6~7min,100%乙腈;7~8min,100~10%乙腈;8~9min,10%乙腈。
[0061]
经过与尿石素a,尿石素b,尿石素c,尿石素d,尿石素m6,异尿石素a和鞣花酸的标样对比,验证了fua329能产生尿石素a,分析结果如图4和图5所示。
[0062]
实施例3:菌株fua329的安全性与益生性分析
[0063]
1.菌株fua329安全性分析
[0064]
溶血实验:取1ml活化后的单菌落接种于abb液体培养基中,37℃厌氧培养12h后,取菌液离心(8000rpm
×
4℃,5min),将菌体沉淀用无菌生理盐水重悬,吸取100μl重悬菌液于含5%的绵羊血琼脂平板上进行三区划线,并以金黄色葡萄球菌作为阳性对照,37℃培养48h后,观察平板上生长菌落的溶血情况(图6)。
[0065]
药敏试验:选用27种抗生素(阿米卡星、诺氟沙星、氧氟沙星、环丙沙星、左氟沙星、红霉素、四环素、头孢呋辛、头孢唑啉、头孢噻吩、头孢噻肟、头孢曲松、头孢他啶、哌拉西啉、氨苄西林、苯唑西林、青霉素g、氨曲南、复方新诺明、呋喃妥因、氯霉素、多粘菌素b、克林霉素、卡那霉素、庆大霉素、链霉素、万古霉素),根据药敏试剂盒(杭州滨河微生物试剂有限公司)进行试验。菌株活化培养至对数生长期,取100μl 10-3
浓度的菌液于abb固体培养基上进行涂布。将含不同浓度的药敏纸片置于abb固体平板上,37℃厌氧培养48h后测量抑菌圈大小,每组试验重复3次求平均值,参考《抗菌药物纸片法敏感性试验的性能标准》判断菌株对不同药物的敏感性。
[0066]
通过溶血活性实验和药敏试纸实验等对菌株fua329的安全性进行研究。通过与β-溶血活性的金黄色葡萄球菌(s.aureus)对比,发现菌株fua329不产生溶血现象,如图3所示。在27种药敏试验中发现菌株fua329对9种抗生素产生耐药性,见下表2。
[0067]
表2菌株fua329药敏试验结果
[0068][0069]
注:r:抗性;i:中介;s:敏感性。
[0070]
2.菌株fua329益生性分析
[0071]
耐酸实验:配制ph值分别为2.0、3.0、4.0、5.0、6.0的abb液体培养基,以1%的接种量分别向不同ph值的abb液体培养基中接入活化后的菌株fua329,37℃厌氧培养后分别于0h、1h、2h、3h取样。采用稀释涂布平板法计算每组试验活菌数,以log cfu/ml记,将ph值6.8
±
0.2的原始abb液体培养基结果作对照组,每组试验重复三次。按下列公式计算菌株的对酸环境的耐受率。
[0072]
存活率(%)=a1/a0×
100%
[0073]
式中:a0、a1分别为对照组和实验组的活菌数。
[0074]
益生菌在被摄入之后,经由消化道到达胃部,因此对胃液耐受能力的大小是益生菌资源开发利用的重要指标,人体胃液的ph一般为2.0~3.0,胃排空时间大约为2~3h,益生菌制品通常是推荐在饭后0.5h食用,因此采用ph为2.0、3.0、4.0、5.0和6.0,保留时间为1、2和3h评估筛选菌株酸耐受性的存活率,检验菌株对胃液中极端酸性环境的耐受能力。结果表明,随着ph的降低和培养时间的延长,菌株的存活率均有不同程度的下降,但是fua329在不同ph条件下处理3h后的存活率均在58%以上,见图8。
[0075]
耐胆盐实验:配制含0.1%、0.2%、0.3%、0.4%、0.5%胆盐和不含胆盐的abb培养基,以1%的接种量分别向abb液体培养基中接入活化后的菌株fua329,37℃厌氧培养后分别于0h、1h、2h、3h取样。采用稀释涂布平板法计算每组试验活菌数,以log cfu/ml记,不含胆盐的原始abb液体培养基结果作对照组,每组试验重复三次,按下列公式计算菌株的对胆盐环境的耐受率。
[0076]
存活率(%)=b1/b0×
100%
[0077]
式中:b0、b1分别为对照组和实验组的活菌数。
[0078]
益生菌菌株要想在人体肠道内发挥其益生作用,必须得能够耐受广泛分布在肠腔中胆盐的抑菌作用,因此,菌株对胆盐的耐受能力也是筛选益生菌的重要标准之一。因此,本研究比较筛选菌株对0.1%-0.5%胆汁的耐受能力,菌株fua329在0.4%和0.5%胆盐培养基中培养3h后存活率均小于60%,而在0.3%、0.2%和0.1%胆盐培养基中培养3h后的存活率分别为61%、70.9%和77.7%。本研究通过体外耐酸和耐胆盐实验证明了菌株fua329具有较好的益生活性,具有潜力成为新型益生菌,见图8。
[0079]
以上所述,仅为本发明的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明公开的技术范围内,可轻易想到变化或替换,都应涵盖在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1