配体、金属有机框架材料和应用以及钙钛矿太阳能电池的制作方法
1.本发明涉及光伏材料技术领域,具体涉及一种配体、金属有机框架材料和应用以及钙钛矿太阳能电池。
背景技术:
2.近年来,随着国民经济的迅速发展,对各种能源的需求量日益增大,由此带来的环境问题日益突出。为此世界各国都在积极地寻找新的能源替代品,也就是清洁绿色能源,比如太阳能、风能等可再生资源。其中太阳能是人类取之不尽,用之不竭的可再生能源,来源广泛,不会造成环境污染,在长期的能源战略当中具有重要地位,也因此推动了世界各国对太阳能利用方面的研究,尤其是光伏发电,光伏发电已成为了近几年发展最快、最有活力的研究领域。
3.随着光伏发电被广泛应用于各行各业,越来越多的人开始把目光投向了研发高效率、低成本的新型太阳能电池,而在众多的新型太阳能电池中,钙钛矿太阳能电池凭借其器件效率高、载流子输运能力强以及吸光系数高等优势脱颖而出,成为了新型太阳能电池领域中的重要研究方向。
4.钙钛矿太阳能电池是一种利用钙钛矿型的有机金属卤化物半导体作为吸光材料的太阳能电池。虽然钙钛矿太阳能电池仅仅问世10年,但是其光电转换率已经达到世界上最先进的硅基太阳能电池的光电转换率。此外钙钛矿太阳能电池与硅基太阳能电池相比较,其光电转换率更高、生产成本更低、更易于生产和制造,在光伏发电领域具有极大的竞争力。但是目前限制钙钛矿太阳能电池发展的因素主要有两点,一是钙钛矿太阳能电池的成分含有铅,会对环境造成严重污染;二是钙钛矿太阳能电池在运行条件下的长期稳定性尚未实现。因此,解决钙钛矿太阳能电池的不稳定性、污染性等问题是该研究领域面临的重要课题。
5.金属有机框架材料(metal organic frameworks,mofs)是一种由金属离子与有机配体组成的多孔配位材料,其比表面积大、结构可调,可以作为钙钛矿太阳能电池的表面修饰剂,通过释放离子来减少由于钙钛矿成膜产生的离子空位,由此钝化钙钛矿的缺陷,从而提高器件的性能和稳定性,在钙钛矿太阳能电池领域展现出了巨大的发展潜力。然而由于大多数的金属有机框架材料的载流子迁移率较低,很难用作高效的电荷传输层,所以开发高导电性的mof材料是十分必要的。
技术实现要素:
6.为了解决现有金属有机框架材料的载流子迁移率低的问题,本发明提出了一种配体、金属有机框架材料和应用以及钙钛矿太阳能电池。
7.本发明的技术方案如下:一种制备金属有机框架材料用配体,其结构式如下:
。
8.一种金属有机框架材料,应用如上所述的制备金属有机框架材料用配体制备而成,所述金属有机框架材料的化学式为[zr2(l)3],其中l为c
30h24
o6s6;所述金属有机框架材料称为mof-et9。
[0009]
本发明还提供了一种如上所述的金属有机框架材料在钙钛矿太阳能电池中的应用。
[0010]
本发明还提供了一种钙钛矿太阳能电池,包括导电玻璃基板、金属电极、空穴传输层、钙钛矿吸收层、电子传输层以及电子萃取层,所述电子萃取层包含如上所述的金属有机框架材料。
[0011]
与现有技术相比,本发明解决了现有金属有机框架材料的载流子迁移率低的问题,具体有益效果为:1.本发明将一种硫基功能化的有机芳香羧酸配体应用于金属有机框架材料的合成,并以该金属有机框架材料作为电子萃取层的原材料,制备钙钛矿太阳能电池,利用硫醇配体及其衍生物独特的高反应活性,与金属中心形成稳定性强的共价键,从而提高钙钛矿太阳能电池器件的稳定性;2.硫醇功能化的金属有机框架材料形成了不溶于水的复合物封装层,可减少接触电阻、捕获可移动的pb
2+
离子,能有效地从钙钛矿太阳能电池中提取电子,优化钙钛矿太阳能电池的光电性能,减轻钙钛矿太阳能电池对环境的污染;3.本发明提供的钙钛矿太阳能电池在am 1.5 g,100 mwcm-2
的模拟太阳光光源条件下光电转换效率为22.7%,是目前金属有机框架材料在太阳电池应用的相关报道中最高的光电转换效率。
附图说明
[0012]
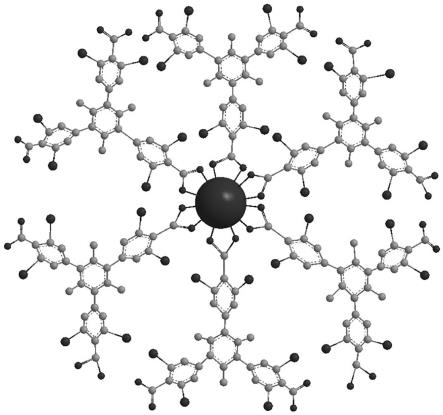
图1为本发明所述金属有机框架材料配体的合成路线示意图;图2 为本发明所述金属有机框架材料mof-et9的空间结构示意图;图3为本发明所述金属有机框架材料mof-et9电导率测试结果示意图;图4为本发明所述钙钛矿太阳能电池的结构组成示意图;图5为本发明所述钙钛矿太阳能电池的j-v曲线测试;图6为本发明所述钙钛矿太阳能电池的稳定性测试。
具体实施方式
[0013]
为使本发明的技术方案更加清楚,下面将结合本发明的说明书附图,对本发明实施例中的技术方案进行清楚、完整地描述,需要说明的是,以下实施例仅用于更好地理解本发明的技术方案,而不应理解为对本发明的限制。
[0014]
本实施例所述制备金属有机框架材料用配体的合成路线如图1所示。其中均三甲苯(cas:108-67-8)、4-溴-2,6-二氟苯甲酸(cas:183065-68-1)、苯基巯醇(cas:100-53-8)均从sigma-aldrich公司直接采购获得。
[0015]
下面描述本发明所述的金属有机框架材料的制备过程和表征结果:第一步、中间体1的合成:在500ml三口瓶中依次加入均三甲苯(6.0g,50mmol)、碘(15.5g,60mmol)、高碘酸(7.0g,32.5mmol)、3ml硫酸、50ml醋酸和10ml蒸馏水。在90℃下搅拌反应10h后,用125ml蒸馏水进行稀释,再依次用水和丙酮进行清洗,得到白色固体21.0g,即为中间体2,收率为84.5%。
[0016]
对获得的中间体2分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱1h nmr (400 mhz, cdcl3):δ 2.34 (s, 9 h);碳谱
13
c nmr (100 mhz, cdcl3):δ 144.82, 106.84, 34.19;质谱表征结果:esi(m/z): [m+h]
+ calcd. for c9h9i3, 497.88; found, 498.61;元素分析测试结果:calcd. for c9h9i3, c, 21.71, h, 1.82; found, c, 21.80, h, 1.91。
[0017]
根据以上分析数据可以证明,得到的中间体1结构式为:。
[0018]
第二步、中间体2的合成:在500ml三口瓶中依次加入中间体1(3.0g,6.03mmol)、4,4,4',4',5,5,5',5'-八甲基-2,2'-双(1,3,2-二氧杂硼烷)(6.3g,25.86mmol)、氯化钯(0.2g,1.1mmol)和乙酸钾(4.0g,2.95mmol),在90℃氮气保护下搅拌24h,反应结束后,反应体系缓慢冷却至25℃,加入25ml蒸馏水,然后用二氯甲烷萃取,每次50ml,萃取三次;萃取后合并有机相,用无水硫酸镁干燥,最后以乙酸乙酯/石油醚作为洗脱剂进行硅胶柱层析,得到无色透明固体2.40g,即为中间体2,收率为80%。
[0019]
对获得的中间体2分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱:1h nmr (400 mhz, cdcl3): δ 2.16 (s, 9 h), 1.23 (s, 36 h).碳谱:
13
c nmr (100 mhz, cdcl3): δ 152.40, 145.88, 83.76, 24.82, 22.25.
质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
27h45
b3o6, 498.08; found, 498.91.元素分析测试结果:calcd. for c
27h45
b3o6, c, 65.11, h, 9.11, o, 19.27; found, c, 66.02, h, 9.91, o, 19.89.根据以上分析数据可以证明,得到的中间体2的结构式为:。
[0020]
第三步、中间体3的合成:在500ml三口瓶中依次加入4-溴-2,6-二氟苯甲酸(4.74g,0.02mol)、碳酸钾(27.6g,0.20mol)和100mln-甲基-2-吡咯烷酮。在氮气保护下反应30min后,加入苯基巯醇(6ml,0.05mol)。在80℃下搅拌反应96h,反应结束后将反应体系缓慢冷却至25℃后,向混合物中加入碘甲烷(3ml,48.19mmol),充分反应后,倒入800ml的蒸馏水中,用二氯甲烷萃取,萃取三次,每次200ml。萃取后合并有机相,用无水硫酸镁干燥。以二氯甲烷/己烷作为洗脱剂进行硅胶柱层析,得到中间体3为6.96g,收率为76%。
[0021]
对获得的中间体3分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱:1h nmr (400 mhz, cdcl3): δ 7.52 (s, 2 h), 7.30 (m, 10 h), 4.22 (s, 4 h), 3.83 (s, 3 h).碳谱:
13
c nmr (100 mhz, cdcl3): δ 164.07, 142.45, 138.38, 129.22, 128.54, 127.33, 124.97, 122.50.质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
22h19
bro2s2, 459.42; found, 460.31.元素分析测试结果:calcd. for c
22h19
bro2s2, c, 57.52, h,4.17, o, 6.96; found, c, 58.02, h, 4.07, o, 7.89.根据以上分析数据可以证明,得到的中间体3的结构式为:
。
[0022]
第四步、中间体4的合成:在500ml三口瓶中依次加入中间体3(2.01g,4.36mmol)、双戊酰二硼(1.11g,4.36mmol)和氯化钯(77mg,0.11mmol),25℃条件下真空干燥4h,在氮气保护下加入无水醋酸钾(857mg,8.73mmol)、16ml无水的1,4-二氧烷。在90℃氮气保护下搅拌12h。反应体系缓慢冷却至25℃,依次加入磷酸钾(2.0mol,5.2ml)、1,3,6,8-四溴芘(522mg,1mmol)。在90℃下反应24h,反应结束后,反应体系缓慢冷却至25℃,将得到的混合物倒入200ml的冷水中,用二氯甲烷萃取,萃取三次,每次100ml。组合有机相用蒸馏水洗涤,洗涤三次,每次100ml,用无水硫酸镁干燥。以二氯甲烷/己烷/乙酸乙酯作为洗脱剂进行硅胶柱层析,得到淡黄色固体2.96g,即为中间体4,收率为54%。
[0023]
对获得的中间体4分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱:1h nmr (400 mhz, cdcl3): δ 7.30 (m, 36 h), 4.21 (d, 12 h), 3.83 (s, 9 h), 2.23 (s, 9 h).碳谱:
13
c nmr (100 mhz, cdcl3): δ 164.89, 141.06, 138.38, 137.94, 133.69, 131.74, 129.22, 128.54, 127.33, 122.92, 119.32, 52.07, 39.76, 18.91.质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
75h66
o6s6, 1255.71; found, 1256.43.元素分析测试结果:calcd. for c
75h66
o6s6, c, 71.74, h, 5.30, o, 7.64; found, c, 72.02, h, 6.07, o, 7.59.根据以上分析数据可以证明,得到的中间体4的结构式为:。
[0024]
第五步、中间体5的合成:将中间体4(125.57mg,0.10mmol)溶解在9ml的四氢呋喃中,然后加入氢氧化钾溶液(8.9mol/l,9ml)。在70℃下搅拌反应24h,反应结束后,反应体系缓慢冷却至25℃,加入10ml的10%盐酸。过滤、洗涤、干燥,得到119mg黄色固体,即为中间体5,收率为98%。
[0025]
对获得的中间体5分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱:1h nmr (400 mhz, cdcl3): δ 7.33 (m, 36 h), 4.22 (m, 12 h), 2.23 (s, 9 h).碳谱:
13
c nmr (100 mhz, cdcl3): δ 167.32, 142.17, 138.38, 137.92, 133.69, 131.74, 129.22, 128.54, 127.33, 123.97, 119.83, 39.76, 18.91.质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
72h60
o6s6, 1213.63; found, 1214.43.元素分析测试结果:calcd. for c
72h60
o6s6, c, 71.26, h, 4.98, o, 7.91; found, c, 72.02, h, 5.87, o, 8.59.根据以上分析数据可以证明,得到的中间体5的结构式为:。
[0026]
第六步、配体的合成:在500ml三口瓶中依次加入中间体5(60.68mg,0.05mmol)、无水氯化铝(240mg,1.8mmol)、5ml二氯甲烷和5ml甲苯,在25℃氮气保护下反应2h。再加入10ml的10%盐酸,在25℃下反应2h,反应结束后,过滤、洗涤、干燥,得到固体30mg,即为配体9,收率为89%。
[0027]
对获得的配体分别做核磁共振氢谱分析、碳谱分析、质谱分析和元素分析测试,结果如下:氢谱:1h nmr (400 mhz, dmso): δ 7.19 (s, 6 h), 2.23 (s, 9 h).碳谱:
13
c nmr (100 mhz, dmso): δ 168.36, 139.02, 138.45, 133.54, 131.86, 125.30, 122.49, 18.74.
质谱表征结果:esi(m/z): [m+h]
+ calcd. for c
30h24
o6s6, 672.88; found, 673.43.元素分析测试结果:calcd. for c
30h24
o6s6, c, 53.55, h, 3.60, o, 14.27; found, c, 54.25, h, 4.25, o,15.01.根据以上分析数据可以证明,得到的配体的结构式为:。
[0028]
第七步、多孔金属有机框架材料的制备:依次将配体(91.2mg,0.39mmol)和氯化锆(91.2mg,0.39mmol)装入厚壁玻璃管中,并向其中加入苯甲酸(478 mg,3.92 mmol)和70ml1mol/l的二甲基乙酰胺溶液,将玻璃管口用氢氧焰密封,置于干燥箱中,在120℃下加热反应24h,反应结束后将反应体系缓慢冷却至25℃,将得到的固体过滤,先用15ml二甲基乙酰胺溶液进行清洗,清洗三次,再用丙酮萃取,每次5ml,萃取五次,干燥后即得到多孔金属有机框架材料,称其为mof-et9。
[0029]
对多孔金属有机框架材料mof-et9材料表征:(1)将合成的mof-et9晶体存在玻璃毛细管中,采用单晶体x射线进行了晶体结构的测试,仪器为bruker-apexⅱ型ccd探测器,用cu kα (λ=1.54178
åꢀ
)x射线源采集,数据是sadabs程序对吸收进行校正,未对消光或衰变进行校正。用shelxtl软件包直接求解,测试结果见表1;表1
所述金属框架有机材料的结构式如下:
。
[0030]
(2)mof-et9材料的电导率测试:测试是在keithley 4200-scs和探针台lakeshore仪器上完成的,器件的制备是选择一颗较大的mof-et9晶体,在其上下表面接上金线,并用银浆连接表面和金线。用两电极法对其加上-5 v~5 v的电压,温度、湿度分别设定为80℃、98%,测试电流的变化得出其 i-v伏安曲线如图3所示,计算得到其电导率为6375s*m-1
,可以证明mof-et9具有良好的导电性。
[0031]
钙钛矿太阳能电池的制备:钙钛矿太阳能电池的制备是以导电玻璃层作为阳极,在其基础上利用旋涂法得到空穴传输层、钙钛矿吸收层、电子传输层以及电子萃取层,最后利用蒸发法获得100纳米的银作为钙钛矿太阳能电池的阴极,具体的操作步骤如下:(1)导电玻璃层的制备:将导电玻璃依次用丙酮、无水乙醇和去离子水超声清洗30min,然后用干燥的氮气吹干,最后在紫外臭氧机处理15min;(2)空穴传输层的制备:取50μl1mol/l的聚[双(4-苯基)(2,4,6-三甲基苯基)胺]溶液滴加到处理后的导电玻璃板上,以3000r/min旋涂30s,然后在120℃下加热15min,冷却备用,得到空穴传输层;(3)钙钛矿吸收层的制备:取50μl0.02mol/l的碘化铅前驱液滴加到空穴传输层薄膜上,待铺展之后,以5000r/min旋涂30s,70℃下加热5min去除溶剂。干燥后在碘化铅薄膜上面滴加50μl的甲基碘化铵前驱液,待其铺展之后,以5000r/min旋涂30s,100℃下加热lh,
即得到钙钛矿吸收层;(4)电子传输层的制备:选取苯基-c
61-丁酸甲酯作为电子传输层材料,苯基-c
61-丁酸甲酯溶于无水氯苯中配置成20mg/ml的溶液,取50μl 0.5mol/l苯基-c
61-丁酸甲酯溶液滴加到钙钛矿薄膜上,以700r/min旋涂30s,得到电子传输层;(5)电子萃取层的制备:在3.9
×
10-4 pa~4.0
×
10-4 pa的条件下,通过有机蒸发源在电子传输层薄膜上蒸镀一层富勒烯(bis c60),然后将mof-et9晶体粉末溶于无水异丙醇中,配置成0.5mg/ml的溶液;取50μl溶液滴加到蒸镀后的电子传输层薄膜上,以4000r/min旋涂30s,得到电子萃取层;(6)金属电极的制备:先将制备得到的电子萃取层避光放置在干燥器上,静置10h,再使用真空蒸镀设备以0.8~1.2 a/s的蒸发速率对上述制备完成的电池结构进行蒸镀,蒸镀后得到100纳米的银电极。
[0032]
通过以上步骤即完成钙钛矿太阳能电池的制备,制备得到的所述钙钛矿太阳能电池的结构组成示意图见图4。
[0033]
钙钛矿太阳能电池的器件表征:通过数字源表(keithley 2400)在am 1.5 g,100 mwcm-2
的模拟太阳光光源条件下对钙钛矿太阳能电池进行电流-电压测试,得到钙钛矿太阳能电池的j-v曲线如图5所示,计算其短路电流j
sc
=25.85ma*cm-2
、开路电压v
oc
=1.21v、填充因子ff=76.59%,光电转换效率pce=22.7%;对其稳定性测试结果如图6所示,可见随着时间的变化其转换效率仍然稳定在22%左右,这表明本实施例制备的钙钛矿太阳能电池中具有良好的光电转换效率和稳定性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1