一种17α-羟基黄体酮及其制备方法与流程
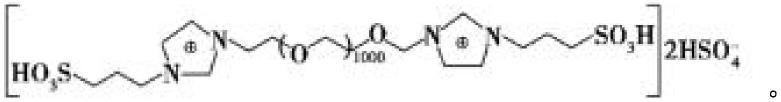
一种17
α-羟基黄体酮及其制备方法
技术领域
1.本发明涉及黄体酮制备技术领域,尤其涉及一种17α-羟基黄体酮及其制备方法。
背景技术:
2.17α-羟基黄体酮是合成激素类药物所需要的中间体。17α-羟基黄体酮是合成安宫黄体酮、泼尼松龙、倍他米松、地塞米松等众多甾体药物的一个关键中间体。
3.目前,17α-羟基黄体酮主要采用4-雄烯二酮进行制备。但是该方法存在所生产的17α-羟基黄体酮的质量不稳定,无法满足更高性能的应用的问题。且上述过程需要经过羟氰化、脱水、羧酮保护、氢化和加成水解等步骤,所述制备工艺繁杂,耗时长,且所需反应温度高,如中国专利cn103524588公开了一种黄体酮的制备方法,其所述制备工艺需要经过羟氰化、脱水、羧酮保护、氢化和加成水解等步骤,其所需的反应温度在100℃左右,反应耗时约30h,极大的降低了生产效率。因此,发展一种耗时短,能耗低,且收率高的17α-羟基黄体酮的制备方法成为本领域亟需。
技术实现要素:
4.有鉴于此,本发明提供了一种17α-羟基黄体酮及其制备方法,以解决现有的17α-羟基黄体酮的制备存在制备工艺繁杂,耗时长,且所需反应温度高的问题。
5.为了达到上述目的,本发明采用如下技术方案:
6.本发明提供了一种17α-羟基黄体酮的制备方法,包括如下步骤:
7.(1)将双降醇、乙二醇和催化剂混合,得到羰基被保护的双降醇;
8.(2)将羰基被保护的双降醇、酸性离子液体、杂多酸和氧化剂混合,反应得到烯酮中间体;
9.(3)将烯酮中间体、酸性离子液体和溶剂混合,反应得到黄体酮;
10.(4)将黄体酮、17α-羟化酶、辅酶和再生酶混合,羟化得到17α-羟基黄体酮。
11.作为优选,所述步骤(1)中,催化剂为盐酸或硫酸;双降醇和乙二醇的质量比为50~60:1~2;催化剂和乙二醇的质量比为0.3~0.6:1。
12.作为优选,所述酸性离子液体为聚乙二烯醇酸性离子液体;步骤(2)所述酸性离子液体的质量和步骤(3)所述酸性离子液体的质量独立的为双降醇质量的2~3%。
13.作为优选,所述步骤(2)中,杂多酸为磷钼杂多酸;氧化剂为双氧水或高氯酸;酸性离子液体、杂多酸和氧化剂的质量比为1:10~15:5~8。
14.作为优选,所述步骤(2)中,反应的温度为40~50℃,反应的时间为5~6h。
15.作为优选,所述步骤(3)中,溶剂为甲醇、异丙醇或正丁醇;酸性离子液体和溶剂的质量体积比为1g:50~80ml。
16.作为优选,所述步骤(3)中,反应的温度为50~60℃,反应的时间为2~4h。
17.作为优选,所述步骤(4)中,辅酶为核黄素或硫胺素;再生酶为甲酸脱氢酶、葡萄糖脱氢酶或氢化酶;17α-羟化酶的用量为黄体酮质量的10~20%;17α-羟化酶、辅酶和再生酶
的质量比为1:0.2~0.5:0.3~0.6。
18.作为优选,所述步骤(4)中,羟化的温度为20~30℃,羟化的时间为2~3h,羟化的ph值为6.8~7.2。
19.本发明还提供了所述17α-羟基黄体酮的制备方法制备得到的17α-羟基黄体酮。
20.经由上述的技术方案可知,与现有技术相比,本发明有益效果如下:
21.本发明通过化学与酶法结合制备得到17α-羟基黄体酮,所需反应时间短,反应所需温度低,降低了能耗;同时本发明所述原料简单易得,降低了反应成本;且本发明所得17α-羟基黄体酮的纯度和收率高。
具体实施方式
22.本发明提供了一种17α-羟基黄体酮的制备方法,包括如下步骤:
23.(1)将双降醇、乙二醇和催化剂混合,得到羰基被保护的双降醇;
24.(2)将羰基被保护的双降醇、酸性离子液体、杂多酸和氧化剂混合,反应得到烯酮中间体;
25.(3)将烯酮中间体、酸性离子液体和溶剂混合,反应得到黄体酮;
26.(4)将黄体酮、17α-羟化酶、辅酶和再生酶混合,羟化得到17α-羟基黄体酮。
27.在本发明中,所述步骤(1)中,催化剂优选为盐酸或硫酸,进一步优选为盐酸;盐酸的质量分数优选为45~50%,进一步优选为46~48%;硫酸的质量分数优选为40~60%,进一步优选为45~55%;双降醇和乙二醇的质量比优选为50~60:1~2,进一步优选为52~55:1.2~1.6;催化剂和乙二醇的质量比优选为0.3~0.6:1,进一步优选为0.4~0.5:1。
28.在本发明中,所述酸性离子液体优选为聚乙二烯醇酸性离子液体;步骤(2)所述酸性离子液体的质量和步骤(3)所述酸性离子液体的质量独立的优选为双降醇质量的2~3%,进一步优选为双降醇质量的2.5~2.8%;
29.所述聚乙二烯醇酸性离子液体的结构式如下:
[0030][0031]
在本发明中,所述步骤(1)中,得到羰基被保护的双降醇前,将混合所得产物进行减压蒸馏;减压蒸馏的压强优选为10~30kpa,进一步优选为15~25kpa;减压蒸馏的温度优选为60~100℃,进一步优选为75~85℃。
[0032]
在本发明中,所述步骤(1)的反应式如下:
[0033][0034]
在本发明中,所述步骤(2)中,杂多酸优选为磷钼杂多酸;氧化剂优选为双氧水或高氯酸;双氧水的浓度优选为30~40%,进一步优选为32~38%;高氯酸的浓度优选为50~
72%,进一步优选为60~70%;酸性离子液体、杂多酸和氧化剂的质量比优选为1:10~15:5~8,进一步优选为1:11~14:6~7。
[0035]
在本发明中,所述步骤(2)中,反应的温度优选为40~50℃,进一步优选为45~48℃,反应的时间优选为5~6h,进一步优选为5.5h。
[0036]
在本发明中,所述步骤(2)中,反应结束后,将所得产物顺次经过浓缩干燥和抽滤得到烯酮中间体;
[0037]
浓缩干燥的温度优选为70~100℃,进一步优选为80~90℃。
[0038]
在本发明中,所述步骤(2)的反应式如下:
[0039][0040]
在本发明中,所述步骤(3)中,溶剂优选为甲醇、异丙醇或正丁醇,进一步优选为甲醇或正丁醇;酸性离子液体和溶剂的质量体积比优选为1g:50~80ml,进一步优选为1g:60~70ml。
[0041]
在本发明中,所述步骤(3)中,反应的温度优选为50~60℃,进一步优选为55~58℃;反应的时间优选为2~4h,进一步优选为3~3.5h。
[0042]
在本发明中,所述步骤(3)的反应式如下:
[0043][0044]
在本发明中,所述步骤(3)中,反应结束后,将反应所得产物与硫酸混合,脱除保护基团,后冷却至室温,静置1~3h后抽滤得到黄体酮;
[0045]
所述反应所得产物与硫酸的质量体积比优选为1g:10~20ml,进一步优选为1g:12~15ml;硫酸的质量分数优选为40~60%,进一步优选为45~55%;混合的时间优选为10~30min,进一步优选为15~25min;静置的时间优选为1.5~2.5h,进一步优选为2h。
[0046]
在本发明中,所述步骤(4)中,辅酶优选为核黄素或硫胺素,进一步优选为核黄素;再生酶优选为甲酸脱氢酶、葡萄糖脱氢酶或氢化酶,进一步优选为葡萄糖脱氢酶;17α-羟化酶的用量优选为黄体酮质量的10~20%,进一步优选为黄体酮质量的12~18%;17α-羟化酶、辅酶和再生酶的质量比优选为1:0.2~0.5:0.3~0.6,进一步优选为1:0.3~0.4:0.4~0.5。
[0047]
在本发明中,所述步骤(4)中,羟化的温度优选为20~30℃,进一步优选为25~26
℃;羟化的时间优选为2~3h,进一步优选为2.5h;羟化的ph值优选为6.8~7.2,进一步优选为7。
[0048]
在本发明中,所述步骤(4)中,羟化结束后,将所得产物顺次用硫酸和水洗涤,然后干燥得到17α-羟基黄体酮;
[0049]
所述洗涤的次数优选为2~4次,进一步优选为3次;烘干的温度优选为70~90℃,进一步优选为75~85℃。
[0050]
本发明还提供了所述17α-羟基黄体酮的制备方法制备得到的17α-羟基黄体酮。
[0051]
下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
[0052]
实施例1
[0053]
(1)在烧杯中加入100g双降醇、2g乙二醇和0.6g硫酸(质量分数为45%)混合20min,然后在20kpa、80℃下减压蒸馏得到羰基被保护的双降醇;
[0054]
(2)在三口烧瓶中加入步骤(1)所得羰基被保护的双降醇、2g聚乙二烯醇酸性离子液体、20g磷钼杂多酸和11g双氧水(浓度为35%)混合,在搅拌的条件下,40℃反应5h,然后在80℃下浓缩干燥,后抽滤得到烯酮中间体;
[0055]
(3)在烧杯中加入步骤(2)所得烯酮中间体、2.1g聚乙二烯醇酸性离子液体和105ml甲醇混合,在50℃下反应2h,然后加入100ml硫酸(质量分数为40%)搅拌20min后冷却至室温,静置1h后抽滤得到黄体酮;
[0056]
(4)将步骤(3)所得6g黄体酮、1.2g17α-羟化酶、0.24g硫胺素和0.36g甲酸脱氢酶混合,在25℃、ph为7的条件下羟化2h,得到17α-羟基黄体酮。
[0057]
对本实施例所得17α-羟基黄体酮的收率和纯度进行检测并计算,得到本实施例所得17α-羟基黄体酮的收率为90%,纯度为98%。
[0058]
实施例2
[0059]
(1)在烧杯中加入110g双降醇、2.1g乙二醇和0.84g硫酸(质量分数为45%)混合20min,然后在22kpa、85℃下减压蒸馏得到羰基被保护的双降醇;
[0060]
(2)在三口烧瓶中加入步骤(1)所得羰基被保护的双降醇、2.2g聚乙二烯醇酸性离子液体、23g磷钼杂多酸和13.2g双氧水(浓度为35%)混合,在搅拌的条件下,45℃反应5h,然后在80℃下浓缩干燥,后抽滤得到烯酮中间体;
[0061]
(3)在烧杯中加入步骤(2)所得烯酮中间体、2.3g聚乙二烯醇酸性离子液体和115ml甲醇混合,在55℃下反应3h,然后加入105ml硫酸(质量分数为45%)搅拌20min后冷却至室温,静置1h后抽滤得到黄体酮;
[0062]
(4)将步骤(3)所得7.5g黄体酮、1.5g17α-羟化酶、0.6g硫胺素和0.6g甲酸脱氢酶混合,在25℃、ph为7的条件下羟化2.5h,得到17α-羟基黄体酮。
[0063]
对本实施例所得17α-羟基黄体酮的收率和纯度进行检测并计算,得到本实施例所得17α-羟基黄体酮的收率为90.2%,纯度为97.8%。
[0064]
实施例3
[0065]
(1)在烧杯中加入90g双降醇、1.5g乙二醇和0.9g硫酸(质量分数为45%)混合20min,然后在20kpa、80℃下减压蒸馏得到羰基被保护的双降醇;
[0066]
(2)在三口烧瓶中加入步骤(1)所得羰基被保护的双降醇、1.8g聚乙二烯醇酸性离
子液体、18g磷钼杂多酸和12.6g双氧水(浓度为35%)混合,在搅拌的条件下,48℃反应6h,然后在80℃下浓缩干燥,后抽滤得到烯酮中间体;
[0067]
(3)在烧杯中加入步骤(2)所得烯酮中间体、1.85g聚乙二烯醇酸性离子液体和90ml甲醇混合,在60℃下反应3h,然后加入98ml硫酸(质量分数为45%)搅拌20min后冷却至室温,静置1h后抽滤得到黄体酮;
[0068]
(4)将步骤(3)所得5.5g黄体酮、1.1g17α-羟化酶、0.22g硫胺素和0.44g甲酸脱氢酶混合,在25℃、ph为7的条件下羟化3h,得到17α-羟基黄体酮。
[0069]
对本实施例所得17α-羟基黄体酮的收率和纯度进行检测并计算,得到本实施例所得17α-羟基黄体酮的收率为91.2%,纯度为97.5%。
[0070]
由实施例1~3可知,本发明通过化学-酶法合成17α-羟基黄体酮,简化了工艺步骤,减少了反应温度和时间,降低了反应能耗。同时,最终得到的17α-羟基黄体酮的纯度和产率得以提高,本发明所得17α-羟基黄体酮的纯度在97.5%以上,收率达到了90%以上。
[0071]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1