一种靶向TSPO受体的PET显像剂的制备方法及应用
一种靶向tspo受体的pet显像剂的制备方法及应用
技术领域
1.本发明涉及一种靶向tspo受体的pet显像剂的制备方法及应用,属于放射性药物化学技术领域。
背景技术:
2.正电子发射断层显像(positron emission computerized tomography,pet)作为医学影像的重要手段,可以在细胞和分子层面上反映疾病情况。
18
f-fdg pet已成功应用于肿瘤学、神经学和心脏血管等领域。然而,
18
f-fdg作为非特异性显像剂,炎症显像往往会产生假阳性结果。此外,心脏和大脑中的较高的
18
f-fdg显像剂积累,使这些器官或组织附近的炎性病灶检测困难,影响检测的灵敏度和特异性。巨噬细胞是固有免疫的重要组成细胞,可在局部炎性环境中活化成“m1”型或“m2”型巨噬细胞,其中“m1”型巨噬细胞发挥促进炎症和抑制细胞增殖的作用,而“m2”型巨噬细胞发挥抗炎、促进细胞增殖和组织修复的作用。近年来,多项研究表明活化的巨噬细胞与某些心血管疾病、神经系统疾病、自身免疫性疾病以及肿瘤的发生发展密切相关。因此,对活化巨噬细胞进行靶向显像有助于多种疾病的早期诊断和靶向治疗。
3.相对分子质量为18kd的转位蛋白(translocator protein,tspo),又称外周苯二氮受体(peripheral benzodiazepine receptor,pbr),主要分布于线粒体外膜,在巨噬细胞、单核细胞、活化的小胶质细胞和星形细胞上高表达。
4.tspo显像剂可用于多种疾病研究。在神经系统疾病方面,colasanti等人通过对11名多发性硬化(multiple sclerosis,ms)患者和11名正常人进行
11
c-pbr111 pet扫描,发现
11
c-pbr111在ms患者脑白质病灶的摄取较正常人高,且病灶的显像剂摄取与ms严重程度成正相关,说明
11
c-pbr111 pet显像可定量评估ms患者脑白质的炎症情况并指导临床用药。guly
á
s等人利用
11
c-vinpocetine pet观察9名脑卒中患者脑中tspo变化,发现在脑卒中后一周,缺血核心和梗死灶周围区域的放射性摄取增加,且随脑卒中后时间的延长,上述区域放射性摄取程度稳定下降,表明脑卒中后小胶质细胞的活化具有时间依赖性,因此
11
c-vinpocetine pet具有观察脑卒中患者小胶质细胞活化区域和评估脑卒中病情的潜力。
5.james等人发现,
18
f-ge180 pet评价了阿尔茨海默病(alzheimer's disease,ad)治疗药物lm11a-31在ad模型小鼠中调控小胶质细胞的活化情况,说明
18
f-ge180在监测ad小鼠神经炎症和评价小胶质细胞的活化情况方面具有一定的敏感性。zinnhardt等人利用小鼠神经胶质瘤模型,证明了
18
f-dpa-714 pet/ct可反映神经胶质瘤不同阶段的炎性微环境,为临床诊疗提供信息。然而,由于tspo成像不能区分肿瘤细胞与肿瘤周围炎性细胞的表达,因此其在脑肿瘤中的临床应用有限。在外周炎症性疾病方面,gaemperli等人对9名有症状和27名无症状颈动脉狭窄的患者进行
11
c-pk11195 pet/ct扫描,通过免疫荧光病理结果证明
11
c-pk11195 pet/ct可以通过对活化的巨噬细胞显像,区分有症状和无症状动脉粥样斑块。hatori等人和xie等人也通过建立相应疾病鼠模型,证实
18
f-fedac pet/ct可用于肝纤维化疾病的动态监测及非酒精性脂肪肝的定量检测和分期。
6.第一代tspo显像剂
11
c-pk11195的合成,使得以tspo为靶点的正电子显像剂成为小胶质细胞活化的替代标志物。
11
c-pk11195显像剂被用于多种神经炎性疾病的临床前和临床研究,但由于
11
c-pk11195的低脑渗透性、高非特异性和
11
c半衰期较短,以
18
f-fedaa1106,
18
f-pbr28,
18
f-dpa714为代表的第二代tspo特异性显像剂应运而生。第二代tspo显像剂,虽然在受体特异性和图像信噪比方面较前有所提高,但由于tspo基因外显子4(rs6971)的多态性导致丙氨酸-苏氨酸替代(a147t),使tspo分为高亲和力(ala/ala)、混合亲和力(ala/thr)和低亲和力(thr/thr)3种结合类型。不同显像剂对不同tspo结合类型的差异,使对第二代tspo显像剂定量分析和比较图像存在困难。且有研究发现,部分第二代tspo显像剂在对thr/thr型tspo的病人进行显像时,显像剂的特异性结合难以与非特异性结合区分,因此限制了第二代tspo显像剂的临床应用。
7.11
c-er176作为第三代显像剂,具有比第一、二代更好的特异性和信噪比,且未观察到明显的rs6971的多态性依赖,可更好地反映tspo表达和小胶质细胞活化情况,所以其临床应用价值亟需大量实验验证。但是c-11半衰期仅有20.3min,如果能用半衰期较长的f-18(110min)代替c-11对其进行放射性标记,而又不影响该药物的性质,对于该药物在临床上的推广应用将具有十分重要的意义。
技术实现要素:
8.本发明的目的是:针对现有的靶向tspo受体的显像剂存在的问题与缺陷,提出并制备一种
18
f标记的靶向tspo受体的pet显像剂
18
f-tfqc,其放射性化学纯度高,具有良好的生物稳定性,有足够长的半衰期,在体内聚集时间较短,能够快速排出体内,能够有效识别靶向tspo受体的炎症病灶。
9.为了实现上述目的,本发明公开了一种靶向tspo受体的pet显像剂
18
f-tfqc,该pet显像剂
18
f-tfqc的放射性化学纯度》99%,其化学结构式为:
[0010][0011]
优选地,所述的pet显像剂
18
f-tfqc是由如下所示的前体化合物br-cf
2-qc进行放射性核素f-18标记后得到:
[0012][0013]
本发明还提供了一种用于合成权利要求1所述的pet显像剂
18
f-tfqc的前体化合物
br-cf
2-qc,其化学结构式为:
[0014][0015]
本发明还提供了上述的前体化合物br-cf
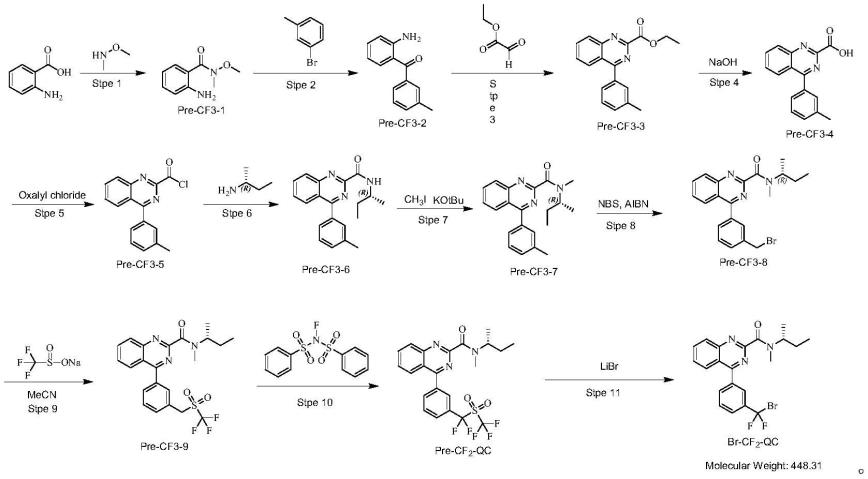
2-qc的制备方法,通过如下所示的化学合成路线进行制备:
[0016][0017]
本发明还提供了上述的靶向tspo受体的pet显像剂
18
f-tfqc在制备炎症的诊断试剂或试剂盒中的应用,可用于pet/ct或pet/mr显像。
[0018]
优选地,包括用于制备脑神经炎症的诊断试剂或试剂盒。
[0019]
与现有技术相比,本发明的有益效果在于:
[0020]
(1)本发明首次通过前体化合物br-cf
2-qc进行放射性核素f-18标记后合成了
18
f-tfqc,
18
f-tfqc的放射性化学纯度大于99%,本发明的制备方法简单快捷,该制备方法的放射化学产率约为(11.90
±
1.40)%(衰减校正后);
[0021]
(2)进一步地,本发明还设计了前体化合物br-cf
2-qc的化学合成路线,简单快捷,易纯化;
[0022]
(3)本发明所述的正电子显像剂
18
f-tfqc能够作为靶向炎症的pet显像探针,由于其穿透血脑屏障的效果较好,
18
f-tfqc有望成为脑神经炎症的pet候选显像探针,本发明的
18
f-tfqc显像剂对靶向tspo受体的炎症诊断筛选、预测预后和疗效监测方面具有重要的临床价值。
附图说明
[0023]
图1为本发明的pet探针
18
f-tfqc的化学结构式;
[0024]
图2为pet探针
18
f-tfqc在正常小鼠体内各脏器和组织中的生物分布图;
[0025]
图3为pet探针
18
f-tfqc在大鼠体内的活体显像图。
具体实施方式
[0026]
为使本发明更明显易懂,兹以优选实施例,并配合附图作详细说明如下。
[0027]
实施例1
[0028]
前体br-cf
2-qc的合成:
[0029][0030]
步骤1:n2保护下,于500ml的三口烧瓶中加入邻氨基苯甲酸(13.714g,100mmol),无水thf(160ml),冷却到0℃,加入n,n'-羰基二咪唑(16.215g,100mmol),反应液恢复到室温,搅拌2h,加入二甲羟胺盐酸盐(97.54g,100mmol),三乙胺(10.12g,100mmol)和thf(80ml)溶液,反应过夜,lc-ms检测原料反应完全。反应液加入h2o(200ml),加入ea(150ml
×
3)萃取三次,收集有机相,加入无水硫酸钠干燥,过滤,浓缩,柱层析(pe:ea=1:1),得产品pre-cf3-1(14.4g),产率:80%。
[0031]
步骤2:n2保护下,于500ml的三口烧瓶中加入间溴甲苯(13.3g,77.7mmol),再加入thf(100ml),冷却至-78℃,缓慢滴加正丁基锂(77.7ml,155.4mmol),保温搅拌1h,缓慢滴加pre-cf3-1(14.0g,77.7mmol)和thf溶液(100ml)在-78℃,约30min滴加完毕。恢复至室温搅拌过夜。lc-ms检测原料反应完全。倒入饱和氯化铵溶液,加入ea(150ml
×
3)萃取三次,收集有机相干燥、浓缩,柱层析(pe:ea=50:1)得产品pre-cf3-2:7.3g,产率:44.5%。
[0032]
步骤3:向250ml反应瓶中依次加入pre-cf3-2、乙醛酸乙酯、醋酸铵、无水乙醇和h2o。室温搅拌72h,lc-ms检测大部分原料反应完全。浓缩部分无水乙醇,加入ea(50ml
×
3)萃取三次,收集有机相干燥、浓缩,柱层析(pe:ea=5:95),得产品pre-cf3-3:3.6g,产率:37.5%。
[0033]
步骤4:向100ml的三口烧瓶中加入pre-cf3-3(3.5g,12.0mmol)、naoh(0.96g,24.0mmol)和无水乙醇(40ml),室温搅拌过夜。tlc监测原料反应完全,浓缩去乙醇,加入盐酸(1n,20ml),调成ph=1,加入ea(40ml
×
3)萃取三次,收集有机相,减压浓缩至干,得产品pre-cf3-4:2.5g,产率:80.5%。
[0034]
步骤5:n2保护下,向100ml三口烧瓶中,依次加入pre-cf3-4(2.3g,8.7mmol),再加入草酰氯(2.2g,17.4mmol)和dcm(25ml),滴加少量dmf,室温搅拌过夜,tlc点板原料反应完全,浓缩至干,再用油泵拉干,得粗品pre-cf3-5:1.82g,产率:74.2%。
[0035]
步骤6:n2保护下,向100ml三口烧瓶中,依次加入pre-cf3-5(1.8g,6.4mmol),再加入n-甲基-2-丁胺(0.47g,6.4mmol)、三乙胺(1.94g,19.2mmol)和dcm(20ml),室温搅拌2h,tlc监测原料反应完全。柱层析分离,得产品pre-cf3-6:1.75g,产率:85.6%。
[0036]
步骤7:n2保护下,向100ml三口烧瓶中,依次加入pre-cf3-6(1.7g,5.3mmol),再加入thf(20ml),冷却至0℃,加入kotbu(1.8g,15.9mmol),保持0℃搅拌1h,缓慢加入ch3i(0.91g,6.4mmol),加料完毕后恢复至室温搅拌16h,lc监测原料反应完全。反应液倒入饱和氯化铵溶液(25ml)里,加入ea(25mlx3)萃取三次,收集有机相,柱层析,得产品:1.14g,产率:64.5%。
[0037]
步骤8:n2保护,向50ml三口烧瓶中,依次加入pre-cf3-7(1.1g,3.3mmol)、nbs(0.71g,3.9mmol)、aibn(0.16g,0.99mmol)和dce(15ml),升温至80℃,反应16h,lc-ms检测有产品生成,不用后处理,浓缩至干,投下一步。得产品pre-cf3-8:0.72g,产率:53.2%。
[0038]
步骤9:n2保护下,向50ml三口烧瓶中,依次加入pre-cf3-8(0.7g,1.7mmol)、三氟代甲烷亚磺酸钠(0.27g,1.7mmol)和acn(乙腈,15ml),升温至80℃,反应16h,lc-ms检测原料反应完全,冷却到室温,浓缩,柱层析,pe:ea=2:1,得产品pre-cf3-9:0.67g,产率:85.3%。
[0039]
步骤10:n2保护下,向50ml三口烧瓶中,依次加入pre-cf3-9(0.6g,1.3mmol)、nfsi(n-氟代双苯磺酰胺,0.83g,2.65mmol)、k3po4(0.83g,3.9mmol)和dmf(15ml),室温搅拌反应16h,lc-ms检测原料反应完全,加入饱和氯化铵溶液(15ml),搅拌30分钟,加入ea(20ml
×
3)萃取三次,柱层析,pe:ea=2:1,得产品pre-cf
2-qc:0.23g,产率:35.4%。
[0040]
步骤11:n2保护下,向50ml三口烧瓶中,依次加入pre-tfqc(pre-cf
2-qc)、libr和mecn,加热至80℃,搅拌反应16hrs,lc-ms检测原料反应完全,浓缩,加入ea和饱和食盐水,分液,柱层析分离(hex:ea=1:1),得到前体化合物br-cf
2-qc 140mg。
[0041]
实施例2
[0042]
目标化合物pet探针
18
f-tfqc的合成:
[0043][0044]
18
f-通过日本住友hm-20de加速器生产得到,具体标记实验在日本住友f-18多功能合成模块(f18-multi-p)上进行,具体步骤包括:用10ml 1m k2co3和60ml去离子水活化好的qma柱捕获加速器轰击出的
18
f-,然后用20mg teab溶于0.5ml去离子水和0.5ml乙腈的混合溶液将qma柱上的
18
f-洗脱入反应瓶,分别以120℃、100℃干燥两次,再向反应瓶中加入1ml无水乙腈溶解的5mg前体br-cf
2-qc,110℃反应20min。反应结束后冷却至室温,经制备
radio-hplc(柱子:agilent c18,5μm,9.4
×
250mm;流动相:6.0/4.0乙腈/水(含0.1% tfa);流速:3ml/min)分离得到
18
f-tfqc。用活度剂测量终产物活度,经衰变校正至反应结束,计算所得
18
f-tfqc的放射化学产率约(11.90
±
1.40)%(衰减校正后)。经质控产物放化纯度大于99%。
[0045]
应用实施例1
[0046]
本发明pet探针
18
f-tfqc的体外稳定性实验:
[0047]
以实施例2所得的
18
f-tfqc约1mci分别置于100μl 0.9%生理盐水中,充分混匀后37℃下存放。分别在0.5h、1h、3h、6h取样,在分析型hplc上检验其纯度变化。hplc结果表明此pet探针6h后纯度与标记刚完成结果相同,说明分子探针非常稳定,几乎没有分解。
[0048]
应用实施例2
[0049]
本发明pet探针
18
f-tfqc的生物分布实验:
[0050]
以实施例2所得的
18
f-tfqc约100μci/只经静脉注射进8周龄雄性icr小鼠21只,分别在15min、30min、1h、1.5h、2h、3h和4h时各处死3只icr小鼠,收集包括血、心、肝、脾、肺、肾、胃、小肠、骨、肌肉和脑组织进行称量及放射性计数。进行衰变校正后,将各个组织样品的计数与标准计数比较,结果表示为%id/g(每克样品组织的放射性占注射剂量的百分含量),即为各个脏器对
18
f-tfqc的相对吸收值,生物学分布显示
18
f-tfqc经血液循环迅速分布全身各处,主要浓聚于肺部,其次是心、脾、肾,其余组织和器官聚集较少,4h后大部分能够排泄,如图2所示。
[0051]
应用实施例3
[0052]
本发明pet探针
18
f-tfqc的活体显像试验:
[0053]
以实施例2所得的
18
f-tfqc约1mci/只经尾静脉分别注射入癫痫模型sd大鼠(实验组)及正常sd大鼠(对照组)。
[0054]
结果如图3所示,在正常sd大鼠(对照组)大脑海马区未见明显显像剂摄取,在癫痫模型sd大鼠(实验组)大脑右侧海马区可见明显显像剂浓聚。
[0055]
该显像结果说明
18
f-tfqc作为靶向tspo受体的pet显像剂,能够有效识别癫痫病灶。
[0056]
上述实施例仅为本发明的优选实施例,并非对本发明任何形式上和实质上的限制,应当指出,对于本技术领域的普通技术人员,在不脱离本发明的前提下,还将可以做出若干改进和补充,这些改进和补充也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1