一种受阻自由基对引发的含氟化合物及其制备方法和应用
1.本发明涉及有机合成技术领域,尤其涉及一种受阻自由基对引发的含氟化合物及其制备方法和应用。
背景技术:
2.将全氟烷基或其他卤素基团引入有机骨架的策略,在药物合成、材料制备领域具有重要的意义。该过程可以赋予底物材料抗菌、高渗透性和代谢稳定性等有益特性。氟代烷基碘是一种易于获得的化学原料,其毒性低,对多种官能团具有很好的耐受性。目前,将全氟碘代烷基基团引入化合物中常用的方法分为以下三种:1.通过向反应体系中加入过量碱或将强极性溶剂作为体系的反应溶剂:强碱可以与全氟碘代烷烃发生单电子转移过程(set),导致碘基团的离去和全氟烷基自由基的生成,生成的烷基自由基与烯烃底物完成后续的加成反应得到氟烷基化产物;2.过渡金属光催化剂催化:过渡金属光催化剂在光的照射下通过电子跃迁变为激发态,激发态的光催化剂很容易与底物的碘基团结合并使之离去,碘离去后同样会生成上述的全氟烷基自由基,后续完成原子转移自由基加成(atra)反应;3.自由基引发剂引发:在自由基引发剂的引发条件下(通常为加热或光照),碘和全氟烷基之间的c-i键发生均裂生成全氟烷基自由基,进而加成底物的双键位点。
3.目前,上述方法1需要加入过量添加剂,例如强碱和碱性盐,或者在强极性溶剂中进行反应,对官能团的耐受有限;方法2需加入过渡金属,过渡金属价格高且容易残留在体系中不易除去,使得应用受限;方法3可用的卤代试剂和烯烃底物的种类十分有限。因此,发展优越的自由基引发剂方法,解决适用卤代烃的种类和底物的种类有限的问题至关重要。
技术实现要素:
4.本发明的目的在于提供一种受阻自由基对引发的含氟化合物及其制备方法和应用,所述方法适用卤代烃底物范围广。
5.为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了一种受阻自由基对引发的含氟化合物的制备方法,包括以下步骤:
7.将烯烃底物、卤代试剂、路易斯酸催化剂、路易斯碱催化剂和有机溶剂混合,在蓝光光源条件下进行加成反应,得到含氟化合物;
8.所述烯烃底物包括烷基端烯烃、烷基内烯烃或芳基烯烃。
9.优选的,所述烷基端烯烃包括:
[0010][0011]
优选的,所述烷基内烯烃包括:
[0012][0013]
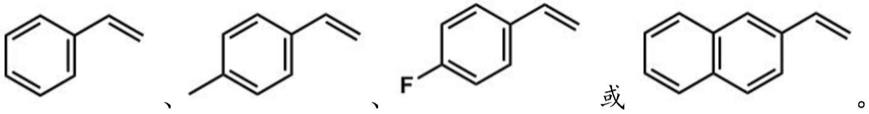
所述芳基烯烃包括:
[0014][0015]
优选的,所述卤代试剂包括:
[0016][0016]
cbr4或chbr3。
[0017]
优选的,所述路易斯碱催化剂包括n,n-二甲基苯胺或n,n-二乙基苯胺;所述路易斯酸催化剂为三(五氟苯基)硼。
[0018]
优选的,所述路易斯酸催化剂和路易斯碱催化剂的摩尔比为(0.1~0.3):(0.1~0.3)。
[0019]
优选的,所述路易斯酸催化剂、卤代试剂和烯烃底物的摩尔比为(0.1~0.3):(1~3):1。
[0020]
优选的,所述加成反应的温度为室温,时间为1~24h;所述加成反应所用光源为led灯,所述led灯的功率为5~80w,波长为400~460nm。
[0021]
本发明提供了上述技术方案所述含氟化合物在制备抗菌药物、表面活性剂或耐热材料中的应用。
[0022]
本发明提供了一种受阻自由基对引发的含氟化合物的制备方法,包括以下步骤:将烯烃底物、卤代试剂、路易斯酸催化剂、路易斯碱催化剂和有机溶剂混合,在蓝光光源条件下进行加成反应,得到含氟化合物;所述烯烃底物包括烷基端烯烃、烷基内烯烃或芳基烯烃。本发明将路易斯酸和路易斯碱混合使用作为温和高效的引发剂,路易斯酸用于单电子氧化路易斯碱,路易斯碱会向路易斯酸转移一个电子,分别生成路易斯酸自由基阴离子和路易斯碱自由基阳离子,这两个自由基离子组成“受阻自由基对”,而生成的路易斯碱自由基阳离子可以结合卤代试剂中的卤元素,引发卤代试剂中碳-卤键的均裂,均裂后生成的自由基可以对烯烃底物的双键位点发生加成,得到含氟化合物。
[0023]
本发明的催化剂、原料易得,操作方便,反应条件温和,路易斯酸易于合成,路易斯碱催化剂、卤化试剂和烯烃底物均为市售。路易斯酸碱之间的电子转移条件温和且高效,反应在室温条件下光照数小时(3h)即可完成,关键过程在于催化剂路易斯酸和碱之间高效的单电子转移作用,其次是生成的路易斯碱阳离子自由基可以很容易地结合原料卤化物中的卤素原子。
[0024]
本发明方法适用的卤代烃底物范围广:路易斯碱具有较强的亲核性,路易斯碱与路易斯酸发生单电子转移后,生成的α位碳原子中心自由基为二级自由基,亲核性相比于二甲基苯胺α位碳原子自由基更强,其可以活化较为惰性的溴,因而不仅可以完成碳-碘键的活化,还可以实现碳-溴键的活化,扩展了卤代化合物的范围。
[0025]
本发明方法实现了100%的原子效率:本发明所述加成反应为原子转移自由基加成过程(atra),卤代试剂均裂后生成的卤素和烷基(或芳基)分别加成在双键的两个碳上,
没有其他副产物的生成,是一种100%原子效率、快速的反应过程。路易斯碱向路易斯酸(三五氟苯基硼)转移一个电子后,生成的苯胺自由基阳离子的亲核性足以活化多种卤代试剂,仅需加入催化剂量的路易斯酸碱即可引发加成反应。
具体实施方式
[0026]
本发明提供了本发明提供了一种受阻自由基对引发的含氟化合物的制备方法,包括以下步骤:
[0027]
将烯烃底物、卤代试剂、路易斯酸催化剂、路易斯碱催化剂和有机溶剂混合,在蓝光光源条件下进行加成反应,得到含氟化合物;
[0028]
所述烯烃底物包括烷基端烯烃、烷基内烯烃或芳基烯烃。
[0029]
在本发明中,若无特殊说明,所需制备原料或试剂均为本领域技术人员熟知的市售商品。
[0030]
在本发明中,所述烯烃底物包括烷基端烯烃、烷基内烯烃或芳基烯烃;
[0031]
所述烷基端烯烃优选包括:
[0032][0033]
在本发明中,所述烷基内烯烃优选包括:
[0034][0035]
在本发明中,所述芳基烯烃优选包括:
[0036][0037]
在本发明中,所述卤代试剂优选包括:
[0038]038]
cbr4或chbr3。
[0039]
在本发明中,所述路易斯碱催化剂优选包括n,n-二甲基苯胺或n,n-二乙基苯胺;本发明限定特定种类的路易斯碱催化剂,所用苯胺类路易斯碱与路易斯酸之间的氧化还原电势相近,单电子转移效率更高。
[0040][0041]
在本发明中,所述路易斯酸催化剂优选为三(五氟苯基)硼(b(c6f5)3),结构式为:
[0042][0043]
在本发明中,所述三五氟苯基硼b(c6f5)3的制备方法优选为:将溴五氟苯(66.69g,0.27mol)和600ml无水己烷溶剂置于1000ml史莱克瓶中,在氮气保护、-78℃条件下,向其中滴加正丁基锂的己烷溶液(2.5m,10.8ml,0.27mol),20min完成滴加,将所得混合液在该温度下搅拌40min后,快速加入三氯化硼的己烷溶液(210.9g,50%(w/w),0.09mol),将所得混合液在-78℃条件下搅拌10min后,缓慢恢复至室温搅拌1h,反应结束后在真空条件下移去溶剂,将剩余固体在氮气保护下转移至升华器中,110℃升华得到产物三五氟苯基硼,为白
色晶体,产物质量39.2g,产率85%。
[0044]
在本发明中,所述路易斯酸催化剂和路易斯碱催化剂的摩尔比优选为(0.1~0.3):(0.1~0.3),更优选为1:1;所述路易斯酸催化剂、卤代试剂和烯烃底物的摩尔比优选为(0.1~0.3):(1~3):1,更优选为(0.2~0.3):(1.2~3):1。
[0045]
在本发明中,所述有机溶剂优选为氘代氯仿(cdcl3),本发明所用有机溶剂氘代氯仿对于反应中的所有催化剂、原料都具有很好的溶解性,此外氘代氯仿的极性适中,不会与自由基中间体发生络合而降低自由基的反应活性,有助于c-x键断裂。本发明对所述有机溶剂的用量没有特殊的限定,保证反应顺利进行即可。
[0046]
本发明对所述烯烃底物、卤代试剂、路易斯酸催化剂、路易斯碱催化剂和有机溶剂混合没有特殊的限定,按照本领域熟知的过程将物料混合均匀即可。
[0047]
在本发明的实施例中,为了核磁定量分析中计算产率,所述混合还包括加入内标物均三甲苯;所述内标物与烯烃底物的摩尔比优选为1:1;计算方法如下:内标均三甲苯的所有甲基峰积分记为9时,产物中氢的位置积分除以该位点氢的个数,乘以100%,即为产率。
[0048]
在本发明中,所述加成反应在蓝光光源条件下进行;所述加成反应的温度优选为室温,时间优选为1~24h,更优选为3h;所述加成反应所用光源为led灯,所述led灯的功率为5~80w,更优选为40w;波长优选为400~460nm;所述加成反应优选在氩气环境中进行。本发明利用光源发出的光为反应体系提供激发能量,使得路易斯酸和路易斯碱之间的单电子转移发生。
[0049]
完成所述加成反应后,本发明优选将所得产物进行硅胶柱色谱纯化,得到含氟化合物;所述硅胶柱色谱纯化所用洗脱剂优选为己烷和乙酸乙酯混合溶剂,所述己烷与乙酸乙酯的体积比优选为20:1~10:1。
[0050]
本发明提供了上述技术方案所述含氟化合物在制备抗菌药物、表面活性剂或耐热材料中的应用。本发明对所述应用的方法没有特殊的限定,按照本领域熟知的方法应用即可。
[0051]
下面将结合本发明中的实施例,对本发明中的技术方案进行清楚、完整地描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0052]
以下实施例中,所用三五氟苯基硼b(c6f5)3的制备方法为:将溴五氟苯(66.69g,0.27mol)和600ml无水己烷溶剂置于1000ml史莱克瓶中,在氮气保护、-78℃条件下,向其中滴加正丁基锂的己烷溶液(2.5m,10.8ml,0.27mol),20min完成滴加,将所得混合液在该温度下搅拌40min后,快速加入三氯化硼的己烷溶液(210.9g,50%(w/w),0.09mol),将所得混合液在-78℃条件下搅拌10min后,缓慢恢复至室温搅拌1h,反应结束后在真空条件下移去溶剂,将剩余固体在氮气保护下转移至升华器中,110℃升华,得到产物三五氟苯基硼,为白色晶体,产物质量39.2g,产率85%。
[0053]
实施例1
[0054]
(4,4,5,5,6,6,7,7,7-九氟-2-碘庚基)苯c
13h10
f9i(3aa)的制备:
[0055]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,
0.02mmol),溶剂cdcl3(500μl),催化剂n,n-二甲基苯胺(phnme2,2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃烯丙基苯(11.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol);将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h;反应结束后,将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3aa,产率98%。
[0056]1h nmr(500mhz,cdcl3)δ7.35(dq,j=14.4,7.1hz,3h,h
ar
),7.23(d,j=6.8hz,2h,h
ar
),4.49(dq,j=8.8,6.3hz,1h,chi),3.33(dd,j=14.6,5.7hz,1h,ch2rf),3.23(dd,j=14.6,8.9hz,1h,ch2rf),2.92(tp,j=24.4,8.1hz,2h,phch2).
19
f nmr(471mhz,cdcl3)δ-80.45
‑‑
81.52(m,3f,cf3),-112.21(ddq,j=269.9,24.6,11.9,11.4hz,1f,ch2cf2),-113.19
–‑
114.65(m,1f,ch2cf2),-124.56(q,j=9.0hz,2f,cf2),-125.89(ddt,j=19.9,13.2,6.6hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ138.55,128.95,128.64,127.35,47.04,40.73(t,j=20.8hz),19.24.hrms(esi):calculated for c
13h10
f9[m-i]:377.0633,found:377.0648.结构式如下:
[0057][0058]
实施例2
[0059]
1-甲氧基-4-(4,4,5,5,6,6,7,7,7-九氟-2-碘庚基)苯c
14h10
f9io(3ba)的制备:
[0060]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃1-烯丙基-4-甲氧基苯(14.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol);将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h;反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ba,产率96%。
[0061]1h nmr(500mhz,cdcl3)δ7.14(d,j=8.7hz,2h,h
ar
),6.90(d,j=8.6hz,2h,h
ar
),4.45(dq,j=8.6,6.4hz,1h,chi),3.84(s,3h,och3),3.31
–
3.12(m,2h,ch2rf),3.01
–
2.77(m,2h,arch2).
19
f nmr(471mhz,cdcl3)δ-81.02(t,j=9.9hz,3f,cf3),-112.27(ddq,j=269.8,25.7,13.5,12.6hz,1f,ch2cf2),-113.94(ddq,j=270.9,26.1,13.4,12.6hz,1f,ch2cf2),-124.54(q,j=9.2hz,2f,cf2),-125.89(tq,j=11.3,6.4,5.8hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ158.81,130.64,130.03,113.98,55.23,46.23,40.50,20.12.结构式如下:
[0062][0063]
实施例3
[0064]
(5,5,6,6,7,7,7,8,8-九氟-3-碘辛基)苯c
14h12
f9i(3ca)的制备:
[0065]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷
(41.4mg,0.12mmol),烯烃丁-3-烯-1-基苯(13.2mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h;反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ca,产率94%。
[0066]1h nmr(500mhz,cdcl3)δ7.33(t,j=7.6hz,2h,h
ar
),7.26(d,j=7.1hz,3h,h
ar
),4.37
–
4.23(m,1h,chi),3.11
–
2.68(m,4h,ch2r
f and phch2),2.26
–
2.05(m,2h,ch2).
19
f nmr(471mhz,cdcl3)δ-81.02(t,j=9.4hz,3f,cf3),-111.62(ddt,j=270.6,44.0,12.1hz,1f,ch2cf2),-114.03
–‑
115.46(m,1f,ch2cf2),-124.12
–‑
124.97(m,2f,cf2),-125.88(dtd,j=25.9,13.2,12.2,4.6hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ139.86,128.61,128.48,126.39,53.41,41.79,35.69,19.99.结构式如下:
[0067][0068]
实施例4
[0069]
1,2,3,4,5-五氟-6-(3,3,4,4,5,5,6,6,-九氟-1-碘己基)苯c
13
h5f
14
i(3da)的制备:
[0070]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃1-烯丙基-2,3,4,5,6-五氟苯(20.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3da,产率90%。
[0071]1h nmr(500mhz,cdcl3)δ4.53(ddt,j=10.2,8.1,5.0hz,1h,chi),3.52
–
3.26(m,2h,arch2),3.21
–
2.75(m,2h,ch2rf).
19
f nmr(471mhz,cdcl3)δ-81.01(t,j=9.7hz,3f,cf3),-110.05
–‑
112.20(m,1f,ch2cf2),-112.85
–‑
116.20(m,1f,ch2cf2),-124.43(tt,j=12.6,6.7hz,2f,cf2),-125.88(dtd,j=18.2,12.8,12.4,4.5hz,2f,cf2),-142.16(dd,j=22.0,8.1hz,2f,f
ar
),-154.40(t,j=20.8hz,1f,f
ar
),-161.54(td,j=21.6,7.8hz,2f,f
ar
).
13
c nmr(126mhz,cdcl3)δ41.81,33.78,14.42.结构式如下:
[0072][0073]
实施例5
[0074]
(4r)-1-甲基-4-(4,4,5,5,6,6,7,7-九氟-2-碘庚基)环己烷-1-烯c
14h16
f9i(3ea)的制备:
[0075]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃r-柠檬烯(13.2mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ea,产率98%。
[0076]1h nmr(500mhz,cdcl3)δ5.40(s,1h,chi),3.39
–
2.95(m,2h,ch2rf),2.30(s,1h,c=ch),2.22(s,3h,ch3),2.18
–
1.90(m,4h,ch2),1.71(s,3h,ch3),1.51
–
1.33(m,2h,ch2),0.67(dt,j=60.9,10.7hz,1h,ch).
19
f nmr(471mhz,cdcl3)δ-81.03(t,j=10.0hz,3f,cf3),-109.08
–‑
112.78(m,2f,ch2cf2),-124.30(ddd,j=40.6,21.6,8.8hz,2f,cf2),-125.67(ddp,j=20.1,13.5,6.3,5.9hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ46.46,45.43,45.14
–
44.75(m),34.64,34.16,31.15,30.48,30.04,29.15,23.18.结构式如下:
[0077][0078]
实施例6
[0079]
(3,3,4,4,5,5,6,6-九氟-1-碘己基)环己烷c
12h14
f9i(3fa)的制备:
[0080]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃乙烯基环己烷(11.0mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3fa,产率98%。
[0081]1h nmr(500mhz,cdcl3)δ4.38(td,j=6.7,3.0hz,1h,chi),3.06
–
2.68(m,2h,ch2rf),2.04
–
1.61(m,5h,ch2),1.51
–
1.06(m,5h,ch2),0.86(tt,j=11.1,3.2hz,1h,ch).
19
f nmr(471mhz,cdcl3)δ-80.24
–‑
81.93(m,3f,cf3),-112.88(ddq,j=270.0,27.1,14.1,13.1hz,1f,ch2cf2),-114.92(ddq,j=271.6,28.4,14.6,12.9hz,1f,ch2cf2),-124.51(q,j=11.2,9.2hz,2f,cf2),-125.88(dd,j=14.6,9.1hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ44.18,38.98(t,j=20.9hz),33.70,30.27,29.72,26.02,25.75,25.53.hrms(esi):calculated for c
12h14
f9[m-i]:329.0946,found:329.0921.结构式如下:
[0082]
[0083]
实施例7
[0084]
(1,1,2,2,3,3,4,4,-九氟-6-碘十一烷c
11h14
f9i(3ga)的制备:
[0085]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃1-庚烯(9.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ga,产率98%。
[0086]1h nmr(500mhz,cdcl3)δ4.45
–
4.27(m,1h,chi),3.09
–
2.66(m,2h,ch2rf),1.82(dtt,j=28.2,9.7,5.0hz,2h,ch2chi),1.67
–
1.15(m,6h,ch2),0.94(t,j=6.9hz,3h,ch3).
19
f nmr(471mhz,cdcl3)δ-80.68
–‑
81.37(m,3f,cf3),-111.45
–‑
112.60(m,1f,ch2cf2),-114.17
–‑
115.49(m,1f,ch2cf2),-123.99
–‑
125.23(m,2f,cf2),-125.90(td,j=20.0,18.0,12.5hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ77.00,41.80
–
41.37(m),40.31,30.66,29.21,22.41,20.80,13.95..结构式如下:
[0087][0088]
实施例8
[0089]
(1,1,2,2,3,3,4,4,-九氟-6-碘十八烷c
18h28
f9i(3ha)的制备:
[0090]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃1-十四烯(19.6mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ha,产率98%。
[0091]1h nmr(500mhz,cdcl3)δ4.36(tt,j=8.9,4.6hz,1h,chi),3.03
–
2.68(m,2h,ch2rf),1.82(dqd,j=28.1,9.8,4.7hz,2h,ch2chi),1.66
–
1.10(m,20h,ch2),0.91(t,j=6.8hz,3h,ch3).
19
f nmr(471mhz,cdcl3)δ-81.05(t,j=9.9hz,3f,cf3),-111.11
–‑
112.78(m,1f,ch2cf2),-114.03
–‑
116.02(m,1f,ch2cf2),-124.58(p,j=8.7hz,2f,cf2),-125.10
–‑
126.55(m,2f,cf2).
13
c nmr(126mhz,cdcl3)δ41.59(t,j=20.9hz),40.36,31.92,29.63,29.59,29.54,29.35,28.50,22.69,20.80,14.10.结构式如下:
[0092][0093]
实施例9
[0094]
(12-溴-1,1,2,2,3,3,4,4,-九氟-6-碘十二烷c
12h15
f9ibr(3ja)的制备:
[0095]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷
(41.4mg,0.12mmol),8-溴-1-辛烯(19.0mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ja,产率98%。
[0096]1h nmr(500mhz,cdcl3)δ4.35(tt,j=8.9,4.7hz,1h),3.44(t,j=6.8hz,2h),2.87(dddd,j=66.7,27.9,15.9,8.5hz,2h),2.04
–
1.14(m,11h).
19
f nmr(471mhz,cdcl3)δ-81.00(t,j=9.5hz),-111.90(dd,j=271.7,30.5hz),-114.16
–‑
115.44(m),-124.14
–‑
124.94(m),-125.87(dtd,j=18.7,12.8,12.1,5.0hz).
13
c nmr(126mhz,cdcl3)δ41.91
–
41.28(m),40.13,33.72,32.60,29.41,27.89,27.66,20.53..结构式如下:
[0097][0098]
实施例10
[0099]
三异丙基(4,4,5,5,6,6,7,7,7-九氟-2碘庚基)硅烷c
16h26
f9isi(3la)的制备:
[0100]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯丙基三异丙基硅烷(19.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3la,产率98%。
[0101]1h nmr(500mhz,cdcl3)δ4.45(tt,j=7.9,3.9hz,1h,chi),2.47
–
2.20(m,2h,ch2rf),1.81(t,j=3.6hz,1h,ch2r
si
),1.08(dd,j=5.4,3.0hz,21h,ch3chr
si
),0.95(d,j=4.4hz,1h,ch2r
si
).
19
f nmr(471mhz,cdcl3)δ-81.02(t,j=9.7hz,3f,cf3),-113.60(ddq,j=78.0,26.1,13.1hz,2f,ch2cf2),-124.78(q,j=9.5hz,2f,cf2),-125.94(h,j=9.1,7.7hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ63.53,41.50,19.93,18.80,11.30.结构式如下:
[0102][0103]
实施例11
[0104]
(1-3,3,4,4,5,5,6,6,6-九氟-2-碘己基)-1h-吲哚c
15h11
f9in(3ma)的制备:
[0105]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),1-烯丙基-1h-吲哚(15.7mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3ma,产率67%。
[0106]1h nmr(500mhz,cdcl3)δ7.68(d,j=7.8hz,1h,h
ar
),7.31(t,j=7.4hz,1h,h
ar
),
7.28
–
7.26(m,1h,h
ar
),7.22
–
7.11(m,2h,h
ar
),6.57(d,j=3.2hz,1h,h
ar
),4.76
–
4.63(m,1h,chi),4.63
–
4.49(m,2h,ch2rn),2.85(dddd,j=55.9,35.7,15.7,7.6hz,2h,ch2rf).
19
f nmr(471mhz,cdcl3)δ-80.99(t,j=10.1hz,3f,cf3),-111.29
–‑
112.71(m,1f,ch2cf2),-112.91
–‑
114.49(m,1f,ch2cf2),-124.43(q,j=9.5hz,2f,cf2),-125.86(td,j=13.4,4.6hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ128.83,127.74,122.24,121.42,120.15,108.81,102.47,77.01,54.65,14.87.结构式如下:
[0107][0108]
实施例12
[0109]
1-氟-4-(3,3,4,4,5,5,6,6,6-九氟-1-碘己基)苯c
12
h7f
10
i(3va)的制备:
[0110]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),1-氟-4-乙烯基苯(12.2mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3va,产率67%。
[0111]1h nmr(500mhz,cdcl3)δ7.47
–
7.37(m,2h,h
ar
),7.11
–
6.92(m,2h,h
ar
),5.46(dd,j=10.1,4.9hz,1h,chi),3.44
–
3.05(m,2h,ch2rf).
19
f nmr(471mhz,cdcl3)δ-81.03(t,j=9.6hz,3f,cf3),-111.58
–‑
113.01(m,1f,ch2cf2),-114.13
–‑
115.56(m,1f,ch2cf2),-124.47(t,j=10.3hz,2f,cf2),-125.93(dtd,j=25.6,12.9,12.1,4.4hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ138.60,128.57,115.83,42.95
–
42.46(m),15.38.结构式如下:
[0112][0113]
实施例13
[0114]
2-(3,3,4,5,5,6,6-九氟-1-碘己基)萘c
16h10
f9i(3wa)的制备:
[0115]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),2-乙烯基萘(15.4mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=20:1的混合溶剂作为洗脱剂,得到含氟化合物3wa,产率67%。
[0116]1h nmr(500mhz,cdcl3)δ8.02
–
7.73(m,4h,h
ar
),7.64
–
7.42(m,4h,h
ar
),5.43(dd,j
=8.8,3.2hz,1h,chi),2.82
–
2.65(m,1h,ch2rf),2.65
–
2.44(m,1h,ch2rf).
19
f nmr(471mhz,cdcl3)δ-81.00(t,3f,j=9.7hz,cf3),-112.60(ddd,j=274.1,29.9,13.3hz,1f,ch2cf2),-113.94(ddd,j=272.4,27.8,12.9hz,1f,ch2cf2),-124.52(t,j=9.6hz,2f,cf2),-125.90(q,j=12.9hz,2f,cf2).
13
c nmr(126mhz,cdcl3)δ133.22,128.93,128.04,127.77,126.57,126.41,124.68,123.28,68.11,39.79.结构式如下:
[0117][0118]
实施例14
[0119]
1,1,1,2,2,3,3,4,4,5,5,6,6-十三氟-8-碘十三烷c
13h14f13
i(3gb)的制备:
[0120]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂全氟碘代己烷(53.5mg,0.12mmol),1-庚烯(9.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=10:1的混合溶剂作为洗脱剂,得到含氟化合物3gb,产率99%。
[0121]1h nmr(500mhz,cdcl3).δ4.36(dddd,j=9.5,8.3,5.5,4.2hz,1h,chi),3.06
–
2.71(m,2h,ch2rf),1.82(dddd,j=31.8,19.5,9.7,4.8hz,2h,ch2chi),1.64
–
1.22(m,6h,ch2),0.94(t,j=7.0hz,3h,ch3).
19
f nmr(377mhz,cdcl3)δ-80.87(t,j=10.3hz,3f,cf3),-110.92
–‑
112.69(m,1f,ch2cf2),-113.82
–‑
115.44(m,1f,ch2cf2),-121.84(dq,j=22.6,9.9,6.4hz,2f,cf2),-122.43
–‑
123.12(m,2f,cf2),-123.67(d,j=16.0hz,2f,cf2),-126.19(td,j=14.9,12.6,6.5hz,2f,cf2).
13
c nmr(126mhz,cdcl3).δ41.68(t,j=21.0hz),40.30,30.66,29.21,22.40,20.84,13.92.结构式如下:
[0122][0123]
实施例15
[0124]
8,8,9,9,10,10,11,11-八氟-6,13-二碘十八烷c
18h28
f8i2(3gf)的制备:
[0125]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂1,1,2,2,3,3,4,4,-八氟-1,4-二碘丁烷(54.5mg,0.12mmol),1-庚烯(19.6mg,0.20mmol)和内标均三甲苯(12.0mg,0.10mmol)。随后将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=10:1的混合溶剂作为洗脱剂,得到含氟化合物3gf,产率99%。
[0126]1h nmr(500mhz,cdcl3).δ4.37(tt,j=8.8,4.7hz,1h,chi),2.85(dddd,j=72.5,34.3,15.7,8.7hz,2h,ch2ch3),1.82(ttd,j=19.5,9.8,4.7hz,2h,ch2rf),1.65
–
1.19(m,6h,ch2),0.93(t,j=6.9hz,3h,ch3).
19
f nmr(471mhz,cdcl3)δ-111.19
–‑
112.40(m,2f,
ch2cf2),-114.03
–‑
115.44(m,2f,ch2cf2),-123.51(p,j=12.6,12.1hz,4f,ch2cf2).
13
c nmr(126mhz,cdcl3)δ41.82(t,j=20.0hz),40.33,30.69,29.23,22.43,21.46,13.98.结构式如下:
[0127][0128]
实施例16
[0129]
1,1,1-三氟-4-碘代烷c7h
12
f3i(3gg)的制备:
[0130]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnme2(2.4mg,0.02mol),卤代试剂1,1,1-三氟-2-碘乙烷(21.0mg,0.12mmol),1-庚烯(19.6mg,0.20mmol)和内标均三甲苯(12.0mg,0.10mmol)。随后将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=10:1的混合溶剂作为洗脱剂,得到含氟化合物3gg,产率61%。
[0131]1h nmr(500mhz,cdcl3).δ4.10(tt,j=8.9,4.5hz,1h,chi),2.53
–
2.34(m,1h,ch2chi),2.33
–
2.14(m,1h,ch2chi),2.14
–
1.97(m,2h,ch2chi),1.93(dddd,j=14.8,10.2,8.7,4.7hz,1h,ch2cf3),1.73(ddt,j=14.8,10.3,5.2hz,1h,ch2cf3),1.62
–
1.24(m,6h,ch2),0.93(t,j=7.0hz,3h,ch3).
19
f nmr(377mhz,cdcl3)δ-65.90(t,j=11.0hz,3f,cf3).
13
c nmr(126mhz,cdcl3)δ40.60,35.98,34.42
–
33.81(m),32.77,30.90,29.08,22.46,13.98.结构式如下:
[0132][0133]
实施例17
[0134]
1,1,3-三溴辛烷c8h
15
br3(3gj)的制备:
[0135]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnet2(3.0mg,0.02mol),卤代试剂三溴化碳(30.3mg,0.12mmol),1-庚烯(9.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=10:1的混合溶剂作为洗脱剂,得到含氟化合物3gj,产率73%。
[0136]1h nmr(500mhz,cdcl3)δ5.93(dd,j=9.6,4.0hz,1h,chbr2),4.15(dddd,j=11.8,8.8,5.1,3.7hz,1h,chbr),2.91
–
2.74(m,2h,ch2chbr2),1.98
–
1.81(m,2h,ch2chbr),1.63
–
1.28(m,6h,ch2),0.98
–
0.89(m,3h,ch3).
13
c nmr(126mhz,cdcl3)δ54.41,53.50,43.57,38.46,31.06,26.89,22.45,13.97.结构式如下:
[0137][0138]
实施例18
[0139]
1,1,1,3-四溴辛烷c8h
14
br4(3gk)的制备:
[0140]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(10.2mg,0.02mmol),溶剂cdcl3(500μl),催化剂phnet2(3.0mg,0.02mol),卤代试剂四溴化碳(39.8mg,0.12mmol),1-庚烯(9.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h;反应结束后将所得反应混合物通过硅胶柱色谱法纯化,使用体积比为己烷:乙酸乙酯=10:1的混合溶剂作为洗脱剂,得到含氟化合物3gk,产率73%。
[0141]1h nmr(500mhz,cdcl3)δ4.23(dq,j=9.0,4.5hz,1h,chbr),3.86(dd,j=16.2,4.5hz,1h,ch2r
br
),3.57(dd,j=16.1,4.9hz,1h,ch2r
br
),2.10(dddd,j=14.2,10.0,6.0,4.2hz,1h,ch2),1.99(dtd,j=14.3,9.4,4.7hz,1h,ch2),1.70
–
1.59(m,1h,ch2),1.59
–
1.48(m,1h,ch2),1.46
–
1.32(m,4h,ch2),1.01
–
0.86(m,3h,ch3).
13
c nmr(126mhz,cdcl3)δ66.93,52.09,39.72,36.36,30.92,27.04,22.50,14.02.结构式如下:
[0142][0143]
对比例1
[0144]
改变反应光照条件:
[0145]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(5.1mg,0.01mmol),溶剂cdcl3(500μl),催化剂phnme2(3.6mg,0.03mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃烯丙基苯(11.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温可见光下放置3h,反应结束后进行核磁测量,得到产物c
13h10
f9i,产率0%。
[0146]
对比例2
[0147]
改变路易斯酸催化剂:
[0148]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂bph3(2.4mg,0.01mmol),溶剂cdcl3(500μl),催化剂phnme2(3.6mg,0.03mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃烯丙基苯(11.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后进行核磁测量,得到产物c
13h10
f9i,产率19%。
[0149]
对比例3
[0150]
改变路易斯碱催化剂:
[0151]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(5.1mg,0.01mmol),溶剂cdcl3(500μl),催化剂nbn3(8.6mg,0.03mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃烯丙基苯(11.8mg,0.10mmol)和内标均三甲苯(12.0mg,
0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后进行核磁测量,得到产物c
13h10
f9i,产率34%。
[0152]
对比例4
[0153]
改变反应溶剂:
[0154]
在充满氩气的手套箱中,向2ml的核磁反应管中依次加入催化剂b(c6f5)3(5.1mg,0.01mmol),溶剂cd2cl2(500μl),催化剂phnme2(3.6mg,0.03mol),卤代试剂全氟碘代丁烷(41.4mg,0.12mmol),烯烃烯丙基苯(11.8mg,0.10mmol)和内标均三甲苯(12.0mg,0.10mmol),将核磁反应管从手套箱中取出并在室温,40w,460nm led灯下照射3h,反应结束后进行核磁测量,得到产物c
13h10
f9i,产率38%。
[0155]
与对比例1采用可见光相比,本发明采用led灯光源,为强度更强的蓝光光源,蓝光的能量能激发路易斯酸向路易斯碱的单电子转移。而可见光中强度太低,不能引发反应,无法得到含氟产物。
[0156]
与对比例2~3相比,本发明采用特定种类的路易斯酸和路易斯碱催化剂,能够显著提高产率。
[0157]
与对比例4相比,本发明采用氘代氯仿作为溶剂,其极性对于生成的自由基中间体极性较适中,有助于c-x键断裂,能提高产率。
[0158]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1