一种丝素蛋白颗粒的制备方法
1.本发明涉及生物医药技术领域,具体涉及一种丝素蛋白颗粒的制备方法。
背景技术:
2.近年来,为了优化小分子药物以及蛋白质和生物酶等生物制剂的治疗效果,许多以纳米材料为基础的药物递送系统得以开发并利用。这些药物递送系统不仅提高了药物的生物利用度、减少毒副作用,还能实现药物的靶向释放和控制释放。进一步提高药物递送系统的生物安全性,降低其炎症反应和免疫原反应,开发价格低廉、重复性高且易于生产、易于临床转化的纳米载体具有重大意义。
3.然而,目前丝素蛋白(silk fibroin,sf)微纳米材料的制备过程多涉及有机溶剂,如丙酮、环己烷等,会为丝基生物材料带来不必要的生物毒性;此外,为保证丝基药物递送系统以及医疗器械和敷料在生物降解程度以及机械强度等的一致性和稳定性,丝素蛋白微纳米材料粒径的均一性和可调节性显得尤为重要。丝素蛋白微纳米材料的形成与其丝素蛋白分子的亲疏水性质密切相关,而外界环境的变化会给丝素蛋白分子的亲疏水性带来巨大影响。因此,如何制备出粒径均一且可调节的丝素蛋白微纳米颗粒一直是个难点。
技术实现要素:
4.针对现有技术的不足,本发明提出了一种丝素蛋白颗粒的制备方法来制备产品具有高度均一的粒径分布、大范围的粒径调节尺度、高生物安全性的丝素蛋白颗粒。
5.本发明的目的可以通过以下技术方案实现:
6.一种丝素蛋白颗粒的制备方法,包括以下步骤:
7.将sf溶液与pva溶液混合并进行超声处理,其中sf溶液与pva溶液的质量浓度比例为1:2至1:25;超声结束后,将sf溶液与pva溶液的混合溶液置于容器中,利用烘箱烘干水分,得到sf和pva形成的薄膜;
8.将薄膜转移至离心管中,加水溶解薄膜,通过离心分离获得丝素蛋白颗粒沉淀,弃去上清,水洗沉淀3~5次,进行冷冻干燥得到粒径均一的丝素蛋白颗粒。sf分子在pva溶液中,因sf与pva分子间氢键和亲疏水相互作用以及sf分子内氢键作用强弱发生不同程度的自聚,形成粒径均一可调的丝素蛋白颗粒。上述sf为丝素蛋白(silk fibroin),pva为聚乙烯醇(polyvinyl alcohol)。
9.在一些实施例中,sf溶液通过天然蚕茧进行制备,制备方式为:将天然蚕茧除蛹后,进行脱胶、溶解、透析处理,最终获得sf溶液。
10.在一些实施例中,所述sf溶液与pva溶液的体积比为1:4。
11.在一些实施例中,所述sf溶液的质量浓度为0.1wt%~5wt%。
12.在一些实施例中,所述pva溶液的质量浓度为1.25wt%~10.0wt%。
13.在一些实施例中,所述超声处理的条件为超声能量为800瓦(w)、频率为40千赫兹(khz)、时间为30分钟(min)。
14.在一些实施例中,所述离心分离的温度为25摄氏度、转速为11000转/分钟(rpm)、时间为20min。
15.在一些实施例中,所述烘箱的烘干温度为37~60摄氏度(℃)、烘干时间为6小时(h)。
16.在一些实施例中,所述sf溶液的质量浓度为0.05~0.1wt%,通过上述方式进行制备可得到纳米级丝素蛋白颗粒,粒径范围为320.59
±
14.81~360.55
±
3.65nm,其中最佳pdi=0.04。
17.在一些实施例中,所述sf溶液的质量浓度为0.2~0.6wt%,通过上述方式进行制备可得到亚微米级丝素蛋白颗粒,粒径范围为687.78
±
14.77~987.66
±
55.30nm,其中最佳pdi=0.05。
18.在一些实施例中,所述sf溶液的质量浓度为0.7~5.0wt%,通过上述方式进行制备可得到微米级丝素蛋白颗粒,粒径范围为1030.90
±
138.76~2582.61
±
331.84nm,其中最佳pdi=0.07。
19.本发明的有益效果:
20.本发明提供的粒径均一可调的丝素蛋白微/纳米颗粒制备方法不需要特殊的设备和技术辅助、制备工艺简单、成本低、耗时短,可进行工业化规模生产;并且丝素蛋白颗粒的制备过程中不涉及有机溶剂,使其在以丝素蛋白颗粒为基础的生物医药领域具有非常可观的应用前景。
附图说明
21.下面结合附图对本发明作进一步的说明。
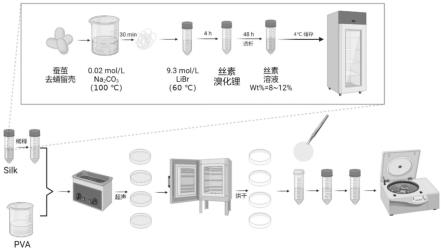
22.图1为本技术的制备方法的示意图;
23.图2为本技术的不同粒径范围丝素蛋白颗粒的扫描电子显微镜图:(a)纳米级丝素蛋白颗粒;(b)亚微米级丝素蛋白颗粒;(c)微米级丝素蛋白颗粒。
具体实施方式
24.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。
25.实施例1
26.纳米级、粒径均一丝素蛋白颗粒的制备:
27.将表面光洁的蚕茧除去蚕蛹,茧壳剪成一分钱硬币大小碎片,称取5克(g)茧壳碎片备用;在2升(l)烧杯中加入1l浓度为0.02毫摩尔/升(mmol/l)的碳酸钠(na2co3)溶液搅拌加热至沸腾(搅拌器参数:200rpm、100℃);将备用茧壳碎片缓慢加入沸腾的na2co3溶液中,搅拌使溶液与茧壳碎充分接触;30min后将除胶的蚕丝捞出,挤干水分,去离子水洗涤后挤干水分,反复洗涤三次,将挤干水分的去胶蚕丝置于60℃烘箱中干燥,去除水分,称重,约3g;利用12ml浓度为9.2摩尔/升(mol/l)的溴化锂(libr)溶液溶解去胶蚕丝,溶液呈现琥珀色,将溶液转移至透析袋中(截留分子量mwco=3300),在去离子水中透析48h,分别在透析
开始后的1h、2h、4h、16h、40h、46h更换透析液,获得丝素蛋白溶液。
28.将丝素蛋白溶液稀释至质量浓度为0.05~0.1wt%,同时配置质量浓度为0.1wt%~3.0wt%的pva溶液;将2.5ml丝素溶液滴入10ml的pva溶液,对混合溶液加以800w、40khz的超声处理30min;超声结束后,移取10ml混合溶液置于直径为10cm的聚苯乙烯培养皿中,使混合溶液在培养皿中均匀展开;将培养皿置于37~60℃烘箱中干燥6h去除水分;用镊子从培养皿中挑出干燥的薄膜,置于50ml离心管中;向管中加入30ml去离子水,在60℃水浴中充分浸泡、溶解薄膜;待薄膜溶解后,离心(离心参数:室温、11000rpm、20min),弃去上清,用30ml去离子水洗涤沉淀3~5次,直至分散的重悬液无泡沫。经激光粒度仪检测,该丝素蛋白颗粒粒径为320.59
±
14.81~360.55
±
3.65nm,最佳pdi=0.04。
29.本实施例结果说明,本发明的制备方法可以在纳米级尺度范围内获得粒径高度均一的丝素蛋白颗粒。
30.实施例2
31.亚微米级、粒径均一丝素蛋白颗粒的制备:
32.将2.5ml的sf溶液(浓度:0.2~0.6wt%)滴入10ml的pva溶液(浓度:5.0~10.0wt%)后,利用800w、40khz超声处理溶液30min;超声结束后,移取10ml混合溶液于直径10cm的聚苯乙烯培养皿中,使溶液在培养皿中均匀展开;将培养皿放置在60℃烘箱中干燥6h,去除水分;用镊子从培养皿中挑出干燥的薄膜,置于50ml离心管中;向离心管中加入30ml去离子水,在37~60℃水浴中充分浸泡、溶解薄膜;待薄膜充分溶解后,离心(离心参数:室温、11000rpm、20min),弃去上清,用30ml去离子水洗涤沉淀3~5次,直至分散的重悬液中无泡沫。经激光粒度仪检测,该方法丝素蛋白颗粒粒径为687.78
±
14.77~987.66
±
55.30nm,最佳pdi=0.05。
33.本实施例结果说明,本发明所制备的丝素蛋白颗粒,粒径可以在亚微米尺度调节且均一度高。
34.实施例3
35.微米级、粒径均一丝素蛋白颗粒的制备:
36.将丝素蛋白母液稀释至质量浓度为0.7~5.0wt%,配置质量浓度为1.0~10.0wt%的pva溶液;将2.5ml丝素溶液滴入10ml的pva溶液后,对混合溶液施加800w、40khz的超声处理30min;超声结束后,移取10ml混合溶液于直径10cm的聚苯乙烯培养皿中,使溶液在培养皿中均匀展开;将培养皿放置在37~60℃烘箱中干燥6h,去除水分;用镊子从培养皿中挑出干燥的薄膜,置于50ml离心管中;向离心管中加入30ml去离子水,在60℃水浴中充分浸泡、溶解薄膜;待薄膜充分溶解后,离心(离心参数:室温、11000rpm、20min),弃去上清,用30ml去离子水洗涤沉淀3~5次,直至分散的重悬液中无泡沫。经激光粒度仪检测,丝素蛋白颗粒粒径为1030.90
±
138.76~2582.61
±
331.84nm,最佳pdi=0.07。
37.本实施例结果说明,本发明所制备的丝素颗粒,可在微米级尺度调节粒径大小,并且粒径均一度高。
38.统计学分析
39.统计数据以平均值
±
标准误的形式给出,origin统计软件处理数据,组件比较采用单因素方差分析,两组比较采用t检验,p<0.05为具有显著差异。实验结果均重复3次以上。
40.以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1