一种幽门螺杆菌双靶点的引物组合及其LAMP检测方法和应用
一种幽门螺杆菌双靶点的引物组合及其lamp检测方法和应用
技术领域
1.本发明涉及分子诊断的快速检测技术领域,具体涉及一种幽门螺杆菌双靶点的引物组合及其lamp检测方法和应用。
背景技术:
2.幽门螺旋杆菌(helicobacterpylori,hp)是一种定植于胃黏膜形态呈螺旋形或弧形弯曲状的微需氧革兰氏阴性菌,世界上超过一半的人口长期被hp感染。hp持续感染会导致慢性胃炎,严重可演变为消化性溃疡、癌前病变(萎缩、肠上皮化生和发育不良)和胃癌。hp感染是胃癌形成的主要因素,被世界卫生组织列为i类致癌因子,与未感染人群相比,感染hp的人群患胃癌的风险增加了2-8倍。大多数情况下,hp感染为无症状,约10%的感染者出现胃部病变,其中1%-3%的人会进展为胃癌。鉴于目前幽门螺杆菌缺少商业化疫苗且多重耐药性问题日益严重,临床上对其根除效果不佳,因此,精准的检测技术是预防幽门螺杆菌感染的关键,也是评估感染后治疗效果的重要手段。
3.目前临床上用于hp的检测方法分为侵入性和非侵入性两大类,侵入性方法主要包括胃镜取胃粘膜组织进行免疫组化检测、细菌培养法、快速尿素酶试验(rut,rapidurease test)及血清抗体检测等;非侵入性方法包括14c/13c呼气试验(14c/13c-ubt,14c/13curea breath test)、唾液抗体、尿液抗体和粪便抗原检测(hpsa,hp stool antigen)等。上述方法中不同程度存在操作复杂、检测滞后、灵敏度不高、有创伤等缺点,且无法识别细菌是否致病。因此,建立一种无创、快捷、准确的致病hp检测方法是众多学者研究的目标。
4.精准的检测技术是根除幽门螺杆菌的基础,尽管传统检测技术众多,但在敏感性与特异性等诸多方面存在不足,在这些检测技术指导下的用药方案也导致诸多问题,如国内外研究均表明,近年来幽门螺杆菌的耐药率明显增加,且有产生多重耐药的趋势。因此,开发准确、简便的检测方法克服治疗过程中面临的问题迫在眉睫。所有的hp都携带有尿素酶b基因(ureb),但hp的重要毒力因子细胞毒素相关基因a(cytotoxin associated genea,caga)才是引起胃癌发生的关键因素,caga+菌株引起胃癌发生风险高,而caga-菌株胃癌风险较低,因此,caga基因被认为高毒力hp菌株最重要的标志物。
技术实现要素:
5.针对上述问题,本发明提供一种幽门螺杆菌双靶点的引物组合及其lamp检测方法和应用,应用hp通用基因ureb和致病基因caga设计开发一款基于lamp技术的hp检测试剂,可实现快速、无创、精确鉴别检测感染hp和感染致病性hp,从而指导用药方案,降低由hp感染造成的胃癌的发病率,也为全民自测hp提供参考。
6.本发明采用下述的技术方案:
7.一种幽门螺杆菌双靶点的引物组合包括:ureb引物组和caga引物组;所述ureb引物组包括引物f3-1、b3-1、fip-1、bip-1、loof-1、loob-1;所述ureb引物组各引物序列依次见序列表序列号1-6;所述caga引物组包括引物f3-6、b3-6、fip-6、bip-6、loof-6、loob-6;
所述caga引物组各引物序列依次见序列表序列号31-36。
8.本发明还提供一种幽门螺杆菌双靶点的lamp检测方法,所述lamp检测方法使用幽门螺杆菌双靶点的引物组合进行lamp扩增。
9.进一步的,幽门螺杆菌双靶点的lamp检测方法包括:
10.s1:所述ureb引物组和caga引物组分别与lamp反应液配制成25μl反应体系,然后通过lamp反应进行扩增;
11.s2:反应结束,通过肉眼观察反应体系颜色变化判断检测样品中是否含有幽门螺杆菌核酸物质和高毒力株幽门螺杆菌核酸物质。
12.进一步的,所述反应体系包括1.4mmol/ldntp mix、20mmol/ltris-hcl、10mmol/lkcl、10mmol/l(nh4)2so4、6mmol/lmgso4、0.1%triton x-100、320u/ml bst dna聚合酶、10μmol/l酸碱指示剂。
13.进一步的,所述lamp反应条件为60-65℃恒温30-60min。
14.进一步的,所述反应体系用酸碱指示剂建立可视化检测系统;所述酸碱指示剂选自苯酚红、酚红、溴百里酚蓝、中性红、甲酚红、玫红酸中的一种。
15.进一步的,所述酸碱指示剂为苯酚红。
16.进一步的,所述步骤s2中ureb引物组反应体系为橙黄色且caga引物组反应体系为橙黄色,则体系中含有高毒力幽门螺杆菌核酸物质;ureb引物组反应体系为紫红色且caga引物组应体系为紫红色,则体系中既不含幽门螺杆菌核酸物质也不含高毒力幽门螺杆菌核酸物质;ureb引物组反应体系为橙黄色且caga引物组应体系为紫红色,则体系中含有幽门螺杆菌核酸物质。
17.本发明还提供一种幽门螺杆菌双靶点的引物组合在检测幽门螺杆菌和高毒力幽门螺杆菌试剂盒中的应用。
18.本发明的有益效果是:
19.本发明提供的幽门螺杆菌双靶点的lamp检测方法用时短、反应快,30分钟就能出检测结果;本检测方法特异性高,能同时快速精确鉴别感染hp和感染致病性hp,为治疗方案的确定提供有效参考;本检测方法不需要昂贵器材,只需维持60℃即可完成检测,使检测更加便利;所用的lamp检测方法费用低,从而降低检测成本,能够应用于通用型幽门螺杆菌和高毒力株幽门螺杆菌的检测试剂盒中。
附图说明
20.为了更清楚地说明本发明实施例的技术方案,下面将对实施例的附图作简单地介绍,显而易见地,下面描述中的附图仅仅涉及本发明的一些实施例,而非对本发明的限制。
21.图1幽门螺杆菌ureb通用基因引物组合1-4筛选结果;
22.图2幽门螺杆菌caga毒力基因引物组合1-4筛选结果;
23.图3 ureb引物组合反应温度筛选结果;
24.图4 caga引物组合反应温度筛选结果;
25.图5 ureb引物组合反应时间筛选结果;
26.图6 caga引物组合反应时间筛选结果;
27.图7 ureb引物组合lamp特异性检测结果;
28.图8 caga引物组合lamp特异性检测结果;
29.图9 ureb引物组合lamp灵敏度检测结果;
30.图10 caga引物组合lamp灵敏度检测结果;
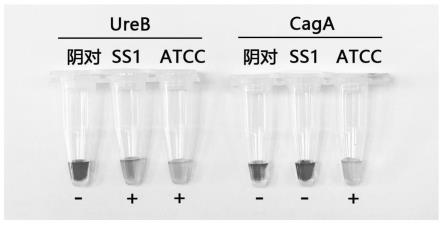
31.图11幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp检测结果
具体实施方式
32.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。下述实施例中所用实验方法如无特殊说明,均为常规方法;所用材料、试剂等,如无特殊说明,均可从商业途径得到。
33.选取hp caga-菌株ss1和caga+菌株atcc 43504(菌株均为实验保藏株)用于建立ureb通用基因和caga毒力基因双靶点lamp检测方法。将所述ureb引物组和caga引物组分别与lamp反应液配制成25μl体系在60-65℃恒温条件下反应30-60min后可得到反应结果。利用酸碱指示剂苯酚红建立可视化检测系统,在反应结束后肉眼观察体系为橙黄色则为阳性结果,体系为紫红色则为阴性结果。
34.实施例一幽门螺杆菌ureb通用基因和caga毒力基因引物设计与筛选
35.根据幽门螺杆菌ureb基因(genebank登录号:af508016.1)和caga基因(genebank登录号:ab015413.1)序列,应用primerexplorerv5软件各设计出4套引物组后用于后续验证,引物序列见下表1和表2。引物合成自生工生物有限公司。经实验验证,ureb基因引物组1和caga基因引物组6具有较好的检测能力。如图1所示,ureb基因引物组1能识别出阴阳性样本,而引物组2和3不能识别阳性样本,引物组合4阴性样本中出现非特异性扩增。如图2所示,caga基因引物组5和8不能工作,引物组6能识别出阴阳性样本,引物组7出现非特异性扩增。因此,ureb引物组选用引物组1,caga引物组选用引物组6用于后续建立幽门螺杆菌ureb通用基因和caga致病基因双靶点lamp检测方法。
36.表1 ureb基因引物
[0037][0038][0039]
表2 caga基因引物
[0040][0041][0042]
实施例二幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp反应扩增温度筛选
[0043]
为了筛选出ureb和caga引物组合进行lamp反应的最佳扩增温度,分别在60℃、61℃、62℃、63℃、64℃、65℃和66℃的恒定温度下反应60min对ureb和caga引物组的扩增温度进行验证。如图3和图4所示,ureb和caga引物组合在60℃-65℃时均可以识别出阴阳性样本,在66℃时出现非特异性扩增。因此,选择60℃-65℃的温度均可以得到较好的扩增效果。
[0044]
实施例三幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp反应扩增时间筛选
[0045]
为了筛选出ureb和caga引物组合在恒定温度下(60℃)进行lamp反应的扩增时间,分别验证ureb和caga引物组扩增10min、20min、30min、40min、50min和60min后的扩增情况。结果如图5所示,ureb引物组在60℃温度下扩增30min可出现阳性扩增。如图6所示,caga引物组在60℃温度下扩增20min即可出现阳性扩增。因此,为了统一ureb和caga引物组合的扩增时间,选择30-60min均可获得阳性扩增。
[0046]
实施例四幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp检测的特异性
[0047]
为了ureb和caga引物组合的特异性,分别应用幽门螺杆菌ss1菌株(caga-)、幽门螺杆菌atcc 43504菌株(caga+)、牛链球菌、牛球虫和甲型链球菌、乙型链球菌、肺炎链球菌、金黄色葡萄球菌、流感嗜血杆菌、副溶血弧菌、铜绿假单胞菌、大肠杆菌、志贺氏菌、沙门氏菌等12种对照菌株进行实验。牛链球菌、乙型链球菌和甲型链球菌购自宁波明舟生物科技有限公司,其余菌种为四川大学华西基础医学与法医学院微生物教研室保存菌株。如图7所示,应用可视化lamp法验证ureb引物组仅对hp ss1和atcc 43504菌株产生阳性扩增;如图8所示,应用可视化lamp法验证caga引物组仅对hpatcc 43504菌株产生阳性扩增。因此,基于幽门螺杆菌ureb通用基因和caga毒力基因建立的双靶点lamp检测法具有很好的特异性。
[0048]
实施例五幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp检测的灵敏度
[0049]
为了确定幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp检测的灵敏度,分别将hp ss1菌株和atcc 43504菌株培养物制成菌悬液,将标准菌液稀释成1.0
×
108cfu/ml-1.0
×
102cfu/ml的梯度样本,在60℃恒定温度下扩增30min进行检测。结果如图9所示,应用lamp可视化检测系统ureb引物组合在60℃恒温扩增30min条件下能对1.0
×
108cfu/ml-1.0
×
101cfu/ml的样本进行扩增。说明ureb引物组用于建立的lamp检测方法最低检测限为1.0
×
102cfu/ml。结果如图10所示,应用lamp可视化检测系统caga引物组在60℃恒温扩增30min条件下能对1.0
×
108cfu/ml-1.0
×
102cfu/ml的样本进行扩增。说明caga引物组用于建立的lamp检测方法最低检测限为1.0
×
102cfu/ml。综上,幽门螺杆菌ureb通用基因和caga毒力基因引物组合建立双靶点lamp检测的灵敏度为1.0
×
102cfu/ml。
[0050]
实施例六基于幽门螺杆菌ureb通用基因和caga毒力基因双靶点lamp检测
[0051]
将hp ss1菌株和atcc 43504菌株作为样本进行检测。结果如图11所示,ureb引物组对ss1菌株和atcc 43504菌株均能产生阳性扩增,caga基因引物组对ss1菌株不能产生阳性扩增,对atcc 43504菌株产生阳性扩增。因此,本方法可以识别菌株是否产生caga毒力因子,对识别致病性hp有应用价值。
[0052]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1